CYP17A1 - CYP17A1
| Steroidowa 17-alfa-hydroksylaza/17,20 liaza | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||||
| Nr WE | 1.14.14.19 | ||||||||
| Nr CAS | 9029-67-8 | ||||||||
| Alt. nazwy | P450c17, CYP17A1, 17-alfa-hydroksylaza steroidowa/17,20 liaza, CYPXVII, cytochrom P450 17A1, cytochrom p450 XVIIA1, cytochrom P450-C17, cytochrom P450, rodzina 17, podrodzina A, polipeptyd 1, 17-alfa-monooksygenaza steroidowa, cytochrom P450c17, 4.1.2.30, aldolaza 17-alfa-hydroksyprogesteronu, cytochrom P450, podrodzina XVII (17-alfa-hydroksylaza steroidowa), 17-alfa-hydroksylaza steroidowa/liaza 17,20, IPR033282 | ||||||||
| Bazy danych | |||||||||
| IntEnz | Widok IntEnz | ||||||||
| BRENDA | Wpis BRENDY | ||||||||
| ExPASy | Widok NiceZyme | ||||||||
| KEGG | Wpis KEGG | ||||||||
| MetaCyc | szlak metaboliczny | ||||||||
| PRIAM | profil | ||||||||
| Struktury WPB | RCSB PDB PDBe Suma PDB | ||||||||
| |||||||||
Cytochromu P450, 17A1 ( steroid 17α-monooksygenazy , 17α-hydroksylazy , 17-a-hydroksylazy , 17,20-liazy , 17,20-desmolaza ) jest enzymem z hydroksylazy typu, który u człowieka jest kodowany przez CYP17A1 genu na chromosomie 10 . Jest wszechobecnie wyrażany w wielu tkankach i typach komórek, w tym siatkową nadnerczy i zona pasmowatej z kory nadnerczy , jak gonad tkanek. Wykazuje aktywność zarówno 17α-hydroksylazy, jak i 17,20-liazy i jest kluczowym enzymem w szlaku steroidogennym, który wytwarza progestyny , mineralokortykosteroidy , glukokortykoidy , androgeny i estrogeny . Dokładniej, enzym działa na pregnenolon i progesteron, dodając grupę hydroksylową (-OH) w pozycji węgla 17 (C17) pierścienia D steroidu (aktywność 17α-hydroksylazy, EC 1.14.14.19 ) lub działa na 17α-hydroksyprogesteron i 17α-hydroksypregnenolon do oddzielenia łańcucha bocznego od jądra steroidowego ( aktywność 17,20- liazy , EC 1.14.14.32 ).
Struktura
Gen
CYP17A1 gen znajduje się na chromosomie 10 w 10q24.3 zespołu i zawiera 8 eksonów . CDNA tego genu obejmuje długość 1527 bp . Ten gen koduje członka nadrodziny enzymów cytochromu P450 . Białka cytochromu P450 są ogólnie uważane za monooksygenazy, które katalizują wiele reakcji zaangażowanych w metabolizm leków i syntezę cholesterolu , steroidów i innych lipidów , w tym niezwykłe rozerwanie wiązania węgiel-węgiel katalizowane przez ten enzym.
CYP17A1 genu może też zawierać warianty związane ze zwiększonym ryzykiem choroby niedokrwiennej wieńcowej .
Białko
CYP17A1 to białko o masie 57,4 kDa należące do rodziny cytochromów P450. Białko kodowane przez jego cDNA składa się z 508 reszt aminokwasowych . Jako enzym, CYP17A1 posiada miejsce aktywne, które łączy się z grupą protetyczną hemu , aby katalizować reakcje biosyntezy. W oparciu o znane konstrukcje, a związany z dwoma niesteroidowe inhibitory abirateronu i galeterone , CYP17A1 posiada kanoniczna cytochromu P450 krotnie obecne w innych złożonych enzymów P450, które uczestniczą w steroidów lub cholesterolu metabolizmu, chociaż orientuje steroidowych ligandów wobec helis F i G prostopadle do grupy hemu, a nie do arkusza β1.
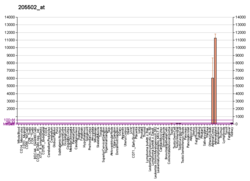
Wyrażenie
Expression of CYP17A1 stwierdzono we wszystkich tradycyjnych steroidogennych tkanek poza łożysko , w tym reticularis zona i zona pasmowatej w korze nadnerczy , że komórki Leydiga tych jąder , z pęcherzyka Graafa komórkach tych jajników , a ostatnio, w luteinizowane komórki ziarniste w pęcherzykach jajnikowych . Oprócz klasycznej tkanki steroidogennej, CYP17A1 wykryto również w sercu , nerkach i tkance tłuszczowej . U płodu donoszono o występowaniu CYP17A1 w nerkach , grasicy i śledzionie .
Funkcjonować
CYP17A1 jest członkiem nadrodziny enzymów cytochromu P450 zlokalizowanych w retikulum endoplazmatycznym . Białka z tej rodziny to monooksygenazy, które katalizują syntezę cholesterolu , steroidów i innych lipidów oraz biorą udział w metabolizmie leków. CYP17A1 ma zarówno aktywność 17α-hydroksylazy ( EC 1.14.14.19 ), jak i aktywność 17,20-liazy ( EC 1.14.14.32 ). Aktywność 17α-hydroksylazy CYP17A1 jest wymagana do wytwarzania glikokortykoidów, takich jak kortyzol, ale aktywność hydroksylazy i 17,20-liazy CYP17A1 jest wymagana do wytwarzania androgennych i estrogennych steroidów płciowych poprzez przekształcenie 17α-hydroksypregnenolonu w dehydroepiandrosteron ( DHEA) . Mutacje w tym genie są związane z izolowanym niedoborem 17α-hydroksylazy steroidowej, niedoborem 17α-hydroksylazy/17,20-liazy, pseudohermafrodytyzmem i przerostem nadnerczy .
Ponadto aktywność 17,20-liazy zależy od oksydoreduktazy cytochromu P450 (POR), cytochromu b5 (CYB5) i fosforylacji . Cytochrom b5 działa jako czynnik ułatwiający aktywność 17,20 liazy CYP17A1 i może przekazać drugi elektron niektórym P450. U ludzi produkcja testosteronu przez pregnenolon do 17-OHPreg i DHEA przez CYP17A1 wymaga POR. Ludzkie białko CYP17A1 jest fosforylowane na resztach seryny i treoniny przez kinazę białkową zależną od cAMP . Fosforylacja białka zwiększa aktywność 17,20-liazy, podczas gdy defosforylacja praktycznie eliminuje tę aktywność.
Znaczenie kliniczne
Mutacje w tym genie są związane z rzadkimi postaciami wrodzonego przerostu nadnerczy , szczególnie niedoborem 17α-hydroksylazy/17,20-liazy i izolowanym niedoborem 17,20-liazy .
U ludzi gen CYP17A1 jest w dużej mierze związany z efektami endokrynologicznymi i metabolizmem hormonów steroidowych. Ponadto mutacje w genie CYP17A1 są związane z rzadkimi postaciami wrodzonego przerostu nadnerczy , w szczególności niedoborem 17α-hydroksylazy/17,20-liazy i izolowanym niedoborem 17,20-liazy. Podsumowując, CYP17A1 jest ważnym celem hamowania w leczeniu raka prostaty, ponieważ wytwarza androgen niezbędny do wzrostu komórek nowotworowych. Zmniejszona aktywność enzymatyczna CYP17A1 jest związana z niepłodnością spowodowaną hipogonadyzmem hipogonadotropowym. U kobiet następuje zatrzymanie folikulogenezy, natomiast u mężczyzn zanik jąder z proliferacją komórek śródmiąższowych i zahamowaniem spermatogenezy. Chociaż na ogół nie ma owulacji, istnieją doniesienia o przypadkach kobiet z niedoborem 17α-hydroksylazy, które przeszły spontaniczną pierwszą miesiączkę z cyklicznymi miesiączkami.
Marker kliniczny
Wielomiejscowe badanie oceny ryzyka genetycznego oparte na kombinacji 27 loci, w tym genu CYP17A1, zidentyfikowało osoby o zwiększonym ryzyku zarówno incydentów, jak i nawrotów choroby wieńcowej, a także zwiększone korzyści kliniczne z leczenia statynami. Badanie opierało się na badaniu kohortowym społeczności (badanie Malmo Diet and Cancer) oraz czterech dodatkowych randomizowanych, kontrolowanych badaniach kohortowych z prewencją pierwotną (JUPITER i ASCOT) i kohortami prewencji wtórnej (CARE i PROVE IT-TIMI 22).
Jako cel narkotykowy
Inhibitory CYP17A1
Obecnie FDA zatwierdziła tylko jeden inhibitor CYP17A1, abirateron, który zawiera rusztowanie steroidowe, które jest podobne do endogennych substratów CYP17A1. Abirateron jest strukturalnie podobny do substratów innych enzymów cytochromu P450 zaangażowanych w steroidogenezę, a interferencja może wiązać się z działaniami niepożądanymi. Oczekuje się, że zastosowanie rusztowań niesteroidowych umożliwi zaprojektowanie związków, które oddziałują bardziej selektywnie z CYP17A1. Silne inhibitory enzymu CYP17A1 zapewniają ostatnią linię obrony przed androgenezą ektopową w zaawansowanym raku prostaty.
Lek octan abirateronu , stosowany w leczeniu opornego na kastrację raka prostaty , blokuje biosyntezę androgenów poprzez hamowanie enzymu CYP17A1. Octan abirateronu wiąże się w miejscu aktywnym enzymu i koordynuje żelazo hemu poprzez jego azot pirydynowy, naśladując substrat.
Od 2014 roku galeteron jest w badaniach klinicznych III fazy dotyczących raka prostaty opornego na kastrację .
Ketokonazol jest starszym inhibitorem CYP17A1, który jest obecnie rzadko stosowany. Jednak ketokonazol kompetycyjnie hamuje CYP17A1, dlatego jego skuteczność będzie zależeć od stężenia ketokonazolu. Jest to w przeciwieństwie do octanu abirateronu , który trwale (a nie konkurencyjnie) wyłącza CYP17A1, gdy się z nim zwiąże.
Seviteronel (VT-464) jest nowym inhibitorem CYP17A1, którego celem jest uniknięcie jednoczesnego leczenia glikokortydami. W 2010 roku przeszedł różne fazy badań klinicznych i modeli przedklinicznych jako lek na raka prostaty lub raka piersi.
Steroidogeneza
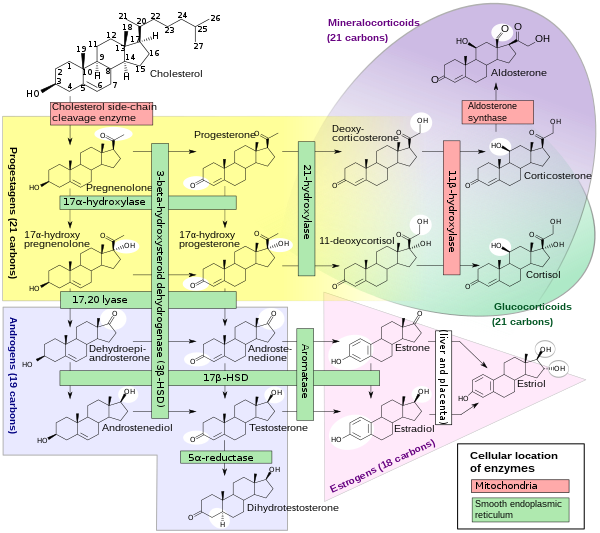
Steroidogeneza , pokazująca, po lewej stronie, obie reakcje 17α-hydroksylazy i oba działania 17,20 liazy.
|
Dodatkowe obrazy
Zobacz też
Bibliografia
Dalsza lektura
- Miura K, Yasuda K, Yanase T, Yamakita N, Sasano H, Nawata H, Inoue M, Fukaya T, Shizuta Y (październik 1996). „Mutacja genu cytochromu P-45017 alfa (CYP17) u japońskiego pacjenta, który wcześniej zgłaszano jako hiperaldosteronizm reagujący na glikokortykoidy: z przeglądem japońskich pacjentów z mutacjami CYP17” . Czasopismo Endokrynologii Klinicznej i Metabolizmu . 81 (10): 3797–801. doi : 10.1210/jcem.81.10.8855840 . PMID 8855840 .
- Miller WL, Geller DH, Auchus RJ (1999). „Molekularna podstawa wyizolowanego niedoboru 17,20 liazy”. Badania endokrynologiczne . 24 (3–4): 817–25. doi : 10.3109/07435809809032692 . PMID 9888582 .
- Strauss JF (listopad 2003). „Kilka nowych przemyśleń na temat patofizjologii i genetyki zespołu policystycznych jajników”. Roczniki Nowojorskiej Akademii Nauk . 997 (1): 42-8. Kod Bib : 2003NYASA.997...42S . doi : 10.1196/annals.1290.005 . PMID 14644808 . S2CID 23559461 .
- Haider SM, Patel JS, Poojari CS, Neidle S (lipiec 2010). „Modelowanie molekularne na kompleksach inhibitorów i dynamice miejsca aktywnego cytochromu P450 C17, cel w terapii raka prostaty”. Czasopismo Biologii Molekularnej . 400 (5): 1078–98. doi : 10.1016/j.jmb.2010.05.069 . PMID 20595043 .
Zewnętrzne linki
- CYP17A1+białko,+człowiek w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)
- Lokalizacja genomu ludzkiego CYP17A1 i strona szczegółów genu CYP17A1 w przeglądarce genomu UCSC .