25I-NBOMe - 25I-NBOMe
 | |
 | |
| Dane kliniczne | |
|---|---|
| Drogi administracji |
Policzkowego ( sublabial ), podjęzykowo , wdmuchuje się , wdychanie , dożylnie , domięśniowo , doodbytniczo |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| ChemSpider | |
| UNII | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Dane chemiczne i fizyczne | |
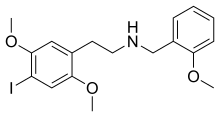
| Formuła | C 18 H 22 I N O 3 |
| Masa cząsteczkowa | 427.282 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
| Część serii na |
| Psychodelia |
|---|
25I-NBOMe ( 2C-I- NBOMe , Cimbi-5 , również skracane do " 25I ") jest syntetycznym halucynogenem, który jest używany w badaniach biochemicznych do mapowania wykorzystania przez mózg receptora serotoninowego typu 2A ; bywa też wykorzystywany do celów rekreacyjnych. Pochodna rodziny podstawionej fenetylaminy 2C-I , jest najbardziej znanym członkiem rodziny 25-NB . Został odkryty w 2003 roku przez chemika Ralfa Heima z Wolnego Uniwersytetu w Berlinie , który opublikował swoje odkrycia w swojej rozprawie doktorskiej. Związek został następnie zbadany przez zespół z Purdue University kierowany przez Davida Nicholsa .
Węgla-11 oznaczony jako wersja z 25I-NBOME, [11C] Cimbi-5, zsyntetyzowano i zatwierdzone jako radioizotopu za pomocą pozytronowej tomografii emisyjnej (PET) w Kopenhadze. Będąc pierwszym radioligandem PET pełnego agonisty receptora 5-HT 2A , [11C] -CIMBI-5 wydaje się obiecujący jako bardziej funkcjonalny marker tych receptorów, szczególnie w ich stanach wysokiego powinowactwa.
Uliczne i medialne pseudonimy tego narkotyku to: „N-Bomb”, „Solaris”, „Smiles” i „Wizard”.
Wykorzystanie rekreacyjne
Chociaż 25I-NBOMe odkryto w 2003 r., jako powszechny narkotyk rekreacyjny pojawił się dopiero w 2010 r., kiedy to po raz pierwszy został sprzedany przez sprzedawców specjalizujących się w dostarczaniu markowych leków . W kontekście slangu nazwa związku jest często skracana do „25I” lub po prostu nazywana „N-Bomb”. Według sondażu z 2014 r., 25I-NBOMe był najczęściej używanym produktem z serii NBOMe. Do 2013 roku w literaturze medycznej coraz częściej pojawiały się opisy przypadków zatrucia 25I-NBOMe, z lub bez potwierdzenia analitycznego leku w organizmie.
Powszechnie mówi się, że 25I-NBOMe jest nieaktywny po podaniu doustnym; jednak widoczne przedawkowania wystąpiły po podaniu doustnym. Typowe drogi podania obejmują podjęzykowe , podpoliczkowe i donosowe. W przypadku podawania podjęzykowego i podpoliczkowego, 25I-NBOMe jest często nakładany na arkusze bibuły, których małe części ( wypustki ) trzymane są w ustach, aby umożliwić wchłanianie przez błonę śluzową jamy ustnej. Istnieją doniesienia o dożylnym wstrzyknięciu roztworu 25I-NBOMe i paleniu leku w postaci sproszkowanej.
Ze względu na swoją moc i znacznie niższy koszt niż tak zwane klasyczne lub tradycyjne psychedeliki, blottery 25I-NBOMe są czasami błędnie przedstawiane jako blottery LSD lub mylone z nimi. Nawet małe ilości 25I-NBOMe mogą wytworzyć dużą liczbę blotterów. Sprzedawcy mieliby importować 25I-NBOMe luzem (np. 1 kilogramowe pojemniki) i odsprzedawać pojedyncze dawki ze znacznym zyskiem.
Dawkowanie
25I-NBOMe jest silny, działając w dawkach submiligramowych. Powszechna dawka chlorowodorku wynosi 600–1200 µg . Brytyjska Rada Doradcza ds. Nadużywania Narkotyków stwierdza, że powszechna dawka wynosi od 50 do 100 µg, chociaż inne źródła wskazują, że liczby te są nieprawidłowe; Erowid wstępnie sugeruje, że dawka progowa dla ludzi wynosi 50–250 µg, przy małej dawce 200–600 µg, zwykłej dawce 500–800 µg i mocnej dawce 700–1500 µg. Na tym poziomie siły działania nie jest możliwe dokładne odmierzenie pojedynczej dawki proszku 25I-NBOMe bez wagi analitycznej , a próba dokonania tego może narazić użytkownika na znaczne ryzyko przedawkowania.
Efekty
Efekty 25I-NBOMe zwykle trwają 6-10 godzin, jeśli są przyjmowane podjęzykowo lub dopoliczkowo (między dziąsłem a policzkiem). Kiedy jest wdmuchiwany (wciągnięty), efekty zwykle trwają 4-6 godzin.
25I-NBOMe ma podobne efekty do LSD, chociaż użytkownicy zgłaszają więcej negatywnych skutków pod wpływem i większe ryzyko szkód po użyciu w porównaniu z klasycznymi psychedelikami.
Opisy przypadków siedmiu brytyjskich mężczyzn, którzy zgłosili się na izbę przyjęć po potwierdzonym analitycznie zatruciu 25I-NBOMe, sugerują następujące potencjalne działania niepożądane: „tachykardia (n = 7), nadciśnienie (4), pobudzenie (6), agresja, omamy wzrokowe i słuchowe (6), drgawki (3), hiperpyreksja (3), klonus (2), podwyższona liczba białych krwinek (2), podwyższona kinaza kreatynowa (7), kwasica metaboliczna (3) i ostre uszkodzenie nerek (1).”
25I-NBOMe może być spożywany w postaci płynu, proszku lub papieru i może być wciągany przez nos, wstrzykiwany, mieszany z jedzeniem lub wędzony, ale najczęściej podaje się go podjęzykowo.
Toksyczność
Rekreacyjne stosowanie 25I-NBOMe niesie ze sobą znaczne ryzyko toksyczności zarówno farmakologicznej, jak i behawioralnej. 25I-NBOMe jest substancją stosunkowo nową i niewiele wiadomo na temat jej zagrożeń farmakologicznych lub interakcji z innymi substancjami. LD 50 nie została jeszcze ustalona. Jest bardzo silnym agonistą serotoniny i, ze względu na jego działanie psychodeliczne i niejednoznaczny status prawny, jest lekiem designerskim, z doniesieniami o użyciu rekreacyjnym począwszy od 2010 roku. rządy do kontrolowania jego posiadania, produkcji i sprzedaży. Strona internetowa Erowid stwierdza, że 25I-NBOMe jest niezwykle silny i nie należy go wciągać, a lek „wydaje się, że doprowadził do kilku zgonów w ciągu ostatniego roku”. Zgłoszono również kilka nieprowadzących do zgonu przedawkowania, które wymagały przedłużonej hospitalizacji.
Według doniesień, według stanu na sierpień 2015 r., 25I-NBOMe doprowadził do co najmniej 19 zgonów z powodu przedawkowania w Stanach Zjednoczonych. W czerwcu 2012 r. dwoje nastolatków w Grand Forks w Północnej Dakocie i East Grand Forks w stanie Minnesota śmiertelnie przedawkowało substancję, która rzekomo była 25I-NBOMe, co skutkowało długimi wyrokami dla dwóch zaangażowanych stron i federalnym aktem oskarżenia przeciwko sieci z siedzibą w Teksasie sprzedawca. 21-letni mężczyzna z Little Rock w stanie Arkansas zmarł w październiku 2012 roku po zażyciu płynnej kropli leku do nosa na festiwalu muzycznym. Podobno wcześniej spożywał napoje alkoholowe zawierające kofeinę przez „kilka godzin”. Nie jest jasne, jakie inne leki mógł zażywać, ponieważ autopsje na ogół nie sprawdzają obecności badanych substancji chemicznych. W styczniu 2013 roku 18-latek w Scottsdale w Arizonie zmarł po spożyciu 25I-NBOMe sprzedawanego jako LSD; badanie toksykologiczne nie wykazało żadnych innych leków w organizmie osoby. Podejrzewa się, że narkotyk jest przyczyną śmierci w innym incydencie w Scottsdale w Arizonie w kwietniu 2013 r. Jest również przytaczany w przypadku śmierci 21-letniej kobiety w sierpniu 2013 r. i śmierci 17-latka w Minnesocie w Styczeń 2014, a także śmierć 15-latka w Waszyngtonie we wrześniu 2014 roku.
25I-NBOMe był powiązany z wieloma zgonami w Australii. W marcu 2012 roku mężczyzna w Australii zmarł w wyniku obrażeń odniesionych w wyniku wbiegnięcia na drzewa i słupy energetyczne pod wpływem alkoholu 25I-NBOMe.
25I-NBOME został połączony z głównych przypadku w dniu 20 stycznia 2016 roku w Cork , Republic of Ireland , które opuściły sześciu nastolatków hospitalizowanych, z których jeden później zmarł. Według doniesień co najmniej jeden z nastolatków doznał zatrzymania akcji serca , a także ekstremalnego krwawienia wewnętrznego.
25I-NBOMe prawdopodobnie wykazuje funkcjonalną selektywność wobec receptora 5HT 2A podobną do innych halucynogenów fenetylaminowych , aktywując kaskadę sygnału fosfolipazy A2 , która jest odpowiedzialna za uwalnianie tromboksanu A2 , wyzwalając agregację płytek krwi. Nadmierne stężenia TXA2 mogą prowadzić do zakrzepicy , która w połączeniu z działaniem obkurczającym naczynia 25I-NBOMe jest głównym czynnikiem ryzyka niedokrwienia serca , niebezpiecznego stanu, którego objawy są obecne w kilku raportach toksykologicznych.
Farmakologia
| Chwytnik | K d (nm) | ± |
|---|---|---|
| 5-HT 2A | 0,044 | |
| 5-HT 2B | 231 | 73 |
| 5-HT 2C | 2 | |
| 5-HT 6 | 73 | 12 |
| μ-opioid | 82 | 14 |
| -opioidowy | 288 | 50 |
| H 1 | 189 | 35 |
25I-NBOME działa jako bardzo silny pełny agonista dla ludzkiej 5-HT 2A receptora , ze stałą dysocjacji ( K d ) od 0,044 nM, co około szesnaście razy moc 2C-I sama na ten receptor. Radioznakowany forma 25I-NBOME mogą być wykorzystywane do mapowania rozkład 5-HT 2A receptorów w mózgu.
25I-NBOME indukuje odpowiedź głowicy skurcz u myszy, który jest całkowicie zamknięty przez selektywne 5-HT 2A antagonisty, co sugeruje jego psychodeliczne efektów pośredniczy 5-HT 2A . Badanie to sugeruje, że 25I-NBOMe jest około 14 razy silniejszy niż 2C-I in vivo .
Podczas gdy badania in vitro wykazały, że pochodne N- benzylowe 2C-I miały znacznie większą moc w porównaniu z 2C-I, pochodne N- benzylowe pokrewnego związku DOI były nieaktywne.
25I-NBOMe ma również słabsze interakcje z wieloma innymi receptorami. K d wartości dla współdziałania z następującymi celami były większe niż 500 nm: 5-HT 1A , D 3 , H 2 , 5-HT 1D , α 1A adrenergicznego , δ opioidów , wychwyt zwrotny serotoniny transportowy , 5-HT 5A , 5-HT 1B , D 2 , 5-HT 7 , D 1 , 5-HT 3 , 5-HT 1E , D 5 , muskarynowy M 1- M 5 , H 3 , oraz transporter wychwytu dopaminy .
Chemia
Podobnie jak inne cząsteczki 2C- X- NBOMe, 25I-NBOMe jest pochodną rodziny 2C fenetylamin opisanych przez chemika Alexandra Shulgina w jego książce PiHKAL . W szczególności 25I-NBOMe jest pochodną N- benzylową cząsteczki fenetylaminy 2C-I , utworzoną przez dodanie 2-metoksybenzylu (BnOMe) do azotu (N) szkieletu fenetylaminy. Ta substytucja znacząco zwiększa siłę cząsteczki.
Analogi
25I-NB*:
- 25I-NBF
- 25I-NBMD
- 25I-NB34MD
- 25I-NBOH
- 25I-NBOMe (NBOMe-2CI)
- 25I-NB3OMe
- 25I-NB4OMe
Synteza
25I-NBOMe jest zwykle syntetyzowany z 2C-I i 2-metoksybenzaldehydu poprzez redukcyjne alkilowanie . Można to zrobić stopniowo, najpierw wytwarzając iminę, a następnie redukując powstałą iminę borowodorkiem sodu lub w bezpośredniej reakcji z triacetoksyborowodorkiem sodu .
Społeczeństwo i kultura
Status prawny
Australia
25I-NBOMe zostało wyraźnie określone w prawie narkotykowym stanu Queensland w kwietniu 2012 r. oraz w Nowej Południowej Walii w październiku 2013 r., podobnie jak niektóre pokrewne związki, takie jak 25B-NBOMe. Australijski rząd federalny nie ma konkretnych przepisów dotyczących żadnej z N-benzylofenetylamin.
Kanada
Na dzień 31 października 2016 r.; 25I-NBOMe jest substancją kontrolowaną (Schedule III) w Kanadzie.
Chiny
Od października 2015 r. 25I-NBOMe jest substancją kontrolowaną w Chinach.
Unia Europejska
We wrześniu 2014 r. Unia Europejska wprowadziła zakaz 25I-NBOMe we wszystkich swoich państwach członkowskich.
Izrael
Izrael zakazał 25I-NBOMe w 2013 roku.
Rosja
Rosja była pierwszym krajem, który uchwalił szczegółowe przepisy dotyczące serii NBOMe. Wszystkie narkotyki z serii NBOMe, w tym 25I-NBOMe, stały się nielegalne w Rosji w październiku 2011 roku.
Zjednoczone Królestwo
Substancja ta jest lekiem klasy A w Wielkiej Brytanii w wyniku klauzuli catch-all N- benzylofenetyloaminy zawartej w ustawie o nadużywaniu narkotyków z 1971 roku .
Stany Zjednoczone
15 listopada 2013 r. DEA dodała 25I-NBOMe (oraz 25C- i 25B-NBOMe) do Harmonogramu I, korzystając ze swoich uprawnień do planowania awaryjnego, czyniąc te związki NBOMe „tymczasowo” w Harmonogramie I na 2 lata. W listopadzie 2015 r. tymczasowe grafikowanie zostało przedłużone o dodatkowy rok, podczas gdy ustalono stałe grafikowanie. 25I-NBOMe, 25B-NBOMe i 25C-NBOMe są obecnie substancjami Schedule 1 zgodnie z 21 CFR 1308.11(d).
Rumunia
W 2011 roku Rumunia zakazała stosowania wszelkich substancji psychoaktywnych.
Serbia
25I-NBOMe została wpisana na listę substancji zabronionych w marcu 2015 roku.
Szwecja
Riksdag dodał 25I-NBOMe do Ustawy o karach za środki odurzające zgodnie ze szwedzkim harmonogramem I ( „substancje, materiały roślinne i grzyby, które normalnie nie mają zastosowania medycznego” ) z dniem 1 sierpnia 2013 r., opublikowanym przez Agencję Produktów Medycznych (MPA) w rozporządzeniu LVFS 2013:15 wymienione jako 25I-NBOMe i 2-(4-jodo-2,5-dimetoksyfenylo)-N-(2-metoksybensylo)etanamina .
Tajwan
Zgodnie z europejską zasadą z 2014 roku 25I-NBOMe został umieszczony w klasie 4 substancji zabronionych.
Brazylia
Wszystkie narkotyki z rodziny NBOMe, w tym 25I-NBOMe, są nielegalne.
