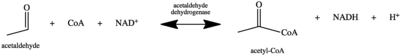Dehydrogenaza aldehydu octowego - Acetaldehyde dehydrogenase
| Dehydrogenaza aldehydu octowego (acetylowanie) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
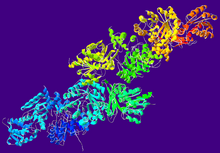 Struktura krystalograficzna dehydrogenazy aldehydu octowego z Pseudomonas sp .
| |||||||||
| Identyfikatory | |||||||||
| Nr WE | 1.2.1.10 | ||||||||
| Nr CAS | 9028-91-5 | ||||||||
| Bazy danych | |||||||||
| IntEnz | Widok IntEnz | ||||||||
| BRENDA | Wpis BRENDY | ||||||||
| ExPASy | Widok NiceZyme | ||||||||
| KEGG | Wpis KEGG | ||||||||
| MetaCyc | szlak metaboliczny | ||||||||
| PRIAM | profil | ||||||||
| Struktury WPB | RCSB PDB PDBe Suma PDB | ||||||||
| Ontologia genów | AmiGO / QuickGO | ||||||||
| |||||||||
Dehydrogenazy aldehydu octowego ( EC 1.2.1.10 ) to enzymy dehydrogenazy , które katalizują konwersję aldehydu octowego do kwasu octowego . Utlenianie aldehydu octowego do octanu można podsumować w następujący sposób:
Aldehyd octowy + NAD + + Koenzym A ↔ Acetylo-CoA + NADH + H +
U ludzi istnieją trzy znane geny, które kodują tę aktywność enzymatyczną, ALDH1A1 , ALDH2 i niedawno odkryty ALDH1B1 (znany również jako ALDH5 ). Enzymy te należą do większej klasy dehydrogenaz aldehydowych .
Numer CAS tego typu enzymu [9028-91-5].
Struktura
Cysteina -302 jest jedną z trzech kolejnych reszt Cys i jest kluczowa dla katalitycznej funkcji enzymu . Reszta jest alkilowana przez jodoacetamid zarówno w izoenzymach cytozolowych, jak i mitochondrialnych, z modyfikacjami do Cys-302, wskazującymi na aktywność katalityczną z innymi resztami. Ponadto, powyższa sekwencja Gln-Gly-Gln-Cys jest konserwowana w obu izozymach zarówno dla człowieka, jak i konia, co jest zgodne z tym, że Cys-302 ma kluczowe znaczenie dla funkcji katalitycznej.
Jak odkryto na podstawie ukierunkowanej mutagenezy , glutaminian -268 jest kluczowym składnikiem wątrobowej dehydrogenazy acetaldehydowej i ma również kluczowe znaczenie dla aktywności katalitycznej. Ponieważ aktywność w mutantach nie mogła zostać przywrócona przez dodanie ogólnych zasad, sugeruje się, że reszta działa jako ogólna zasada do aktywacji niezbędnej reszty Cys-302.
U bakterii, acylująca dehydrogenaza aldehydu octowego tworzy dwufunkcyjny heterodimer z zależną od metalu aldolazą 4-hydroksy-2-ketowalerianową . Wykorzystywana w bakteryjnej degradacji toksycznych związków aromatycznych, struktura krystaliczna enzymu wskazuje, że związki pośrednie są przenoszone bezpośrednio między miejscami aktywnymi przez hydrofobowy kanał pośredni, zapewniając niereaktywne środowisko, w którym można przenieść reaktywny związek pośredni aldehydu octowego z miejsca aktywnego aldolazy do dehydrogenazy aldehydu octowego aktywna strona. Taka komunikacja między białkami pozwala na efektywny transfer substratów z jednego miejsca aktywnego do drugiego.
Ewolucja
Chociaż oba izozymy (ALDH1 i ALDH2) nie mają wspólnej podjednostki, homologia między ludzkimi białkami ALDH1 i ALDH2 wynosi 66% na poziomie nukleotydów kodujących i 69% na poziomie aminokwasów , co jest 91% homologii między ludzkim ALDH1 a końskim ALDH1. Takie odkrycie jest zgodne z dowodami sugerującymi wczesną ewolucyjną rozbieżność między izoenzymami cytozolowymi i mitochondrialnymi , jak widać w 50% homologii między mitochondrialnymi i cytozolowymi aminotransferazami asparaginianowymi.
Rola w metabolizmie alkoholu
W wątrobie , etanol przekształca się nieszkodliwe kwasu octowego (Kwas główny w ocet ) w procesie dwuetapowym. W pierwszym etapie etanol jest przekształcany w aldehyd octowy przez dehydrogenazę alkoholową . W drugim etapie aldehyd octowy jest przekształcany w kwas octowy przez dehydrogenazę acetaldehydową. Aldehyd octowy jest bardziej toksyczny niż alkohol i jest odpowiedzialny za wiele objawów kaca .
Około 50% osób pochodzenia północno-wschodnioazjatyckiego ma dominującą mutację w genie dehydrogenazy aldehydu octowego , co czyni ten enzym mniej skutecznym, co powoduje reakcję upierzenia alkoholem , znaną również jako zespół upierzenia azjatyckiego. Podobną mutację stwierdza się u około 5–10% niebieskookich blondynów pochodzenia północnoeuropejskiego. U tych osób aldehyd octowy gromadzi się po wypiciu alkoholu, prowadząc do objawów zatrucia aldehydem octowym, w tym charakterystycznego zaczerwienienia skóry oraz zwiększonej częstości akcji serca i oddychania. Inne objawy mogą obejmować silne skurcze brzucha i dróg moczowych, uderzenia gorąca i zimna, obfite pocenie się i głębokie złe samopoczucie . Osoby z niedoborem aktywności dehydrogenazy aldehydu octowego znacznie rzadziej stają się alkoholikami , ale wydają się być bardziej narażone na uszkodzenie wątroby, astmę wywołaną alkoholem i zarażenie się rakiem części ustnej gardła i przełyku z powodu nadmiernej ekspozycji na aldehyd octowy.
Pokazuje to, że w wielu toksycznych działaniach etanolu pośredniczy metabolit aldehydu octowego, a zatem mogą być łagodzone przez substancje takie jak fomepizol, które skutecznie zmniejszają stopień konwersji etanolu do aldehydu octowego in vivo .
ALDH2, który ma mniejszą K M do acetaldehydu niż ALDH1 i występuje głównie w macierzy mitochondrialnej jest głównym enzymem metabolizmu aldehydu octowego i trzy genotypy. Pojedyncza mutacja punktowa (G → A) w eksonie 12 genu ALDH2 powoduje zastąpienie glutaminy lizyną w reszcie 487, w wyniku czego powstaje enzym ALDH2K. ALDH2K ma wydłużony K M NAD + , co powoduje, że praktycznie nieaktywny przy stężeniach komórkowych NAD + . Ponieważ ALDH2 jest randomizowanym tetramerem, hetero-zmutowany genotyp jest obniżony do zaledwie 6% aktywności w porównaniu z typem dzikim, podczas gdy homo-zmutowane genotypy mają praktycznie zerową aktywność enzymatyczną. Podjednostka z niedoborem ALDH2 dominuje w hybrydyzacji z podjednostką typu dzikiego, co skutkuje inaktywacją izoenzymu przez zakłócanie aktywności katalitycznej i zwiększenie obrotu. Zmienność genetyczna ALDH2 jest ściśle skorelowana z uzależnieniem od alkoholu , z heterozygotami o zmniejszonym ryzyku w porównaniu z homozygotami typu dzikiego i indywidualnymi homozygotami z niedoborem ALDH2 o bardzo niskim ryzyku alkoholizmu.
Lek disulfiram (Antabuse) zapobiega utlenianiu aldehydu octowego do kwasu octowego i jest stosowany w leczeniu alkoholizmu. ALDH1 jest silnie hamowany przez disulfiram, podczas gdy ALDH2 jest odporny na jego działanie. Reszta cysteiny w 302 w ALDH1 i 200 w ALDH2 jest zaangażowana jako miejsce wiązania disulfiramu w enzymie i służy jako miejsce tiolowe wrażliwe na disfulfiram. Kowalencyjne wiązanie disulfiramu z tiolem blokuje wiązanie jednej z reszt cysteinowych z jodoacetamidem, tym samym inaktywując enzym i znacznie obniżając aktywność katalityczną. Aktywność można odzyskać działając 2-merkaptoetanolem , ale nie glutationem .
Metronidazol (Flagyl), który jest stosowany w leczeniu niektórych infekcji pasożytniczych, a także rzekomobłoniastego zapalenia okrężnicy, ma podobne działanie do disulfiramu. Coprine (który jest aminokwasem występującym w niektórych grzybach koprynoidowych ) metabolizuje in vivo do 1-aminocyklopropanolu, co również powoduje podobne efekty.
Rola w metabolizmie tłuszczów
ALDH1 bierze udział w metabolizmie witaminy A. Modele zwierzęce sugerują, że brak genu jest związany z ochroną przed otyłością trzewną ( PMC 2233696 ).
Zobacz też
Bibliografia
Zewnętrzne linki
- aldehyd octowy + dehydrogenaza w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)