Acetylocholina - Acetylcholine
 | |
| Dane kliniczne | |
|---|---|
| Inne nazwy | ACh |
| Dane fizjologiczne | |
| Tkanki źródłowe | neurony ruchowe , przywspółczulny układ nerwowy , mózg |
| Tkanki docelowe | mięśnie szkieletowe , mózg, wiele innych narządów |
| Receptory | nikotynowy , muskarynowy |
| Agoniści | nikotyna , muskaryna , inhibitory cholinesterazy |
| Antagoniści | tubokuraryna , atropina |
| Prekursor | cholina , acetylo-CoA |
| Biosynteza | acetylotransferaza cholinowa |
| Metabolizm | acetylocholinoesteraza |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Numer E | E1001(i) (dodatkowe chemikalia) |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.000.118 |
| Dane chemiczne i fizyczne | |
| Formuła | C 7 H 16 N O 2 |
| Masa cząsteczkowa | 146,210 g·mol -1 |
Acetylocholina ( ACh ) jest organiczną substancją chemiczną, która działa w mózgu i ciele wielu rodzajów zwierząt (w tym ludzi) jako neuroprzekaźnik — wiadomość chemiczna uwalniana przez komórki nerwowe w celu wysyłania sygnałów do innych komórek, takich jak neurony, komórki mięśniowe i gruczoły komórki. Jego nazwa pochodzi od ich struktury chemicznej: jest ester z kwasem octowym i choliny . Części ciała, które używają lub są dotknięte przez acetylocholinę są określane jako cholinergiczne . Substancje, które zwiększają lub zmniejszają ogólną aktywność układu cholinergicznego, nazywane są odpowiednio cholinergicznymi i antycholinergicznymi .
Acetylocholina jest neuroprzekaźnikiem używanym w złączu nerwowo-mięśniowym — innymi słowy, jest substancją chemiczną uwalnianą przez neurony ruchowe układu nerwowego w celu aktywacji mięśni. Ta właściwość oznacza, że leki wpływające na układy cholinergiczne mogą mieć bardzo niebezpieczne skutki, od paraliżu po drgawki. Acetylocholina jest również neuroprzekaźnikiem w autonomicznym układzie nerwowym , zarówno jako wewnętrzny przekaźnik dla współczulnego układu nerwowego, jak i jako końcowy produkt uwalniany przez przywspółczulny układ nerwowy . Acetylocholina jest głównym neuroprzekaźnikiem przywspółczulnego układu nerwowego.
W mózgu acetylocholina działa jako neuroprzekaźnik i neuromodulator . Mózg zawiera wiele obszarów cholinergicznych, z których każdy ma inne funkcje; takie jak odgrywanie ważnej roli w pobudzeniu, uwadze, pamięci i motywacji.
Acetylocholina została również wykryta w komórkach pochodzenia nienerwowego i drobnoustrojach. Ostatnio enzymy związane z jego syntezą, degradacją i wychwytem komórkowym zostały prześledzone do wczesnych początków jednokomórkowych eukariontów. Patogen protista Acanthamoeba spp. wykazali obecność ACh, który dostarcza sygnały wzrostu i proliferacji poprzez zlokalizowany w błonie homolog receptora muskarynowego M1.
Częściowo ze względu na jego funkcję aktywującą mięśnie, ale także ze względu na jego funkcje w autonomicznym układzie nerwowym i mózgu, wiele ważnych leków wywiera swoje działanie poprzez zmianę transmisji cholinergicznej. Liczne jady i toksyny wytwarzane przez rośliny, zwierzęta i bakterie, a także chemiczne środki nerwowe, takie jak Sarin , powodują szkody poprzez unieczynnienie lub hiperaktywację mięśni poprzez ich wpływ na połączenie nerwowo-mięśniowe. Leki działające na muskarynowe receptory acetylocholiny , takie jak atropina , mogą być trujące w dużych ilościach, ale w mniejszych dawkach są powszechnie stosowane w leczeniu niektórych chorób serca i oczu. Skopolamina , która działa głównie na receptory muskarynowe w mózgu, może powodować majaczenie , halucynacje i amnezję . Uzależniające właściwości nikotyny wynikają z jej wpływu na nikotynowe receptory acetylocholiny w mózgu.
Chemia
Acetylocholina to cząsteczka choliny , która została acetylowana przy atomie tlenu . Ze względu na obecność silnie polarnej, naładowanej grupy amonowej , acetylocholina nie przenika przez błony lipidowe. Z tego powodu cząsteczka wprowadzona zewnętrznie pozostaje w przestrzeni pozakomórkowej i nie przechodzi przez barierę krew-mózg.
Biochemia
Acetylocholina jest syntetyzowana w niektórych neuronach przez enzym acetylotransferazę cholinową ze związków choliny i acetylo-CoA . Neurony cholinergiczne są zdolne do wytwarzania ACh. Przykładem centralnego obszaru cholinergicznego jest jądro podstawne Meynerta w części podstawnej przodomózgowia. Enzym acetylocholinoesteraza przekształca acetylocholinę w nieaktywne metabolity cholinę i octan . Enzym ten występuje obficie w szczelinie synaptycznej, a jego rola w szybkim usuwaniu wolnej acetylocholiny z synapsy jest niezbędna dla prawidłowego funkcjonowania mięśni. Niektóre neurotoksyny działają poprzez hamowanie acetylocholinesterazy, prowadząc w ten sposób do nadmiaru acetylocholiny w połączeniu nerwowo-mięśniowym , powodując paraliż mięśni potrzebnych do oddychania i zatrzymując bicie serca.
Funkcje
Acetylocholina działa zarówno w ośrodkowym układzie nerwowym (OUN), jak i obwodowym układzie nerwowym (PNS). W OUN projekcje cholinergiczne z podstawy przodomózgowia do kory mózgowej i hipokampu wspierają funkcje poznawcze tych obszarów docelowych. W PNS acetylocholina aktywuje mięśnie i jest głównym neuroprzekaźnikiem autonomicznego układu nerwowego.
Efekty komórkowe
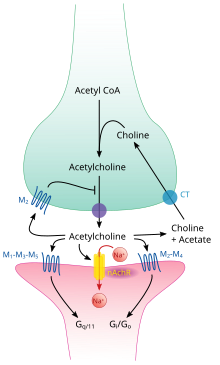
Podobnie jak wiele innych substancji biologicznie czynnych, acetylocholina wywiera swoje działanie poprzez wiązanie i aktywację receptorów znajdujących się na powierzchni komórek. Istnieją dwie główne klasy receptorów acetylocholiny, nikotynowe i muskarynowe . Ich nazwa pochodzi od substancji chemicznych, które mogą selektywnie aktywować każdy typ receptora bez aktywowania drugiego: muskarynę to związek występujący w grzybie Amanita muscaria ; nikotyna znajduje się w tytoniu.
Receptory nikotynowe acetylocholiny są bramkowanymi ligandami kanałami jonowymi przepuszczającymi jony sodu , potasu i wapnia . Innymi słowy, są to kanały jonowe osadzone w błonach komórkowych, zdolne do przełączania się ze stanu zamkniętego do otwartego, gdy zwiąże się z nimi acetylocholina; w stanie otwartym przepuszczają jony. Receptory nikotynowe dzielą się na dwa główne typy, znane jako typ mięśniowy i typ neuronalny. Typ mięśniowy może być selektywnie blokowany przez kurarę , a neuronalny przez heksametonium . Główna lokalizacja receptorów typu mięśniowego znajduje się na komórkach mięśniowych, jak opisano bardziej szczegółowo poniżej. Receptory typu neuronalnego zlokalizowane są w zwojach autonomicznych (zarówno współczulnych, jak i przywspółczulnych) oraz w ośrodkowym układzie nerwowym.
Receptory muskarynowe acetylocholiny mają bardziej złożony mechanizm i wpływają na komórki docelowe przez dłuższy czas. U ssaków zidentyfikowano pięć podtypów receptorów muskarynowych, oznaczonych od M1 do M5. Wszystkie z nich działają jako receptory sprzężone z białkiem G , co oznacza , że wywierają swoje działanie poprzez system drugiego przekaźnika . Podtypy M1, M3 i M5 są G Q -coupled; zwiększają wewnątrzkomórkowe poziomy IP 3 i wapnia poprzez aktywację fosfolipazy C . Ich wpływ na komórki docelowe jest zwykle pobudzający. Podtypy M2 i M4 są sprzężone z G i /G o ; obniżają wewnątrzkomórkowe poziomy cAMP poprzez hamowanie cyklazy adenylanowej . Ich wpływ na komórki docelowe jest zwykle hamujący. Receptory muskarynowe acetylocholiny znajdują się zarówno w ośrodkowym układzie nerwowym, jak i obwodowym układzie nerwowym serca, płuc, górnego odcinka przewodu pokarmowego i gruczołów potowych.
Połączenie nerwowo-mięśniowe
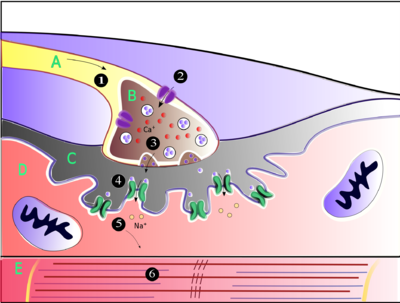
Acetylocholina jest substancją wykorzystywaną przez układ nerwowy do aktywacji mięśni szkieletowych , rodzaju mięśni poprzecznie prążkowanych. Są to mięśnie wykorzystywane do wszystkich rodzajów ruchów dowolnych, w przeciwieństwie do tkanki mięśni gładkich , która bierze udział w szeregu mimowolnych czynności, takich jak przemieszczanie pokarmu przez przewód pokarmowy i zwężanie naczyń krwionośnych. Mięśnie szkieletowe są bezpośrednio kontrolowane przez neurony ruchowe zlokalizowane w rdzeniu kręgowym lub, w kilku przypadkach, pniu mózgu . Te neurony ruchowe wysyłają swoje aksony przez nerwy ruchowe , z których wyłaniają się, aby połączyć się z włóknami mięśniowymi w specjalnym typie synapsy zwanym złączem nerwowo-mięśniowym .
Kiedy neuron ruchowy generuje potencjał czynnościowy , przemieszcza się szybko wzdłuż nerwu, aż dotrze do połączenia nerwowo-mięśniowego, gdzie inicjuje proces elektrochemiczny, który powoduje uwolnienie acetylocholiny do przestrzeni między końcówką presynaptyczną a włóknem mięśniowym. Cząsteczki acetylocholiny wiążą się następnie z receptorami nikotynowych kanałów jonowych na błonie komórek mięśniowych, powodując otwarcie kanałów jonowych. Jony sodu przepływają następnie do komórki mięśniowej, inicjując sekwencję kroków, które ostatecznie powodują skurcz mięśni .
Czynniki, które zmniejszają uwalnianie acetylocholiny (a tym samym wpływają na kanały wapniowe typu P ):
- Antybiotyki ( klindamycyna , polimyksyna )
- Magnez: antagonizuje kanały wapniowe typu P
- Hipokalcemia
- Leki przeciwdrgawkowe
- Diuretyki ( furosemid )
- Zespół Eatona-Lamberta : hamuje kanały wapniowe typu P
- Miastenia gravis
- Toksyna botulinowa : hamuje białka SNARE
Blokery kanału wapniowego (nifedypina, diltiazem) nie wpływają na kanały P. Leki te mają wpływ na kanały wapniowe typu L .
Autonomiczny układ nerwowy
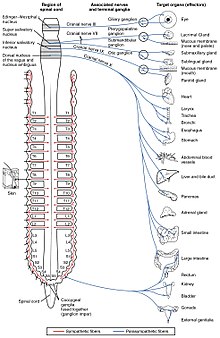
Autonomicznego układu nerwowego reguluje szeroki zakres mimowolnych i nieświadome funkcji ciała. Jego główne gałęzie to współczulny układ nerwowy i przywspółczulny układ nerwowy . Mówiąc ogólnie, funkcją współczulnego układu nerwowego jest mobilizowanie ciała do działania; wyrażeniem często przywoływanym w celu opisania tego jest walka lub ucieczka . Funkcją przywspółczulnego układu nerwowego jest wprowadzenie organizmu w stan sprzyjający odpoczynkowi, regeneracji, trawieniu i reprodukcji; fraza często przywoływana, aby ją opisać, to „odpoczynek i trawienie” lub „karm i rozmnażaj”. Oba te systemy wykorzystują acetylocholinę, ale na różne sposoby.
Na schematycznym poziomie układ nerwowy współczulny i przywspółczulny są zorganizowane zasadniczo w ten sam sposób: neurony przedzwojowe w ośrodkowym układzie nerwowym wysyłają projekcje do neuronów zlokalizowanych w zwojach autonomicznych, które wysyłają projekcje wyjściowe do praktycznie każdej tkanki ciała. W obu gałęziach połączenia wewnętrzne, wypustki z ośrodkowego układu nerwowego do zwojów autonomicznych, wykorzystują acetylocholinę jako neuroprzekaźnik do unerwienia (lub pobudzenia) neuronów zwojów. W przywspółczulnym układzie nerwowym połączenia wyjściowe, wypustki z neuronów zwojowych do tkanek nienależących do układu nerwowego, również uwalniają acetylocholinę, ale działają na receptory muskarynowe. We współczulnym układzie nerwowym połączenia wyjściowe uwalniają głównie noradrenalinę , chociaż acetylocholina jest uwalniana w kilku punktach, takich jak unerwienie sudoruchowe gruczołów potowych.
Bezpośrednie efekty naczyniowe
Acetylocholina zawarta w surowicy wywiera bezpośredni wpływ na napięcie naczyniowe poprzez wiązanie się z receptorami muskarynowymi obecnymi na śródbłonku naczyniowym . Komórki te reagują poprzez zwiększenie produkcji tlenku azotu , który sygnalizuje rozluźnienie otaczającego mięśnia gładkiego, co prowadzi do rozszerzenia naczyń krwionośnych .
Ośrodkowy układ nerwowy
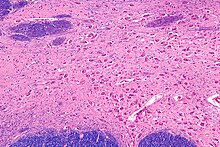
W ośrodkowym układzie nerwowym ACh ma różnorodny wpływ na plastyczność, pobudzenie i nagrodę . ACh odgrywa ważną rolę w zwiększaniu czujności po przebudzeniu, w podtrzymywaniu uwagi oraz w uczeniu się i zapamiętywaniu.
Wykazano, że uszkodzenie układu cholinergicznego (wytwarzającego acetylocholinę) w mózgu jest związane z deficytami pamięci związanymi z chorobą Alzheimera . Wykazano również, że ACh promuje sen REM .
W pochodzący pnia acetylocholiny z jądra Pedunculopontine i nakrywki laterodorsal jądro znanych jako mezo Poncjańskich nakrywki obszarze lub pontomesencephalotegmental złożone. W podstawnym przodomózgowiu pochodzi z jądra podstawnego Meynerta i jądra przyśrodkowego przegrody :
- W pontomesencephalotegmental złożone działa głównie na receptorów M1 w pniu mózgu , głębokich móżdżku jąder , jądra mostu , locus coeruleus , szew jądra , bocznej siatkowego jądra i dolnej oliwek . Projektuje również do wzgórza wzgórza , osłony , jąder podstawy i przodomózgowia podstawy .
- Jądro podstawne Meynerta działa głównie na receptory M1 w korze nowej .
- Jądro przegrody przyśrodkowej działa głównie na receptory M1 w hipokampie i częściach kory mózgowej .
Ponadto ACh pełni funkcję ważnego wewnętrznego przekaźnika w prążkowiu , który jest częścią jąder podstawnych . Jest uwalniany przez interneurony cholinergiczne . U ludzi, naczelnych i gryzoni, te interneurony reagują na istotne bodźce środowiskowe reakcjami, które są czasowo wyrównane z odpowiedziami neuronów dopaminergicznych istoty czarnej .
Pamięć
Acetylocholina jest zaangażowana w uczenie się i pamięć na kilka sposobów. Lek antycholinergiczny, skopolamina , utrudnia zdobywanie nowych informacji u ludzi i zwierząt. U zwierząt zakłócenie dostarczania acetylocholiny do kory nowej upośledza uczenie się prostych zadań rozróżniających, porównywalnych do zdobywania informacji faktycznych, a zakłócenie dostarczania acetylocholiny do hipokampa i przyległych obszarów korowych powoduje zapominanie, porównywalne z amnezją następczą u ludzi .
Choroby i zaburzenia
Miastenia gravis
Choroba myasthenia gravis , charakteryzująca się osłabieniem i zmęczeniem mięśni, występuje, gdy organizm niewłaściwie wytwarza przeciwciała przeciwko receptorom nikotynowym acetylocholiny, a tym samym hamuje prawidłowe przekazywanie sygnału acetylocholiny. Z biegiem czasu płyta końcowa silnika ulega zniszczeniu. Leki, które kompetycyjnie hamują acetylocholinoesterazę (np. neostygmina, fizostygmina lub przede wszystkim pirydostygmina) są skuteczne w leczeniu objawów tego zaburzenia. Pozwalają one endogennie uwolnionej acetylocholinie na więcej czasu na interakcję z odpowiednim receptorem, zanim zostaną dezaktywowane przez acetylocholinoesterazę w szczelinie synaptycznej (przestrzeni między nerwem a mięśniem).
Farmakologia
Blokowanie, utrudnianie lub naśladowanie działania acetylocholiny ma wiele zastosowań w medycynie. Leki działające na układ acetylocholiny są albo agonistami receptorów, stymulującymi układ, albo antagonistami, hamującymi go. Agoniści i antagoniści receptora acetylocholiny mogą wywierać wpływ bezpośrednio na receptory lub wywierać swoje działanie pośrednio, np. przez oddziaływanie na enzym acetylocholinoesterazę , który degraduje ligand receptora. Agoniści zwiększają poziom aktywacji receptora, antagoniści go obniżają.
Sama acetylocholina nie ma wartości terapeutycznej jako lek do podawania dożylnego ze względu na jej wieloaspektowe (nieselektywne) działanie i szybką dezaktywację przez cholinoesterazę. Stosowany jest jednak w postaci kropli do oczu w celu obkurczenia źrenicy podczas operacji zaćmy, co ułatwia szybki powrót do zdrowia pooperacyjnego.
Receptory nikotynowe
Nikotyna wiąże się i aktywuje nikotynowe receptory acetylocholiny , naśladując działanie acetylocholiny na te receptory. Gdy współdziała ACh z nikotynowego receptora ACh otwiera Na + kanał i Na + jony do przepływu przez membranę. Powoduje to depolaryzację i powoduje pobudzający potencjał postsynaptyczny. Tak więc ACh pobudza mięśnie szkieletowe; odpowiedź elektryczna jest szybka i krótkotrwała. Kurary to trucizny strzał, które działają na receptory nikotynowe i zostały wykorzystane do opracowania klinicznie użytecznych terapii.
Receptory muskarynowe
Atropina jest nieselektywnym konkurencyjnym antagonistą z acetylocholiną na receptorach muskarynowych.
Inhibitory cholinesterazy
Wielu agonistów receptora ACh działa pośrednio poprzez hamowanie enzymu acetylocholinoesterazy . Wynikająca z tego akumulacja acetylocholiny powoduje ciągłą stymulację mięśni, gruczołów i ośrodkowego układu nerwowego, co może skutkować śmiertelnymi konwulsjami, jeśli dawka jest wysoka.
Są przykładami inhibitorów enzymów i nasilają działanie acetylocholiny poprzez opóźnianie jej degradacji; niektóre były używane jako środki nerwowe ( gaz nerwowy Sarin i VX ) lub pestycydy ( organofosforany i karbaminiany ). Wiele toksyn i jadów wytwarzanych przez rośliny i zwierzęta zawiera również inhibitory cholinesterazy. W praktyce klinicznej podaje się je w małych dawkach w celu odwrócenia działania środków zwiotczających mięśnie , leczenia miastenii oraz objawów choroby Alzheimera ( rywastygmina , która zwiększa aktywność cholinergiczną mózgu).
Inhibitory syntezy
Organiczne związki rtęci , takie jak metylortęć , wykazują wysokie powinowactwo do grup sulfhydrylowych , co powoduje dysfunkcję enzymu acetylotransferazy cholinowej. To hamowanie może prowadzić do niedoboru acetylocholiny i może mieć wpływ na funkcje motoryczne.
Inhibitory uwalniania
Toksyna botulinowa (Botox) działa poprzez hamowanie uwalniania acetylocholiny, podczas gdy jad pająka czarnej wdowy ( alfa-latrotoksyna ) ma działanie odwrotne. Zahamowanie ACh powoduje paraliż . Po ugryzieniu przez pająka czarnej wdowy doświadcza się marnowania zapasów ACh i mięśnie zaczynają się kurczyć. Jeśli i kiedy zapasy się wyczerpią, następuje paraliż .
Biologia porównawcza i ewolucja
Acetylocholina jest wykorzystywana przez organizmy we wszystkich dziedzinach życia do różnych celów. Uważa się, że cholina, prekursor acetylocholiny, była używana przez organizmy jednokomórkowe miliardy lat temu do syntezy fosfolipidów błony komórkowej. W następstwie ewolucji transporterów choliny obfitość wewnątrzkomórkowej choliny utorowała drogę do włączenia choliny do innych szlaków syntetycznych, w tym produkcji acetylocholiny. Acetylocholina jest wykorzystywana przez bakterie, grzyby i wiele innych zwierząt. Wiele zastosowań acetylocholiny opiera się na jej działaniu na kanały jonowe za pośrednictwem GPCR, takich jak białka błonowe.
Dwa główne typy receptorów acetylocholiny, receptory muskarynowe i nikotynowe, zbieżnie wyewoluowały, aby odpowiadać na acetylocholinę. Oznacza to, że zamiast wyewoluować ze wspólnego homologa, receptory te wyewoluowały z oddzielnych rodzin receptorów. Szacuje się, że rodzina receptorów nikotynowych liczy sobie ponad 2,5 miliarda lat. Podobnie uważa się, że receptory muskarynowe oddzieliły się od innych GPCR co najmniej 0,5 miliarda lat temu. Obie te grupy receptorów wyewoluowały liczne podtypy o unikalnym powinowactwie do ligandów i mechanizmach sygnalizacji. Różnorodność typów receptorów umożliwia acetylocholinie tworzenie różnych odpowiedzi w zależności od aktywowanych typów receptorów i pozwala na dynamiczną regulację procesów fizjologicznych przez acetylocholinę.
Historia
W 1867 Adolf von Baeyer rozwiązał struktury choliny i acetylocholiny i zsyntetyzował je, nazywając w badaniu „ acetyloneuryną ”. Cholina jest prekursorem acetylocholiny. To dlatego Frederick Walker Mott i William Dobinson Halliburton zauważyli w 1899 roku, że zastrzyki z choliny obniżają ciśnienie krwi zwierząt. Acetylocholina została po raz pierwszy zauważona jako biologicznie aktywna w 1906 roku, kiedy Reid Hunt (1870-1948) i René de M. Taveau odkryli, że obniża ona ciśnienie krwi w wyjątkowo małych dawkach.
W 1914 Arthur J. Ewins jako pierwszy wydobył acetylocholinę z natury. Zidentyfikował to jako zanieczyszczenie obniżające ciśnienie krwi pochodzące z niektórych ekstraktów sporyszu Claviceps purpurea , na prośbę Henry'ego Halletta Dale'a . Później, w 1914 roku, Dale przedstawił wpływ acetylocholiny na różne typy synaps obwodowych, a także zauważył, że obniża ona ciśnienie krwi kotów poprzez wstrzyknięcia podskórne nawet w dawkach rzędu jednego nanograma .
Pojęcie neuroprzekaźników było nieznane przed 1921 rokiem, kiedy Otto Loewi zauważył, że nerw błędny wydziela substancję, która hamuje mięsień sercowy podczas pracy jako profesor na Uniwersytecie w Grazu . Nazwał go vagusstoff („substancja błędna ”), zauważył, że jest strukturalnym analogiem choliny i podejrzewał, że jest to acetylocholina. W 1926 Loewi i E. Navratil wywnioskowali, że związek ten jest prawdopodobnie acetylocholiną, ponieważ vagusstoff i syntetyczna acetylocholina traciły swoją aktywność w podobny sposób w kontakcie z lizatami tkankowymi zawierającymi enzymy rozkładające acetylocholinę (obecnie znane jako cholinoesterazy ). Ten wniosek został powszechnie przyjęty. Późniejsze badania potwierdziły funkcję acetylocholiny jako neuroprzekaźnika.
W 1936 roku HH Dale i O. Loewi otrzymali Nagrodę Nobla w dziedzinie fizjologii lub medycyny za badania nad acetylocholiną i impulsami nerwowymi.
Zobacz też
- Ann Srebro
- Acetylocholinesteraza
- Połączenie nerwowo-mięśniowe
- Receptor nikotynowy acetylocholiny
- Receptor muskarynowy acetylocholiny
Konkretne referencje
Bibliografia ogólna
- Brenner GM, Stevens CW (2006). Farmakologia (wyd. 2). Filadelfia PA: WB Saunders. Numer ISBN 1-4160-2984-2.
- Kanadyjskie Stowarzyszenie Farmaceutów (2000). Kompendium Farmacji i Specjalności (wyd. 25). Toronto ON: Webcom. Numer ISBN 0-919115-76-4.
- Carlson NR (2001). Fizjologia zachowania (wyd. 7). Needham Heights MA: Allyn i Bacon. Numer ISBN 0-205-30840-6.
- Gershon MD (1998). Drugi mózg . Nowy Jork NY: Harper Collins. Numer ISBN 0-06-018252-0.
- Siegal A, Sapru HN (2006). „Rozdz. 15” . Essential Neuroscience (Poprawione 1st ed.). Filadelfia: Lippincott, Williams & Wilkins. s. 255–267 .
- Hasselmo ME (luty 1995). „Neuromodulacja i funkcja korowa: modelowanie fizjologicznych podstaw zachowania”. Zachowuj się. Mózg Res . 67 (1): 1-27. doi : 10.1016/0166-4328(94)00113-T . PMID 7748496 . S2CID 17594590 . jako PDF
- Yu AJ, Dayan P (maj 2005). „Niepewność, neuromodulacja i uwaga”. Neuron . 46 (4): 681-92. doi : 10.1016/j.neuron.2005.04.026 . PMID 15944135 . S2CID 15980355 . jako PDF

