Antyandrogen - Antiandrogen
| Antyandrogen | |
|---|---|
| Klasa leków | |
Bikalutamid , niesteroidowy antyandrogen i najszerzej stosowany antagonista receptora androgenowego w leczeniu raka prostaty .
| |
| Identyfikatory klas | |
| Synonimy | Antagoniści androgenów; Blokery androgenów; Blokery testosteronu |
| Posługiwać się | • Mężczyźni i chłopcy: rak prostaty ; łagodny przerost gruczołu krokowego ; Wypadanie włosów na skórze głowy ; parafilie ; hiperseksualność ; przestępcy seksualni ; przedwczesne dojrzewanie ; Priapizm • Kobiety i dziewczęta: Trądzik ; łojotok ; Ropne zapalenie apokrynowych gruczołów potowych ; hirsutyzm ; Wypadanie włosów na skórze głowy ; hiperandrogenizm ; Terapia hormonalna transpłciowa |
| Kod ATC | L02BB |
| Cel biologiczny |
receptor androgenowy ; receptor progesteronu ; receptor estrogenowy ; receptor GnRH ; 5a-reduktaza ; CYP17A1 (17α-hydroksylaza/ |
| Klasa chemiczna | Sterydowy ; niesteroidowy ; Peptyd |
| Zewnętrzne linki | |
| Siatka | D000726 |
| W Wikidanych | |
Antyandrogeny , znane również jako antagoniści androgenów lub blokery testosteronu , to klasa leków, które zapobiegają pośredniczeniu androgenów, takich jak testosteron i dihydrotestosteron (DHT), w ich biologicznych skutkach w organizmie. Ich działanie polega na blokowaniu się receptora androgenowego (AR) i / lub hamowania lub tłumienia androgenów produkcji . Można je traktować jako funkcjonalne przeciwieństwa agonistów AR , na przykład androgenów i sterydów anabolicznych (SAA), takich jak testosteron, DHT i nandrolon oraz selektywnych modulatorów receptora androgenowego (SARM), takich jak enobosarm . Antyandrogeny są jednym z trzech typów antagonistów hormonów płciowych , obok antyestrogenów i antyprogestagenów .
Antyandrogeny są stosowane w leczeniu szeregu schorzeń zależnych od androgenów . U mężczyzn antyandrogeny są stosowane w leczeniu raka prostaty , przerostu prostaty , wypadania włosów na skórze głowy , nadmiernego popędu płciowego , nietypowych i problematycznych popędów seksualnych oraz wczesnego dojrzewania płciowego . U kobiet antyandrogeny stosuje się w leczeniu trądziku , łojotoku , nadmiernego wzrostu włosów , wypadania włosów na skórze głowy i wysokiego poziomu androgenów , takich jak te, które występują w zespole policystycznych jajników (PCOS). Antyandrogeny są również stosowane jako składnik feminizacji terapii hormonalnej dla transpłciowych kobiet i jak blokery dojrzewania w transpłciowych dziewcząt .
Skutki uboczne antyandrogenów zależą od rodzaju antyandrogenu i konkretnego antyandrogenu, o którym mowa. W każdym razie, częste działania niepożądane antyandrogenów u mężczyzn należą tkliwość piersi , powiększenie piersi , feminizacji , uderzenia gorąca , zaburzenia seksualne , niepłodność oraz osteoporozę . U kobiet antyandrogeny są znacznie lepiej tolerowane , a antyandrogeny działające tylko poprzez bezpośrednie blokowanie androgenów wiążą się z minimalnymi skutkami ubocznymi. Ponieważ jednak estrogeny są wytwarzane z androgenów w organizmie, antyandrogeny, które hamują produkcję androgenów, mogą powodować niski poziom estrogenów i związane z tym objawy, takie jak uderzenia gorąca, nieregularne miesiączki i osteoporoza u kobiet przed menopauzą .
Istnieje kilka różnych głównych typów antyandrogenów. Należą do nich antagoniści AR , inhibitory syntezy androgenów i antygonadotropiny . Antagoniści AR działają poprzez bezpośrednie blokowanie działania androgenów, podczas gdy inhibitory syntezy androgenów i antygonadotropiny działają poprzez obniżanie poziomu androgenów. Antagonistów AR można dalej podzielić na antyandrogeny steroidowe i antyandrogeny niesteroidowe ; inhibitory syntezy androgenów można dalej podzielić głównie na inhibitory CYP17A1 i inhibitory 5α-reduktazy ; a antygonadotropiny można dalej podzielić na modulatory hormonu uwalniającego gonadotropiny (modulatory GnRH), progestageny i estrogeny .
Zastosowania medyczne
Antyandrogeny są stosowane w leczeniu szeregu schorzeń zależnych od androgenów zarówno u mężczyzn, jak iu kobiet. Stosuje się je w leczeniu mężczyzn z rakiem prostaty , łagodnym przerostem gruczołu krokowego , wypadaniem włosów , hiperseksualnością , parafiliami i priapizmem , a także u chłopców z przedwczesnym dojrzewaniem . U kobiet i dziewcząt antyandrogeny stosuje się w leczeniu trądziku , łojotoku , ropnego zapalenia apokrynowych gruczołów potowych , hirsutyzmu i hiperandrogenizmu . Antyandrogeny są również stosowane w transpłciowych kobiet jako składnik feminizacji terapię hormonalną i jak blokery dojrzewania w transpłciowych dziewcząt .
Mężczyźni i chłopcy
Rak prostaty
Androgeny, takie jak testosteron, a zwłaszcza DHT, są bardzo zaangażowane w rozwój i progresję raka prostaty. Pełnią one rolę czynników wzrostu w gruczole krokowym , stymulowanie podziału komórek i wzrostu tkanki . W związku z tym metody terapeutyczne zmniejszające sygnalizację androgenową w gruczole krokowym, określane zbiorczo jako terapia deprywacji androgenowej , są w stanie znacząco spowolnić przebieg raka prostaty i wydłużyć życie mężczyzn z tą chorobą. Chociaż antyandrogeny są skuteczne w spowalnianiu progresji raka prostaty, na ogół nie są skuteczne, a z czasem choroba adaptuje się i terapia deprywacji androgenów w końcu staje się nieskuteczna. W takim przypadku można rozważyć inne metody leczenia, takie jak chemioterapia .
Najczęstszymi metodami terapii deprywacji androgenów obecnie stosowanymi w leczeniu raka prostaty są kastracja (z modulatorem GnRH lub orchiektomia ), niesteroidowe antyandrogeny oraz inhibitor syntezy androgenów octan abirateronu . Kastrację można stosować samodzielnie lub w połączeniu z jednym z dwóch pozostałych zabiegów. Kiedy kastracja jest połączona z niesteroidowym antyandrogenem, takim jak bikalutamid , ta strategia jest określana jako połączona blokada androgenów (znana również jako całkowita lub maksymalna blokada androgenów). Enzalutamid , apalutamid i octan abirateronu są specjalnie zatwierdzone do stosowania w połączeniu z kastracją w leczeniu opornego na kastrację raka prostaty. Monoterapię niesteroidowym antyandrogenem bikalutamidem stosuje się również w leczeniu raka prostaty jako alternatywę dla kastracji o porównywalnej skuteczności, ale o innym i potencjalnie korzystnym profilu działań niepożądanych.
Estrogen w wysokich dawkach był pierwszym funkcjonalnym antyandrogenem stosowanym w leczeniu raka prostaty. Był szeroko stosowany, ale w dużej mierze został porzucony w tym wskazaniu na rzecz nowszych środków o ulepszonych profilach bezpieczeństwa i mniejszej liczbie feminizujących skutków ubocznych. Octan cyproteronu został opracowany w następstwie wysokich dawek estrogenu i jest jedynym steroidowym antyandrogenem szeroko stosowanym w leczeniu raka prostaty, ale w dużej mierze został zastąpiony przez niesteroidowe antyandrogeny, które są nowsze i mają większą skuteczność, tolerancję i bezpieczeństwo . Bikalutamid, podobnie jak enzalutamid, w dużej mierze zastąpiły wcześniejsze niesteroidowe antyandrogeny, flutamid i nilutamid , które obecnie są rzadko stosowane. Wcześniejsze inhibitory syntezy androgenów, aminoglutetymid i ketokonazol, były jedynie w ograniczonym stopniu stosowane w leczeniu raka prostaty ze względu na obawy związane z toksycznością i zostały zastąpione octanem abirateronu.
Oprócz aktywnego leczenia raka prostaty, antyandrogeny są skuteczne jako profilaktyka (zapobieganie) w zmniejszaniu ryzyka rozwoju raka prostaty. W tym celu oceniano tylko w ograniczonym stopniu antyandrogeny, ale inhibitory 5α-reduktazy finasteryd i dutasteryd oraz antagonista steroidów AR, spironolakton , powiązano ze znacznie zmniejszonym ryzykiem raka prostaty. Ponadto warto zauważyć, że rak prostaty występuje niezwykle rzadko u kobiet transpłciowych, które przez dłuższy czas stosowały feminizującą terapię hormonalną.
Powiększona prostata
Inhibitory 5α-reduktazy finasteryd i dutasteryd są stosowane w leczeniu łagodnego przerostu gruczołu krokowego, stanu, w którym gruczoł krokowy powiększa się, co powoduje niedrożność dróg moczowych i dyskomfort. Są skuteczne, ponieważ androgeny działają jako czynniki wzrostu w gruczole krokowym. Antyandrogeny octan chlormadinonu i oxendolone i antyandrogeny funkcjonalne allylestrenol i gestonorone kapronian są zatwierdzone w niektórych krajach w leczeniu łagodnego przerostu gruczołu krokowego.
Wypadanie włosów na skórze głowy
Inhibitory 5α-reduktazy, takie jak finasteryd, dutasteryd i alfatradiol, oraz miejscowy niesteroidowy antagonista receptorów AR, topilutamid (flurydyl), są zatwierdzone do leczenia łysienia typu modelowego, znanego również jako łysienie skóry głowy lub łysienie. Ten stan jest zwykle spowodowany przez androgeny, więc antyandrogeny mogą spowolnić lub zatrzymać jego postęp. Systemowe antyandrogeny oprócz inhibitorów 5α-reduktazy na ogół nie są stosowane w leczeniu wypadania włosów u mężczyzn ze względu na zagrożenia takie jak feminizacja (np. ginekomastia) i dysfunkcje seksualne. Zostały one jednak ocenione i zgłoszone jako skuteczne w tym wskazaniu.
Trądzik
Antyandrogeny na ogół nie są stosowane w leczeniu trądziku u mężczyzn ze względu na wysokie ryzyko feminizacji (np. ginekomastii) i dysfunkcji seksualnych. Zostały jednak zbadane pod kątem trądziku u mężczyzn i okazały się skuteczne. Klaskoteron , miejscowy antyandrogen, jest skuteczny w leczeniu trądziku u mężczyzn i może zostać zatwierdzony w tym wskazaniu w przyszłości.
Dewiacja seksualna
Androgeny zwiększają popęd płciowy iz tego powodu antyandrogeny są w stanie zmniejszyć popęd płciowy u mężczyzn. W związku z tym antyandrogeny są stosowane w leczeniu stanów dewiacji seksualnych, takich jak hiperseksualność (nadmiernie wysoki popęd seksualny) i parafilie (nietypowe, a czasem społecznie nieakceptowane zainteresowania seksualne), jak pedofilia (pociąg seksualny do dzieci). Były używane do zmniejszania popędu seksualnego u przestępców seksualnych , aby zmniejszyć prawdopodobieństwo recydywy (powtarzania się przestępstw). Antyandrogeny stosowane w tych wskazaniach obejmują octan cyproteronu , octan medroksyprogesteronu i modulatory GnRH.
Wczesne dojrzewanie
Antyandrogeny są stosowane w leczeniu przedwczesnego dojrzewania u chłopców. Działają przeciwstawiając się działaniu androgenów i opóźniając rozwój drugorzędowych cech płciowych oraz początek zmian popędu płciowego i funkcji do bardziej odpowiedniego wieku. Antyandrogeny stosowane w tym celu obejmują octan cyproteronu , octan medroksyprogesteronu , modulatory GnRH, spironolakton , bikalutamid i ketokonazol . Spironolakton i bikalutamid wymagają połączenia z inhibitorem aromatazy, aby zapobiec skutkom działania estrogenów , które nie są zwalczane , podczas gdy pozostałe można stosować samodzielnie.
Długotrwałe erekcje
Antyandrogeny są skuteczne w leczeniu nawracającego priapizmu (potencjalnie bolesne erekcje prącia trwające dłużej niż cztery godziny).
Kobiety i dziewczęta
Stan skóry i włosów
Antyandrogeny są stosowane w leczeniu chorób skóry i włosów zależnych od androgenów, w tym trądziku, łojotoku, ropnego zapalenia apokrynowych gruczołów potowych, hirsutyzmu i typowego wypadania włosów u kobiet. Wszystkie te schorzenia są zależne od androgenów, dlatego antyandrogeny są skuteczne w ich leczeniu. Najczęściej stosowanymi antyandrogenami w tych wskazaniach są octan cyproteronu i spironolakton . Flutamid był również szeroko badany pod kątem takich zastosowań, ale wypadł z łask ze względu na jego związek z hepatotoksycznością . Bikalutamid , który ma stosunkowo minimalne ryzyko hepatotoksyczności, został przebadany w leczeniu hirsutyzmu i okazał się skuteczny podobnie jak flutamid i może być stosowany zamiast niego. Oprócz antagonistów AR, doustne środki antykoncepcyjne zawierające etynyloestradiol są skuteczne w leczeniu tych stanów i mogą być łączone z antagonistami AR.
Wysoki poziom androgenów
Hiperandrogenizm to stan u kobiet, w którym poziom androgenów jest nadmiernie i nienormalnie wysoki. Jest powszechnie obserwowany u kobiet z PCOS, a także występuje u kobiet z chorobami interpłciowymi, takimi jak wrodzony przerost nadnerczy . Hiperandrogenizm jest związany z wirylizacją – to znaczy rozwojem męskich drugorzędowych cech płciowych, takich jak m.in. męski owłosienie twarzy i ciała (lub hirsutyzm), pogłębienie głosu , zwiększenie masy i siły mięśni oraz poszerzenie ramion . Zależne od androgenów choroby skóry i włosów, takie jak trądzik i wypadanie włosów, mogą również wystąpić w hiperandrogenizmie, a zaburzenia miesiączkowania , takie jak brak miesiączki , są często obserwowane. Chociaż antyandrogeny nie leczą podstawowej przyczyny hiperandrogenizmu (np. PCOS), są w stanie zapobiegać i odwracać jego przejawy i skutki. Podobnie jak w przypadku chorób skóry i włosów zależnych od androgenów, najczęściej stosowanymi antyandrogenami w leczeniu hiperandrogenizmu u kobiet są octan cyproteronu i spironolakton. Alternatywnie można stosować inne antyandrogeny, takie jak bikalutamid.
Terapia hormonalna transpłciowa
Antyandrogeny są stosowane w celu zapobiegania lub wsteczny maskulinizacji i ułatwienia feminizacji w transpłciowych kobiet , którzy są w trakcie terapii hormonalnej i które nie zostały poddane operacji sex przeniesieniu lub zabieg usunięcia jąder . Oprócz estrogenów głównymi antyandrogenami stosowanymi w tym celu są octan cyproteronu, spironolakton i modulatory GnRH. W tym wskazaniu stosuje się również niesteroidowe antyandrogeny, takie jak bikalutamid. Oprócz stosowania u transpłciowych kobiet, antyandrogeny, głównie modulatory GnRH, są stosowane jako blokery dojrzewania, aby zapobiec dojrzewaniu u transpłciowych dziewcząt, dopóki nie będą starsze i gotowe do rozpoczęcia terapii hormonalnej.
Dostępne formy
Istnieje kilka różnych rodzajów antyandrogenów, w tym:
- Antagoniści receptora androgenowego: leki, które wiążą się bezpośrednio i blokują AR. Leki te obejmują niesteroidowe antyandrogeny, octan cyproteronu , octan megestrolu , octan chlormadinonu , spironolakton , oxendolone i ozateron (weterynaryjny) oraz niesteroidowe antyandrogeny flutamid , bikalutamid , nilutamid , topilutamide , enzalutamid i apalutamide . Oprócz octanu cyproteronu i octanu chlormadinonu, kilka innych progestyn stosowanych w doustnych środkach antykoncepcyjnych i/lub w HTZ w okresie menopauzy, w tym dienogest , drospirenon , medrogeston , octan nomegestrolu , promegeston i trimegeston, również wykazuje różne stopnie działania antagonistycznego wobec AR.
- Inhibitory syntezy androgenów: leki, które bezpośrednio hamują enzymatyczną biosyntezę androgenów, takich jak testosteron i/lub DHT. Przykłady obejmują inhibitory CYP17A1 ketokonazol , octan abirateronu i sewiteronel , inhibitor CYP11A1 (P450scc) aminoglutetymid oraz inhibitory 5α-reduktazy finasteryd , dutasteryd , epristeryd , alfatradiol i ekstrakt z palmy sabałowej ( Serenoa ). Szereg innych antyandrogenów, w tym octan cyproteronu, spironolakton, medrogeston, flutamid, nilutamid i bifluranol , również słabo hamują syntezę androgenów.
- Antigonadotropins: Leki, które hamują hormonu uwalniającego gonadotropinę (GnRH), indukowanej uwalniania gonadotropiny i następczej aktywacji gonad produkcji androgenów. Przykłady obejmują modulatory GnRH jak leuproreliny (A agonisty GnRH ) i cetroreliksu (A antagonisty GnRH ), progestageny , takie jak allylestrenol , octan chlormadinonu, octan cyproteronu, gestonorone kapronian , kapronian hydroksyprogesteronu , octan medroksyprogesteronu , megestrol, octan azoteronu etylu (weterynaryjny) i oxendolone, oraz estrogeny, takie jak estradiol , estry estradiolu , etynyloestradiol , sprzężone estrogeny i dietylostilbestrol .
- Różne: Leki, które przeciwstawiają się działaniu androgenów za pomocą środków innych niż powyższe. Przykłady obejmują estrogen, zwłaszcza doustnie i syntetycznych (na przykład, etynyloestradiol , dietylostilbestrol ), które stymulują SHBG (SHBG) wytwarzanie w wątrobie , a tym samym zmniejszyć wolne, a więc bioaktywne poziomy testosteronu i DHT; antykortykotropiny, takie jak glukokortykoidy , które hamują wytwarzanie androgenów nadnerczowych indukowane przez hormon adrenokortykotropowy (ACTH) ; oraz immunogeny i szczepionki przeciwko androstendionowi, takie jak albumina ovandrotonu i albumina androstendionu , które obniżają poziom androgenów poprzez wytwarzanie przeciwciał przeciwko androstendionowi i prekursorowi androgenu (stosowane tylko w weterynarii ).
Niektóre antyandrogeny łączą wiele z powyższych mechanizmów. Przykładem jest steroidowy antyandrogenowy octan cyproteronu, który jest silnym antagonistą AR, silnym progestagenem i stąd antygonadotropiną, słabym glukokortykoidem i stąd antykortykotropiną oraz słabym inhibitorem syntezy androgenów.
Skutki uboczne
Skutki uboczne antyandrogenów różnią się w zależności od rodzaju antyandrogenu – a mianowicie, czy jest to selektywny antagonista AR, czy obniża poziom androgenów – a także od obecności poza docelowym działaniem danego antyandrogenu. Na przykład, podczas gdy antyandrogeny antygonadotropowe, takie jak modulatory GnRH i octan cyproteronu, są związane z wyraźną dysfunkcją seksualną i osteoporozą u mężczyzn, selektywni antagoniści AR, tacy jak bikalutamid, nie są kojarzeni z osteoporozą i wiązani są z jedynie minimalną dysfunkcją seksualną. Uważa się, że różnice te są związane z faktem, że antygonadotropiny tłumią poziomy androgenów, a przez to wydłużają poziomy bioaktywnych metabolitów androgenów, takich jak estrogeny i neurosteroidy, podczas gdy selektywni antagoniści AR podobnie neutralizują działanie androgenów, ale pozostawiają nienaruszone poziomy androgenów, a tym samym ich metabolitów (i faktycznie może nawet je zwiększyć w wyniku ich działania prognadotropowego ). Jako inny przykład, steroidowe antyandrogeny, octan cyproteronu i spironolakton, oprócz ich aktywności antyandrogenowej mają działanie poza celem, w tym działanie progestogenne , antymineralokortykoidowe i/lub glukokortykoidowe , a te działania poza celem mogą skutkować dodatkowymi skutkami ubocznymi.
U mężczyzn głównymi skutkami ubocznymi antyandrogenów są demaskulinizacja i feminizacja . Te działania niepożądane obejmują ból/tkliwość piersi i ginekomastię ( rozwój / powiększenie piersi ), zmniejszony wzrost/gęstość owłosienia ciała , zmniejszoną masę i siłę mięśni , kobiece zmiany w masie i rozmieszczeniu tkanki tłuszczowej oraz zmniejszoną długość prącia i rozmiar jąder . Stwierdzono, że odsetek ginekomastii u mężczyzn stosujących selektywną monoterapię antagonistą AR wynosi od 30 do 85%. Ponadto antyandrogeny mogą powodować niepłodność , osteoporozę , uderzenia gorąca , zaburzenia seksualne (w tym utratę libido i zaburzenia erekcji ), depresję , zmęczenie , anemię i zmniejszenie objętości nasienia/ejakulatu u mężczyzn. Odwrotnie, skutki uboczne selektywnych antagonistów AR u kobiet są minimalne. Jednak antyandrogeny antygonadotropowe , takie jak octan cyproteronu, mogą powodować hipoestrogenizm , brak miesiączki i osteoporozę u kobiet przed menopauzą, a także inne działania niepożądane.
Szereg antyandrogenów jest związanych z hepatotoksycznością . Należą do nich, w różnym stopniu, octan cyproteronu, flutamid, nilutamid, bikalutamid, aminoglutetymid i ketokonazol. Z kolei spironolakton, enzalutamid i inne antyandrogeny nie są związane z istotnymi wskaźnikami hepatotoksyczności. Jednakże, chociaż nie stwarzają ryzyka hepatotoksyczności, spironolakton niesie ryzyko hiperkaliemii, a enzalutamid – drgawek .
U kobiet będących w ciąży , antyandrogeny mogą zakłócać androgenów pośredniczy różnicowania płciowego z genitaliów i mózgu męskich płodów . Przejawia się to przede wszystkim jako niejednoznaczne genitalia – czyli niedostatecznie wirylizowane lub sfeminizowane genitalia, które anatomicznie są skrzyżowaniem penisa i pochwy – i teoretycznie także jako kobiecość . Jako takie, antyandrogeny są teratogenami , a kobiety w ciąży nie powinny być leczone antyandrogenem. Ponadto kobietom, które mogą lub mogą zajść w ciążę, zdecydowanie zaleca się przyjmowanie antyandrogenów tylko w połączeniu z odpowiednią antykoncepcją .
Przedawkować
Antyandrogeny są stosunkowo bezpieczne w przypadku ostrego przedawkowania .
Interakcje
Inhibitory i induktorów z cytochromu P450, enzymów, może współdziałać z różnymi antyandrogenów.
Mechanizm akcji
Antagoniści receptora androgenowego
| Pogarszać | RBA |
|---|---|
| Metrybolon | 100 |
| Dihydrotestosteron | 85 |
| Octan cyproteronu | 7,8 |
| Bikalutamid | 1,4 |
| Nilutamid | 0,9 |
| Hydroksyflutamid | 0,57 |
| Flutamid | <0,0057 |
|
Uwagi: |
|
| Antyandrogen | Względna moc |
|---|---|
| Bikalutamid | 4.3 |
| Hydroksyflutamid | 3,5 |
| Flutamid | 3,3 |
| Octan cyproteronu | 1,0 |
| Zanoterone | 0,4 |
| Opis: Względne siły doustnie podawanych antyandrogenów w antagonizowaniu 0,8 do 1,0 mg/kg podskórnie indukowanego propionianem testosteronu wzrostu masy prostaty brzusznej u wykastrowanych niedojrzałych samców szczurów. Źródła: Zobacz szablon. | |
Antagoniści AR działają poprzez bezpośrednie wiązanie i kompetycyjne wypieranie androgenów, takich jak testosteron i DHT, z AR, zapobiegając w ten sposób aktywacji receptora i pośredniczeniu w ich skutkach biologicznych. Ze względu na budowę chemiczną antagoniści AR dzielą się na dwa typy : steroidowe i niesteroidowe. Sterydowi antagoniści AR są strukturalnie pokrewni hormonom steroidowym, takim jak testosteron i progesteron , podczas gdy niesteroidowi antagoniści AR nie są steroidami i są strukturalnie różne. Sterydowi antagoniści AR mają tendencję do wychodzenia poza docelowe działanie hormonalne ze względu na ich strukturalne podobieństwo do innych hormonów steroidowych. W przeciwieństwie do tego, niesteroidowi antagoniści AR są selektywni dla AR i nie wykazują poza docelową aktywnością hormonalną. Z tego powodu są czasami określane jako „czyste” antyandrogeny.
Chociaż są one opisywane jako antyandrogeny i rzeczywiście ogólnie wykazują tylko takie efekty, większość lub wszyscy steroidowi antagoniści AR nie są w rzeczywistości cichymi antagonistami AR, ale raczej słabymi częściowymi agonistami i są w stanie aktywować receptor przy braku silniejszych agonistów AR, takich jak testosteron i DHT. Może to mieć implikacje kliniczne w specyficznym kontekście leczenia raka prostaty. Przykładowo, steroidowi antagoniści AR są zdolni do zwiększania masy prostaty i przyspieszania wzrostu komórek raka prostaty przy braku silniejszych agonistów AR, a spironolakton, jak stwierdzono w opisach przypadków, przyspiesza progresję raka prostaty. Ponadto, podczas gdy octan cyproteronu powoduje niejednoznaczne narządy płciowe poprzez feminizację płodów płci męskiej po podaniu ciężarnym zwierzętom, stwierdzono, że powoduje maskulinizację narządów płciowych płodów żeńskich zwierząt ciężarnych. W przeciwieństwie do steroidowych antagonistów AR, niesteroidowi antagoniści AR są cichymi antagonistami AR i nie aktywują receptora. Być może dlatego mają one większą skuteczność niż steroidowi antagoniści AR w leczeniu raka prostaty i jest ważnym powodem, dla którego w dużej mierze zastąpiły je w tym wskazaniu w medycynie.
Antyandrogeny niesteroidowe mają stosunkowo niskie powinowactwo do AR w porównaniu do steroidowych ligandów AR. Na przykład bikalutamid ma około 2% powinowactwa DHT do AR i około 20% powinowactwa CPA do AR. Jednak pomimo ich niskiego powinowactwa do AR, brak słabej częściowej aktywności agonistycznej NSAA wydaje się poprawiać ich moc w porównaniu z antyandrogenami steroidowymi. Na przykład, chociaż flutamid ma około 10-krotnie niższe powinowactwo do AR niż CPA, wykazuje w testach biologicznych równą lub nieco większą siłę działania na CPA jako antyandrogen . Ponadto krążące terapeutyczne stężenia niesteroidowych antyandrogenów są bardzo wysokie, rzędu tysięcy razy wyższe niż testosteronu i DHT, co pozwala im skutecznie konkurować i blokować sygnalizację AR.
Antagoniści AR mogą nie wiązać się ani blokować błonowych receptorów androgenowych (mAR), które różnią się od klasycznego jądrowego AR. Jednak mAR nie wydają się być zaangażowane w maskulinizację . Świadczy o tym doskonale kobiecy fenotyp kobiet z całkowitym zespołem niewrażliwości na androgeny . Te kobiety mają kariotyp 46,XY (tj. są genetycznie „męskie”) i wysoki poziom androgenów, ale mają wadliwy AR iz tego powodu nigdy nie maskulinizują się. Są opisywane jako bardzo kobiece, zarówno fizycznie, jak i psychicznie i behawioralnie.
Antagoniści domeny N-terminalnej
Antagoniści AR domeny N-końcowej są nowym typem antagonisty AR, który, w przeciwieństwie do wszystkich obecnie sprzedawanych antagonistów AR, wiąże się raczej z domeną N-końcową (NTD) AR niż z domeną wiążącą ligand (LBD). Podczas gdy konwencjonalni antagoniści AR wiążą się z LBD AR i kompetycyjnie wypierają androgeny, zapobiegając w ten sposób aktywacji receptora, antagoniści AR NTD wiążą się kowalencyjnie z NTD AR i zapobiegają interakcjom białko-białko po aktywacji, które są wymagane do aktywności transkrypcyjnej . Jako takie są niekonkurencyjnymi i nieodwracalnymi antagonistami AR. Przykłady antagonistów AR NTD obejmują eter diglicydylowy bisfenolu A (BADGE) i jego pochodne EPI-001 , ralaniten (EPI-002) i octan ralanitenu (EPI-506). Antagoniści AR NTD są badani pod kątem potencjalnego leczenia raka prostaty i uważa się, że mogą mieć większą skuteczność jako antyandrogeny w porównaniu z konwencjonalnymi antagonistami AR. Zgodnie z tym poglądem, antagoniści AR NTD są aktywni przeciwko splicingowym wariantom AR, którymi nie są konwencjonalni antagoniści AR, a antagoniści AR NTD są odporni na mutacje przejmowania funkcji w AR LBD, które przekształcają antagonistów AR w agonistów AR i często występują w raku prostaty.
Degradery receptora androgenowego
Selektywne degradatory receptora androgenowego (SARD) to kolejny nowy rodzaj antyandrogenów, który został niedawno opracowany. Działają poprzez zwiększenie degradacji AR i są analogiczne do selektywnych degradatorów receptorów estrogenowych (SERD), takich jak fulwestrant (lek stosowany w leczeniu raka piersi z dodatnim receptorem estrogenowym ). Podobnie jak w przypadku antagonistów AR NTD, uważa się, że SARD mogą mieć większą skuteczność niż konwencjonalni antagoniści AR iz tego powodu są badane w leczeniu raka prostaty. Przykładem SARD jest dimetylokurkumina (ASC-J9), która jest opracowywana jako lek miejscowy do potencjalnego leczenia trądziku. SARD, takie jak dimetylokurkumina, różnią się od konwencjonalnych antagonistów AR i antagonistów AR NTD tym, że niekoniecznie muszą wiązać się bezpośrednio z AR.
Inhibitory syntezy androgenów
Inhibitory syntezy androgenów to inhibitory enzymów, które zapobiegają biosyntezie androgenów. Proces ten zachodzi głównie w gonadach i nadnerczach , ale także w innych tkankach, takich jak gruczoł krokowy , skóra i mieszki włosowe . Leki te obejmują aminoglutetymid, ketokonazol i octan abirateronu. Aminoglutetymid hamuje enzym rozszczepiający łańcuchy boczne cholesterolu, znany również jako P450scc lub CYP11A1, który jest odpowiedzialny za konwersję cholesterolu do pregnenolonu i , w konsekwencji, produkcję wszystkich hormonów steroidowych, w tym androgenów. Ketokonazol i octan abirateronu są inhibitorami enzymu CYP17A1, znanego również jako 17α-hydroksylaza/17,20-liaza, który odpowiada za konwersję steroidów pregnanowych do androgenów oraz mineralokortykoidów w glikokortykoidy. Ponieważ wszystkie te leki oprócz androgenów zapobiegają tworzeniu glukokortykoidów, muszą być łączone z glukokortykoidem, takim jak prednizon, aby uniknąć niewydolności nadnerczy . Obecnie opracowywany nowszy lek do leczenia raka prostaty, sewiteronel , jest selektywny w hamowaniu funkcji 17,20-liazy CYP17A1 iz tego powodu, w przeciwieństwie do wcześniejszych leków, nie wymaga jednoczesnego leczenia glikokortykosteroidem.
Inhibitory 5α-reduktazy
Inhibitory 5α-reduktazy, takie jak finasteryd i dutasteryd, są inhibitorami 5α-reduktazy , enzymu odpowiedzialnego za tworzenie DHT z testosteronu. DHT jest od 2,5 do 10 razy silniejszy niż testosteron jako androgen i jest wytwarzany w sposób tkankowo selektywny w oparciu o ekspresję 5α-reduktazy. Tkanki, w których DHT tworzy się w szybkim tempie, obejmują gruczoł krokowy , skórę i mieszki włosowe . Zgodnie z tym, DHT bierze udział w patofizjologii łagodnego przerostu gruczołu krokowego, wypadania włosów i hirsutyzmu, a do leczenia tych stanów stosuje się inhibitory 5α-reduktazy.
Antygonadotropiny
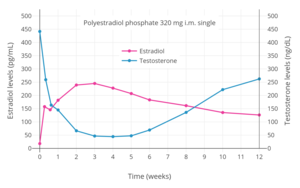

Antigonadotropins są leki, które hamują GnRH, w którym pośredniczy wydzielanie z gonadotropin z przysadki . Gonadotropiny obejmują hormon luteinizujący (LH) i hormon folikulotropowy (FSH) i są hormonami peptydowymi, które sygnalizują gonadom wytwarzanie hormonów płciowych . Tłumiąc wydzielanie gonadotropin, antygonadotropiny hamują produkcję hormonów płciowych w gonadach, a przez to zwiększenie poziomu krążących androgenów. Modulatory GnRH , w tym zarówno agoniści, jak i antagoniści GnRH , są silnymi antygonadotropinami, które są w stanie obniżyć poziom androgenów o 95% u mężczyzn. Ponadto estrogeny i progestageny są antygonadotropinami poprzez wywieranie ujemnego sprzężenia zwrotnego na osi podwzgórze-przysadka-gonady (oś HPG). Estrogeny w wysokich dawkach są w stanie hamować poziom androgenów do poziomu kastracji u mężczyzn, podobnie jak modulatory GnRH, podczas gdy progestageny w wysokich dawkach są w stanie obniżyć poziom androgenów o około 70 do 80% u mężczyzn.
Przykłady agonistów GnRH obejmują leuprorelinę (leuprolid) i goserelinę , podczas gdy przykładem antagonisty GnRH jest cetroreliks . Estrogenów, które są lub które zostały wykorzystane jako antigonadotropins zawierają estradiol, estrów estradiolu , takich jak walerianian estradiolu , estradiolu, undecylan i fosforan poliestradiolu , sprzężone estrogeny, etynyloestradiol, dietylostilbestrol (już powszechnie stosowane), oraz bifluranol . Progestogeny stosowane jako antygonadotropiny obejmują octan chlormadinonu, octan cyproteronu, kapronian gestonoronu, kapronian hydroksyprogesteronu , octan medroksyprogesteronu, octan megestrolu i oksendolon.
Różnorodny
Modulatory globulin wiążących hormony płciowe
Poza działaniem antygonadotropowym, estrogeny są również funkcjonalnymi antyandrogenami poprzez zmniejszenie wolnych stężeń androgenów poprzez zwiększenie produkcji wątrobowej globuliny wiążącej hormony płciowe (SHBG) i zwiększenie poziomu krążącego SHBG. Stwierdzono, że złożone doustne środki antykoncepcyjne zawierające etynyloestradiol zwiększają poziom krążącego SHBG u kobiet od 2 do 4 razy i zmniejszają stężenie wolnego testosteronu o 40 do 80%. Stwierdzono jednak, że złożone doustne środki antykoncepcyjne, które zawierają szczególnie androgenny lewonorgestrel progestagenowy, zwiększają poziom SHBG tylko o 50 do 100%, prawdopodobnie dlatego, że aktywacja AR w wątrobie ma odwrotny skutek niż estrogen i hamuje produkcję SHBG. Lewonorgestrel i niektóre inne progestyny 19-nortestosteronu stosowane w złożonych doustnych środkach antykoncepcyjnych, takie jak noretisteron, również bezpośrednio wiążą się i wypierają androgeny z SHBG, co może dodatkowo antagonizować funkcjonalne działanie antyandrogenne etynyloestradiolu. Badanie wykazało, że u mężczyzn leczenie stosunkowo niską dawką 20 μg/dobę etynyloestradiolu przez 5 tygodni zwiększało poziom krążącego SHBG o 150%, a ze względu na towarzyszący temu spadek poziomu wolnego testosteronu zwiększał całkowity poziom krążącego testosteronu o 50% ( poprzez zmniejszone ujemne sprzężenie zwrotne androgenów na osi HPG).
Modulatory globulin wiążących kortykosteroidy
Estrogeny w dużych dawkach mogą częściowo hamować produkcję androgenów w nadnerczach. Badanie wykazało, że leczenie dużą dawką etynyloestradiolu (100 μg/dobę) zmniejszyło poziom głównych androgenów krążących w nadnerczach o 27 do 48% u kobiet transpłciowych . Obniżony poziom androgenów nadnerczowych z estrogenami jest widoczny w przypadku doustnych i syntetycznych estrogenów, takich jak etynyloestradiol i fosforan estramustyny, ale jest minimalny w przypadku pozajelitowych bioidentycznych form estradiolu, takich jak fosforan poliestradiolu . Uważa się, że jest ona pośredniczona przez mechanizm wątrobowy , prawdopodobnie zwiększone wytwarzanie globuliny wiążącej kortykosteroidy (CBG) oraz poziomy i kompensacyjne zmiany w wytwarzaniu steroidów nadnerczowych (np. przetaczanie syntezy androgenów w nadnerczach do wytwarzania kortyzolu ). Na uwagę zasługuje w tym względzie, że estrogeny doustne i syntetyczne, ze względu na doustne pierwsze przejście i odporność na metabolizm wątrobowy , mają znacznie silniejszy wpływ na syntezę białek wątrobowych niż estradiol podawany drogą pozajelitową. Obniżenie poziomu androgenów w nadnerczach przy zastosowaniu terapii estrogenowej w dużych dawkach może być korzystne w leczeniu raka prostaty .
Antykortykotropiny
Antykortykotropiny, takie jak glikokortykosteroidy i mineralokortykosteroidy, działają poprzez wywieranie negatywnego sprzężenia zwrotnego na oś podwzgórze-przysadka-nadnercza ( oś HPA), hamując w ten sposób wydzielanie hormonu uwalniającego kortykotropinę (CRH), a tym samym hormonu adrenokortykotropowego (ACTH; kortykotropina) i w konsekwencji hamując jego wytwarzanie od androgenów prohormonów jak dehydroepiandrosteronu (DHEA), siarczanu dehydroepiandrosteronu (DHEA-S) i androstenodionu w nadnerczach . Rzadko stosuje się je klinicznie jako funkcjonalne antyandrogeny, ale jako takie stosuje się je w przypadku wrodzonego przerostu nadnerczy u dziewcząt i kobiet, w którym występuje nadmierna produkcja i poziom androgenów nadnerczowych z powodu niedoboru glikokortykoidów, a co za tym idzie nadaktywności osi HPA.
Substancje uczulające na insulinę
U kobiet z insulinoopornością , takich jak te z zespołem policystycznych jajników , poziom androgenów jest często podwyższony. Metformina , lek uwrażliwiający na insulinę , ma u takich kobiet pośrednie działanie antyandrogenne, obniżając poziom testosteronu nawet o 50%, wtórnie do korzystnego wpływu na wrażliwość na insulinę.
Immunogeny i szczepionki
Albumina Ovandrotone (Fecundin, Ovastim) i Androvax (albumina androstendionowa) to immunogeny i szczepionki przeciwko androstendionowi, które są stosowane w medycynie weterynaryjnej w celu poprawy płodności (wskaźnika rozrodu) owiec (dorosłych samic owiec). Uważa się, że wytwarzanie przeciwciał przeciwko androstendionowi przez te środki obniża poziom krążącego androstendionu i jego metabolitów (np. testosteronu i estrogenów), co z kolei zwiększa aktywność osi HPG poprzez zmniejszenie ujemnego sprzężenia zwrotnego i zwiększa tempo owulacji , w większej płodności i płodności.
Chemia
Antyandrogeny, można podzielić na kilka różnych rodzajów, w oparciu o strukturę chemiczną , w tym niesteroidowe antyandrogeny , niesteroidowe antyandrogeny i peptydów . Antyandrogeny steroidowe obejmują związki takie jak octan cyproteronu , spironolakton , estradiol , octan abirateronu i finasteryd ; niesteroidowe antyandrogeny obejmują związki takie jak bikalutamid , elagolix , dietylostilbestrol , aminoglutetymid i ketokonazol ; a peptydy obejmują analogi GnRH, takie jak leuprorelina i cetroreliks .
Historia
Antygonadotropiny, takie jak estrogeny i progestageny, zostały po raz pierwszy wprowadzone w latach 30. XX wieku. Korzystny wpływ deprywacji androgenów poprzez kastrację chirurgiczną lub terapię wysokimi dawkami estrogenów na raka prostaty odkryto w 1941 roku. Antagonistów AR odkryto po raz pierwszy na początku lat sześćdziesiątych. Sterydowy antyandrogenowy octan cyproteronu został odkryty w 1961 i wprowadzony w 1973 i jest często opisywany jako pierwszy antyandrogen, który został wprowadzony na rynek. Jednak spironolakton został wprowadzony w 1959 roku, chociaż jego działanie antyandrogenowe nie zostało rozpoznane lub wykorzystane dopiero później i początkowo było niezamierzonym działaniem poza docelowym. Oprócz spironolaktonu, octan chlormadinonu i octan megestrolu są antyandrogenami steroidowymi, które są słabsze niż octan cyproteronu, ale zostały również wprowadzone wcześniej, w latach 60. XX wieku. Inne wczesne antyandrogeny steroidowe, które zostały opracowane w tym czasie, ale nigdy nie zostały wprowadzone do obrotu, obejmują benorteron (SKF-7690; 17α-metylo- B- nortestosteron), BOMT (Ro 7-2340), cyproteron (SH-80881) i trimetylotrienolon (R- 2956).
Niesteroidowy antyandrogen, flutamid, został po raz pierwszy zgłoszony w 1967 roku. Został wprowadzony w 1983 roku i był pierwszym niesteroidowym antyandrogenem na rynku. Inny wczesny niesteroidowy antyandrogen, DIMP (Ro 7-8117), który jest strukturalnie spokrewniony z talidomidem i jest stosunkowo słabym antyandrogenem, został po raz pierwszy opisany w 1973 roku i nigdy nie został wprowadzony na rynek. Po flutamidzie w 1989 r. pojawił się nilutamid, a w 1995 r. bikalutamid. Oprócz tych trzech leków, które zostały uznane za niesteroidowe antyandrogeny pierwszej generacji, w 2012 i 2018 r. wprowadzono niesteroidowe antyandrogeny drugiej generacji – enzalutamid i apalutamid . Różnią się one od wcześniejszych antyandrogenów niesteroidowych tym, że w porównaniu są znacznie skuteczniejsze.
Inhibitory syntezy androgenów, aminoglutetymid i ketokonazol, zostały wprowadzone na rynek odpowiednio w 1960 i 1977 r., a nowszy lek, octan abirateronu, został wprowadzony w 2011 r. Modulatory GnRH po raz pierwszy wprowadzono w latach 80. XX wieku. Inhibitory 5α-reduktazy finasteryd i dutasteryd zostały wprowadzone odpowiednio w 1992 i 2002 roku. Elagolix , pierwszy doustnie aktywny modulator GnRH, który został wprowadzony na rynek, został wprowadzony na rynek w 2018 roku.
Oś czasu
Poniżej znajduje się kalendarium wydarzeń w historii antyandrogenów:
- 1941: Hudgins i Hodges pokazują, że pozbawienie androgenów poprzez terapię wysokimi dawkami estrogenów lub kastrację chirurgiczną leczy raka prostaty
- 1957: po raz pierwszy zostaje zsyntetyzowany steroidowy antyandrogen spironolakton
- 1960: Spironolakton zostaje po raz pierwszy wprowadzony do użytku medycznego jako antymineralokortykoid
- 1961: Po raz pierwszy zostaje zsyntetyzowany steroidowy antyandrogenowy octan cyproteronu
- 1962: Po raz pierwszy doniesiono, że spironolakton powoduje ginekomastię u mężczyzn
- 1963: Odkryto antyandrogenne działanie octanu cyproteronu
- 1966: Benorteron jest pierwszym znanym antyandrogenem badanym klinicznie w leczeniu trądziku i hirsutyzmu u kobiet
- 1967: Po raz pierwszy doniesiono, że znany antyandrogen, benorteron, wywołuje ginekomastię u mężczyzn
- 1967: Pierwsza synteza niesteroidowego antyandrogenu, flutamidu pierwszej generacji
- 1967: Octan cyproteronu został po raz pierwszy przebadany klinicznie w celu leczenia odchyleń seksualnych u mężczyzn
- 1969: Octan cyproteronu został po raz pierwszy zbadany w leczeniu trądziku, hirsutyzmu, łojotoku i wypadania włosów na skórze głowy u kobiet
- 1969: Odkryto antyandrogenne działanie spironolaktonu
- 1972: Pierwsze doniesienie o antyandrogennej aktywności flutamidu
- 1973: Octan cyproteronu został po raz pierwszy wprowadzony do użytku medycznego w leczeniu odchyleń seksualnych
- 1977: Po raz pierwszy opisano nilutamid antyandrogenowy pierwszej generacji
- 1978: Spironolakton jest po raz pierwszy badany w leczeniu hirsutyzmu u kobiet
- 1979: Po raz pierwszy badana jest łączona blokada androgenów
- 1980: Po raz pierwszy osiągnięto kastrację medyczną za pomocą analogu GnRH
- 1982: Po raz pierwszy opisano antyandrogenowy bikalutamid pierwszej generacji
- 1982: Opracowano połączoną blokadę androgenową w przypadku raka prostaty
- 1983: W Chile po raz pierwszy wprowadza się flutamid do użytku medycznego w leczeniu raka prostaty
- 1987: Nilutamid zostaje po raz pierwszy wprowadzony we Francji do użytku medycznego w leczeniu raka prostaty
- 1989: Stwierdzono, że połączona blokada androgenów przez flutamid i analog GnRH jest lepsza niż sam analog GnRH w przypadku raka prostaty
- 1989: Flutamid zostaje po raz pierwszy wprowadzony do użytku medycznego w Stanach Zjednoczonych w leczeniu raka prostaty
- 1989: Flutamid jest po raz pierwszy badany w leczeniu hirsutyzmu u kobiet
- 1992: Po raz pierwszy opisano inhibitor syntezy androgenów octan abirateronu
- 1995: Bikalutamid zostaje po raz pierwszy wprowadzony do użytku medycznego w leczeniu raka prostaty
- 1996: Nilutamid zostaje po raz pierwszy wprowadzony do użytku medycznego w Stanach Zjednoczonych w leczeniu raka prostaty
- 2006: Po raz pierwszy opisano niesteroidowy antyandrogen enzalutamid drugiej generacji
- 2007: Po raz pierwszy opisano niesteroidowy antyandrogenowy apalutamid drugiej generacji
- 2011: Octan abirateronu zostaje po raz pierwszy wprowadzony do użytku medycznego w leczeniu raka prostaty
- 2012: Enzalutamid zostaje po raz pierwszy wprowadzony do użytku medycznego w leczeniu raka prostaty
- 2018: Apalutamid zostaje po raz pierwszy wprowadzony do użytku medycznego w leczeniu raka prostaty
- 2018: Elagolix jest pierwszym doustnym aktywnym antagonistą GnRH, który zostanie wprowadzony do użytku medycznego
- 2019: Relugolix jest drugim aktywnym doustnie antagonistą GnRH, który zostanie wprowadzony do użytku medycznego
Społeczeństwo i kultura
Etymologia
Termin antyandrogen jest ogólnie używany w odniesieniu do antagonistów AR, jak opisał Dorfman (1970):
Antyandrogeny to substancje, które zapobiegają ekspresji androgenów w miejscach docelowych. Działanie hamujące tych substancji należy zatem odróżnić od związków, które zmniejszają syntezę i/lub uwalnianie czynników podwzgórza (uwalniających), od hormonów przedniego płata przysadki (gonadotropin, zwłaszcza hormonu luteinizującego) oraz od materiału, który działa bezpośrednio na gonady hamują biosyntezę i/lub wydzielanie androgenów.
Jednak pomimo powyższego, termin ten może być również używany do opisania funkcjonalnych antyandrogenów, takich jak inhibitory syntezy androgenów i antygonadotropiny, w tym nawet estrogeny i progestageny. Na przykład progestagen i stąd antygonadotropina octan medroksyprogesteronu jest czasami opisywany jako steroidowy antyandrogen, mimo że nie jest antagonistą AR.
Badania
Administracja miejscowa
Odnotowano duże zainteresowanie i wysiłki w opracowaniu miejscowych antagonistów AR do leczenia stanów zależnych od androgenów, takich jak trądzik i łysienie typu u mężczyzn. Niestety, podczas gdy ogólnoustrojowe podawanie antyandrogenów jest bardzo skuteczne w leczeniu tych stanów, rozczarowująco stwierdzono, że podawanie miejscowe ma ogólnie ograniczoną i jedynie umiarkowaną skuteczność, nawet gdy zastosowano steroidowych antagonistów AR o wysokim powinowactwie , takich jak octan cyproteronu i spironolakton. Co więcej, w konkretnym przypadku leczenia trądziku miejscowi antagoniści AR okazują się znacznie mniej skuteczni w porównaniu do ustalonych metod leczenia, takich jak nadtlenek benzoilu i antybiotyki .
Opracowano szereg antagonistów AR do stosowania miejscowego, ale ich rozwój nie został ukończony i dlatego nigdy nie wprowadzono ich na rynek. Należą do nich steroidowi antagoniści AR klaskoteron , cyproteron , rosterolon i topteron oraz niesteroidowi antagoniści AR cioteronel , octan inokoteronu , RU-22930 , RU-58642 i RU-58841 . Jednak jeden miejscowy antagonista receptorów AR, topilutamid (flurydyl), został wprowadzony w kilku krajach europejskich do leczenia typowego wypadania włosów u mężczyzn. Ponadto w niektórych krajach europejskich w tym samym wskazaniu wprowadzono miejscowy inhibitor 5α-reduktazy i słaby estrogen, alfatradiol , chociaż jego skuteczność jest kontrowersyjna. Spironolakton został wprowadzony na rynek we Włoszech w postaci kremu do stosowania miejscowego pod marką Spiroderm do leczenia trądziku i hirsutyzmu, ale ten preparat został wycofany i dlatego nie jest już dostępny.
Antykoncepcja dla mężczyzn
Antyandrogeny, takie jak octan cyproteronu, badano pod kątem potencjalnego zastosowania jako męskich hormonalnych środków antykoncepcyjnych . Chociaż skutecznie hamują męską płodność , ich stosowanie jako monoterapii wykluczają skutki uboczne, takie jak niedobór androgenów (np. demaskulinizacja , dysfunkcje seksualne , uderzenia gorąca , osteoporoza ) i feminizacja (np. ginekomastia ). Kombinacja pierwotnej antygonadotropiny, takiej jak octan cyproteronu w celu zapobiegania płodności i androgenu, takiego jak testosteron, w celu zapobiegania ogólnoustrojowemu niedoborowi androgenów, powodująca selektywne działanie antyandrogenne miejscowo w jądrach, została szeroko przebadana i wykazała obiecujące wyniki, ale nie została zatwierdzona do użytku klinicznego w tym czasie. Undekanian dimetandrolonu (kod rozwojowy CDB-4521), działający po podaniu doustnym podwójny SAA i progestagen, jest badany jako potencjalny męski środek antykoncepcyjny i jako pierwsza męska pigułka antykoncepcyjna .
Rak piersi
Antyandrogeny, takie jak bikalutamid , enzalutamid i octan abirateronu, są badane pod kątem potencjalnego leczenia raka piersi , w tym potrójnie ujemnego raka piersi z ekspresją AR i innych typów raka piersi z ekspresją AR.
Różnorodny
Antyandrogeny mogą być skuteczne w leczeniu zaburzeń obsesyjno-kompulsyjnych .
Zobacz też
Bibliografia
Dalsza lektura
- Neumann, F.; Steinbeck, H. (1974). „Antyandrogeny”. Androgeny II i Antyandrogeny / Androgeny II i Antyandrogeny . s. 235–484. doi : 10.1007/978-3-642-80859-3_6 . Numer ISBN 978-3-642-80861-6.
- Graf, K.-J.; Brotherton, J.; Neumann, F. (1974). „Kliniczne zastosowania antyandrogenów”. Androgeny II i Antyandrogeny / Androgeny II i Antyandrogeny . s. 485-542. doi : 10.1007/978-3-642-80859-3_7 . Numer ISBN 978-3-642-80861-6.
