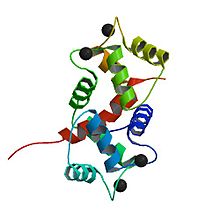
Kalmodulina - Calmodulin
| Kalmodulina | |||||||
|---|---|---|---|---|---|---|---|

| |||||||
| Identyfikatory | |||||||
| Symbol | Krzywka | ||||||
| WPB | 1OSA | ||||||
| UniProt | P62158 | ||||||
| |||||||

Kalmoduliny ( CaM ) (skrót cal cium- moduł ated prote w ), jest wielofunkcyjnym białkiem pośredni messenger wiązania wapnia ekspresji we wszystkich komórkach eukariotycznych . Jest to wewnątrzkomórkowy cel wtórnego przekaźnika Ca 2+ , a wiązanie Ca 2+ jest wymagane do aktywacji kalmoduliny. Po związaniu z Ca2 + kalmodulina działa jako część szlaku przekazywania sygnału wapniowego , modyfikując swoje interakcje z różnymi białkami docelowymi , takimi jak kinazy lub fosfatazy .
Struktura
Kalmodulina to małe, wysoce konserwowane białko o długości 148 aminokwasów (16,7 kDa). Białko ma dwie w przybliżeniu symetryczne domeny kuliste (domeny N i C), z których każda zawiera parę motywów ręki EF oddzielonych elastycznym regionem łącznikowym, co daje łącznie cztery miejsca wiązania Ca2 + , po dwa w każdej domenie kulistej. W stanie wolnym od Ca2 + , helisy, które tworzą cztery ręce EF, są zwinięte w zwartej orientacji, a łącznik centralny jest nieuporządkowany; w stanie nasyconym Ca2 + , helisy ręki EF przyjmują otwartą orientację w przybliżeniu prostopadłą do siebie, a łącznik centralny tworzy rozciągniętą alfa-helisę w strukturze krystalicznej, ale pozostaje w dużej mierze nieuporządkowany w roztworze. Domena C ma wyższe powinowactwo wiązania do Ca 2+ niż domena N.
Kalmodulina jest strukturalnie dość podobna do troponiny C , innego białka wiążącego Ca2 + zawierającego cztery motywy EF-hand. Jednakże, troponiny C zawiera dodatkową alfa-helisy na swoim N-końcu i jest konstytutywnie związany celu, troponiny . Dlatego nie wykazuje takiej samej różnorodności rozpoznawania celu jak kalmodulina.
Znaczenie elastyczności w kalmodulinie
Zdolność kalmoduliny do rozpoznawania ogromnego zakresu białek docelowych wynika w dużej mierze z jej elastyczności strukturalnej. Oprócz elastyczności centralnej domeny łącznika, domeny N i C przechodzą cykl konformacyjny otwarty-zamknięty w stanie związanym Ca2 + . Kalmodulina wykazuje również dużą zmienność strukturalną i podlega znacznym wahaniom konformacyjnym, gdy jest związana z celami. Co więcej, głównie hydrofobowy charakter wiązania kalmoduliny z większością jej celów pozwala na rozpoznanie szerokiego zakresu sekwencji białek docelowych. Razem te cechy umożliwiają kalmodulinie rozpoznawanie około 300 docelowych białek wykazujących różne motywy sekwencji wiążącej CaM.
Mechanizm
Wiązanie Ca 2+ przez ręce EF powoduje otwarcie domen N i C, co odsłania hydrofobowe powierzchnie wiążące cel. Powierzchnie te oddziałują z komplementarnymi segmentami niepolarnymi na docelowych białkach, zazwyczaj składających się z grup masywnych aminokwasów hydrofobowych oddzielonych 10-16 aminokwasami polarnymi i/lub zasadowymi. Elastyczna domena centralna kalmoduliny umożliwia białku owijanie się wokół celu, chociaż znane są alternatywne sposoby wiązania. „Knoniczne” cele kalmoduliny, takie jak kinazy łańcucha lekkiego miozyny i CaMKII , wiążą się tylko z białkiem związanym z Ca 2+ , podczas gdy niektóre białka, takie jak kanały NaV i białka z motywem IQ , również wiążą się z kalmoduliną w przypadku braku Ca 2+ . Wiązanie kalmoduliny indukuje rearanżacje konformacyjne w białku docelowym poprzez „wzajemnie indukowane dopasowanie”, co prowadzi do zmian w funkcji białka docelowego.
Wiązanie wapnia przez kalmodulinę wykazuje znaczną kooperację , co czyni kalmodulinę niezwykłym przykładem monomerycznego (jednołańcuchowego) białka wiążącego kooperatywnie. Ponadto wiązanie celu zmienia powinowactwo wiązania kalmoduliny z jonami Ca2 + , co pozwala na złożoną interakcję allosteryczną między Ca2 + a interakcjami wiążącymi cel. Ten wpływ wiązania na celu Ca 2+ powinowactwie uważa się, aby umożliwić Ca 2+ aktywacji białek, które są związane z konstytutywną kalmoduliny, takich jak małe przewodnictwo Ca 2+ (SK) -aktywowany kanałów potasowych.
Chociaż kalmodulina działa głównie jako białko wiążące Ca2 + , koordynuje również inne jony metali. Na przykład, w obecności typowych wewnątrzkomórkowych stężeń Mg2 + (0,5-1,0 mM) i spoczynkowych stężeń Ca2 + (100 nM), miejsca wiązania Ca2 + kalmoduliny są przynajmniej częściowo nasycone przez Mg2 + . Ten Mg 2+ jest wypierany przez wyższe stężenia Ca 2+ generowane przez zdarzenia sygnalizacyjne. Podobnie, Ca2 + może sam zostać wyparty przez inne jony metali, takie jak trójwartościowe lantanowce, które wiążą się z kieszeniami wiążącymi kalmoduliny nawet silniej niż Ca2 + . Chociaż takie jony zniekształcają strukturę kalmoduliny i generalnie nie są istotne fizjologicznie ze względu na ich niedobór in vitro , mimo to znalazły szerokie zastosowanie naukowe jako reporterów struktury i funkcji kalmoduliny.
Rola w zwierzętach
Kalmodulina pośredniczy w wielu kluczowych procesach, takich jak stan zapalny , metabolizm , apoptoza , skurcz mięśni gładkich , ruch wewnątrzkomórkowy, pamięć krótkotrwała i długotrwała oraz odpowiedź immunologiczna . Wapń uczestniczy w wewnątrzkomórkowym systemie sygnalizacji , działając jako dyfuzyjny drugi posłaniec do bodźców początkowych. Czyni to poprzez wiązanie różnych celów w komórce, w tym dużej liczby enzymów , kanałów jonowych , akwaporyn i innych białek. Kalmodulina jest wyrażana w wielu typach komórek i może mieć różne lokalizacje subkomórkowe, w tym cytoplazmę , w organellach lub powiązaną z błonami osocza lub organelli, ale zawsze znajduje się wewnątrzkomórkowo. Wiele białek, z którymi wiąże się kalmodulina, nie jest w stanie samodzielnie wiązać wapnia i wykorzystuje kalmodulinę jako czujnik wapnia i przetwornik sygnału. Kalmodulina może również wykorzystywać zapasy wapnia w retikulum endoplazmatycznym i retikulum sarkoplazmatycznym . Kalmodulina może podlegać modyfikacjom potranslacyjnym, takim jak fosforylacja , acetylacja , metylacja i rozszczepienie proteolityczne , z których każda ma potencjał modulowania jej działania.
Konkretne przykłady
Rola w skurczu mięśni gładkich
Kalmodulina odgrywa ważną rolę w sprzęganiu skurczu wzbudzenia (EC) i inicjacji cyklu mostkowego w mięśniach gładkich , ostatecznie powodując skurcz mięśni gładkich. Aby aktywować skurcz mięśni gładkich, głowa lekkiego łańcucha miozyny musi zostać ufosforylowana. Ta fosforylacja jest dokonywana przez kinazę lekkiego łańcucha miozyny (MLC) . Ta kinaza MLC jest aktywowana przez kalmodulinę, gdy jest związana przez wapń, co powoduje, że skurcz mięśni gładkich jest zależny od obecności wapnia, poprzez wiązanie kalmoduliny i aktywację kinazy MLC.
Innym sposobem, w jaki kalmodulina wpływa na skurcze mięśni, jest kontrolowanie ruchu Ca 2+ zarówno przez błony komórkowe, jak i retikulum sarkoplazmatyczne . W Ca 2+ kanały , takie jak receptora rianodyny siateczki sarkoplazmatycznej, może być hamowane przez kalmoduliny związanej z wapniem, co wpływa na całkowity poziom wapnia w komórce. Pompy wapniowe usuwają wapń z cytoplazmy lub przechowują go w retikulum endoplazmatycznym, a ta kontrola pomaga regulować wiele dalszych procesów.
Jest to bardzo ważna funkcja kalmoduliny, ponieważ pośrednio odgrywa rolę w każdym procesie fizjologicznym, na który ma wpływ skurcz mięśni gładkich, takim jak trawienie i skurcz tętnic (co pomaga w rozprowadzaniu krwi i regulacji ciśnienia krwi ).
Rola w metabolizmie
Kalmodulina odgrywa ważną rolę w aktywacji kinazy fosforylazy , co ostatecznie prowadzi do odszczepienia glukozy od glikogenu przez fosforylazę glikogenu .
Kalmodulina odgrywa również ważną rolę w metabolizmie lipidów , wpływając na kalcytoninę . Kalcytonina jest hormonem polipeptydowym, który obniża poziom Ca 2+ we krwi i aktywuje kaskady białek G, co prowadzi do wytwarzania cAMP. Działanie kalcytoniny można zablokować poprzez hamowanie działania kalmoduliny, co sugeruje, że kalmodulina odgrywa kluczową rolę w aktywacji kalcytoniny.
Rola w pamięci krótkotrwałej i długotrwałej
Ca2 + /calmodulin-zależna kinaza białkowa II (CaMKII) odgrywa kluczową rolę w rodzaju plastyczności synaptycznej znanej jako długotrwałe wzmocnienie (LTP), które wymaga obecności wapnia/kalmoduliny. CaMKII przyczynia się do fosforylacji wystąpienia receptor AMPA , który zwiększa wrażliwość receptorów AMPA. Ponadto badania pokazują, że hamowanie CaMKII zaburza działanie LTP.
Rola w roślinach

Podczas gdy drożdże mają tylko jeden gen CaM, rośliny i kręgowce zawierają zachowaną ewolucyjnie formę genów CaM. Różnica między roślinami i zwierzętami w sygnalizacji Ca2 + polega na tym, że rośliny zawierają rozszerzoną rodzinę CaM oprócz postaci zachowanej ewolucyjnie. Kalmoduliny odgrywają zasadniczą rolę w rozwoju roślin i adaptacji do bodźców środowiskowych.
Wapń odgrywa kluczową rolę w integralności strukturalnej ściany komórkowej i systemu błon komórkowych. Jednak wysokie poziomy wapnia mogą być toksyczne dla metabolizmu energii komórkowej rośliny, a zatem stężenie Ca 2+ w cytozolu jest utrzymywane na poziomie submikromolowym poprzez usunięcie cytozolowego Ca 2+ do apoplastu lub światła organelli wewnątrzkomórkowych . Impulsy Ca 2+ powstające w wyniku zwiększonego napływu i wypływu działają jako sygnały komórkowe w odpowiedzi na bodźce zewnętrzne, takie jak hormony, światło, grawitacja, czynniki stresu abiotycznego, a także interakcje z patogenami.
Rośliny zawierają białka związane z CaM (CML) oprócz typowych białek CaM. CML mają około 15% podobieństwa aminokwasów do typowych CaM. Arabidopsis thaliana zawiera około 50 różnych genów CML, co prowadzi do pytania, w jakim celu te różnorodne zakresy białek służą funkcji komórkowej. Wszystkie gatunki roślin wykazują tę różnorodność w genach CML. Różne CaM i CML różnią się powinowactwem do wiązania i aktywacji enzymów regulowanych przez CaM in vivo . Stwierdzono również, że CaM lub CML są zlokalizowane w różnych przedziałach organelli.
Wzrost i rozwój roślin
W Arabidopsis białko DWF1 odgrywa enzymatyczną rolę w biosyntezie brasinosteroidów, hormonów steroidowych roślin niezbędnych do wzrostu. Interakcja zachodzi między CaM i DWF1, a DWF1 niezdolny do wiązania CaM nie jest w stanie wytworzyć fenotypu regularnego wzrostu u roślin. Dlatego CaM jest niezbędny dla funkcji DWF1 we wzroście roślin.
Wiadomo również, że białka wiążące CaM regulują rozwój rozrodczy u roślin. Na przykład kinaza białkowa wiążąca CaM w tytoniu działa jako negatywny regulator kwitnienia. Jednak te kinazy białkowe wiążące CaM są również obecne w merystemie wierzchołkowym pędu tytoniu, a wysokie stężenie tych kinaz w merystemie powoduje opóźnione przejście do kwitnienia rośliny.
Kinaza receptora S- locus (SRK) to kolejna kinaza białkowa, która oddziałuje z CaM. SRK bierze udział w odpowiedziach na samoniezgodność w interakcjach pyłek-słupek w Brassica .
Cele CaM w Arabidopsis są również zaangażowane w rozwój i zapłodnienie pyłku. Transportery Ca 2+ są niezbędne do wzrostu łagiewki pyłkowej . Dzięki temu na wierzchołku łagiewki pyłkowej utrzymywany jest stały gradient Ca 2+ w celu wydłużenia podczas procesu zapłodnienia. Podobnie CaM jest również niezbędny w wierzchołku łagiewki pyłkowej, gdzie jego główna rola polega na kierowaniu wzrostem łagiewki pyłkowej.
Interakcja z drobnoustrojami
Tworzenie się guzków
Ca 2+ odgrywa istotną rolę w tworzeniu guzków w roślinach strączkowych. Azot jest niezbędnym pierwiastkiem wymaganym przez rośliny, a wiele roślin strączkowych, niezdolnych do samodzielnego wiązania azotu, łączy się symbiotycznie z bakteriami wiążącymi azot, które redukują azot do amoniaku. To ustalenie interakcji między rośliną strączkową a Rhizobium wymaga czynnika Nod wytwarzanego przez bakterie Rhizobium . Czynnik Nod jest rozpoznawany przez komórki włosów korzeniowych, które są zaangażowane w powstawanie brodawek w roślinach strączkowych. Charakteryzuje się, że odpowiedzi Ca 2+ o różnym charakterze są zaangażowane w rozpoznawanie czynnika Nod. Na czubku włośnika pojawia się strumień Ca 2+, po którym początkowo następuje powtarzająca się oscylacja Ca 2+ w cytozolu, a wokół jądra pojawia się skok Ca 2+ . DMI3, niezbędny gen dla funkcji sygnalizacyjnych czynnika Nod poniżej sygnatury skoków Ca 2+ , może rozpoznawać sygnaturę Ca 2+ . Ponadto kilka genów CaM i CML w Medicago i Lotus ulega ekspresji w guzkach.
Obrona patogenów
Wśród różnorodnych strategii obronnych stosowanych przez rośliny przeciwko patogenom, sygnalizacja Ca2 + jest coraz bardziej powszechna. Poziomy wolnego Ca 2+ w cytoplazmie wzrastają w odpowiedzi na infekcję patogenną. Sygnatury Ca 2+ tego rodzaju zwykle aktywują system obronny roślin poprzez indukcję genów związanych z obroną i nadwrażliwą śmierć komórek. CaMs, CMLs i białka wiążące CaM to niektóre z niedawno zidentyfikowanych elementów szlaków sygnałowych obronnych roślin. Kilka genów CML w tytoniu , fasoli i pomidorze reaguje na patogeny. CML43 jest białkiem spokrewnionym z CaM, które wyizolowane z genu APR134 w odpornych na chorobę liściach Arabidopsis do analizy ekspresji genów, jest szybko indukowane, gdy liście są inokulowane Pseudomonas syringae . Geny te znajdują się również w pomidorach ( Solanum lycopersicum ). CML43 z APR134 wiąże się również z jonami Ca2 + in vitro, co pokazuje, że CML43 i APR134 są zatem zaangażowane w zależną od Ca2 + sygnalizację podczas odpowiedzi immunologicznej roślin na patogeny bakteryjne. Ekspresja CML9 w Arabidopsis thaliana jest szybko indukowana przez bakterie fitopatogenne, flagellinę i kwas salicylowy. Ekspresja SCaM4 i SCaM5 soi w transgenicznym tytoniu i Arabidopsis powoduje aktywację genów związanych z odpornością na patogeny, a także skutkuje zwiększoną odpornością na szerokie spektrum infekcji patogenami. To samo nie dotyczy soi SCaM1 i SCaM2, które są wysoce konserwatywnymi izoformami CaM. W białko BAG6 CaM jest białkiem wiążącym, który wiąże się krzywkę tylko w przypadku braku Ca 2+ , a nie obecności w niej. W BAG6 odpowiada za nadwrażliwą reakcję zaprogramowanej śmierci komórki w celu zapobieżenia rozprzestrzenianiu się infekcji patogenem lub ograniczenia wzrostu patogenu. Mutacje w białkach wiążących CaM mogą mieć poważny wpływ na odpowiedź obronną roślin na infekcje patogenami. Cykliczne kanały bramkowane nukleotydami (CNGC) są funkcjonalnymi kanałami białkowymi w błonie plazmatycznej, które mają zachodzące na siebie miejsca wiązania CaM transportujące dwuwartościowe kationy, takie jak Ca2 + . Jednak dokładna rola pozycjonowania CNGC w tym szlaku obrony roślin jest nadal niejasna.
Abiotyczna reakcja na stres u roślin
Zmiana wewnątrzkomórkowego poziomu Ca2 + jest wykorzystywana jako sygnał dla różnych odpowiedzi na bodźce mechaniczne, zabiegi osmotyczne i solne oraz szoki zimna i ciepła. Różne typy komórek korzenia wykazują różną odpowiedź Ca 2+ na stres osmotyczny i solny, co implikuje specyficzność komórkową wzorców Ca 2+ . W odpowiedzi na stres zewnętrzny CaM aktywuje dekarboksylazę glutaminianową (GAD), która katalizuje konwersję L- glutaminianowej do GABA. Ścisła kontrola syntezy GABA jest ważna dla rozwoju roślin, a zatem zwiększone poziomy GABA mogą zasadniczo wpływać na rozwój roślin. Dlatego stres zewnętrzny może wpływać na wzrost i rozwój roślin, a CaM jest zaangażowany w tę ścieżkę kontrolującą ten efekt.
Przykłady roślin
Sorgo
Sorgo roślinne jest dobrze ugruntowanym organizmem modelowym i może przystosować się w gorącym i suchym środowisku. Z tego powodu jest używany jako model do badania roli kalmoduliny w roślinach. Sorgo zawiera sadzonki, które wyrażają bogate w glicynę białko wiążące RNA , SbGRBP. To konkretne białko może być modulowane przez wykorzystanie ciepła jako stresora. Jego unikalna lokalizacja w jądrze komórkowym i cytozolu świadczy o interakcji z kalmoduliną, która wymaga użycia Ca 2+ . Wystawiając roślinę na wszechstronne warunki stresowe , może powodować tłumienie różnych białek, które umożliwiają komórkom roślinnym tolerowanie zmian środowiskowych. Wykazano, że te modulowane białka stresu oddziałują z CaM. W CaMBP geny eksprymowane w sorgo przedstawione są jako „rośliny” modelu do badania tolerancji na ciepło i stresem suszy .
Arabidopsis
W badaniu Arabidopsis thaliana setki różnych białek wykazały możliwość wiązania CaM w roślinach.
Członkowie rodziny
- Kalmodulina 1 ( CALM1 )
- Kalmodulina 2 ( CALM2 )
- Kalmodulina 3 ( CALM3 )
- pseudogen 1 kalmoduliny 1 ( CALM1P1 )
- Kalmodulinopodobny 3 ( CALML3 )
- Kalmodulinopodobny 4 ( CALML4 )
- Kalmodulinopodobny 5 ( CALML5 )
- Kalmodulinopodobny 6 ( CALML6 )
Inne białka wiążące wapń
Kalmodulina należy do jednej z dwóch głównych grup białek wiążących wapń, zwanych białkami ręki EF . Druga grupa, zwana aneksynami , wiąże wapń i fosfolipidy, takie jak lipokortyna . Wiele innych białek wiąże wapń, chociaż wiązanie wapnia może nie być uważane za ich główną funkcję w komórce.
Zobacz też
- Strona Proteopedia dotycząca kalmoduliny i jej zmiany konformacyjnej
- Kinaza białkowa
- Ca 2+ /kinaza białkowa zależna od kalmoduliny
Bibliografia
Zewnętrzne linki
- „Glikoproteina związana z mieliną” . Cząsteczka miesiąca . WPB RCSB. Lipiec 2020. Zarchiwizowane od oryginału w dniu 2010-05-29 . Pobrano 2021-06-19 .
- Nelson M, Chazin W. „Strona główna dla Calmodulin” . Biblioteka danych białek wiążących wapń EF-Hand . Uniwersytet Vanderbilta . Źródło 2008-03-22 .
- Ikura M (2000). "Docelowa baza danych Calmodulin" . Czasopismo Genomiki Strukturalnej i Funkcjonalnej . Ontario Cancer Institute, Uniwersytet w Toronto. 1 (1): 8–14. doi : 10.1023/a:1011320027914 . PMID 12836676 . S2CID 23097597 . Źródło 2008-03-22 .
- Kalmodulina w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)
- InterPro : IPR015754