difosgen - Diphosgene
| |

| |
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
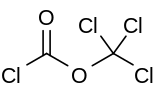
trichlorometyl chloromrówczan | |
| Inne nazwy
chloromrówczan trichlorometylu
| |
| identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.007.242 |
| Numer RTECS | LQ7350000 |
| |
| |
| Nieruchomości | |
| C 2 Cl 4 O 2 | |
| Masa cząsteczkowa | 197,82 g / mol |
| Wygląd | ciekłe w temperaturze pokojowej |
| Gęstość | 1,65 g / cm 3 |
| Temperatura topnienia | -57 ° C (-71 ° F, 216 K) |
| Temperatura wrzenia | 128 ° C (262 ° K, 401 K) |
| nierozpuszczalny | |
| zagrożenia | |
| główne zagrożenia | toksyczny |
| Zwroty (nieaktualna) | 26 / 28-34 |
| Zwroty S (nieaktualna) | 26-28-36 / 37 / 39-45 |
| Temperatura zapłonu | 32 ° C (90 ° C, 305 K) |
| Związki pokrewne | |
|
Związki pokrewne
|
COCl 2 Cl 2 |
|
Jeśli nie zaznaczono inaczej, dane dla materiałów w ich warunków standardowych (25 ° C [77 ° F], 100 kPa). | |
|
| |
| referencje Infobox | |
Difosgen jest związek chemiczny o wzorze ClCO 2 CCI 3 . Ten bezbarwny płyn jest cennym reagentem w syntezie związków organicznych. Difosgenu związane z fosgenem i ma podobną toksyczność, ale bardziej typowo obsługiwane, ponieważ jest on ciekły, podczas gdy fosgen jest gazem.
Zawartość
Produkcji i zastosowania
Difosgenu wytworzyć rodników chlorowania chloromrówczanu metylu pod światłem UV :
- Cl-CO-OCH 3 + 3 Cl 2 - (HV) → Cl-CO-OCCl 3 + 3 HCl
Inną metodą jest rodnikiem chlorowania mrówczanu metylu:
- 'H-CO-OCH 3 + 4 Cl 2 - (HV) → Cl-CO-OCCl 3 + 4 HCI
Difosgen fosgen zamienia się podczas ogrzewania lub po katalizy z węglem . Jest zatem użyteczne reakcje tradycyjnie uzależnionych fosgenu. Na przykład, konwersja aminy język izocyjanianów , amin drugorzędowych w karbamoilowych chlorków, kwasów karboksylowych język chlorków kwasowych i formamidów do izocyjanki . Difosgen stanowi źródło dwóch równoważników fosgenu:
- 2 RNH 2 + ClCO 2 Cl 3 → 2 RNCO + 4 HCI
Z a- aminokwasów difosgen daje chlorek kwasowy izocyjanianów, OCNCHRCOCl lub N bezwodniki kwasów karboksy, amino, w zależności od warunków.
To hydrolizuje do uwolnienia HCl w wilgotnym powietrzu.
Difosgen jest stosowany w niektórych preparatów laboratoryjnych, ponieważ jest łatwiejszy w obsłudze niż fosgenu.
Rola w walce
Difosgen został pierwotnie opracowany jako środek płuc do wojny chemicznej , kilka miesięcy po pierwszym użyciu fosgenu. Był on używany jako gaz trujący w artyleryjskich pocisków przez Niemcy w czasie I wojny światowej . Pierwsze odnotowane użycie bitwy było w maju 1916 roku został opracowany difosgen ponieważ opary mogłyby zniszczyć filtry w maskach gazowych w użyciu w tym czasie.
Bezpieczeństwo
Difosgen ma stosunkowo wysokie ciśnienie pary 10 mmHg (1,3 kPa) w temperaturze 20 ° C i rozkłada się fosgen około 300 ° C. Narażenie na difosgen jest podobny do zagrożenia fosgen i MSDS powinny być konsultowane.
Zobacz też
Referencje
Linki zewnętrzne
- Podręcznik opieki medycznej .
- Podręcznik NATO , zawiera porady leczenie
- arkusz materiału bezpieczeństwo danych (PDF, do fosgenu i difosgen traktowane jako jedno).
- MSDS dla difosgen specjalnie
