Rak endometrium - Endometrial cancer
| Rak endometrium | |
|---|---|
| Inne nazwy | Rak macicy |
 | |
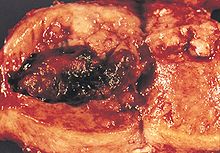
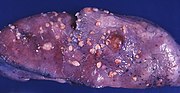
| Lokalizacja i rozwój raka endometrium. | |
| Specjalność | Onkologia , ginekologia |
| Objawy | Krwawienie z pochwy , ból podczas oddawania moczu lub stosunku płciowego , ból miednicy |
| Zwykły początek | Po menopauzie |
| Czynniki ryzyka | Otyłość , nadmierna ekspozycja na estrogeny , wysokie ciśnienie krwi , cukrzyca , wywiad rodzinny |
| Metoda diagnostyczna | Biopsja endometrium |
| Leczenie | Histerektomia brzuszna , radioterapia , chemioterapia , terapia hormonalna |
| Rokowanie | Przeżycie pięcioletnie ~80% (USA) |
| Częstotliwość | 3,8 mln (łącznie dotknięte w 2015 r.) |
| Zgony | 89 900 (2015) |
Rak śluzówki macicy jest rakiem , który powstaje z błony śluzowej macicy (The okładziny z macicy lub macicy). Jest to wynik nieprawidłowego wzrostu komórek, które mają zdolność do inwazji lub rozprzestrzeniania się na inne części ciała. Pierwszym objawem jest najczęściej krwawienie z pochwy niezwiązane z miesiączką . Inne objawy to ból przy oddawaniu moczu , ból podczas stosunku płciowego lub ból miednicy . Rak endometrium występuje najczęściej po menopauzie .
Około 40% przypadków dotyczy otyłości . Rak endometrium wiąże się również z nadmierną ekspozycją na estrogeny , wysokim ciśnieniem krwi i cukrzycą . Podczas gdy przyjmowanie samego estrogenu zwiększa ryzyko raka endometrium, przyjmowanie zarówno estrogenu, jak i progestagenu w połączeniu, jak w przypadku większości tabletek antykoncepcyjnych , zmniejsza to ryzyko. Od dwóch do pięciu procent przypadków dotyczy genów odziedziczonych po rodzicach. Rak endometrium jest czasami luźno określany jako „ rak macicy ”, chociaż różni się od innych postaci raka macicy, takich jak rak szyjki macicy , mięsak macicy i choroba trofoblastyczna . Najczęstszym typem raka endometrium jest rak endometrioidalny , który stanowi ponad 80% przypadków. Rak endometrium jest powszechnie diagnozowany poprzez biopsję endometrium lub pobieranie próbek podczas procedury zwanej rozszerzeniem i łyżeczkowaniem . Cytologiczne nie jest zazwyczaj wystarczająca, aby pokazać raka endometrium. Regularne badania przesiewowe u osób z normalnym ryzykiem nie są wymagane.
Wiodącą opcją leczenia raka endometrium jest histerektomia brzuszna (całkowite usunięcie chirurgiczne macicy) wraz z usunięciem jajowodów i obustronnych jajników , tzw. obustronne wycięcie jajowodów . W bardziej zaawansowanych przypadkach można również zalecić radioterapię , chemioterapię lub terapię hormonalną . Jeśli choroba zostanie zdiagnozowana we wczesnym stadium , wynik jest korzystny, a ogólny pięcioletni wskaźnik przeżycia w Stanach Zjednoczonych wynosi ponad 80%.
W 2012 roku nowotwory endometrium pojawiły się u 320 000 kobiet i spowodowały 76 000 zgonów. To sprawia, że jest to trzecia najczęstsza przyczyna zgonów w przypadku nowotworów, które dotykają tylko kobiety, za rakiem jajnika i szyjki macicy. Jest bardziej powszechny w krajach rozwiniętych i jest najczęstszym nowotworem żeńskiego układu rozrodczego w krajach rozwiniętych. Wskaźniki zachorowań na raka endometrium wzrosły w wielu krajach między latami 80. a 2010 r. Uważa się, że jest to spowodowane rosnącą liczbą osób starszych i rosnącym wskaźnikiem otyłości.
Symptomy i objawy
Krwawienie z pochwy lub plamienie u kobiet po menopauzie występuje w 90% przypadków raka endometrium. Krwawienie jest szczególnie częste w przypadku gruczolakoraka , występujące w dwóch trzecich wszystkich przypadków. Nieprawidłowe cykle miesiączkowe lub wyjątkowo długie, obfite lub częste epizody krwawienia u kobiet przed menopauzą mogą również być oznaką raka endometrium.
Objawy inne niż krwawienie nie są powszechne. Inne objawy obejmują cienką, białą lub przejrzystą wydzielinę z pochwy u kobiet po menopauzie. Bardziej zaawansowana choroba wykazuje bardziej oczywiste objawy lub oznaki, które można wykryć w badaniu fizykalnym . Macica może się powiększyć lub rak może się rozprzestrzeniać, powodując ból w dole brzucha lub skurcze miednicy. Bolesny stosunek płciowy lub bolesne lub trudne oddawanie moczu to rzadsze objawy raka endometrium. Macica może również wypełniać się ropą ( pyometrea ). Spośród kobiet z tymi rzadszymi objawami (wydzielina z pochwy, ból miednicy i ropa) 10-15% ma raka.
Czynniki ryzyka
Czynniki ryzyka raka endometrium obejmują otyłość , cukrzycę , raka piersi , stosowanie tamoksyfenu , brak dziecka , późną menopauzę, wysoki poziom estrogenu i podeszły wiek. Badania imigracyjne (badania migracyjne), które badają zmianę ryzyka zachorowania na raka w populacjach przemieszczających się między krajami o różnym stopniu zachorowania na raka, pokazują, że istnieje pewien element środowiskowy raka endometrium. Te środowiskowe czynniki ryzyka nie są dobrze scharakteryzowane.
Hormony
Większość czynników ryzyka raka endometrium wiąże się z wysokim poziomem estrogenów. Uważa się, że około 40% przypadków ma związek z otyłością. W otyłości nadmiar tkanki tłuszczowej zwiększa konwersję androstendionu do estronu , estrogenu. Wyższy poziom estronu we krwi powoduje mniejszą lub brak owulacji i naraża endometrium na stale wysokie poziomy estrogenów. Otyłość powoduje również, że z krwi usuwa się mniej estrogenu. Zespół policystycznych jajników (PCOS), który również powoduje nieregularną lub brak owulacji, wiąże się z wyższymi wskaźnikami raka endometrium z tych samych powodów, co otyłość. W szczególności otyłość, cukrzyca typu II i insulinooporność są czynnikami ryzyka raka endometrium typu I. Otyłość zwiększa ryzyko raka endometrium o 300–400%.
Estrogenowa terapia zastępcza w okresie menopauzy, gdy nie jest zrównoważona (lub „przeciwstawiana”) progestynem, jest kolejnym czynnikiem ryzyka. Wyższe dawki lub dłuższe okresy terapii estrogenowej wiążą się z wyższym ryzykiem raka endometrium. Kobiety o mniejszej wadze są bardziej narażone na działanie estrogenów bez przeciwstawiania się. Dłuższy okres płodności – zarówno od wczesnej pierwszej miesiączki, jak i późnej menopauzy – jest również czynnikiem ryzyka. Estrogen, który nie jest zwalczany, zwiększa ryzyko zachorowania na raka endometrium 2–10-krotnie, w zależności od masy ciała i długości terapii. U trans mężczyzn, którzy przyjmują testosteron i nie przeszli histerektomii, konwersja testosteronu do estrogenu za pośrednictwem androstendionu może prowadzić do większego ryzyka raka endometrium.
Genetyka
Zaburzenia genetyczne mogą również powodować raka endometrium. Ogólnie przyczyny dziedziczne przyczyniają się do 2–10% przypadków raka endometrium. Zespół Lyncha , autosomalne dominujące zaburzenie genetyczne, które powoduje głównie raka jelita grubego , powoduje również raka endometrium, zwłaszcza przed menopauzą. Kobiety z zespołem Lyncha mają 40-60% ryzyko zachorowania na raka endometrium, wyższe niż ryzyko zachorowania na raka jelita grubego (jelita) lub jajnika. Rak jajnika i endometrium rozwija się jednocześnie u 20% osób. Rak endometrium prawie zawsze rozwija się przed rakiem jelita grubego, średnio 11 lat wcześniej. Karcynogeneza w zespole Lyncha pochodzi z mutacji w genach MLH1 lub MLH2 , które uczestniczą w procesie naprawy niedopasowania , który umożliwia komórce korygowanie błędów w DNA. Inne geny zmutowane w zespole Lyncha obejmują MSH2 , MSH6 i PMS2 , które są również genami naprawy niedopasowania. Kobiety z zespołem Lyncha stanowią 2-3% przypadków raka endometrium; niektóre źródła podają, że to nawet 5%. W zależności od mutacji genu kobiety z zespołem Lyncha mają różne ryzyko raka endometrium. W przypadku mutacji MLH1 ryzyko wynosi 54%; z MSH2, 21%; a z MSH6 16%.
Kobiety z rodzinną historią raka endometrium są bardziej zagrożone. Dwa geny najczęściej związane z niektórymi innymi nowotworami kobiecymi, BRCA1 i BRCA2 , nie powodują raka endometrium. Istnieje wyraźny związek z tymi genami, ale można to przypisać stosowaniu tamoksyfenu, leku, który sam może powodować raka endometrium w przypadku raka piersi i jajnika. Dziedziczny stan genetyczny Zespół Cowdena może również powodować raka endometrium. Kobiety z tym zaburzeniem mają 5-10% ryzyka zachorowania na raka endometrium w ciągu całego życia, w porównaniu do 2-3% ryzyka u kobiet zdrowych.
Stwierdzono również, że powszechna zmienność genetyczna wpływa na ryzyko raka endometrium w zakrojonych na szeroką skalę badaniach asocjacyjnych całego genomu . Szesnaście regionów genomowych powiązano z rakiem endometrium, a powszechne warianty wyjaśniają do 7% rodzinnego ryzyka względnego.
Inne problemy zdrowotne
Niektóre terapie innych form raka zwiększają ryzyko zachorowania na raka endometrium w ciągu całego życia, które wynosi od 2 do 3%. Tamoksyfen, lek stosowany w leczeniu raka piersi z dodatnim estrogenem , jest związany z rakiem endometrium u około 0,1% kobiet, zwłaszcza starszych kobiet, ale korzyści dla przeżycia z tamoksyfenu na ogół przewyższają ryzyko raka endometrium. Jeden do dwóch lat leczenia tamoksyfenem w przybliżeniu podwaja ryzyko raka endometrium, a pięcioletni kurs leczenia zwiększa to ryzyko czterokrotnie. Podobny lek, raloksyfen , nie zwiększał ryzyka raka endometrium. Wcześniejszy rak jajnika jest czynnikiem ryzyka raka endometrium, podobnie jak wcześniejsza radioterapia miednicy. W szczególności guzy z komórek ziarnistych jajnika i błoniaki są guzami związanymi z rakiem endometrium.
Niska funkcja immunologiczna ma również związek z rakiem endometrium. Wysokie ciśnienie krwi jest również czynnikiem ryzyka, ale może to wynikać z jego związku z otyłością. Regularne siedzenie przez dłuższy czas wiąże się z wyższą śmiertelnością z powodu raka endometrium. Ryzyko nie jest niwelowane przez regularne ćwiczenia, choć jest ono obniżone.
Czynniki ochronne
Palenie i stosowanie progestyny chronią przed rakiem endometrium. Palenie zapewnia ochronę poprzez zmianę metabolizmu estrogenu oraz promowanie utraty wagi i wczesnej menopauzy. Ten efekt ochronny utrzymuje się długo po zaprzestaniu palenia. Progestyna jest obecna w złożonej doustnej pigułce antykoncepcyjnej i hormonalnej wkładce domacicznej (IUD). Złożone doustne środki antykoncepcyjne zmniejszają ryzyko tym bardziej im dłużej są stosowane: o 56% po czterech latach, 67% po ośmiu latach i 72% po dwunastu latach. To zmniejszenie ryzyka trwa przez co najmniej piętnaście lat po zaprzestaniu stosowania antykoncepcji. Otyłe kobiety mogą potrzebować większych dawek progestyny, aby być chronionym. Posiadanie więcej niż pięciu niemowląt (wielka liczba dzieci) jest również czynnikiem ochronnym, a posiadanie co najmniej jednego dziecka zmniejsza ryzyko o 35%. Karmienie piersią przez ponad 18 miesięcy zmniejsza ryzyko o 23%. Zwiększona aktywność fizyczna zmniejsza indywidualne ryzyko o 38-46%. Istnieją wstępne dowody na to, że spożywanie soi ma działanie ochronne.
Patofizjologia
|
Rak endometrium powstaje, gdy występują błędy w prawidłowym wzroście komórek endometrium . Zwykle, gdy komórki starzeją się lub ulegają uszkodzeniu, umierają , a ich miejsce zajmują nowe komórki. Rak zaczyna się, gdy nowe komórki tworzą się niepotrzebnie, a stare lub uszkodzone komórki nie umierają tak, jak powinny. Nagromadzenie dodatkowych komórek często tworzy masę tkanki zwaną wzrostem lub guzem. Te nieprawidłowe komórki rakowe mają wiele nieprawidłowości genetycznych, które powodują ich nadmierny wzrost.
W 10–20% raków endometrium, głównie stopnia 3 (najwyższy stopień histologiczny ), stwierdza się mutacje w genie supresorowym nowotworu , zwykle p53 lub PTEN . W 20% przerostów endometrium i 50% nowotworów endometrioidalnych PTEN cierpi na mutację powodującą utratę funkcji lub mutację zerową , co czyni ją mniej skuteczną lub całkowicie nieskuteczną. Utrata funkcji PTEN prowadzi do regulacji w górę szlaku PI3k/Akt/mTOR, co powoduje wzrost komórek. Szlak p53 może być albo stłumiony, albo silnie aktywowany w raku endometrium. Kiedy zmutowana wersja p53 ulega nadekspresji, rak jest szczególnie agresywny. Mutacje P53 i niestabilność chromosomów są związane z nowotworami surowiczymi, które przypominają nowotwory jajnika i jajowodu. Uważa się, że raki surowicze rozwijają się z raka śródnabłonkowego endometrium .
Mutacje związane z utratą funkcji PTEN i p27 są związane z dobrym rokowaniem, szczególnie u otyłych kobiet. HER-2 / neu oncogene , co oznacza, ze złym rokowaniem, wyraża się w 20% i surowiczego raka endometrialnego. Mutacje CTNNB1 (beta-katenina; gen transkrypcyjny ) stwierdza się w 14–44% raków endometrium i mogą wskazywać na dobre rokowanie, ale dane są niejasne. Mutacje beta-kateniny są często spotykane w rakach endometrium z komórkami płaskonabłonkowymi . Mutacje FGFR2 stwierdza się w około 10% raków endometrium, a ich znaczenie prognostyczne jest niejasne. SPOP to kolejny gen supresorowy guza, który w niektórych przypadkach raka endometrium jest zmutowany: 9% jasnokomórkowych raków endometrium i 8% surowiczych raków endometrium ma mutacje w tym genie.
Raki typu I i typu II (wyjaśnione poniżej) mają zwykle różne mutacje. ARID1A, który często zawiera mutację punktową w raku endometrium typu I, jest również zmutowany w 26% raków jasnokomórkowych endometrium i 18% raków surowiczych. Wyciszanie epigenetyczne i mutacje punktowe kilku genów są powszechnie spotykane w raku endometrium typu I. Mutacje w genach supresorowych guza są powszechne w raku endometrium typu II. PIK3CA jest powszechnie zmutowany w rakach typu I i typu II. U kobiet z rakiem endometrium związanym z zespołem Lyncha często występuje niestabilność mikrosatelitarna .
Rozwój hiperplazji endometrium (przerost komórek endometrium) jest istotnym czynnikiem ryzyka, ponieważ hiperplazja może i często rozwija się w gruczolakoraka, chociaż rak może rozwijać się bez obecności hiperplazji. W ciągu dziesięciu lat 8–30% atypowych przerostów endometrium przekształca się w raka, podczas gdy w przypadku nieatypowych przerostów – 1–3%. Rozrost atypowy to taki, w którym widoczne są nieprawidłowości w jądrach . Przedrakowe przerosty endometrium są również określane jako śródnabłonkowa neoplazja endometrium . Mutacje w genie KRAS mogą powodować przerost endometrium, a tym samym raka endometrium typu I. Hiperplazja endometrium występuje zwykle po 40 roku życia. Dysplazja gruczołów endometrium występuje z nadekspresją p53 i rozwija się w raka surowiczego.
Diagnoza
Rozpoznanie raka endometrium stawia się najpierw poprzez badanie fizykalne, biopsję endometrium lub rozszerzenie i łyżeczkowanie (usunięcie tkanki endometrium; D&C). Tkanka ta jest następnie badana histologicznie pod kątem cech raka. W przypadku wykrycia raka można wykonać obrazowanie medyczne, aby sprawdzić, czy rak rozprzestrzenił się lub zaatakował tkankę.
Badanie
Rutynowe badania przesiewowe osób bezobjawowych nie są wskazane, ponieważ choroba jest wysoce uleczalna we wczesnych, objawowych stadiach. Zamiast tego kobiety, szczególnie kobiety w okresie menopauzy, powinny być świadome objawów i czynników ryzyka raka endometrium. Badanie przesiewowe szyjki macicy , takie jak wymaz Pap , nie jest użytecznym narzędziem diagnostycznym w przypadku raka endometrium, ponieważ rozmaz będzie prawidłowy w 50% przypadków. Rozmaz Pap może wykryć chorobę, która rozprzestrzeniła się na szyjkę macicy. Wyniki badania miednicy często są prawidłowe, zwłaszcza we wczesnych stadiach choroby. Zmiany w wielkości, kształcie lub konsystencji macicy lub otaczających ją struktur podtrzymujących mogą wystąpić, gdy choroba jest bardziej zaawansowana. Zwężenie szyjki macicy, zwężenie ujścia szyjki macicy, jest oznaką raka endometrium, gdy w macicy znajduje się ropa lub krew (pyometra lub hematometra ).
Kobiety z zespołem Lyncha powinny rozpocząć coroczne badanie biopsyjne w wieku 35 lat. Niektóre kobiety z zespołem Lyncha decydują się na profilaktyczną histerektomię i salpingooforektomię, aby znacznie zmniejszyć ryzyko raka endometrium i jajnika.
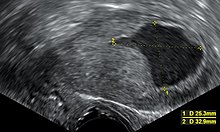
USG przezpochwowe w celu zbadania grubości endometrium u kobiet z krwawieniem po menopauzie jest coraz częściej stosowane w diagnostyce raka endometrium w Stanach Zjednoczonych. W Wielkiej Brytanii zarówno biopsja endometrium , jak i przezpochwowe USG stosowane łącznie są standardem postępowania w diagnostyce raka endometrium. Jednorodność tkanki widoczna w ultrasonografii przezpochwowej może pomóc w określeniu, czy grubość jest rakowata. Same wyniki badań ultrasonograficznych nie są rozstrzygające w przypadku raka endometrium, dlatego należy w połączeniu zastosować inną metodę przesiewową (na przykład biopsję endometrium). Inne badania obrazowe mają ograniczone zastosowanie. Skany CT są wykorzystywane do przedoperacyjnego obrazowania guzów, które w badaniu fizykalnym wydają się zaawansowane lub mają podtyp wysokiego ryzyka (z wysokim ryzykiem przerzutów ). Mogą być również wykorzystywane do badania chorób pozamiednicowych. MRI może się przydać przy ustalaniu, czy nowotwór rozprzestrzenił się na szyjce macicy lub jeśli jest to gruczolakorak kanału szyjki macicy. MRI jest również przydatny do badania pobliskich węzłów chłonnych.
Rozszerzenie i łyżeczkowanie lub biopsja endometrium służą do uzyskania próbki tkanki do badania histologicznego. Biopsja endometrium jest opcją mniej inwazyjną, ale może nie dawać jednoznacznych wyników za każdym razem. Histeroskopia pokazuje jedynie grubą anatomię endometrium, która często nie wskazuje na raka i dlatego nie jest stosowana, chyba że w połączeniu z biopsją. Histeroskopię można wykorzystać do potwierdzenia diagnozy raka. Nowe dowody wskazują, że D&C ma wyższy odsetek wyników fałszywie ujemnych niż biopsja endometrium.
Przed rozpoczęciem leczenia zaleca się wykonanie kilku innych badań. Obejmują one rentgenowskie klatki piersiowej, badania funkcji wątroby , badania funkcji nerek oraz badanie pod kątem poziomu CA-125 , o markera nowotworowego , który może być podwyższona w przypadku raka endometrium.
Klasyfikacja
Raki endometrium mogą być nowotworami wywodzącymi się z komórek nabłonkowych (raki), mieszanymi nowotworami nabłonkowymi i mezenchymalnymi (carcinosarcoma) lub nowotworami mezenchymalnymi.
Tradycyjna klasyfikacja raków endometrium opiera się na cechach klinicznych i endokrynnych (Typ I i Typ II) lub histopatologicznych (endometrioidalne, surowicze i jasnokomórkowe). Niektóre nowotwory są trudne do sklasyfikowania i mają cechy nakładające się na więcej niż jedną kategorię. W szczególności guzy endometrioidalne o wysokim stopniu złośliwości mają zwykle cechy zarówno typu I, jak i typu II.
Rak
Zdecydowana większość nowotworów endometrium to raki (zwykle gruczolakoraki), co oznacza, że wywodzą się z pojedynczej warstwy komórek nabłonka , które wyściełają endometrium i tworzą gruczoły endometrium. Istnieje wiele mikroskopowych podtypów raka endometrium, ale są one ogólnie podzielone na dwie kategorie, Typ I i Typ II, w oparciu o cechy kliniczne i patogenezę. Te dwa podtypy są odmienne genetycznie.
Rak endometrium typu I występuje najczęściej przed menopauzą i w okolicach menopauzy. W Stanach Zjednoczonych są one częstsze u białych kobiet , szczególnie tych z historią przerostu endometrium. Raki endometrium typu I są często o niskim stopniu złośliwości, minimalnie inwazyjne w leżącej poniżej ścianie macicy ( mięśniówce macicy ), są zależne od estrogenów i mają dobre wyniki leczenia. Raki typu I stanowią 75–90% raka endometrium.
Rak endometrium typu II występuje zwykle u osób starszych, po menopauzie, w Stanach Zjednoczonych częściej występuje u kobiet rasy czarnej i nie wiąże się ze zwiększoną ekspozycją na estrogeny ani przerostem endometrium w wywiadzie. Raki endometrium typu II są często o wysokim stopniu złośliwości, z głęboką inwazją do leżącej poniżej ściany macicy (myometrium), są typu surowiczego lub jasnokomórkowego i wiążą się z gorszym rokowaniem. W ocenie objawów mogą wyglądać na nabłonkowego raka jajnika . Mają tendencję do pojawiania się później niż guzy typu I i są bardziej agresywne, z większym ryzykiem nawrotu i/lub przerzutów.
gruczolakorak endometrioidalny
W gruczolakoraku endometrioidalnym komórki rakowe rosną w sposób przypominający prawidłowe endometrium, z wieloma nowymi gruczołami utworzonymi z nabłonka walcowatego z pewnymi nieprawidłowymi jądrami . Gruczolakoraki endometrioidalne o niskim stopniu złośliwości mają dobrze zróżnicowane komórki, nie naciekają mięśniówki macicy i są obserwowane razem z przerostem endometrium. Gruczoły guza tworzą się bardzo blisko siebie, bez tkanki zrębowej , która normalnie je oddziela. Gruczolakorak endometrioidalny wyższego stopnia ma mniej dobrze zróżnicowane komórki, ma bardziej solidne warstwy komórek nowotworowych, które nie są już zorganizowane w gruczoły i są związane z atrofią endometrium. Istnieje kilka podtypów gruczolakoraka endometrialnego o podobnych rokowaniach, w tym warianty komórek kosmkowo-gruczołowych, wydzielniczych i rzęskowych. Istnieje również podtyp charakteryzujący się zróżnicowaniem płaskonabłonkowym . Niektóre gruczolakoraki endometrioidalne mają ogniska raka śluzowego.
Mutacje genetyczne najczęściej związane z gruczolakorakiem endometrialnym znajdują się w genach PTEN, supresor nowotworu; PIK3CA, kinaza ; KRAS, GTPaza działająca w transdukcji sygnału ; oraz CTNNB1, zaangażowane w adhezję i sygnalizację komórkową. Gen CTNNB1 (beta-katenina) jest najczęściej zmutowany w podtypie płaskonabłonkowym gruczolakoraka endometrioidalnego.
Poważny rak
Rak surowiczy jest guzem endometrium typu II, który stanowi 5–10% rozpoznanego raka endometrium i jest powszechny u kobiet po menopauzie z atrofią endometrium i kobiet rasy czarnej. Surowiczy rak endometrium jest agresywny i często atakuje myometrium i daje przerzuty w obrębie otrzewnej (postrzegane jako zbrylanie sieci ) lub układu limfatycznego. Histologicznie występuje z wieloma nietypowymi jądrami, strukturami brodawkowatymi i, w przeciwieństwie do gruczolakoraków endometrioidalnych, komórkami zaokrąglonymi zamiast komórek kolumnowych. Około 30% surowiczych raków endometrium ma również ciała psammoma . Raki surowicze rozprzestrzeniają się inaczej niż większość innych nowotworów endometrium; mogą rozprzestrzeniać się poza macicę bez inwazji mięśniówki macicy.
Mutacje genetyczne obserwowane w raku surowiczym to niestabilność chromosomowa i mutacje w TP53 , ważnym genie supresorowym nowotworu.
Rak jasnokomórkowy
Rak jasnokomórkowy to guz endometrium typu II, który stanowi mniej niż 5% zdiagnozowanego raka endometrium. Podobnie jak rak surowiczokomórkowy, jest zwykle agresywny i ma złe rokowania. Histologicznie charakteryzuje się cechami wspólnymi dla wszystkich czystych komórek : tytułowa przezroczysta cytoplazma po wybarwieniu H&E i widocznymi, odrębnymi błonami komórkowymi. System sygnalizacji komórkowej p53 nie jest aktywny w raku jasnokomórkowym endometrium. Ta forma raka endometrium występuje częściej u kobiet po menopauzie.
rak śluzowy
Raki śluzowe są rzadką postacią raka endometrium, stanowiącą mniej niż 1-2% wszystkich zdiagnozowanych nowotworów endometrium. Śluzowe raki endometrium są najczęściej w I i I stopniu zaawansowania, co daje dobre rokowanie. Zazwyczaj mają dobrze zróżnicowane komórki kolumnowe zorganizowane w gruczoły z charakterystyczną mucyną w cytoplazmie. Raki śluzowe należy odróżnić od gruczolakoraka szyjki macicy .
Rak mieszany lub niezróżnicowany
Raki mieszane to te, które mają zarówno komórki typu I, jak i typu II, z których jedna stanowi co najmniej 10% guza. Należą do nich złośliwy guz mieszany Müllera , który wywodzi się z nabłonka endometrium i ma złe rokowania.
Niezróżnicowane raki endometrium stanowią mniej niż 1-2% rozpoznanych nowotworów endometrium. Mają gorsze rokowanie niż guzy III stopnia. Histologicznie guzy te wykazują arkusze identycznych komórek nabłonkowych bez identyfikowalnego wzoru.
Inne nowotwory
Rak płaskonabłonkowy bez przerzutów i rak przejściowokomórkowy występują bardzo rzadko w endometrium. Rak płaskonabłonkowy endometrium ma złe rokowania. Od czasu scharakteryzowania w 1892 roku w literaturze medycznej odnotowano go mniej niż 100 razy. Aby można było zdiagnozować pierwotnego raka płaskonabłonkowego endometrium (PSCCE), nie może być żadnego innego pierwotnego raka endometrium lub szyjki macicy i nie może on być połączony z nabłonkiem szyjki macicy. Ze względu na rzadkość występowania tego nowotworu nie ma wytycznych dotyczących jego leczenia ani typowego leczenia. Wspólne przyczyny genetyczne pozostają nieopisane. Pierwotne raki przejściowokomórkowe endometrium są jeszcze rzadsze; Do 2008 r. zgłoszono 16 przypadków. Jego patofizjologia i leczenie nie zostały scharakteryzowane. Histologicznie TCCE przypomina raka endometrioidalnego i różni się od innych raków z komórek przejściowych.
Mięsak
W przeciwieństwie do raka endometrium, rzadko występujące mięsaki podścieliskowe endometrium to nowotwory wywodzące się z niegruczołowej tkanki łącznej endometrium. Zazwyczaj są nieagresywne, a jeśli się powtórzą, mogą zająć dekady. Najczęstsze są przerzuty do płuc i jamy miednicy lub otrzewnej. Zazwyczaj mają receptory estrogenowe i/lub progesteronowe. Rokowanie w przypadku mięsaka podścieliska endometrium o niskim stopniu złośliwości jest dobre, z 60–90% 5-letnim przeżyciem. Niezróżnicowany mięsak endometrium o wysokim stopniu złośliwości (HGUS) ma gorsze rokowanie, z wysokim odsetkiem nawrotów i 25% 5-letnim przeżyciem. Rokowanie w HGUS jest podyktowane tym, czy rak zaatakował tętnice i żyły. Bez inwazji naczyń pięcioletnie przeżycie wynosi 83%; spada do 17%, gdy obserwuje się inwazję naczyń. Najlepsze rokowanie ma ESS w stadium I, z 5-letnim przeżyciem 98% i 10-letnim przeżyciem 89%. ESS stanowi 0,2% nowotworów macicy.
Przerzut
Rak endometrium często daje przerzuty do jajników i jajowodów, gdy nowotwór znajduje się w górnej części macicy, a szyjki macicy, gdy nowotwór znajduje się w dolnej części macicy. Rak zwykle najpierw rozprzestrzenia się na mięśniówkę macicy i błonę surowiczą , a następnie na inne struktury rozrodcze i miednicy. Kiedy zajęty jest układ limfatyczny , węzły miednicy i okołoaortalne są zwykle zajęte jako pierwsze, ale bez określonego wzorca, w przeciwieństwie do raka szyjki macicy. Bardziej odległe przerzuty są przenoszone przez krew i często występują w płucach, a także w wątrobie, mózgu i kościach. Rak endometrium daje przerzuty do płuc w 20-25% przypadków, więcej niż jakikolwiek inny rak ginekologiczny.
Histopatologia
Istnieje trzypoziomowy system klasyfikacji histologicznej nowotworów endometrium, od nowotworów z komórkami dobrze zróżnicowanymi (stopień I) do komórek bardzo słabo zróżnicowanych (stopień III). Nowotwory stopnia I są najmniej agresywne i mają najlepsze rokowanie, podczas gdy nowotwory stopnia III są najbardziej agresywne i prawdopodobnie nawracają. Raki stopnia II są pośrednie między stopniami I i III pod względem różnicowania komórek i agresywności choroby.
Histopatologia nowotworów endometrium jest bardzo zróżnicowana. Najczęstszym objawem jest dobrze zróżnicowany gruczolakorak endometrioidalny, który składa się z licznych, małych, stłoczonych gruczołów o różnym stopniu atypii jądra, aktywności mitotycznej i stratyfikacji. Często pojawia się to na tle przerostu endometrium. Gruczolakoraka Franka można odróżnić od hiperplazji atypowej na podstawie wykrycia wyraźnej inwazji zrębu lub gruczołów typu „back-to-back”, które reprezentują nieniszczące zastąpienie zrębu endometrium przez nowotwór. Wraz z postępem choroby dochodzi do infiltracji mięśniówki macicy.
Inscenizacja
Rak endometrium jest klasyfikowany chirurgicznie za pomocą systemu oceny stopnia zaawansowania raka FIGO . System stopniowania FIGO 2009 przedstawia się następująco:
| Scena | Opis |
|---|---|
| IA | Guz ogranicza się do macicy z mniej niż połową inwazji mięśniówki macicy |
| IB | Guz ogranicza się do macicy z ponad połową inwazji mięśniówki macicy |
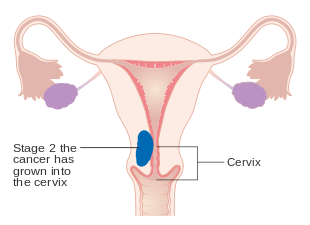
| II | Guz obejmuje macicę i podścielisko szyjne |
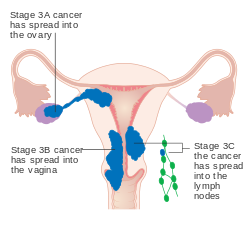
| IIIA | Guz atakuje błonę surowiczą lub przydatki |
| IIIB | Pochwy i / lub parametrial zaangażowanie |
| IIIC1 | Zajęcie węzłów chłonnych miednicy |
| IIIC2 | Zajęcie węzłów chłonnych okołoaortalnych, z zajęciem węzłów miednicy lub bez |
| IVA | Guz nacieka błonę śluzową pęcherza i/lub błonę śluzową jelita |
| IVB | Przerzuty odległe, w tym przerzuty w jamie brzusznej i/lub w węzłach chłonnych pachwinowych |
Inwazja myometrium i zajęcie węzłów chłonnych miednicy i okołoaortalnych są najczęstszymi wzorcami rozprzestrzeniania się. Czasami włączany jest stopień 0, w tym przypadku jest on określany jako „ rak in situ ”. W 26% przypuszczalnie wczesnych stadiów raków śródoperacyjna ocena stopnia zaawansowania wykazała przerzuty do miednicy i odległe, co wymagało kompleksowego określenia stopnia zaawansowania chirurgicznego.
Kierownictwo
Chirurgia
Początkowym leczeniem raka endometrium jest operacja; 90% kobiet z rakiem endometrium jest leczonych jakąś formą operacji. Leczenie chirurgiczne zazwyczaj składa się z histerektomii, w tym obustronnego wycięcia jajników i jajowodów, które polega na usunięciu macicy oraz jajników i jajowodów. Węzłów chłonnych lub usunięcie miednicy i okołoaortalnych węzłów chłonnych , jest wykonana z histologiczne guzów stopnia II lub powyżej. Limfadenektomia jest rutynowo wykonywana we wszystkich stadiach raka endometrium w Stanach Zjednoczonych, ale w Wielkiej Brytanii węzły chłonne są zazwyczaj usuwane tylko w przypadku choroby w stadium II lub wyższym. Temat limfadenektomii i korzyści, jakie daje przeżycie w I stadium choroby, jest wciąż dyskutowany. U kobiet z przypuszczalną chorobą w stadium I w przeglądzie systematycznym z 2017 r. nie znaleziono dowodów na to, że limfadenektomia zmniejsza ryzyko zgonu lub nawrotu raka w porównaniu z brakiem limfadenektomii. Kobiety, które przeszły limfadenektomię, są bardziej narażone na chorobowość ogólnoustrojową związaną z zabiegiem chirurgicznym lub obrzękiem limfatycznym/tworzeniem limfocyst. W III i IV stopniu zaawansowania chirurgia cytoredukcyjna jest normą, można również uwzględnić biopsję sieci . W IV stopniu zaawansowania choroby, gdzie występują przerzuty odległe, w ramach terapii paliatywnej można zastosować zabieg chirurgiczny. Laparotomia , zabieg na otwartym brzuchu, jest tradycyjną procedurą chirurgiczną; jednak u osób z przypuszczalnym pierwotnym rakiem endometrium we wczesnym stadium laparoskopia (operacja przez dziurkę od klucza) wiąże się ze zmniejszoną chorobowością operacyjną i podobnym całkowitym i wolnym od choroby przeżyciem. Zaleca się usunięcie macicy przez brzuch zamiast usuwania macicy przez pochwę, ponieważ daje to możliwość zbadania i uzyskania popłuczyn z jamy brzusznej w celu wykrycia dalszych objawów raka. Inscenizacja raka odbywa się podczas operacji.
Nieliczne przeciwwskazania do zabiegu obejmują nieoperacyjny guz, masywną otyłość, szczególnie ryzykowną operację lub chęć zachowania płodności. Te przeciwwskazania występują w około 5–10% przypadków. Kobiety, które chcą zachować płodność i mają raka w stadium I o niskim stopniu zaawansowania, mogą być leczone progestynami, z równoczesną terapią tamoksyfenem lub bez. Terapię tę można kontynuować do czasu, gdy nowotwór nie zareaguje na leczenie lub do zakończenia ciąży. Perforacja macicy może wystąpić podczas D&C lub biopsji endometrium. Skutki uboczne operacji usunięcia raka endometrium mogą w szczególności obejmować dysfunkcję seksualną, czasowe nietrzymanie moczu i obrzęk limfatyczny , a także częstsze skutki uboczne każdej operacji, w tym zaparcia .
Terapia dodatkowa
Istnieje wiele możliwych terapii dodatkowych. Po operacji można zastosować radioterapię i/lub chemioterapię w przypadku nowotworów wysokiego ryzyka lub raka o wysokim stopniu złośliwości. Nazywa się to terapią adjuwantową .
Chemoterapia
Chemioterapia adiuwantowa to niedawna innowacja, składająca się z kombinacji paklitakselu (lub innych taksanów, takich jak docetaksel ), doksorubicyny (i innych antracyklin ) oraz platyn (w szczególności cisplatyny i karboplatyny ). Stwierdzono, że chemioterapia adiuwantowa zwiększa przeżywalność w stadium III i IV raka bardziej niż dodatkowa radioterapia . Mutacje w genach naprawy niedopasowania, takie jak te występujące w zespole Lyncha, mogą prowadzić do oporności na platyny, co oznacza, że chemioterapia z użyciem platyn jest nieskuteczna u osób z tymi mutacjami. Skutki uboczne chemioterapii są powszechne. Należą do nich wypadanie włosów , niski poziom neutrofili we krwi i problemy żołądkowo-jelitowe.
W przypadkach, gdy operacja nie jest wskazana, alternatywą jest chemioterapia paliatywna ; chemioterapia w wyższych dawkach wiąże się z dłuższym przeżyciem. Chemioterapia paliatywna, zwłaszcza z użyciem kapecytabiny i gemcytabiny , jest również często stosowana w leczeniu nawrotowego raka endometrium.
Dane naukowe o niskiej pewności sugerują, że u kobiet z nawrotowym rakiem endometrium, które przeszły chemioterapię, przyjmowanie leków hamujących szlak mTOR może zmniejszyć ryzyko pogorszenia się choroby w porównaniu z częstszą chemioterapią lub terapią hormonalną. Chociaż inhibitory mTOR mogą zwiększać ryzyko wystąpienia wrzodów przewodu pokarmowego.
Radioterapia
Radioterapia adiuwantowa jest powszechnie stosowana we wczesnym stadium (stadium I lub II) raka endometrium. Może być dostarczana poprzez brachyterapię dopochwową (VBT), która staje się preferowaną drogą ze względu na jej zmniejszoną toksyczność, lub radioterapię wiązką zewnętrzną (EBRT). Brachyterapia polega na umieszczeniu źródła promieniowania w zaatakowanym narządzie; w przypadku raka endometrium źródło promieniowania umieszcza się bezpośrednio w pochwie. Radioterapia wiązką zewnętrzną obejmuje wiązkę promieniowania skierowaną na dotknięty obszar z zewnątrz ciała. VBT stosuje się w leczeniu pozostałego raka wyłącznie w pochwie, podczas gdy EBRT można stosować w leczeniu pozostałego raka w miednicy po operacji. Jednak korzyści z radioterapii adiuwantowej są kontrowersyjne. Chociaż EBRT znacznie zmniejsza częstość nawrotów w miednicy, całkowite przeżycie i wskaźniki przerzutów nie ulegają poprawie. VBT zapewnia lepszą jakość życia niż EBRT.
W niektórych przypadkach radioterapię można również zastosować przed zabiegiem chirurgicznym. Gdy obrazowanie przedoperacyjne lub ocena kliniczna wykażą, że guz nacieka szyjkę macicy, przed wykonaniem całkowitej histerektomii można podać promieniowanie . Brachyterapię i EBRT można również stosować pojedynczo lub w połączeniu, gdy istnieje przeciwwskazanie do histerektomii. Obie metody dostarczania radioterapii wiążą się ze skutkami ubocznymi, szczególnie w przewodzie pokarmowym .
Terapia hormonalna
Terapia hormonalna jest korzystna tylko w niektórych typach raka endometrium. Kiedyś uważano, że jest to korzystne w większości przypadków. Jeśli guz jest dobrze zróżnicowany i wiadomo, że ma receptory progesteronu i estrogenu, w leczeniu można zastosować progestyny. Nie ma dowodów na poparcie stosowania progestagenu oprócz zabiegu chirurgicznego w nowo zdiagnozowanym raku endometrium. Około 25% przerzutowych raków endometrioidalnych wykazuje odpowiedź na progestyny. Również mięsaki podścieliska endometrium można leczyć środkami hormonalnymi, w tym tamoksyfenem, kapronianem hydroksyprogesteronu , letrozolem , octanem megestrolu i medroksyprogesteronem . To leczenie jest skuteczne w mięsakach podścieliska endometrium, ponieważ zazwyczaj mają one receptory estrogenowe i/lub progestynowe . Receptory progestynowe działają jako supresory nowotworu w komórkach raka endometrium. Wstępne badania i próby kliniczne wykazały, że te terapie mają wysoki wskaźnik odpowiedzi nawet w przypadku choroby przerzutowej.
W 2010 roku terapia hormonalna ma niejasny efekt u chorych na zaawansowanego lub nawrotowego raka endometrium. Nie ma wystarczających dowodów, aby informować kobiety rozważające hormonalną terapię zastępczą po leczeniu raka endometrium.
Terapia celowana
Dostarlimab został zatwierdzony przez FDA do leczenia raka endometrium ze specyficznym biomarkerem
Monitorowanie
Marker nowotworowy CA-125 jest często podwyższony w raku endometrium i może być stosowany do monitorowania odpowiedzi na leczenie, szczególnie w przypadku raka surowiczokomórkowego lub zaawansowanej choroby. Okresowe badania MRI lub CT mogą być zalecane w przypadku zaawansowanej choroby, a kobiety z rakiem endometrium w wywiadzie powinny otrzymywać częstsze badania miednicy przez pięć lat po leczeniu. Zaleca się wykonywanie badań co trzy do czterech miesięcy przez pierwsze dwa lata po leczeniu, a przez kolejne trzy lata co sześć miesięcy.
Kobiety z rakiem endometrium nie powinny mieć rutynowego obrazowania kontrolnego w celu monitorowania raka, chyba że pojawią się nowe objawy lub markery nowotworowe zaczną rosnąć. Obrazowanie bez tych wskazań jest odradzane, ponieważ jest mało prawdopodobne, aby wykryć nawrót lub poprawić przeżywalność oraz ponieważ ma swoje własne koszty i skutki uboczne. W przypadku podejrzenia nawrotu zaleca się wykonanie badania PET/CT.
Rokowanie
Współczynniki przeżycia
| Scena | 5-letni wskaźnik przeżycia |
|---|---|
| IA | 88% |
| IB | 75% |
| II | 69% |
| III-A | 58% |
| III-B | 50% |
| III-C | 47% |
| IV-A | 17% |
| IV-B | 15% |
Pięcioletnia przeżywalność gruczolakoraka endometrium po odpowiednim leczeniu wynosi 80%. Większość kobiet, ponad 70%, ma raka w stadium I FIGO, który ma najlepsze rokowanie. Nowotwory III stopnia, a zwłaszcza IV stopnia mają gorsze rokowanie, ale są one stosunkowo rzadkie i występują tylko w 13% przypadków. Mediana czasu przeżycia w przypadku raka endometrium w stadium III–IV wynosi od dziewięciu do dziesięciu miesięcy. Starszy wiek wskazuje na gorsze rokowanie. W Stanach Zjednoczonych białe kobiety mają wyższy wskaźnik przeżywalności niż czarne kobiety, które mają tendencję do rozwijania bardziej agresywnych postaci choroby w momencie postawienia diagnozy. Nowotwory z wysoką ekspresją receptora progesteronowego mają dobre rokowanie w porównaniu z nowotworami z niską ekspresją receptora progesteronowego; 93% kobiet z chorobą wysokiego poziomu receptorów progesteronowych przeżyło do trzech lat, w porównaniu z 36% kobiet z chorobą niskiego poziomu receptorów progesteronowych. Choroby serca są najczęstszą przyczyną śmierci wśród osób, które przeżyły raka endometrium, przy czym powszechne są również inne problemy zdrowotne związane z otyłością. Po postawieniu diagnozy jakość życia wiąże się również pozytywnie ze zdrowym trybem życia (brak otyłości, wysokiej jakości dieta, aktywność fizyczna).
Wskaźniki nawrotów
Nawrót raka endometrium we wczesnym stadium waha się od 3 do 17%, w zależności od leczenia pierwotnego i uzupełniającego. Większość nawrotów (75-80%) występuje poza miednicą, a większość pojawia się w ciągu dwóch do trzech lat leczenia — 64% w ciągu dwóch lat i 87% w ciągu trzech lat.
Raki o wyższym stopniu zaawansowania są bardziej podatne na nawroty, podobnie jak te, które zaatakowały myometrium lub szyjkę macicy lub przerzuty do układu limfatycznego. Rak brodawkowaty surowiczy , rak jasnokomórkowy , a endometrialnego raka są podtypy na najwyższym ryzyku nawrotu. Podtypy histologiczne wysokiego stopnia są również obarczone podwyższonym ryzykiem nawrotu.
Najczęstszym miejscem nawrotu jest pochwa ; Najlepsze rokowanie mają nawroty raka endometrium pochwy. W przypadku nawrotu nowotworu, który nie był leczony promieniowaniem, EBRT jest leczeniem pierwszego rzutu i często jest skuteczne. Jeśli rak leczony promieniowaniem nawraca, wytrzewienie miednicy jest jedyną opcją leczenia. Przeprowadzana jest również paliatywna chemioterapia, chirurgia cytoredukcyjna i radioterapia. Radioterapia (VBT i EBRT) w przypadku nawrotu miejscowego pochwy ma 50% pięcioletni wskaźnik przeżycia. Nawroty miednicy leczy się chirurgicznie i radioterapią, a nawroty brzucha są leczone radioterapią i, jeśli to możliwe, chemioterapią. Innymi częstymi miejscami nawrotów są węzły chłonne miednicy, przyaortalne węzły chłonne, otrzewna (28% nawrotów) i płuca, chociaż nawroty mogą również wystąpić w mózgu (<1%), wątrobie (7%), nadnerczach ( 1%), kości (4–7%; zazwyczaj szkielet osiowy ), węzły chłonne poza brzuchem (0,4–1%), śledziona oraz mięśnie/tkanka miękka (2–6%).
Epidemiologia
Od 2014 r. każdego roku u około 320 000 kobiet na całym świecie diagnozuje się raka endometrium, a 76 000 umiera, co czyni go szóstym najczęściej występującym nowotworem u kobiet. Występuje częściej w krajach rozwiniętych, gdzie ryzyko zachorowania na raka endometrium u kobiet w ciągu życia wynosi 1,6%, w porównaniu z 0,6% w krajach rozwijających się. To występuje w 12,9 obecnie 100.000 kobiet rocznie w krajach rozwiniętych.
W Stanach Zjednoczonych rak endometrium jest najczęściej diagnozowanym nowotworem ginekologicznym, a u kobiet czwartym najczęściej występującym nowotworem ogółem, stanowiącym 6% wszystkich przypadków raka u kobiet. Szacuje się, że w tym kraju na rok 2014 diagnozuje się 52 630 kobiet rocznie, a 8590 umiera z powodu tej choroby. Europa Północna, Europa Wschodnia i Ameryka Północna mają najwyższe wskaźniki zachorowań na raka endometrium, podczas gdy Afryka i Azja Zachodnia mają najniższy wskaźnik. Azja odnotowała 41% diagnoz raka endometrium na świecie w 2012 roku, podczas gdy Europa Północna, Europa Wschodnia i Ameryka Północna łącznie stanowiły 48% diagnoz. W przeciwieństwie do większości nowotworów, liczba nowych przypadków wzrosła w ostatnich latach, w tym wzrost o ponad 40% w Wielkiej Brytanii w latach 1993–2013. Część tego wzrostu może być spowodowana wzrostem wskaźników otyłości w krajach rozwiniętych, co wydłuża życie oczekiwania i niższy wskaźnik urodzeń. Średnie ryzyko zachorowania na raka endometrium w ciągu życia wynosi około 2-3% u osób z macicą. W Wielkiej Brytanii diagnozuje się około 7400 przypadków rocznie, aw UE około 88 000.
Rak endometrium pojawia się najczęściej w okresie okołomenopauzalnym (okres tuż przed, tuż po i w trakcie menopauzy), między 50 a 65 rokiem życia; ogólnie 75% raka endometrium występuje po menopauzie. Kobiety poniżej 40 roku życia stanowią 5% przypadków raka endometrium, a 10–15% przypadków występuje u kobiet poniżej 50 roku życia. Ta grupa wiekowa jest jednocześnie zagrożona rozwojem raka jajnika. Światowy średni wiek diagnozy wynosi 63 lat; w Stanach Zjednoczonych średni wiek rozpoznania to 60 lat. Białe Amerykanki są bardziej narażone na raka endometrium niż czarne Amerykanki, z ryzykiem odpowiednio 2,88% i 1,69% w ciągu całego życia. Kobiety japońsko-amerykańskie i amerykańskie latynoski mają niższe stawki, a rdzenne hawajskie kobiety mają wyższe stawki.
Badania
W trakcie badań jest kilka eksperymentalnych terapii raka endometrium, w tym leczenie immunologiczne, hormonalne i chemioterapeutyczne. Trastuzumab (Herceptin), przeciwciało przeciwko białku Her2, było stosowane w nowotworach, o których wiadomo, że są pozytywne dla onkogenu Her2/neu, ale badania wciąż trwają. Badane są również terapie immunologiczne, szczególnie w przypadku raka surowiczego brodawkowatego macicy.
Nowotwory można analizować za pomocą technik genetycznych (w tym sekwencjonowania DNA i immunohistochemii ) w celu ustalenia, czy można zastosować pewne terapie specyficzne dla zmutowanych genów. Inhibitory PARP są stosowane w leczeniu raka endometrium z mutacjami PTEN, w szczególności mutacjami obniżającymi ekspresję PTEN. Inhibitorem PARP , który wykazuje aktywność przeciw rakowi endometrium , jest olaparyb . Badania w tej dziedzinie trwają od 2010 roku.
Trwają badania nad stosowaniem metforminy , leku przeciwcukrzycowego, u otyłych kobiet z rakiem endometrium przed operacją. Wczesne badania wykazały, że jest skuteczny w spowalnianiu tempa proliferacji komórek rakowych. Wstępne badania wykazały, że przedoperacyjne podanie metforminy może zmniejszyć ekspresję markerów nowotworowych. Nie wykazano, aby długotrwałe stosowanie metforminy zapobiegało rozwojowi raka, ale może poprawić ogólne przeżycie.
Temsirolimus , inhibitor mTOR, jest badany jako potencjalny lek. Badania pokazują, że inhibitory mTOR mogą być szczególnie skuteczne w przypadku nowotworów z mutacjami w PTEN. Ridaforolimus (deforolimus) jest również badany jako lek dla osób, które wcześniej przeszły chemioterapię. Wstępne badania były obiecujące, a badanie fazy II nad ridaforolimusem zostało zakończone do 2013 r. Prowadzono również badania nad skojarzonym leczeniem ridaforolimusem/progestyną w przypadku nawrotowego raka endometrium. Bewacizumab i inhibitory kinazy tyrozynowej , które hamują angiogenezę , są badane jako potencjalne metody leczenia raka endometrium z wysokim poziomem czynnika wzrostu śródbłonka naczyniowego . Ixabepilone jest badany jako możliwa chemioterapia zaawansowanego lub nawrotowego raka endometrium. Obecnie trwają badania nad terapią rzadkiego niezróżnicowanego mięsaka endometrium o wysokim stopniu złośliwości, ponieważ nie ma jeszcze ustalonego standardu leczenia tej choroby. Badane chemioterapie obejmują doksorubicynę i ifosfamid .
Trwają również badania nad większą liczbą genów i biomarkerów, które mogą być powiązane z rakiem endometrium. Badany jest efekt ochronny złożonych doustnych środków antykoncepcyjnych i wkładki wewnątrzmacicznej. Wstępne badania wykazały, że wkładka domaciczna z lewonorgestrelem zakładana na rok w połączeniu z 6 comiesięcznymi wstrzyknięciami hormonu uwalniającego gonadotropiny może zatrzymać lub odwrócić postęp raka endometrium u młodych kobiet; szczególnie złożony hiperplazja atypowa, jednak wyniki były niejednoznaczne. Eksperymentalny lek łączący hormon z doksorubicyną jest również badany pod kątem większej skuteczności w nowotworach z receptorami hormonalnymi. Terapia hormonalna, która jest skuteczna w leczeniu raka piersi, w tym stosowanie inhibitorów aromatazy , jest również badana pod kątem zastosowania w raku endometrium. Jednym z takich leków jest anastrozol , który jest obecnie badany pod kątem nawrotów hormonalnie dodatnich po chemioterapii. Trwają również badania nad hormonalnymi metodami leczenia mięsaków podścieliska endometrium. Obejmuje badania leków, takich jak mifepriston , antagonista progestyny oraz aminoglutetymid i letrozol, dwa inhibitory aromatazy.
Trwają badania nad najlepszą metodą obrazowania do wykrywania i określania stopnia zaawansowania raka endometrium. W chirurgii badania wykazały, że całkowita limfadenektomia miednicy wraz z histerektomią w raku endometrium w stadium 1 nie poprawia przeżycia i zwiększa ryzyko wystąpienia negatywnych skutków ubocznych, w tym obrzęku limfatycznego. Inne badania dotyczą możliwości identyfikacji wartowniczych węzłów chłonnych do biopsji poprzez wstrzyknięcie do guza barwnika, który świeci w świetle podczerwonym . Radioterapia modulowana intensywnością jest obecnie badana i już stosowana w niektórych ośrodkach do stosowania w raku endometrium w celu zmniejszenia skutków ubocznych tradycyjnej radioterapii. Ryzyko nawrotu nie zostało jeszcze określone ilościowo. Trwają również badania nad hiperbaryczną terapią tlenową w celu zmniejszenia skutków ubocznych. Na wyniki badania PORTEC 3 oceniającego łączenie radioterapii adjuwantowej z chemioterapią oczekiwano pod koniec 2014 roku.
Nie ma wystarczających dowodów, aby ustalić, czy osoby z rakiem endometrium odnoszą korzyści z dodatkowych interwencji związanych z zachowaniem i stylem życia, które mają na celu utratę nadwagi.
Historia i kultura
Rak endometrium nie jest powszechnie znany w populacji ogólnej, pomimo częstości występowania. Świadomość objawów jest niska, co może prowadzić do późniejszej diagnozy i gorszego przeżycia.
Bibliografia
Zewnętrzne linki
| Klasyfikacja | |
|---|---|
| Zasoby zewnętrzne |