Kwas heksafluorokrzemowy - Hexafluorosilicic acid
|
|

|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
Kwas heksafluorokrzemowy |
|
|
Systematyczna nazwa IUPAC
Heksafluorokrzemian diwodoru |
|
| Inne nazwy
Kwas fluorokrzemowy, kwas fluorokrzemowy, kwas hydrofluorokrzemowy, fluorek krzemu, kwas fluorokrzemowy, heksafluorosilanodiuid oksoniowy, heksafluorokrzemian oksonium (2−)
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.037.289 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 1778 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| F 6 H 2 Si | |
| Masa cząsteczkowa | 144,091 g·mol -1 |
| Wygląd zewnętrzny | przezroczysty, bezbarwny, dymiący płyn |
| Zapach | kwaśny, ostry |
| Gęstość | 1,22 g/cm 3 (25% roztw.) 1,38 g/cm 3 (35% roztw.) 1,46 g/cm 3 (61% roztw.) |
| Temperatura topnienia | ok. 19°C (66°F; 292 K) (60–70% roztwór) < -30 °C (-22°F; 243 K) (35% roztwór) |
| Temperatura wrzenia | 108,5 ° C (227,3 ° F; 381,6 K) (rozkłada się) |
| mieszalny | |
|
Współczynnik załamania ( n D )
|
1.3465 |
| Struktura | |
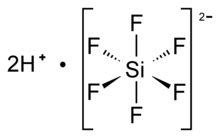
| Oktaedryczny SiF 6 2− | |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna Karta Charakterystyki |
| Piktogramy GHS |

|
| Hasło ostrzegawcze GHS | Zagrożenie |
| H314 | |
| P260 , P264 , P280 , P301+330+331 , P303+361+353 , P304+340 , P305+351+338 , P310 , P321 , P363 , P405 , P501 | |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | Nie palne |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
430 mg/kg (doustnie, szczur) |
| Związki pokrewne | |
|
Inne aniony
|
Kwas heksafluorotytanowy |
|
Inne kationy
|
Heksafluorokrzemian amonu |
|
Związki pokrewne
|
Kwas heksafluorofosforowy Kwas fluoroborowy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Kwas heksafluorokrzemowy jest związkiem nieorganicznym o wzorze chemicznym H
2SiF
6również napisane jako (H
3O)
2[SiF
6] . Jest to bezbarwna ciecz najczęściej spotykana jako rozcieńczony roztwór wodny, stąd też zaproponowano drugą notację chemiczną. Kwas heksafluorokrzemowy ma charakterystyczny kwaśny smak i ostry zapach. Jest produkowany naturalnie na dużą skalę w wulkanach. Powstaje jako współprodukt przy produkcji nawozów fosforowych. Powstały kwas heksafluorokrzemowy jest prawie wyłącznie zużywany jako prekursor trifluorku glinu i syntetycznego kriolitu , które są stosowane w przetwarzaniu aluminium. Sole pochodzące z kwasu heksafluorokrzemowego nazywane są heksafluorokrzemianami .
Struktura
Ogólnie przyjmuje się, że kwas heksafluorokrzemowy składa się z ładunku jonów oksoniowych zrównoważonych przez dianiony heksafluorokrzemianowe oraz wodę. W roztworze wodnym kation hydroniowy (H 3 O + ) jest tradycyjnie utożsamiany z solwatowanym protonem i jako taki wzór tego związku jest często zapisywany jako H
2SiF
6. Rozszerzając tę metaforę, wyizolowany związek jest następnie zapisywany jako H
2SiF
6·2H
2O lub (H
3O)
2SiF
6.The sytuacja jest podobna do tej dla kwasu chloroplatynowego , kwasu fluoroborowego , i kwas heksafluorofosforowy . Heksafluorokrzemian jest anionem oktaedrycznym; odległości wiązania Si–F wynoszą 1,71 Å . Kwas heksafluorokrzemowy jest dostępny w handlu tylko w postaci roztworu.
Produkcja i główne reakcje
Towarowy chemiczny fluorowodór jest wytwarzany z fluorytu poprzez obróbkę kwasem siarkowym . Jako produkt uboczny, w przybliżeniu 50 kg (H 3 O) 2 SiF 6 wytwarzana jest na tonę HF z powodu reakcji z udziałem zanieczyszczeń mineralnych zawierającego krzemionkę. (H 3 O) 2 SiF 6 powstaje również jako produkt uboczny przy produkcji kwasu fosforowego z apatytu i fluoroapatytu . Ponownie, część HF z kolei reaguje z minerałami krzemianowymi, które są nieuniknionym składnikiem surowca mineralnego, dając tetrafluorek krzemu . Utworzony w ten sposób tetrafluorek krzemu dalej reaguje z HF. Proces sieciowy można opisać jako:
-
SiO
2+ 6 HF → SiF2-
6+ 2 godz
3O+
Kwas heksafluorokrzemowy można również wytwarzać przez traktowanie tetrafluorku krzemu kwasem fluorowodorowym.
W wodzie kwas heksafluorokrzemowy łatwo hydrolizuje do kwasu fluorowodorowego i różnych postaci bezpostaciowej i uwodnionej krzemionki („SiO 2 ”). W stężeniu zwykle stosowanym do fluoryzacji wody następuje 99% hydroliza i spada pH. Szybkość hydrolizy wzrasta wraz z pH. Przy pH wody pitnej stopień hydrolizy wynosi zasadniczo 100%.
- H 2 SiF 6 + 2 H 2 O → 6 HF + "SiO 2 "
Neutralizacja roztworów kwasu heksafluorokrzemowego zasadami metali alkalicznych daje odpowiednie sole fluorokrzemianowe metali alkalicznych:
- (H 3 O) 2 SiF 6 + 2 NaOH → Na 2 SiF 6 + 4 H 2 O
Otrzymaną sól sodowa 2 SiF 6 jest stosowany głównie w fluorkowania wody. Pokrewne sole amonu i baru są produkowane podobnie do innych zastosowań.
W pobliżu pH obojętnego sole heksafluorokrzemianowe hydrolizują szybko zgodnie z następującym równaniem:
-
SiF2-
6 + 2 H 2 O → 6 F − + SiO 2 + 4 H +
Zastosowania
Większość kwasu heksafluorokrzemowego jest przekształcana w fluorek glinu i syntetyczny kriolit . Materiały te mają kluczowe znaczenie dla przetwarzania rudy aluminium w metaliczny aluminium . Konwersja do trifluorku glinu jest opisana jako:
- H 2 SiF 6 + Al 2 O 3 → 2 AlF 3 + SiO 2 + H 2 O
Kwas heksafluorokrzemowy jest również przekształcany w różne przydatne sole heksafluorokrzemianowe. Sól potasowa, fluorokrzemian potasu , stosowana jest w produkcji porcelany, sól magnezowa do betonów stwardniałych i jako insektycyd oraz sole barowe do luminoforów.
Kwas heksafluorokrzemowy jest również używany jako elektrolit w procesie elektrolitycznym Bettsa do rafinacji ołowiu.
Kwas heksafluorokrzemowy (oznaczony na etykiecie jako kwas hydrofluorokrzemowy) wraz z kwasem szczawiowym to aktywne składniki używane w produktach czyszczących Iron Out do usuwania rdzy, które są zasadniczo odmianami kwaśnego prania .
Aplikacje niszowe
H 2 SiF 6 to specjalistyczny odczynnik w syntezie organicznej do rozszczepiania wiązań Si–O eterów sililowych . W tym celu jest bardziej reaktywny niż HF. Szybciej reaguje z eterami t - butylodimetylosililowymi ( TBDMS ) niż z eterami triizopropylosililowymi ( TIPS ).
Nałożenie kwasu heksafluorokrzemionkowego na powierzchnię bogatą w wapń, taką jak beton, nada tej powierzchni pewną odporność na atak kwasu.
- CaCO 3 + H 2 O → Ca 2+ + 2 OH - + CO 2
- H 2 SiF 6 → 2 H + + SiF2-
6 -
SiF2-
6 + 2 H 2 O → 6 F − + SiO 2 + 4 H + - Ca 2+ + 2 F − → CaF 2
Fluorek wapnia (CaF 2 ) jest nierozpuszczalnym ciałem stałym odpornym na działanie kwasów.
Kwas heksafluorokrzemowy i jego sole są stosowane jako środki do konserwacji drewna .
sole naturalne
Niektóre rzadkie minerały, spotykane w fumarolach wulkanicznych lub węglowych, to sole kwasu heksafluorokrzemowego. Przykłady obejmują heksafluorokrzemian amonu, który naturalnie występuje jako dwa polimorfy: kryptohalit i bararyt.
Bezpieczeństwo
Kwas heksafluorokrzemowy może uwalniać fluorowodór po odparowaniu, więc wiąże się z podobnym ryzykiem. Wdychanie oparów może powodować obrzęk płuc . Podobnie jak fluorowodór atakuje szkło i kamionkę . LD 50 wartość kwasu heksafluorokrzemowego 430 mg / kg.

