Wodorowęglan - Bicarbonate
|
|

|
|
| Nazwy | |
|---|---|
|
Systematyczna nazwa IUPAC
Wodorotlenek dioksydowęglan (1-) |
|
| Inne nazwy
Wodorowęglan
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| 3DMet | |
| 3903504 | |
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| 49249 | |
| KEGG | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
|
HCO− 3 |
|
| Masa cząsteczkowa | 61,0168 g mol- 1 |
| log P | -0,82 |
| Kwasowość (p K a ) | 10.3 |
| Zasadowość (p K b ) | 7,7 |
| Kwas sprzężony | Kwas węglowy |
| Podstawa sprzężona | Węglan |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
| Referencje do infoboksu | |
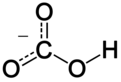
W chemii nieorganicznej , wodorowęglan ( IUPAC -recommended nomenklatury: wodorowęglan ) stanowi kształtka pośrednia w deprotonowanie z kwasem węglowym . Jest anionem wieloatomowym o wzorze chemicznym H C O−
3.
Wodorowęglan pełni kluczową rolę biochemiczną w fizjologicznym systemie buforowania pH .
Termin „wodorowęglan” został wymyślony w 1814 roku przez angielskiego chemika Williama Hyde'a Wollastona . Przedrostek „bi” w „wodorowęglanie” pochodzi z przestarzałego systemu nazewnictwa i opiera się na obserwacji, że jest dwa razy więcej węglanu ( CO2
3) na jon sodu w wodorowęglanie sodu ( NaHCO 3 ) i wodorowęglanach innych niż węglan sodu (Na 2 CO 3 ) i innych węglanach. Imię żyje jako banalne imię .
Właściwości chemiczne
Jon wodorowęglanowy (jon wodorowęglanowy) jest anionem o wzorze empirycznym HCO−
3i masa cząsteczkowa 61,01 daltonów ; składa się z jednego centralnego atomu węgla otoczonego trzema atomami tlenu w układzie trygonalnym planarnym , z atomem wodoru przyłączonym do jednego z tlenów. Jest izoelektroniczny z kwasem azotowym HNO
3. Jon wodorowęglanowy ma ujemny jeden ładunek formalny i jest indywiduum amfiprotycznym, które ma zarówno właściwości kwasowe, jak i zasadowe. Jest to zarówno sprzężonej zasady z kwasem węglowym H
2WSPÓŁ
3; i skoniugowany kwas o CO2
3, jon węglanowy , jak pokazują te reakcje równowagi :
-
WSPÓŁ2
3+ 2 H 2 O ⇌ HCO−
3+ H 2 O + OH − ⇌ H 2 CO 3 + 2 OH −
- H 2 CO 3 + 2 H 2 O ⇌ HCO−
3+ H 3 O + + H 2 O ⇌ CO2
3+ 2 H 3 O + .
Sól wodorowęglanowa tworzy się, gdy dodatnio naładowany jon przyłącza się do ujemnie naładowanych atomów tlenu jonu, tworząc związek jonowy . Wiele wodorowęglanów rozpuszcza się w wodzie w standardowej temperaturze i ciśnieniu ; w szczególności wodorowęglan sodu przyczynia się do całkowitej zawartości rozpuszczonych ciał stałych , co jest powszechnym parametrem oceny jakości wody .
Rola fizjologiczna
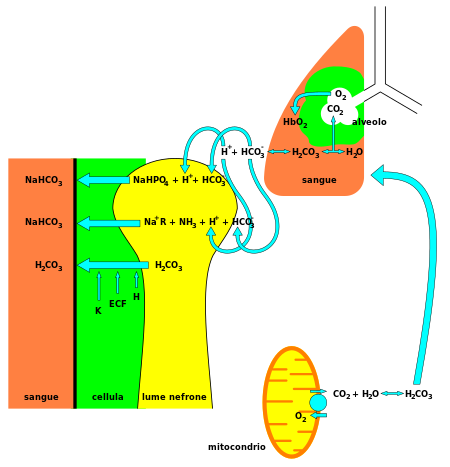
Wodorowęglan ( HCO−
3) jest niezbędnym składnikiem systemu buforowania pH organizmu człowieka (utrzymanie homeostazy kwasowo-zasadowej ). 70% -75% CO 2 w organizmie przekształca się kwas węglowy (H 2 CO 3 ), który jest skoniugowany kwas z HCO−
3 i może szybko się w to zamienić.
Z kwasem węglowym, co centralnych pośrednich gatunków , wodorowęglan - w połączeniu z wodą, jony wodoru i dwutlenku węgla, - formuje ten układ buforujący, który utrzymuje się w stanie równowagi trwałej wymagane zapewnienie szybkiego odporność na zmiany pH w obu kwasowych i zasadowych kierunkach . Jest to szczególnie ważne w celu ochrony tkanek w ośrodkowym układzie nerwowym , w którym wartość pH zmienia się zbyt daleko poza normalny zakres, w obu kierunkach może okazać się fatalne (patrz kwasica lub zasadowicę ).
Dodatkowo wodorowęglan odgrywa kluczową rolę w układzie pokarmowym. Podnosi wewnętrzne pH żołądka po zakończeniu trawienia pokarmu przez wysoce kwaśne soki trawienne. Wodorowęglan działa również w celu regulacji pH w jelicie cienkim. Jest uwalniany z trzustki w odpowiedzi na sekretynę hormonu, która neutralizuje kwaśny treści pokarmowe przedostające się do dwunastnicy z żołądka.
Wodorowęglan w środowisku
Wodorowęglan jest dominującą formą rozpuszczonego węgla nieorganicznego w wodzie morskiej i większości wód słodkich. Jako taki jest ważnym pochłaniaczem w obiegu węgla .
W ekologii słodkowodnej silna aktywność fotosyntetyczna roślin słodkowodnych w świetle dziennym uwalnia gazowy tlen do wody i jednocześnie wytwarza jony wodorowęglanowe. Podnoszą one pH w górę, aż w pewnych okolicznościach stopień zasadowości może stać się toksyczny dla niektórych organizmów lub może sprawić, że inne składniki chemiczne, takie jak amoniak, staną się toksyczne. W ciemności, kiedy nie zachodzi fotosynteza, procesy oddychania uwalniają dwutlenek węgla i nie powstają nowe jony wodorowęglanowe, co powoduje gwałtowny spadek pH.
Inne zastosowania
Najczęstszym soli wodorowęglanowej jonu wodorowęglan sodu , NaHCO 3 , co jest powszechnie znane jako soda oczyszczona . Po podgrzaniu lub wystawieniu na działanie kwasu, takiego jak kwas octowy ( ocet ), wodorowęglan sodu uwalnia dwutlenek węgla . Jest używany jako środek spulchniający w pieczeniu .
Ważną częścią obiegu węgla jest przepływ jonów wodorowęglanowych ze skał wietrzonych przez kwas węglowy zawarty w wodzie deszczowej .
Wodorowęglan amonu jest używany do produkcji herbatników trawiennych .
Diagnostyka
W medycynie diagnostycznej The wartość krwi wodorowęglanu jest jednym z kilku wskaźników stanu równowagi kwasowo-zasadowej fizjologicznych w organizmie. Jest mierzony wraz z dwutlenkiem węgla , chlorkiem , potasem i sodem , aby ocenić poziom elektrolitów w teście elektrolitowym ( opisanym w Current Procedural Terminology , CPT, kod 80051).
Parametr standardowy Stężenie wodorowęglanu (SBC e ) stężenie wodorowęglanu we krwi w P CO 2 40 mm Hg (5,33 kPa), pełne nasycenie tlenem i 36 ° C.
Związki wodorowęglanowe
- Wodorowęglan sodu
- Wodorowęglan potasu
- Wodorowęglan cezu
- Wodorowęglan magnezu
- Wodorowęglan wapnia
- Wodorowęglan amonu
- Kwas węglowy
Zobacz też
Bibliografia
Zewnętrzne linki
- Wodorowęglany w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)
