Białko żelazowo-siarkowe - Iron–sulfur protein
Białka żelazowo-siarkowe (lub białka żelazowo-siarkowe w pisowni brytyjskiej ) to białka charakteryzujące się obecnością klastrów żelazowo-siarkowych zawierających połączone siarczki centra di-, tri- i tetrażelazowe w różnych stopniach utlenienia . Klastry żelazowo-siarkowe znajdują się w różnych metaloproteinach , takich jak ferredoksyny , a także dehydrogenaza NADH , hydrogenazy , koenzym Q – reduktaza cytochromu C , bursztynian – reduktaza koenzymu Q i azotaza. Klastry żelazowo-siarkowe są najlepiej znane ze swojej roli w reakcjach utleniania-redukcji transportu elektronów w mitochondriach i chloroplastach . Zarówno Kompleks I, jak i Kompleks II fosforylacji oksydacyjnej mają wiele klastrów Fe-S. Pełnią one wiele innych funkcji, w tym katalizę, co ilustruje akonitaza , generowanie rodników, co ilustrują enzymy zależne od SAM , oraz jako donory siarki w biosyntezie kwasu liponowego i biotyny . Dodatkowo niektóre białka Fe-S regulują ekspresję genów. Białka Fe-S są podatne na atak biogennego tlenku azotu , tworząc kompleksy dinitrozylo-żelaza . W większości białek Fe-S, końcowe ligandy na Fe są tiolanami , ale istnieją wyjątki.
Występowanie tych białek na szlakach metabolicznych większości organizmów prowadzi niektórych naukowców do teorii, że związki żelaza i siarki odegrały znaczącą rolę w powstawaniu życia w teorii świata żelaza i siarki .
Motywy strukturalne
W prawie wszystkich białkach Fe-S centra Fe są czworościenne, a ligandami końcowymi są centra tiolato-siarkowe z reszt cysteinylowych. Grupy siarczkowe są dwu- lub trójkoordynacyjne. Najczęściej spotykane są trzy różne rodzaje klastrów Fe–S o tych cechach.
Klastry 2Fe–2S
Najprostszy układ polimetaliczny, klaster [Fe 2 S 2 ], składa się z dwóch jonów żelaza połączonych mostkiem z dwoma jonami siarczkowymi i koordynowanych przez cztery ligandy cysteinylowe (w ferredoksynach Fe 2 S 2 ) lub z dwóch cystein i dwóch histydyn (w białkach Rieske'a ). Białka utlenione zawierają dwa jony Fe 3+ , natomiast białka zredukowane zawierają jeden jon Fe 3+ i jeden jon Fe 2+ . Gatunki te występują na dwóch stopniach utlenienia, (Fe III ) 2 i Fe III Fe II . Domena żelazowo-siarkowa CDGSH jest również powiązana z klastrami 2Fe-2S.
Klastry 4Fe–4S
Wspólnym motywem są cztery jony żelaza i cztery jony siarczkowe umieszczone na wierzchołkach gromady typu kubańskiego . Centra Fe są zazwyczaj dodatkowo koordynowane przez ligandy cysteinylowe. W [Fe 4 S 4 ] proteiny transferu elektronów ([Fe 4 S 4 ] ferredoksyna ) może być dalej podzielony na niskim potencjałem (typu bakterii) i wysokim potencjale (HiPIP) ferredoksyna . Ferredoksyny o niskim i wysokim potencjale są powiązane według następującego schematu redoks:
W HiPIP klaster waha się pomiędzy [2Fe 3+ , 2Fe 2+ ] (Fe 4 S 4 2+ ) i [3Fe 3+ , Fe 2+ ] (Fe 4 S 4 3+ ). Potencjały dla tej pary redoks wahają się od 0,4 do 0,1 V. W ferredoksynach bakteryjnych para stanów utlenienia to [Fe 3+ , 3Fe 2+ ] (Fe 4 S 4 + ) i [2Fe 3+ , 2Fe 2+ ] (Fe 4 S 4 2+ ). Potencjały dla tej pary redoks wahają się od -0,3 do -0,7 V. Dwie rodziny klastrów 4Fe-4S mają wspólny stan utlenienia Fe 4 S 4 2+ . Różnicę w parach redoks przypisuje się stopniowi wiązania wodorowego, co silnie modyfikuje zasadowość ligandów tiolanowych cysteinylu. Kolejna para redoks, która jest jeszcze bardziej redukująca niż ferredoksyny bakteryjne, jest zaangażowana w nitrazę .
Niektóre klastry 4Fe-4S wiążą substraty i dlatego są klasyfikowane jako kofaktory enzymów. W akonitazie klaster Fe-S wiąże akonitat w jednym centrum Fe, w którym brakuje liganda tiolanowego. Klaster nie podlega redoks, ale służy jako katalizator kwasu Lewisa do konwersji cytrynianu w izocytrynian . W rodnikowych enzymach SAM klaster wiąże się i redukuje S-adenozylometioninę, tworząc rodnik, który bierze udział w wielu biosyntezach.
Klastry 3Fe–4S
Wiadomo również, że białka zawierają centra [Fe 3 S 4 ], które mają o jedno żelazo mniej niż bardziej powszechne rdzenie [Fe 4 S 4 ]. Trzy jony siarczkowe łączą po dwa jony żelaza, podczas gdy czwarty siarczek łączy trzy jony żelaza. Ich formalne stany utlenienia mogą zmieniać się od [Fe 3 S 4 ] + ( postać all-Fe 3+ ) do [Fe 3 S 4 ] 2- ( postać all-Fe 2+ ). W wielu białkach żelazowo-siarkowych klaster [Fe 4 S 4 ] może zostać odwracalnie przekształcony przez utlenianie i utratę jednego jonu żelaza w klaster [Fe 3 S 4 ]. Np. nieaktywna forma akonitazy posiada [Fe 3 S 4 ] i jest aktywowana przez dodanie Fe 2+ i reduktora.
Inne klastry Fe–S
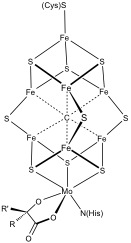
Powszechne są bardziej złożone systemy polimetaliczne. Przykłady obejmują zarówno 8FE i klastrów 7fe w nitrogenozy . Tlenek węgla dehydrogenazy a [fefe] - hydrogenaza wyposażone są niezwykłe klastrów Fe-S. W tolerujących tlen hydrogenazach [NiFe] związanych z błoną znaleziono specjalny, skoordynowany z 6 cysteiną klaster [Fe 4 S 3 ].
Biosynteza
Biosynteza klastrów Fe–S została dobrze zbadana. Biogenezę skupisk żelaza i siarki badano najszerzej w bakteriach E. coli i A. vinelandii oraz drożdżach S. cerevisiae . Do tej pory zidentyfikowano co najmniej trzy różne systemy biosyntetyczne, a mianowicie systemy nif, suf i isc, które po raz pierwszy zidentyfikowano u bakterii. System nif odpowiada za klastry w enzymie nitrazie. Systemy suf i isc są bardziej ogólne.
Najlepiej opisany jest system isc drożdży. Kilka białek tworzy maszynerię biosyntetyczną poprzez szlak isc. Proces przebiega w dwóch głównych etapach: (1) klaster Fe/S jest składany na białku szkieletowym, po czym następuje (2) przeniesienie uformowanego klastra na białka biorcy. Pierwszy etap tego procesu zachodzi w cytoplazmie w prokariotycznych organizmy albo w mitochondriach eukariotycznych organizmów. W organizmach wyższych klastry są zatem transportowane z mitochondrium, aby zostać włączone do enzymów pozamitochondrialnych. Organizmy te posiadają również zestaw białek zaangażowanych w procesy transportu i włączania klastrów Fe/S, które nie są homologiczne do białek występujących w układach prokariotycznych.
Syntetyczne analogi
Syntetyczne analogi naturalnie występujących klastrów Fe-S zostały po raz pierwszy opisane przez Holma i współpracowników. Leczenie soli żelaza mieszaniną tiolany i zapewnia siarczkowych pochodnych, takich jak ( Et 4 N ) 2 Fe 4 S 4 (SCH 2 Ph) 4 ].
Zobacz też
Bibliografia
Dalsza lektura
- Beinert, H. (2000). „Białka żelazowo-siarkowe: starożytne struktury, wciąż pełne niespodzianek”. J. Biol. Inorg. Chem . 5 (1): 2–15. doi : 10.1007/s007750050002 . PMID 10766431 . S2CID 20714007 .
- Beinert, H.; Kiley, PJ (1999). „Białka Fe-S w funkcjach wykrywania i regulacji”. Aktualn. Opinia. Chem. Biol . 3 (2): 152–157. doi : 10.1016/S1367-5931(99)80027-1 . PMID 10226040 .
- Johnsona, MK (1998). „Białka żelaza i siarki: nowe role dla starych klastrów”. Aktualn. Opinia. Chem. Biol . 2 (2): 173–181. doi : 10.1016/S1367-5931(98)80058-6 . PMID 9667933 .
- Komitet Nomenklatury Międzynarodowej Unii Biochemii (NC-IUB) (1979). „Nomenklatura białek żelazowo-siarkowych. Zalecenia 1978” . Eur. J. Biochem . 93 (3): 427–430. doi : 10.1111/j.1432-1033.1979.tb12839.x . PMID 421685 .
- L. Noodleman, T. Lovell, T. Liu, F. Himo i RA Torres (2002). „Wgląd w właściwości i energetykę białek żelazowo-siarkowych od prostych klastrów do nitrazy”. Aktualn. Opinia. Chem. Biol . 6 (2): 259–273. doi : 10.1016/S1367-5931(02)00309-5 . PMID 12039013 .CS1 maint: wiele nazwisk: lista autorów ( link )
- Spiro, TG, wyd. (1982). Białka żelazowo-siarkowe . Nowy Jork: Wiley. Numer ISBN 0-471-07738-0.CS1 maint: wiele nazwisk: lista autorów ( link )
Zewnętrzne linki
- Żelazo-siarka + białka w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)
- Przykłady klastrów żelazowo-siarkowych


