Hormon luteinizujący - Luteinizing hormone
| Gonadotropina kosmówkowa alfa | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | CGA | ||||||
| Alt. symbolika | HCG, GPHa, GPHA1 | ||||||
| Gen NCBI | 1081 | ||||||
| HGNC | 1885 | ||||||
| OMIM | 118850 | ||||||
| RefSeq | NM_000735 | ||||||
| UniProt | P01215 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 6 kw.14-k.21 | ||||||
| |||||||
| Polipeptyd beta hormonu luteinizującego | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | LHB | ||||||
| Gen NCBI | 3972 | ||||||
| HGNC | 6584 | ||||||
| OMIM | 152780 | ||||||
| RefSeq | NM_000894 | ||||||
| UniProt | P01229 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 19 q13.3 | ||||||
| |||||||
Hormon luteinizujący ( LH , znany również jako Lutropina a czasem lutrophin ) jest hormon wytwarzany przez komórkach gonadotropowych w The przedniej przysadki . Produkcja LH jest regulowana przez hormon uwalniający gonadotropiny (GnRH) z podwzgórza. U kobiet gwałtowny wzrost LH (" wzrost LH ") powoduje owulację i rozwój ciałka żółtego . U mężczyzn, u których LH był również nazywany hormonem stymulującym komórki śródmiąższowe ( ICSH ), stymuluje produkcję testosteronu przez komórki Leydiga . Działa synergistycznie z hormonem folikulotropowym ( FSH ).
Struktura
LH hetero dimeryczny glikoproteiny . Każda jednostka monomeryczna jest cząsteczką glikoproteiny ; jedna podjednostka alfa i jedna beta tworzą pełne, funkcjonalne białko.
Jego struktura jest podobna do innych hormonów glikoproteinowych, hormonu folikulotropowego (FSH), hormonu tyreotropowego (TSH) i ludzkiej gonadotropiny kosmówkowej (hCG). Dimer białkowy zawiera 2 podjednostki glikopeptydowe (oznaczone podjednostki alfa i beta), które są niekowalencyjnie związane:
- W podjednostek alfa z FSH, LH, TSH oraz hCG są identyczne i zawierają 92 aminokwasom u ludzi, ale 96 aminokwasom w prawie wszystkich innych gatunków kręgowców (hormony glikoproteinowe nie występują u bezkręgowców).
- Te podjednostki beta różnić. LH posiada podjednostkę beta składającą się ze 120 aminokwasów (LHB), która nadaje mu specyficzne działanie biologiczne i jest odpowiedzialna za specyficzność oddziaływania z receptorem LH . Ta podjednostka beta zawiera sekwencję aminokwasową, która wykazuje dużą homologię z podjednostką beta hCG i obie stymulują ten sam receptor. Jednak podjednostka hCG beta zawiera dodatkowe 24 aminokwasy, a oba hormony różnią się składem reszt cukrowych.
Odmienny skład tych oligosacharydów wpływa na bioaktywność i szybkość degradacji. Biologiczny okres półtrwania LH wynosi 20 minut i jest krótszy niż FSH (3-4 godziny) i hCG (24 godziny). Biologiczny okres półtrwania LH wynosi 23 godziny podskórnie lub końcowy okres półtrwania 10-12 godzin.
Geny
Genem dla podjednostki alfa znajduje się na chromosomie 6q 12.21.
Gen podjednostki beta hormonu luteinizującego zlokalizowany jest w skupisku genów LHB/CGB na chromosomie 19q 13.32. W przeciwieństwie do aktywności genu alfa, aktywność genu podjednostki beta LH jest ograniczona do komórek gonadotropowych przysadki. Jest regulowany przez hormon uwalniający gonadotropiny z podwzgórza . Inhibina , aktywina i hormony płciowe nie wpływają na aktywność genetyczną wytwarzania podjednostki beta LH.
Funkcjonować
Zarówno u mężczyzn, jak iu kobiet, LH działa na komórki endokrynologiczne w gonadach, wytwarzając androgeny.
Efekty u kobiet
LH wspiera komórki otoczki jajników, które dostarczają androgeny i prekursory hormonów do produkcji estradiolu . W czasie menstruacji FSH inicjuje wzrost pęcherzyków , szczególnie wpływając na komórki ziarniste . Wraz ze wzrostem estrogenów w dojrzewającym pęcherzyku dochodzi do ekspresji receptorów LH, co powoduje, że wytwarza on więcej estradiolu . W końcu, gdy pęcherzyk w pełni dojrzałe, skok w 17α-hydroksyprogesteronu produkcji przez pęcherzyk hamują wytwarzanie estrogenów , co prowadzi do zmniejszenia poziomu estrogenu w której pośredniczy ujemnego sprzężenia zwrotnego z GnRH w podwzgórzu , który z kolei pobudza wydzielanie LH z przednia przysadka . Jednak inna teoria piku LH to mechanizm dodatniego sprzężenia zwrotnego z estradiolu . Poziomy rosną w fazie folikularnej, a kiedy osiągną nieznany próg, skutkuje to szczytem LH. Efekt ten jest odwrotny do zwykłego mechanizmu negatywnego sprzężenia zwrotnego prezentowanego na niższych poziomach. Innymi słowy, mechanizm(y) nie są jeszcze jasne. Wzrost produkcji LH trwa tylko od 24 do 48 godzin. Ten „wybuch LH” wyzwala owulację , tym samym nie tylko uwalniając komórkę jajową z pęcherzyka, ale także inicjując przekształcenie pozostałego pęcherzyka w ciałko żółte, które z kolei wytwarza progesteron w celu przygotowania endometrium do ewentualnej implantacji . LH jest niezbędny do utrzymania funkcji lutealnej przez drugie dwa tygodnie cyklu miesiączkowego. W przypadku zajścia w ciążę poziom LH zmniejszy się, a funkcja lutealna zostanie utrzymana dzięki działaniu hCG ( ludzkiej gonadotropiny kosmówkowej ), hormonu bardzo podobnego do LH, ale wydzielanego z nowego łożyska.
Steroidy gonadalne ( estrogeny i androgeny) ogólnie mają negatywny wpływ na uwalnianie GnRH-1 na poziomie podwzgórza i gonadotropów, zmniejszając ich wrażliwość na GnRH. Dodatnie sprzężenie zwrotne estrogenów występuje również w osi gonad u samic ssaków i jest odpowiedzialne za środkowy wyrzut LH, który stymuluje owulację. Chociaż estrogeny hamują uwalnianie kisspeptyny (Kp) z neuronów kiss1 w ARC, estrogeny stymulują uwalnianie Kp z neuronów Kp w AVPV. Wraz ze stopniowym wzrostem poziomu estrogenów przeważa pozytywny efekt, prowadzący do gwałtownego wzrostu LH. Neurony wydzielające GABA, które unerwiają neurony GnRH-1, mogą również stymulować uwalnianie GnRH-1. Te neurony GABA również posiadają ER i mogą być odpowiedzialne za wzrost GnRH-1. Część hamującego działania endorfin na uwalnianie GnRH-1 polega na hamowaniu tych neuronów GABA. Pęknięcie pęcherzyka jajnikowego podczas owulacji powoduje drastyczne zmniejszenie syntezy estrogenu i wyraźny wzrost wydzielania progesteronu przez ciałko żółte w jajniku, przywracając głównie negatywne sprzężenie zwrotne na podwzgórzowe wydzielanie GnRH-1.
Efekty u mężczyzn
LH oddziałuje na komórkach Leydiga w jądrach i reguluje hormonu uwalniającego gonadotropinę (GnRH). Komórki Leydiga produkują testosteron pod kontrolą LH. LH wiąże się z receptorami LH na powierzchni błony komórek Leydiga. Wiązanie się z tym receptorem powoduje wzrost cyklicznego monofosforanu adenozyny (cAMP), wtórnego przekaźnika, który umożliwia translokację cholesterolu do mitochondriów. W mitochondriach cholesterol jest przekształcany w pregnenolon przez CYP11A1. Pregnenolon jest następnie przekształcany w dehydroepiandrosteron (DHEA). DHEA jest następnie przekształcany w androstendion przez dehydrogenazę 3β-hydroksysteroidową (3β-HSD), a następnie w testosteron przez dehydrogenazę 17β-hydroksysteroidową (HSD17B). Początek dojrzewania jest kontrolowany przez dwa główne hormony: FSH inicjuje spermatogenezę, a LH sygnalizuje uwalnianie testosteronu, androgenu, który wywiera zarówno aktywność hormonalną, jak i wewnątrzjądrową na spermatogenezę .
LH jest uwalniany z przysadki i jest kontrolowany przez impulsy hormonu uwalniającego gonadotropiny . Kiedy poziom testosteronu we krwi jest niski, przysadka jest stymulowana do uwalniania LH. Wraz ze wzrostem poziomu testosteronu będzie on oddziaływał na przysadkę poprzez pętlę ujemnego sprzężenia zwrotnego i w konsekwencji hamuje uwalnianie GnRH i LH. Androgeny (w tym testosteron i dihydrotestosteron ) hamują oksydazę monoaminową (MAO) w szyszynce, prowadząc do wzrostu melatoniny i zmniejszenia LH i FSH przez wywołany przez melatoninę wzrost syntezy i wydzielania hormonu hamującego gonadotropinę (GnIH). Testosteron może być również aromatyzowany do estradiolu (E2) w celu zahamowania LH. E2 zmniejsza amplitudę tętna i reakcję na GnRH z podwzgórza do przysadki.
Zmiany poziomu LH i testosteronu we krwi oraz sekrecji tętna są indukowane przez zmiany w podnieceniu seksualnym u mężczyzn.
Normalne poziomy
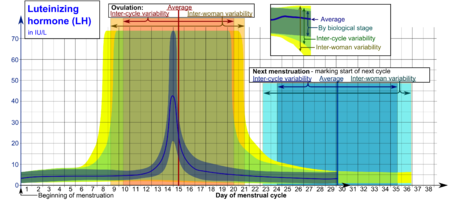
- Zakresy oznaczone jako etap biologiczny mogą być stosowane w ściśle monitorowanych cyklach menstruacyjnych w odniesieniu do innych markerów jej biologicznego postępu, przy czym skala czasu jest skompresowana lub rozciągnięta do tego, o ile odpowiednio szybciej lub wolniej cykl postępuje w porównaniu z cyklem przeciętnym.
- Zakresy oznaczone jako zmienność między cyklami są bardziej odpowiednie do stosowania w niemonitorowanych cyklach, w których znany jest tylko początek miesiączki, ale gdzie kobieta dokładnie zna swoje średnie długości cyklu i czas owulacji oraz że są one w pewnym stopniu średnio regularne, z skala czasu jest skompresowana lub rozciągnięta do tego, o ile średnia długość cyklu kobiety jest odpowiednio krótsza lub dłuższa niż średnia populacji.
- Zakresy oznaczone jako Zmienność między kobietami są bardziej odpowiednie, gdy nie są znane średnie długości cyklu i czas owulacji, ale podano tylko początek miesiączki.
Poziom LH jest zwykle niski w dzieciństwie, au kobiet wysoki po menopauzie . Ponieważ LH jest wydzielany w postaci impulsów, konieczne jest śledzenie jego stężenia przez wystarczający okres czasu, aby uzyskać właściwą informację o jego poziomie we krwi.
W latach reprodukcyjnych typowe poziomy wynoszą od 1 do 20 IU/L. Fizjologiczne wysokie poziomy LH są obserwowane podczas wyrzutu LH (vs) i zwykle trwają 48 godzin.
U mężczyzn w wieku powyżej 18 lat zakresy referencyjne oszacowano na 1,8–8,6 j.m./l.
LH mierzy się w jednostkach międzynarodowych (jm). Przy określaniu ilości LH w próbce w jednostkach j.m. ważne jest, aby wiedzieć, z jakim międzynarodowym standardem skalibrowano Twoją partię LH, ponieważ mogą się one znacznie różnić z roku na rok. W przypadku LH z moczu u człowieka ostatnio zdefiniowano jedną j.m. jako 1/189 ampułki oznaczonej 96/602 i dystrybuowanej przez NIBSC , co odpowiada około 0,04656 µg białka LH na jedną j.m., ale nadal powszechnie stosowane są starsze wersje standardowe. .
Przewidywanie owulacji
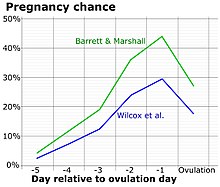
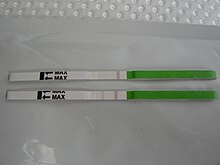
Wykrycie gwałtownego uwalniania hormonu luteinizującego wskazuje na zbliżającą się owulację . LH można wykryć za pomocą zestawów do przewidywania owulacji w moczu (OPK, również zestaw LH), które są wykonywane, zazwyczaj codziennie, w okolicach czasu, w którym można się spodziewać owulacji. Konwersja z odczytu negatywnego na pozytywne sugerowałaby, że owulacja nastąpi w ciągu 24-48 godzin, co daje kobietom dwa dni na odbycie stosunku płciowego lub sztuczne zapłodnienie z zamiarem poczęcia .
Zalecana częstotliwość testów różni się w zależności od producenta. Na przykład test Clearblue jest wykonywany codziennie, a zwiększona częstotliwość nie zmniejsza ryzyka przeoczenia wyrzutu LH. Z drugiej strony chińska firma Nantong Egens Biotechnology zaleca stosowanie ich testu dwa razy dziennie. W przypadku testowania raz dziennie nie stwierdzono istotnej różnicy między badaniem LH rano a wieczorem, w odniesieniu do częstości poczęć, a zalecenia dotyczące pory dnia na wykonanie testu różnią się między producentami a pracownikami służby zdrowia. Testy mogą być odczytywane ręcznie za pomocą paska papieru zmieniającego kolor lub cyfrowo za pomocą elektroniki odczytu.
Testy na obecność hormonu luteinizującego mogą być połączone z testami na estradiol w testach takich jak monitor płodności Clearblue .
Czułość testów LH mierzy się w milijednostkach międzynarodowych , przy czym testy powszechnie dostępne w zakresie 10-40 miu (im mniejsza liczba, tym wyższa czułość).
Ponieważ plemniki mogą zachować żywotność u kobiety przez kilka dni, testy LH nie są zalecane w przypadku praktyk antykoncepcyjnych , ponieważ wyrzut LH zwykle występuje po rozpoczęciu okresu płodności.
Stany chorobowe
Nadmiar
U dzieci z przedwczesnym dojrzewaniem, pochodzenia przysadkowego lub ośrodkowego, stężenia LH i FSH mogą znajdować się w zakresie reprodukcyjnym, a nie na niskim poziomie typowym dla ich wieku.
W okresie rozrodczym u pacjentek z zespołem policystycznych jajników często obserwuje się stosunkowo podwyższone LH ; jednak byłoby niezwykłe, gdyby miały poziom LH poza normalnym zakresem reprodukcyjnym.
Utrzymujące się wysokie poziomy LH wskazują na sytuacje, w których brak jest normalnej ograniczającej informacji zwrotnej z gonady, co prowadzi do wytwarzania zarówno LH, jak i FSH w przysadce. Chociaż jest to typowe w okresie menopauzy, jest nieprawidłowe w wieku rozrodczym. Tam może być oznaką:
- Przedwczesna menopauza
- Szczątkowych gonad , zespół Turnera , Klinefeltera zespół
- Kastracja
- Zespół Swyera
- Zespół policystycznych jajników
- Niektóre formy wrodzonego przerostu nadnerczy
- Niewydolność jąder
- Ciąża - BetaHCG może naśladować LH, więc testy mogą wykazywać podwyższony LH
Uwaga: lekiem hamującym wydzielanie hormonu luteinizującego jest butinazocyna .
Niedobór
Zmniejszone wydzielanie LH może skutkować niewydolnością gonad (hipogonadyzm). Ten stan zwykle objawia się u mężczyzn jako brak produkcji normalnej liczby plemników. U kobiet często obserwuje się brak miesiączki . Stany z bardzo niskimi wydzielinami LH obejmują:
- Zespół Pasqualiniego
- Zespół Kallmanna
- Tłumienie podwzgórza
- Niedoczynność przysadki
- Zaburzenia jedzenia
- Triada lekkoatletka
- Hiperprolaktynemia
- Hipogonadyzm
- Terapia supresji gonad
- Antagonista GnRH
- Agonista GnRH (indukujący początkową stymulację (zaostrzenie), po której następuje trwałe zablokowanie receptora przysadkowego GnRH)
Jako lek
LH jest dostępny zmieszany z FSH w postaci menotropiny i innych postaci gonadotropin moczowych . Bardziej oczyszczone formy gonadotropin moczowych mogą zmniejszać udział LH w stosunku do FSH. Rekombinowany LH jest dostępny jako lutropina alfa (Luveris). Wszystkie te leki należy podawać pozajelitowo. Są one powszechnie stosowane w terapii niepłodności w celu stymulacji rozwoju pęcherzyków, przy czym warto zwrócić uwagę na terapię IVF .
Często leki HCG są stosowane jako substytut LH, ponieważ aktywują ten sam receptor. Stosowana medycznie hCG pochodzi z moczu kobiet w ciąży, jest mniej kosztowna i ma dłuższy okres półtrwania niż LH.
Rola w fosforylacji
Fosforylacja to proces biochemiczny polegający na dodaniu fosforanu do związku organicznego. Steroidogeneza obejmuje procesy, w których cholesterol jest przekształcany w biologicznie aktywne hormony steroidowe. Ostatnie badania pokazują, że LH poprzez szlak sygnałowy PKA reguluje fosforylację i lokalizację DRP1 w mitochondriach komórek steroidogennych jajnika.
Bibliografia
Zewnętrzne linki
- Luteinizacja + hormon w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)