Kwasica metylomalonowa - Methylmalonic acidemia
| kwasica metylomalonowa | |
|---|---|
| Inne nazwy | MMA |
 | |
| Kwas metylomalonowy | |
| Specjalność |
Endokrynologia |
Kwasica metylomalonowa , zwana również kwasicą metylomalonową , jest autosomalnym recesywnym zaburzeniem metabolicznym, które zaburza prawidłowy metabolizm aminokwasów. Jest to klasyczny typ kwasicy organicznej . Skutkiem tego stanu jest niezdolność do prawidłowego trawienia określonych tłuszczów i białek, co z kolei prowadzi do nagromadzenia się toksycznego poziomu kwasu metylomalonowego we krwi.
Kwasica metylomalonowa wywodzi się z kilku genotypów , wszystkich postaci choroby, zwykle diagnozowanych we wczesnym okresie noworodkowym , z postępującą encefalopatią i wtórną hiperamonemią . Zaburzenie może spowodować śmierć, jeśli nie zostanie zdiagnozowane lub nie będzie leczone. Szacuje się, że zaburzenie to ma częstość 1 na 48 000 urodzeń, chociaż wysoka śmiertelność w zdiagnozowanych przypadkach utrudnia dokładne ustalenie. Kwasica metylomalonowa występuje z równą częstością w granicach etnicznych.
Objawy i oznaki
W zależności od dotkniętego genu (genów), zaburzenie to może wykazywać objawy od łagodnych do zagrażających życiu.
- Udar mózgu
- Postępująca encefalopatia
- Napad
- Niewydolność nerek
- Wymioty
- Odwodnienie
- Brak rozwoju i opóźnienia rozwojowe
- Letarg
- Powtarzające się infekcje drożdżakowe
- Kwasica
- Hepatomegalia
- Hipotonia
- Zapalenie trzustki
- Niewydolność oddechowa
Przyczyna
Genetyczny

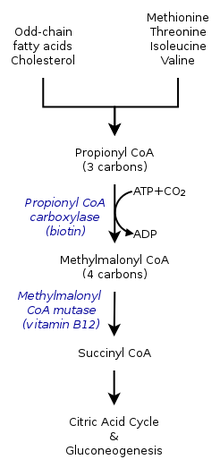
Dziedziczne postaci kwasicy metylomalonowej powodują defekty szlaku metabolicznego, w którym metylomalonylo-koenzym A (CoA) jest przekształcany w sukcynylo-CoA przez enzym mutazę metylomalonylo-CoA.
Witamina B 12 jest także potrzebna do przemiany metylomalonylo-CoA do sukcynylo-CoA. Mutacje prowadzące do wad w witaminy B 12 metabolizmu lub w transporcie często prowadzić do rozwoju metylomalonową acidemia.
Zaburzenie to ma autosomalny recesywny wzór dziedziczenia, co oznacza, że wadliwy gen znajduje się w autosomie , a dwie kopie genu – po jednej od każdego z rodziców – muszą zostać odziedziczone, aby zaburzenie to miało wpływ. Rodzice dziecka z chorobą autosomalną recesywną są nosicielami jednej kopii wadliwego genu, ale zaburzenie to zwykle nie dotyczy.
Odżywcze
Choć nie zawsze zgrupowane razem z dziedziczonych wersjach poważne niedobory odżywcze witaminy B 12 może również skutkować zespołem z identycznymi objawami i zabiegów genetycznych metylomalonową acidemias. Metylomalonylo-CoA wymaga witaminy B 12 , aby utworzyć sukcynylo-CoA. Gdy ilość B 12 jest niewystarczająca do przekształcenia kofaktora metylomalonylo-CoA w sukcynylo-CoA, gromadzeniu niewykorzystanych metylomalonylo-CoA prowadzi ostatecznie do metylomalonowego acidemia. Ta diagnoza jest często używany jako wskaźnik witaminy B 12 niedoboru w surowicy .
Mechanizm
Patofizjologia
W kwasicy metylomalonowej organizm nie jest w stanie rozłożyć aminokwasów metioniny , treoniny , izoleucyny i waliny ; w rezultacie kwas metylomalonowy gromadzi się we krwi i tkankach. Osób dotkniętych z tym zaburzeniem są albo pozbawione funkcjonalnych kopii lub odpowiednie poziomy jednego lub więcej z następujących enzymów: metylomalonylo-CoA mutase , metylomalonylo-CoA epimerazy lub zaangażowanych w adenosylcobalamin syntezy.
Mutaza metylomalonylo-CoA
Szacuje się, że aż 60% przypadków jest wynikiem zmutowanego genu MUT, który koduje białko mutazy metylomalonylo-CoA. Enzym ten jest odpowiedzialny za trawienie potencjalnie toksycznych pochodnych rozkładu wyżej wymienionych aminokwasów i tłuszczów, przede wszystkim cholesterolu , w szczególności enzym ten przekształca metylomalonylo-CoA w sukcynylo-CoA. Bez tego enzymu organizm nie ma możliwości zneutralizowania ani usunięcia kwasu metylomalonowego i związków pokrewnych. Działanie tego enzymu może być również utrudnione przez mutacje w genach MMAA , MMAB i MMADHC , z których każdy koduje białko wymagane do prawidłowego funkcjonowania mutazy metylomalonylo-CoA.
Epimeraza metylomalonylo-CoA
Mutacje w genie MCEE , który koduje białko epimerazy metylomalonylo-CoA, określane również jako racemaza metylomalonylowa, spowodują znacznie łagodniejszą postać zaburzenia niż pokrewny wariant mutazy metylomalonylo-CoA. Podobnie jak mutaza, epimeraza również działa w rozkładaniu tych samych substancji, ale w znacznie mniejszym stopniu niż mutaza. Te fenotypowe różnice spowodowane niedoborem epimerazy w przeciwieństwie do mutase są tak łagodne, że nie jest debata w środowisku medycznym, czy też nie ten niedobór genetyczny może być uznane za zaburzenie lub zespół kliniczny.
Adenozylokobalamina
Znana również jako witamina B12 , ta forma kobalaminy jest wymaganym kofaktorem mutazy metylomalonylo-CoA. Nawet w przypadku funkcjonalnego wersji enzymu fizjologicznie normalnych poziomach, jeśli B 12 nie może być przekształcony w tej aktywnej postaci, mutase będzie w stanie działać.
Postęp
Chociaż nie ma wyraźnych stadiów choroby, kwasica metylomalonowa jest stanem postępującym; objawy tego zaburzenia nasilają się wraz ze wzrostem stężenia kwasu metylomalonowego. Jeśli wyzwalające białka i tłuszcze nie zostaną usunięte z diety, to nagromadzenie może prowadzić do nieodwracalnego uszkodzenia nerek lub wątroby, a ostatecznie do śmierci.
Diagnoza
Jedna z, jeśli nie najczęstsza postać kwasicy organicznej, kwasica metylomalonowa, nie jest widoczna po urodzeniu, ponieważ objawy zwykle nie pojawiają się, dopóki do diety niemowlęcia nie zostaną dodane białka. Z tego powodu objawy zwykle pojawiają się w dowolnym momencie w ciągu pierwszego roku życia. Ze względu na ciężkość i szybkość, z jaką to zaburzenie może powodować powikłania, gdy nie zostanie zdiagnozowane, badanie przesiewowe w kierunku kwasicy metylomalonowej jest często włączane do badania przesiewowego noworodka.
Ze względu na niezdolność do prawidłowego całkowitego rozkładu aminokwasów, produkt uboczny trawienia białek, związek kwasu metylomalonowego, występuje w nieproporcjonalnie dużym stężeniu we krwi i moczu osób dotkniętych chorobą. Te nieprawidłowe poziomy są wykorzystywane jako główne kryteria diagnostyczne do diagnozowania zaburzenia. Zaburzenie to jest zazwyczaj określane za pomocą analizy moczu lub panelu krwi . Obecność kwasicy metylomalonowej można również podejrzewać na podstawie tomografii komputerowej lub rezonansu magnetycznego lub testu na amoniak, jednak testy te nie są w żaden sposób specyficzne i wymagają klinicznej i metabolicznej/korelacji. Podwyższony poziom amoniaku , glicyny i ciał ketonowych może być również obecny we krwi i moczu.
Rodzaje
Kwasica metylomalonowa ma różne diagnozy, wymagania dotyczące leczenia i rokowania, które są determinowane przez konkretną mutację genetyczną powodującą dziedziczną postać choroby. Oto znane genotypy odpowiedzialne za kwasicę metylomalonową:
| OMIM | Nazwa | Gen |
|---|---|---|
| 251100 | typ cblA | MMAA |
| 251110 | typ cblB | MMAB |
| 277400 | typ cblC | MMACHC |
| 277410 | typ cblD | MMADHC |
| 277380 | typ cblF | LMBRD1 |
| 251000 | typ muta | MUT |
Typ mut można dalej podzielić na podtypy mut0 i mut-, przy czym mut0 charakteryzuje się całkowitym brakiem mutazy metylomalonylo-CoA i cięższymi objawami, a mut- charakteryzuje się zmniejszoną aktywnością mutazy.
Stwierdzono, że wersje Mut-, cblB i cblA kwasicy metylomalonowej reagują na kobalaminę. Mut0 to wariant niereagujący.
Leczenie
Dietetyczny
Leczenie wszystkich postaci tego schorzenia polega przede wszystkim na diecie niskobiałkowej oraz, w zależności od wariantu zaburzenia, na który cierpi dana osoba, różnych suplementach diety. Wszystkie warianty reagują na izomer lewo - karnityny, ponieważ niewłaściwy rozkład zaatakowanych substancji powoduje u osób cierpiących na niedobór karnityny. Karnityna pomaga również w usuwaniu acylo-CoA, którego nagromadzenie jest powszechne w dietach niskobiałkowych, przekształcając go w acylo-karnitynę, która może być wydalana z moczem. Chociaż nie wszystkie postaci kwasicy metylomalonylowej reagują na kobalaminę, suplementy cyjanokobalaminy są często stosowane w leczeniu pierwszego rzutu tego zaburzenia. Jeśli dana osoba okaże się reagować zarówno na suplementy kobalaminą, jak i karnityną, może być możliwe, że spożyje substancje zawierające niewielkie ilości problematycznych aminokwasów izoleucynę, treoninę, metioninę i walinę bez powodowania ataku.
Chirurgiczny
Bardziej ekstremalne leczenie obejmuje przeszczep nerki lub wątroby od dawcy bez schorzenia. Obce narządy wytwarzają funkcjonalną wersję wadliwych enzymów i trawią kwas metylomalonowy, jednak wszystkie wady transplantacji narządów mają oczywiście zastosowanie w tej sytuacji. Istnieją dowody sugerujące, że ośrodkowy układ nerwowy może metabolizować metylomalonyl-CoA w układzie odizolowanym od reszty ciała. W takim przypadku przeszczep może nie odwrócić neurologicznych skutków działania kwasu metylomalonowego przed przeszczepem lub zapobiec dalszemu uszkodzeniu mózgu przez ciągłe nagromadzenie.
Rokowanie
Rokowanie będzie się różnić w zależności od ciężkości stanu i indywidualnej odpowiedzi na leczenie. Rokowanie jest zazwyczaj lepsze dla osób z wariantami reagującymi na kobalaminę i mało obiecujące u osób cierpiących na warianty nie reagujące na kobalaminę. Warianty łagodniejsze mają większą częstotliwość pojawiania się w populacji niż te cięższe. Nawet przy modyfikacji diety i ciągłej opiece medycznej zapobieganie uszkodzeniom neurologicznym u osób z kwasicą niereagującą może nie być możliwe. Bez odpowiedniego leczenia lub diagnozy często zdarza się, że pierwszy atak kwasicy kończy się śmiercią.
Pomimo tych wyzwań, odkąd po raz pierwszy zidentyfikowano ją w 1967 r., leczenie i zrozumienie tego stanu poprawiły się do tego stopnia, że nawet osoby z niereagującą postacią kwasicy metylomalonowej są w stanie osiągnąć dorosłość, a nawet nosić i rodzić dzieci bezpiecznie.
Badania
Historia nozologiczna
MMA został po raz pierwszy scharakteryzowany przez Oberholzera i in. w 1967 roku.
Efekty neurologiczne
Od dawna mówiono, że MMA może mieć katastrofalny wpływ na układ nerwowy; jednak mechanizm, za pomocą którego to się dzieje, nigdy nie został określony. Opublikowane 15 czerwca 2015 r. Badania przeprowadzone na temat wpływu kwasu metylomalonowego na neurony izolowane od płodów szczurów w warunkach in vitro z wykorzystaniem grupy kontrolnej neuronów leczonych innym kwasem o podobnym pH . Testy te sugerowały, że kwas metylomalonowy powoduje zmniejszenie rozmiaru komórek i wzrost szybkości apoptozy komórek w sposób zależny od stężenia, przy czym bardziej ekstremalne efekty obserwuje się przy wyższych stężeniach. Co więcej, analiza mikromacierzy tych leczonych neuronów zasugerowała również, że na poziomie epigenetycznym kwas metylomalonowy zmienia szybkość transkrypcji 564 genów, w szczególności tych zaangażowanych w szlaki sygnałowe apoptozy, p53 i MAPK.
Dysfunkcja mitochondriów
Ponieważ konwersja metylomalonylu-CoA do sukcynylo-CoA zachodzi wewnątrz mitochondriów , od dawna podejrzewano , że dysfunkcja mitochondriów w wyniku zmniejszonej funkcji łańcucha transportu elektronów jest cechą MMA. Ostatnie badania wykazały, że w modelach szczurzych mitochondria szczurów dotkniętych tym zaburzeniem osiągają niezwykłe rozmiary, zwane megamitochondriami. Te megamitochondria również wydają się mieć zdeformowane struktury wewnętrzne i utratę bogactwa elektronów w ich wewnętrznej macierzy . Te megamitochondria wykazywały również oznaki zmniejszonej funkcji łańcucha oddechowego, szczególnie w kompleksie oddechowym IV, który działał tylko z około 50% wydajnością. Podobne zmiany stwierdzono w mitochondriach próbki wątroby pobranej podczas przeszczepu 5-letniego chłopca cierpiącego na MMA.
Łagodny fenotyp mut
Ostatnie studia przypadków u kilku pacjentów prezentujących niereagujące MMA mut0 ze specyficzną mutacją oznaczoną p.P86L sugerują, że może istnieć możliwość dalszego podziału w MMA typu mut. Chociaż obecnie nie jest jasne, czy jest to spowodowane konkretną mutacją, czy wczesnym wykryciem i leczeniem, pomimo całkowitego braku odpowiedzi na suplementy kobalaminy, osoby te wydawały się rozwijać w dużej mierze łagodną i prawie całkowicie bezobjawową wersję MMA. Pomimo konsekwentnego wykazywania podwyższonego poziomu kwasu metylomalonowego we krwi i moczu, osoby te wydawały się w dużej mierze w prawidłowym rozwoju.
Wybitne przypadki
- Ryan Stallings, niemowlę z St. Louis, błędnie zdiagnozowano zatrucie glikolem etylenowym zamiast MMA w 1989 roku, co doprowadziło do bezprawnego skazania za morderstwo i dożywocia dla jego matki, Patricii Stallings .
Zobacz też
Uwagi
Bibliografia
Dalsza lektura
- Artykuł GeneReviews na temat kwasicy metylomalonowej
- Artykuł GeneReviews na temat zaburzeń wewnątrzkomórkowego metabolizmu kobalaminy
Zewnętrzne linki
| Klasyfikacja | |
|---|---|
| Zasoby zewnętrzne |