Oksydaza monoaminowa B - Monoamine oxidase B
Oksydaza monoaminowa B , znana również jako MAOB , jest enzymem, który u ludzi jest kodowany przez gen MAOB .
Białko kodowane przez ten gen należy do rodziny monoaminooksydaz flawinowych . Jest to enzym znajdujący się w zewnętrznej błonie mitochondrialnej . Katalizuje deaminację oksydacyjną amin biogennych i ksenobiotycznych oraz odgrywa ważną rolę w katabolizmie amin neuroaktywnych i wazoaktywnych w ośrodkowym układzie nerwowym i tkankach obwodowych (takich jak dopamina). Białko to preferencyjnie rozkłada benzyloaminę i fenetylaminę . Podobnie jak monoaminooksydaza A (MAOA), rozkłada również dopaminę .
Struktura
Monoaminooksydazy B ma hydrofobowy dwustronnego wydłużoną wnękę (na „otwarty” konformacji) zajmuje objętość połączonej blisko 700 nm 3 . H MAO-A ma jedną komorę, która wykazuje kształt okrągły i ma większą objętość niż „substratu” w jamie hMAO-B.
Pierwsza wnęka hMAO-B została nazwana wnęką wejściową (290 Ł 3 ), druga wnęka substratu lub wnęka miejsca aktywnego (~390 Ł 3 ) – pomiędzy obydwoma łańcuchami bocznymi izoleucyny 199 służy jako bramka . W zależności od substratu lub związanego inhibitora, może on występować w formie otwartej lub zamkniętej, co, jak wykazano, jest ważne w określaniu swoistości inhibitora hMAO B. Na końcu wnęki substratu znajduje się koenzym FAD z miejscami dla korzystne wiązanie amin wokół flawiny obejmujące dwie prawie równoległe reszty tyrozylowe (398 i 435), które tworzą to, co nazwano klatką aromatyczną .
Różnice między MAOA i MAOB
MAO-A bierze udział w metabolizmie tyraminy ; hamowanie, w szczególności nieodwracalne hamowanie MAO-A może skutkować niebezpiecznym efektem presyjnym, gdy spożywane są produkty bogate w tyraminę, takie jak sery (nieformalnie znane jako „efekt sera”). MAO-A bierze udział w metabolizmie serotoniny, noradrenaliny i dopaminy, natomiast MAO-B metabolizuje neuroprzekaźnik dopaminy. MAO-B jest enzymem na zewnętrznej błonie mitochondrialnej i katalizuje utlenianie neuroprzekaźników aryloalkiloaminowych
Oksydaza monoaminowa A (MAOA) ogólnie metabolizuje tyraminę, norepinefrynę (NE), serotoninę (5-HT) i dopaminę (DA) (oraz inne mniej istotne klinicznie substancje chemiczne). W przeciwieństwie do tego monoaminooksydaza B (MAOB) metabolizuje głównie dopaminę (DA) (i inne mniej istotne klinicznie substancje chemiczne). Różnice między selektywnością substratową dwóch enzymów wykorzystuje się klinicznie w leczeniu określonych zaburzeń: inhibitory monoaminooksydazy A są typowo stosowane w leczeniu depresji, a inhibitory monoaminooksydazy B są typowo stosowane w leczeniu choroby Parkinsona. Niespecyficzne (tj. połączone MAOA/B) inhibitory mogą stwarzać problemy, gdy są przyjmowane jednocześnie z żywnością zawierającą tyraminę, taką jak ser, ponieważ hamowanie MAOA przez lek powoduje niebezpieczny wzrost poziomu tyraminy w surowicy, co może prowadzić do objawów nadciśnienia. Selektywne inhibitory MAOB omijają ten problem, preferencyjnie hamując MAOB, który głównie metabolizuje DA. Jeśli MAOB jest zahamowany, wtedy więcej DA jest dostępnych dla prawidłowego funkcjonowania neuronów, szczególnie w chorobie Parkinsona.
Role w chorobie i starzeniu się
Choroba Alzheimera (AD) i choroba Parkinsona (PD) są związane z podwyższonym poziomem MAO-B w mózgu. Normalna aktywność MAO-B tworzy reaktywne formy tlenu , które bezpośrednio uszkadzają komórki. Stwierdzono, że poziomy MAO-B wzrastają wraz z wiekiem, co sugeruje rolę w naturalnym spadku funkcji poznawczych związanych z wiekiem i zwiększonym prawdopodobieństwie rozwoju chorób neurologicznych w późniejszym życiu. Bardziej aktywne polimorfizmy genu MAO-B powiązano z negatywną emocjonalnością i podejrzewano, że są one przyczyną depresji . Wykazano również, że aktywność MAO-B odgrywa rolę w uszkodzeniu serca wywołanym stresem. Nadmierna ekspresja poziomy i zwiększone MAO-B w mózgu, są również związane z akumulacją amyloidu beta-peptydów ( Ap ), za pośrednictwem mechanizmów sekretazy białka prekursorowego amyloidu , y-sekretazy , odpowiedzialny za rozwój płytek obserwowane u pacjentów z chorobą Alzheimera i Parkinsona. Dowody sugerują, że wyciszanie MAO-B przez siRNA lub hamowanie MAO-B przez MAOI- B ( Selegline , Rasagiline ) spowalnia progresję, łagodzi i odwraca objawy związane z AD i PD, w tym redukcję blaszek Aβ w mózg.
Modele zwierzęce
Wykazano, że myszy transgeniczne niezdolne do wytwarzania MAO-B są odporne na mysi model choroby Parkinsona. Wykazują również zwiększoną reakcję na stres (jak u myszy z nokautem MAO-A ) i zwiększoną β-PEA . Ponadto wykazują odhamowanie behawioralne i zmniejszone zachowania podobne do lęków.
Wykazano, że hamowanie MAO-B u szczurów zapobiega wielu zmianom biologicznym związanym z wiekiem, takich jak zwyrodnienie nerwu wzrokowego, i wydłuża przeciętną długość życia nawet o 39%.
Skutki niedoboru u ludzi
Podczas gdy ludzie bez genu MAO-A wykazują upośledzenie umysłowe i nieprawidłowości behawioralne, ludzie bez genu MAO-B nie wykazują żadnych nieprawidłowości poza podwyższonym poziomem fenetylaminy w moczu, co rodzi pytanie, czy MAO-B jest rzeczywiście niezbędnym enzymem. Nowsze badania wskazują na znaczenie fenetylaminy i innych amin śladowych , o których obecnie wiadomo, że regulują neuroprzekaźnictwo katecholamin i serotoniny poprzez ten sam receptor co amfetamina , TAAR1 .
Zaproponowano profilaktyczne zastosowanie inhibitorów MAO-B w celu spowolnienia naturalnego starzenia się człowieka u zdrowych osób, ale pozostaje to bardzo kontrowersyjnym tematem.
Selektywne inhibitory
Rozbieżności gatunkowe mogą utrudniać ekstrapolację siły działania inhibitora.
Odwracalny
Naturalny
- Geiparvarin
- Desmetoksyyangonina , składnik ekstraktu z kava ; skromne powinowactwo
- Katechina i epikatechina .
- Czosnek
Syntetyczny
- Safinamid i analogi
- 5 H indeno [1,2-c] pirydazyn-5-ony (patrz wzór 3d)
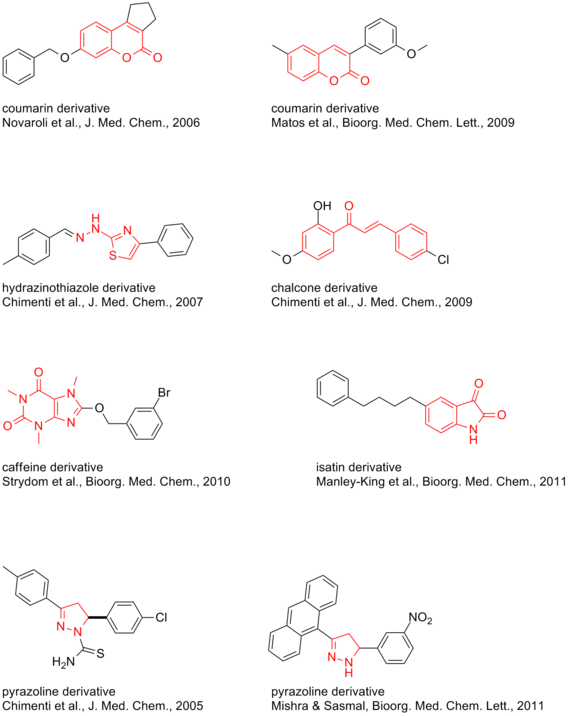
- Podstawione chalkony
- 2- ( N -Metylo- N -benzylaminomethyl) -1 H -pirolo
- 1-(4-arylotiazol-2-ilo)-2-(3-metylocykloheksylideno)hydrazyna
- 2-tiazolilohydrazon
- 3,5-diarylo pirazolo
- Pochodne pirazoliny
- Kilka pochodnych kumaryny i #C19* (patrz model 3d)
- Fenylokumaryny, niezwykle selektywne podtypy i dalsze analogi (patrz model 3d)
- Chromon -3-fenylokarboksyamidy
- Izatin
- ftalimidy
- 8-benzyloksykofeiny i analogi CSC
- ( E, E ) -8- (4-phenylbutadien-1-ylo) caffeines z 2A antagonistycznego składnik
- Indazolo- i indolo-5-karboksyamidy
Nieodwracalne (kowalencyjne)
- Selegilina (Eldepryl, Zelapar , Emsam )
- Rasagilina (Azilect)