Chemia fluoroorganiczna - Organofluorine chemistry

B: izofluran
C: CFC
D: HFC
E: kwas triflinowy
F: Teflon
G: PFOS
H: fluorouracyl
I: fluoksetyna
Chemia fluoroorganiczna opisuje chemię fluoroorganicznych, związków organicznych zawierających wiązanie węgiel-fluor . Związki fluoroorganiczne znajdują różnorodne zastosowania, od środków odpychających oleje i wodę po farmaceutyki , czynniki chłodnicze i odczynniki w katalizie . Oprócz tych zastosowań, niektóre związki fluoroorganiczne są zanieczyszczeniami ze względu na ich wkład w niszczenie warstwy ozonowej , globalne ocieplenie , bioakumulację i toksyczność . Dziedzina chemii fluoru organicznego często wymaga specjalnych technik związanych z obchodzeniem się ze środkami fluorującymi.
Wiązanie węgiel-fluor
Fluor ma kilka charakterystycznych różnic w stosunku do wszystkich innych podstawników spotykanych w cząsteczkach organicznych. W rezultacie właściwości fizyczne i chemiczne fluoroorganicznych mogą być wyróżniające się w porównaniu z innymi organohalogenami .
- Wiązanie węgiel-fluor jest jednym z najsilniejszych w chemii organicznej (średnia energia wiązania około 480 kJ / mol). Jest to znacznie silniejsze niż wiązania węgla z innymi halogenami (średnia energia wiązania np. wiązania C-Cl wynosi około 320 kJ/mol) i jest jednym z powodów wysokiej stabilności termicznej i chemicznej związków fluoroorganicznych.
- Wiązanie węgiel-fluor jest stosunkowo krótki (około 1,4 A).
- Van der Waalsa promień podstawnika fluorowego wynosi tylko 1,47 A, która jest mniejsza niż w jakimkolwiek innym podstawnikiem, w pobliżu atomu wodoru, (1.2). To, wraz z krótką długością wiązania, jest powodem braku sterycznego szczepu w związkach polifluorowanych. To kolejny powód ich wysokiej stabilności termicznej. Ponadto podstawniki fluorowe w związkach polifluorowanych skutecznie chronią szkielet węglowy przed możliwymi atakującymi odczynnikami. Jest to kolejny powód wysokiej stabilności chemicznej związków polifluorowanych.
- Fluor ma najwyższą elektroujemność wszystkich pierwiastków: 3,98. Powoduje to wysoki moment dipolowy wiązania CF (1,41 D).
- Fluor ma najniższą polaryzowalność ze wszystkich atomów: 0,56 10 -24 cm 3 . Powoduje to bardzo słabe siły dyspersji pomiędzy polifluorowanymi cząsteczkami i jest przyczyną często obserwowanego obniżenia temperatury wrzenia przy fluorowaniu oraz jednoczesnej hydrofobowości i lipofobowości związków polifluorowanych, podczas gdy inne związki perhalogenowane są bardziej lipofilowe .
W porównaniu do chlorków i bromków arylowych fluorki arylowe tworzą odczynniki Grignarda tylko niechętnie. Z drugiej strony, aryl fluorki, np fluoro aniliny i fluoru fenole , często poddaje się podstawieniu nukleofilowemu skutecznie.
Rodzaje związków fluoroorganicznych
Fluorowęglowodory
Formalnie fluorowęglowodory zawierają tylko węgiel i fluor. Czasami nazywane są perfluorowęglowodorami. Mogą to być gazy, ciecze, woski lub ciała stałe, w zależności od ich masy cząsteczkowej. Najprostszym fluorowęglowodorem jest gazowy tetrafluorometan (CF 4 ). Ciecze obejmują perfluorooktan i perfluorodekalinę. Podczas gdy fluorowęglowodory z wiązaniami pojedynczymi są stabilne, nienasycone fluorowęglowodory są bardziej reaktywne, szczególnie te z wiązaniami potrójnymi. Fluorowęglowodory są bardziej stabilne chemicznie i termicznie niż węglowodory, co odzwierciedla względną obojętność wiązania CF. Są również stosunkowo lipofobowe . Ze względu na zmniejszone interakcje międzycząsteczkowe van der Waalsa , związki na bazie fluorowęglowodorów są czasami używane jako smary lub są bardzo lotne. Ciecze fluorowęglowe mają zastosowanie medyczne jako nośniki tlenu.
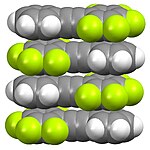
Struktura związków fluoroorganicznych może być charakterystyczna. Jak pokazano poniżej, perfluorowane związki alifatyczne mają tendencję do oddzielania się od węglowodorów. Ten „podobny efekt rozpuszczania” jest związany z użytecznością faz fluorowych i zastosowaniem PFOA w przetwarzaniu fluoropolimerów. W przeciwieństwie do pochodnych alifatycznych, pochodne perfluoroaromatyczne mają tendencję do tworzenia faz mieszanych z niefluorowanymi związkami aromatycznymi, w wyniku oddziaływań donor-akceptor pomiędzy układami pi.
Fluoropolimery
Polimeryczne związki fluoroorganiczne są liczne i mają znaczenie komercyjne. Począwszy od fluorowych gatunku, na przykład z PTFE , aby częściowo fluorowane, np winylidenu fluoru ([CH 2 CF 2 ] n ) i polichlorotrifluoroetylen ([CFClCF 2 ] n ). Fluoropolimer politetrafluoroetylenu (PTFE/Teflon) jest ciałem stałym.
fluorowęglowodory
Wodorofluorowęglowodory (HFC), związki organiczne zawierające atomy fluoru i wodoru, są najpowszechniejszym rodzajem związków fluoroorganicznych. Są one powszechnie stosowane w klimatyzacji i jako czynniki chłodnicze w miejsce starszych chlorofluorowęglowodorów, takich jak R-12 i hydrochlorofluorowęglowodorów, takich jak R-21 . Nie szkodzą warstwie ozonowej tak bardzo, jak związki, które zastępują; jednak przyczyniają się do globalnego ocieplenia . Ich stężenia w atmosferze i wkład w antropogeniczne emisje gazów cieplarnianych gwałtownie wzrastają, powodując międzynarodowe zaniepokojenie ich wymuszaniem radiacyjnym .
Fluorowęglowodory z niewielką liczbą wiązań CF zachowują się podobnie do węglowodorów macierzystych, ale ich reaktywność może być znacznie zmieniona. Na przykład zarówno uracyl , jak i 5-fluorouracyl są bezbarwnymi, wysokotopliwymi krystalicznymi ciałami stałymi, ale ten ostatni jest silnym lekiem przeciwnowotworowym. Zastosowanie wiązania CF w farmaceutykach opiera się na tej zmienionej reaktywności. Kilka leków i agrochemikaliów zawiera tylko jedno centrum fluorowe lub jedną grupę trifluorometylową .
W przeciwieństwie do innych gazów cieplarnianych objętych Porozumieniem Paryskim , wodorofluorowęglowodory prowadzą inne negocjacje międzynarodowe.
We wrześniu 2016 r. tak zwana deklaracja nowojorska wezwała do globalnego ograniczenia stosowania HFC. W dniu 15 października 2016 r., ze względu na wkład tych chemikaliów w zmiany klimatu , negocjatorzy ze 197 krajów zebranych na szczycie Programu Narodów Zjednoczonych ds. Ochrony Środowiska w Kigali w Rwandzie osiągnęli prawnie wiążące porozumienie w sprawie wycofania wodorofluorowęglowodorów (HFC) w poprawce do Protokół Montrealski .
Fluorokarbeny
Jak wskazano w tym artykule, podstawniki fluorowe prowadzą do reaktywności, która znacznie różni się od klasycznej chemii organicznej. Przykład czołową jest difluorocarbene CF 2 , który jest singlet natomiast karbenu (CH 2 ) ma tryplet stanu podstawowego. Ta różnica jest znacząca, ponieważ difluorokarben jest prekursorem tetrafluoroetylenu .
Związki perfluorowane
Związki perfluorowane są pochodnymi fluorowęglowodorów, ponieważ są blisko strukturalnie spokrewnione z fluorowęglowodorami. Posiadają jednak również nowe atomy, takie jak azot , jod , lub grupy jonowe, takie jak perfluorowane kwasy karboksylowe .
Metody przygotowania wiązań C–F
Związki fluoroorganiczne wytwarza się wieloma drogami, w zależności od stopnia i regiochemii poszukiwanego fluorowania oraz charakteru prekursorów. Bezpośrednie fluorowanie węglowodorów za pomocą F 2 , często rozcieńczonego N 2 , jest przydatne w przypadku związków wysoko fluorowanych:
-
r
3CH + F
2 → R
3CF + HF
Jednak takie reakcje są często nieselektywne i wymagają ostrożności, ponieważ węglowodory mogą w niekontrolowany sposób „spalić się” w F
2, analogicznie do spalania węglowodoru w O
2. Z tego powodu opracowano alternatywne metodologie fluorowania. Generalnie takie metody są podzielone na dwie klasy.
Fluorowanie elektrofilowe
Fluorowanie elektrofilowe opiera się na źródłach „F + ”. Często takie reagenty posiadają wiązania NF, na przykład F-TEDA BF 4 . Fluorowanie asymetryczne, w którym tylko jeden z dwóch możliwych produktów enancjomerycznych jest generowany z prochiralnego substratu, opiera się na elektrofilowych odczynnikach fluorujących. Ilustracją tego podejścia jest przygotowanie prekursora środków przeciwzapalnych:
Metody elektrosyntetyczne
Wyspecjalizowana, ale ważna metoda elektrofilowego fluorowania obejmuje elektrosyntezę . Metodę stosuje się głównie do perfluorowania, czyli zastąpienia wszystkich wiązań C–H wiązaniami C–F. Węglowodór jest rozpuszczany lub zawieszany w ciekłym HF, a mieszanina jest poddawana elektrolizie przy 5–6 V przy użyciu anod Ni . Metodę po raz pierwszy zademonstrowano przy przygotowaniu perfluoropirydyny ( C
5F
5N ) z pirydyny ( C
5h
5N ). Opisano kilka odmian tej techniki, w tym zastosowanie stopionego wodorofluorku potasu lub rozpuszczalników organicznych .
Fluorowanie nukleofilowe
Główne działanie alternatywne do elektrofilowego fluorowania, jest oczywiście nukleofilowe fluorowanie za pomocą reagentów, które są źródłami „F - ” dla nukleofilowe zwykle chlorek i bromek. Najprostsze są reakcje metatezy z użyciem fluorków metali alkalicznych . Dla związków alifatycznych jest to czasami nazywane reakcją Finkelsteina , podczas gdy dla związków aromatycznych jest to znane jako proces Halex .
-
r
3CCl + MF → R
3CF + MCI (M = Na, K, Cs)
Monofluorki alkilu można otrzymać z alkoholi i odczynnika Olah (fluorek pirydyniowy) lub innych środków fluoryzujących.
Rozkład tetrafluoroborany arylodiazoniowe w Sandmeyera lub reakcji Schiemann wykorzystać fluoroborany jak F - źródła.
-
ArN
2BF
4 → ArF + N
2 + BF
3
Chociaż fluorowodór może wydawać się mało prawdopodobnym nukleofilem, jest najczęstszym źródłem fluoru w syntezie związków fluoroorganicznych. Takie reakcje są często katalizowane przez fluorki metali, takie jak trifluorek chromu. 1,1,1,2-Tetrafluoroetan , zamiennik CFC, jest wytwarzany przemysłowo przy użyciu tego podejścia:
- Cl 2 C=CClH + 4 HF → F 3 CCFH 2 + 3 HCl
Zauważ, że ta transformacja pociąga za sobą dwa typy reakcji, metatezę (zastąpienie Cl − przez F − ) i hydrofluorowanie alkenu .
Deoksofluorowanie
Środki deoksofluorujące wpływają na zastępowanie grup hydroksylowych i karbonylowych odpowiednio jednym i dwoma fluorkami. Jednym z takich odczynników, przydatnym do fluorku do wymiany tlenków w związkach karbonylowych, jest tetrafluorek siarki :
- RCO 2 H + SF 4 → RCF 3 + SO 2 + HF
Zastępcy Sf 4 obejmują trifluorek dietyloaminosiarki (DAST, NEt 2 SF 3 ) i bis (2-metoksyetylo) aminosiarki trifluorek (deokso-fluoro). Te odczynniki organiczne są łatwiejsze w obsłudze i bardziej selektywne:
Z fluorowanych bloków budulcowych
Wiele związków fluoroorganicznych wytwarza się z odczynników, które dostarczają grupy perfluoroalkilowe i perfluoroarylowe. (Trifluorometylo) trimetylosilanu, CF 3 -Si (CH 3 ) 3 , stosuje się jako źródło trifluorometylo grupy, na przykład. Wśród dostępnych fluorowanych bloki budulcowe CF 3 X (X = Br, I), C 6 C 5 Br i C 3 C 7 I. Gatunki te tworzą związki Grignarda , które następnie można poddać reakcji z różnymi elektrof . Rozwój technologii fluorescencyjnych (patrz poniżej, pod rozpuszczalnikami) prowadzi do opracowania odczynników do wprowadzenia „ogonów fluorescencyjnych”.
Szczególnym, ale znaczącym zastosowaniem podejścia fluorowanych elementów budulcowych jest synteza tetrafluoroetylenu , który jest wytwarzany na dużą skalę przemysłowo za pośrednictwem difluorokarbenu. Proces rozpoczyna się od termicznego (600-800 °C) odchlorowodorowania chlorodifluorometanu :
- CHClF 2 → CF 2 + HCl
- 2CF 2 → C 2 F 4
Fluorodichlorooctan sodu (nr CAS 2837-90-3) jest używany do wytwarzania chlorofluorokarbenu do cyklopropanacji.
18 F-Metody dostawy
Przydatność radiofarmaceutyków zawierających fluor w tomografii emisyjnej 18 F- pozytonów stała się motywacją do opracowania nowych metod tworzenia wiązań C–F. Ze względu na krótki okres półtrwania 18 F, synteza ta musi być bardzo wydajna, szybka i łatwa. Ilustracją tych metod jest przygotowanie glukozy modyfikowanej fluorkiem przez zastąpienie triflatu przez znakowany fluorek nukleofil:
Rola biologiczna
Biologicznie syntetyzowane fluoroorgany znaleziono w mikroorganizmach i roślinach, ale nie w zwierzętach. Najczęstszym przykładem jest fluorooctan, który występuje jako ochrona roślin przed roślinożercami w co najmniej 40 roślinach w Australii, Brazylii i Afryce. Inne biologicznie syntetyzowane organofluory obejmują ω-fluorokwasy tłuszczowe , fluoroaceton i 2-fluorocytrynian, które, jak się uważa, są biosyntetyzowane na szlakach biochemicznych z pośredniego fluoroacetaldehydu. Syntaza adenozylofluorku jest enzymem zdolnym do biologicznej syntezy wiązania węgiel-fluor. Wytworzone przez człowieka wiązania węgiel-fluor są powszechnie spotykane w farmaceutykach i agrochemikaliach, ponieważ zwiększają stabilność struktury węglowej; ponadto stosunkowo mały rozmiar fluoru jest dogodny, ponieważ fluor działa jako przybliżony bioizoster wodoru. Wprowadzenie wiązania węgiel-fluor do związków organicznych jest głównym wyzwaniem dla chemików medycznych stosujących chemię fluoroorganiczną, ponieważ wiązanie węgiel-fluor zwiększa prawdopodobieństwo posiadania skutecznego leku około dziesięciokrotnie. Szacuje się, że 20% farmaceutyków i 30-40% agrochemikaliów to fluoroorganiczne, w tym kilka najlepszych leków. Przykłady obejmują 5-fluorouracyl , fluoksetynę (Prozac), paroksetynę (Paxil), cyprofloksacynę (Cipro), meflochinę i flukonazol .
Aplikacje
Chemia fluoru organicznego ma wpływ na wiele dziedzin życia codziennego i technologii. Wiązanie CF znajduje się między innymi w farmaceutykach , agrochemikaliach , fluoropolimerach , czynnikach chłodniczych , środkach powierzchniowo czynnych , anestetykach , repelentach olejowych , katalizie i hydrofobach .
Farmaceutyki i agrochemikalia
Wiązanie węgiel-fluor jest powszechnie spotykane w środkach farmaceutycznych i agrochemicznych, ponieważ jest ogólnie stabilne metabolicznie i fluoru działa jako bioizoster z wodoru atom. Szacuje się, że jedna piąta farmaceutyków zawiera fluor, w tym kilka najlepszych leków. Przykłady obejmują 5-fluorouracyl , flunitrazepam (Rohypnol), fluoksetynę (Prozac), paroksetynę (Paxil), ciprofloksacynę (Cipro), meflochinę i flukonazol . Etery podstawione fluorem to lotne środki znieczulające , w tym komercyjne produkty metoksyfluran , enfluran , izofluran , sewofluran i desfluran . Środki znieczulające fluorowęglowodorowe zmniejszają ryzyko zapalności eteru dietylowego i cyklopropanu . Jako substytuty krwi stosuje się perfluorowane alkany .
Inhalator propelent
Fluorowęglowodory są również stosowane jako propelent w inhalatorach z dozownikiem stosowanych do podawania niektórych leków na astmę. Obecna generacja propelentu składa się z hydrofluoroalkanów (HFA), które zastąpiły inhalatory na bazie CFC . Inhalatory CFC zostały zakazane od 2008 roku jako część Protokołu Montrealskiego z powodu obaw środowiskowych związanych z warstwą ozonową. Inhalatory z gazem pędnym HFA, takie jak FloVent i ProAir ( Salbutamol ), nie mają wersji generycznych dostępnych od października 2014 r.
Fluorosurfaktanty
Fluorosurfaktanty, które mają polifluorowany „ogon” i hydrofilową „głową”, służą jako surfaktanty, ponieważ koncentrują się na granicy faz ciecz-powietrze ze względu na ich lipofobowość . Fluorosurfaktanty mają niskie energie powierzchniowe i dramatycznie niższe napięcie powierzchniowe. Fluorosurfaktanty: kwas perfluorooktanosulfonowy ( PFOS ) i kwas perfluorooktanowy ( PFOA ) to dwa z najczęściej badanych ze względu na ich wszechobecność, toksyczność i długi czas przebywania u ludzi i dzikich zwierząt.
Rozpuszczalniki
Związki fluorowane często wykazują wyraźne właściwości rozpuszczalności. Powszechnie stosowanymi czynnikami chłodniczymi były dichlorodifluorometan i chlorodifluorometan . CFC mają silny potencjał niszczenia warstwy ozonowej ze względu na homolityczne rozszczepienie wiązań węgiel-chlor; ich użycie jest w dużej mierze zabronione przez Protokół Montrealski . Wodorofluorowęglowodory (HFC), takie jak tetrafluoroetan , służą jako zamienniki CFC, ponieważ nie katalizują zubożenia warstwy ozonowej. Tlen wykazuje wysoką rozpuszczalność w związkach perfluorowęglowodorowych, co ponownie odzwierciedla ich lipofilność. Wykazano, że perfluorodekalina jest substytutem krwi , transportującym tlen do płuc.
Rozpuszczalnik 1,1,1,2-tetrafluoroetan został użyty do ekstrakcji w produktach naturalnych , takich jak taksol , olej z wiesiołka i waniliny . 2,2,2-trifluoroetanol jest rozpuszczalnikiem polarnym odpornym na utlenianie.
Odczynniki fluoroorganiczne
Rozwój chemii fluoroorganicznej przyczynił się do powstania wielu odczynników o wartości wykraczającej poza chemię fluoroorganiczną. Kwas trifluorometanosulfonowy (CF 3 SO 3 H) i kwas trifluorooctowy (CF 3 CO 2 H) są użyteczne w ciągu syntezy organicznej . Ich silne kwasowość nadana elektroujemności od trifluorometylo grupy, która stabilizuje ładunek ujemny. Grupa triflatowa (sprzężona zasada kwasu triflowego) jest dobrą grupą opuszczającą w reakcjach podstawienia.
Fazy fluorescencyjne
Miejscowego zainteresowania w obszarze „zielonej chemii” wysoko fluorowane podstawników, np perfluoroheksyl (C 6 F 13 ) nadają charakterystyczny rozpuszczalność do cząsteczki, która ułatwia oczyszczanie produktów syntezy organicznej . Ta dziedzina, opisywana jako „ chemia fluorowa ”, wykorzystuje koncepcję podobnego rozpuszczania w tym sensie, że związki bogate we fluor rozpuszczają się preferencyjnie w rozpuszczalnikach bogatych we fluor. Ze względu na względną obojętność wiązania CF, takie fazy fluorowe są kompatybilne nawet z ostrymi odczynnikami. Ten temat zrodził techniki „fluorowanego znakowania i ochrony przed fluorem . Przykładem technologii fluorowej jest zastosowanie do redukcji wodorków cyny podstawionych grupą fluoroalkilową, przy czym produkty łatwo oddziela się od zużytego odczynnika cynowego przez ekstrakcję przy użyciu rozpuszczalników fluorowanych.
Hydrofobowe fluorowane ciecze jonowe , takie jak organiczne sole bistriflimidu lub heksafluorofosforanu , mogą tworzyć fazy nierozpuszczalne zarówno w wodzie, jak i rozpuszczalnikach organicznych, tworząc wielofazowe ciecze .
Ligandy fluoroorganiczne w chemii metali przejściowych
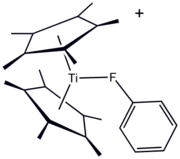
Ligandy fluoroorganiczne od dawna są wykorzystywane w chemii metaloorganicznej i koordynacyjnej . Jedną z zalet ligandów zawierających F jest wygoda spektroskopii 19 F NMR do monitorowania reakcji. Związki fluoroorganiczne mogą służyć jako "donor ligandu sigma", jak zilustrowano tytanu (III) Pochodne [(C 5 Me 5 ) 2 Ti (FC 6 H 5 )] BPH 4 . Najczęściej jednak podstawniki fluorowęglowe są stosowane w celu zwiększenia kwasowości Lewisa centrów metali. Najlepszym przykładem jest „ Eufod ”, kompleks koordynacyjny europu(III), który zawiera ligand acetyloacetonianowy modyfikowany perfluoroheptylem . Ten i pokrewne gatunki są przydatne w syntezie organicznej i jako „odczynniki przesuwające” w spektroskopii NMR .
W obszarze, w którym chemia koordynacyjna i materiałoznawstwo nakładają się na siebie, fluorowanie ligandów organicznych jest wykorzystywane do dostrajania właściwości cząsteczek składowych. Na przykład stopień i regiochemia fluorowania metalowanych ligandów 2-fenylopirydynowych w kompleksach platyny(II) znacząco modyfikuje właściwości emisyjne kompleksów.
Chemia koordynacyjna ligandów fluoroorganicznych obejmuje również technologie fluorowe. Na przykład, trifenylofosfina została zmodyfikowana przez przyłączenie podstawników perfluoroalkilowych, które nadają rozpuszczalność w perfluoroheksanie, jak również nadkrytycznym ditlenku węgla . W konkretnym przykładzie, [(C 8 C 17 C 3 H 6 4-C, 6 H 4 ) 3 P.
Aktywacja obligacji CF
Aktywny obszar chemii metaloorganicznej obejmuje rozrywanie wiązań CF przez odczynniki oparte na metalach przejściowych. Opracowano zarówno reakcje stechiometryczne, jak i katalityczne, które są interesujące z punktu widzenia syntezy organicznej i remediacji ksenochemikaliów. Aktywacja wiązania CF została sklasyfikowana w następujący sposób: „(i) addycja utleniająca fluorowęglowodoru, (ii) tworzenie wiązania M–C z eliminacją HF, (iii) tworzenie wiązania M–C z eliminacją fluorosilanu, (iv) hydroodfluorowanie fluorowęglowodoru za pomocą M– tworzenie wiązań F, (v) atak nukleofilowy na fluorowęglowodór i (vi) odfluorowanie fluorowęglowodoru". Ilustracyjnym reakcja aktywacji CF metalu pośredniczy jest defluorination z fluorohexane przez cyrkonu di wodorek , analogu odczynnika Schwartza :
- (C 5 Me 5 ) 2 ZrH 2 + 1-FC 6 H 13 → (C 5 Me 5 ) 2 ZrH(F) + C 6 H 14
Aniony fluorowęglowe w katalizie Zieglera-Natty
Związki zawierające fluor często występują w anionach niekoordynujących lub słabo koordynujących . Zarówno tetrakis (pentafluorofenylo) boran, B (C 6 C 5 ) 4 - i związane tetrakis [3,5-bis (trifluorometylo) fenylo] boran , są użyteczne w Zieglera-Natty i pokrewnych metodach polimeryzacji alkenu. Podstawniki fluorowane nadają aniony słabo zasadowe i zwiększają rozpuszczalność w słabo zasadowych rozpuszczalnikach, które są kompatybilne z silnymi kwasami Lewisa.
Inżynieria materiałowa
Związki fluoroorganiczne mają wiele niszowych zastosowań w materiałoznawstwie . Dzięki niskiemu współczynnikowi tarcia płynne fluoropolimery są stosowane jako smary specjalne. Smary na bazie fluorowęglowodorów są używane w wymagających zastosowaniach. Reprezentatywne produkty to Fomblin i Krytox , produkowane odpowiednio przez Solvay Solexis i DuPont . Niektóre smary do broni palnej, takie jak „Tetra Gun”, zawierają fluorowęglowodory. Wykorzystując ich niepalność, fluorowęglowodory są stosowane w piance przeciwpożarowej. Związki fluoroorganiczne są składnikami wyświetlaczy ciekłokrystalicznych . Polimeryczny analog kwasu triflowego , nafion, jest kwasem stałym, który jest używany jako membrana w większości niskotemperaturowych ogniw paliwowych . Monomer dwufunkcyjny 4,4'-difluorobenzofenon jest prekursorem polimerów klasy PEEK .
Biosynteza związków fluoroorganicznych
W przeciwieństwie do wielu naturalnie występujących związków organicznych zawierających cięższe halogenki , chlorki, bromki i jodki, znanych jest tylko kilka biologicznie zsyntetyzowanych wiązań węgiel-fluor. Najczęstszym naturalnym gatunkiem fluoroorganicznym jest fluorooctan , toksyna występująca w kilku gatunkach roślin. Inne obejmują kwas fluorooleinowy, fluoroaceton , nukleocydynę (4'-fuoro-5'-O-sulfamoiloadenozynę), fluorotreoninę i 2-fluorocytrynian . Kilka z tych gatunków jest prawdopodobnie biosyntetyzowanych z fluoroacetaldehydu . Enzym fluorinase katalizuje syntezę 5'-fluoro-5-deoksyadenozyny (patrz schemat z prawej strony).
Historia
Chemia fluoroorganiczna rozpoczęła się w XIX wieku wraz z rozwojem chemii organicznej. Pierwsze związki fluoroorganiczne wytworzono stosując antymonu trifluorek jako F - źródło. Niepalność i nietoksyczność chlorofluorowęglowodorów CCl 3 F i CCl 2 F 2 przyciągnęły uwagę przemysłu w latach dwudziestych XX wieku. 6 kwietnia 1938 Roy J. Plunkett, młody chemik naukowy, który pracował w Jackson Laboratory firmy DuPont w Deepwater, New Jersey , przypadkowo odkrył politetrafluoroetylen (PTFE). Kolejne duże wydarzenia, zwłaszcza w USA, skorzystały z wiedzy zdobytej przy produkcji sześciofluorku uranu . Począwszy od późnych lat 40. wprowadzono serię elektrofilowych metod fluorowania, zaczynając od CoF 3 . Ogłoszono fluorowanie elektrochemiczne („ elektrofluorowanie ”), które Joseph H. Simons opracował w latach 30. XX wieku w celu wytworzenia wysoce stabilnych materiałów perfluorowanych kompatybilnych z sześciofluorkiem uranu . Te nowe metodologie umożliwiły syntezę wiązań CF bez użycia pierwiastkowego fluoru i bez polegania na metodach metatetycznych.
W 1957 opisano działanie przeciwnowotworowe 5-fluorouracylu. Raport ten był jednym z pierwszych przykładów racjonalnego projektowania leków. Odkrycie to wywołało wzrost zainteresowania fluorowanymi farmaceutykami i agrochemikaliami. Odkrycie związków gazów szlachetnych , np. XeF 4 , dostarczyło wielu nowych odczynników na początku lat sześćdziesiątych. W 1970 roku, fluorodeoksyglukozy ustalono jako użyteczny odczynnik w 18 F tomografii emisyjnej . W pracy nagrodzonej Nagrodą Nobla wykazano, że CFC przyczyniają się do zubożenia atmosferycznego ozonu. Odkrycie to zaalarmowało świat o negatywnych skutkach związków fluoroorganicznych i zmotywowało do opracowania nowych dróg do związków fluoroorganicznych. W 2002 roku zgłoszono pierwszy enzym tworzący wiązania CF, fluorynazę .
Kwestie środowiskowe i zdrowotne
Tylko kilka związków fluoroorganicznych, takich jak fluorooctan i perfluoroizobuten, jest silnie bioaktywnych i wysoce toksycznych.
Niektóre związki fluoroorganiczne stwarzają znaczne ryzyko i zagrożenia dla zdrowia i środowiska. CFC i HCFC ( hydrochlorofluorowęglowodór ) zubożają warstwę ozonową i są silnymi gazami cieplarnianymi . HFC są silnymi gazami cieplarnianymi i stoją w obliczu wezwania do bardziej rygorystycznych międzynarodowych regulacji i harmonogramów stopniowego wycofywania jako szybko działającego środka redukcji emisji gazów cieplarnianych, podobnie jak perfluorowęglowodory (PFC) i sześciofluorek siarki (SF 6 ).
Ze względu na wpływ związku na klimat, główne gospodarki G-20 zgodziły się w 2013 r. na wspieranie inicjatyw zmierzających do stopniowego wycofywania HCFC. Potwierdzili rolę Protokołu Montrealskiego i Ramowej Konwencji Narodów Zjednoczonych w sprawie zmian klimatu w globalnym rozliczaniu i redukcji HCFC. Stany Zjednoczone i Chiny jednocześnie ogłosiły dwustronne porozumienie o podobnym skutku.
Trwałość i bioakumulacja
Ze względu na siłę wiązania węgiel-fluor, wiele syntetycznych fluorowęglowodorów i związków opartych na fluorowęglowodorach jest trwałych w środowisku. Fluorosurfaktanty, takie jak PFOS i PFOA , są trwałymi globalnymi zanieczyszczeniami. CFC i tetrafluorometan na bazie fluorowęglowodorów zostały zgłoszone w skałach magmowych i metamorficznych . PFOS jest trwałym zanieczyszczeniem organicznym i może szkodzić zdrowiu dzikich zwierząt; potencjalne skutki zdrowotne PFOA dla ludzi są badane przez Panel Naukowy C8.