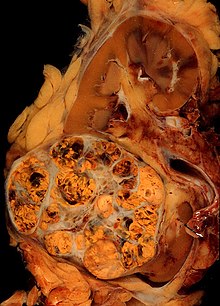
Rak nerkowokomórkowy - Renal cell carcinoma
| Rak nerkowokomórkowy | |
|---|---|
 | |
| Mikrografia najczęstszego typu raka nerkowokomórkowego (jasnokomórkowa) – po prawej stronie obrazu; nerka nie będąca guzem znajduje się po lewej stronie obrazu. Okaz z nefrektomii. Plama H&E | |
| Specjalność | Onkologia |
Rak nerkowokomórkowy ( RCC ) jest rakiem nerki, który wywodzi się z wyściółki proksymalnego kanalika krętego , części bardzo małych kanalików nerkowych, które transportują pierwotny mocz. RCC jest najczęstszym typem raka nerki u dorosłych, odpowiedzialnym za około 90-95% przypadków. Występowanie RCC wskazuje na przewagę mężczyzn nad kobietami w stosunku 1,5:1. RCC najczęściej występuje między 6. a 7. dekadą życia.
Wstępne leczenie to najczęściej częściowe lub całkowite usunięcie chorej nerki (nerek). Tam, gdzie rak nie dał przerzutów (rozprzestrzenił się na inne narządy) lub głębiej zagnieździł się w tkankach nerki, pięcioletni wskaźnik przeżycia wynosi 65-90%, ale jest on znacznie obniżony, gdy rak się rozprzestrzenił.
Organizm jest wyjątkowo dobry w ukrywaniu objawów, w wyniku czego ludzie z rakiem nerkowokomórkowym często mają zaawansowaną chorobę, zanim zostanie wykryta. Początkowe objawy RCC często obejmują krew w moczu (występuje u 40% chorych w momencie pierwszej wizyty lekarskiej), ból w okolicy lędźwiowej (40%), guz w jamie brzusznej lub boku (25%), utratę wagi (33%), gorączka (20%), wysokie ciśnienie krwi (20%), nocne poty i ogólne złe samopoczucie . W przypadku przerzutów RCC najczęściej rozprzestrzenia się na węzły chłonne , płuca , wątrobę , nadnercza , mózg lub kości. Immunoterapia i terapia celowana poprawiły perspektywy dla przerzutowego RCC.
RCC jest również związany z wieloma zespołami paranowotworowymi (PNS), które są stanami spowodowanymi przez hormony wytwarzane przez guz lub przez atak organizmu na nowotwór i występują u około 20% osób z RCC. Zespoły te najczęściej dotyczą tkanek, które nie zostały zaatakowane przez nowotwór. Najczęstsze PNS obserwowane u osób z rakiem nerkowokomórkowym to: wysoki poziom wapnia we krwi , wysoka liczba czerwonych krwinek , wysoka liczba płytek krwi i wtórna amyloidoza .
Symptomy i objawy
W przeszłości lekarze oczekiwali od osoby przedstawienia trzech wyników. Ta klasyczna triada to 1: krwiomocz , czyli obecność krwi w moczu, 2: ból w boku, czyli ból po stronie ciała między biodrem a żebrami, oraz 3: masa brzuszna, podobna do wzdęcia, ale większy. Obecnie wiadomo, że ta klasyczna triada objawów występuje tylko w 10–15% przypadków i zwykle wskazuje na zaawansowane stadium raka nerkowokomórkowego (RCC). Obecnie RCC jest często bezobjawowy (co oznacza niewiele lub brak objawów) i jest na ogół wykrywany przypadkowo, gdy dana osoba jest badana pod kątem innych dolegliwości.
Inne oznaki i objawy mogą obejmować krwiomocz ; ból lędźwi; masa brzucha; złe samopoczucie , czyli ogólne złe samopoczucie; utrata masy ciała i/lub utrata apetytu; niedokrwistość wynikająca z depresji erytropoetyny ; erytrocytoza (zwiększona produkcja czerwonych krwinek ) z powodu zwiększonego wydzielania erytropoetyny; żylaki powrózka nasiennego , czyli u mężczyzn powiększenie splotu wiciowatego żył drenujących jądro (częściej jądra lewego) nadciśnienie (wysokie ciśnienie krwi) wynikające z wydzielania reniny przez guz; hiperkalcemia , czyli podwyższenie poziomu wapnia we krwi; zaburzenia snu lub nocne poty; nawracające gorączki ; i chroniczne zmęczenie.
Czynniki ryzyka
Styl życia
Największe czynniki ryzyka RCC są związane ze stylem życia; szacuje się , że palenie tytoniu, otyłość i nadciśnienie (wysokie ciśnienie krwi) stanowią do 50% przypadków. Narażenie zawodowe na niektóre chemikalia, takie jak azbest, kadm, ołów, rozpuszczalniki chlorowane, produkty petrochemiczne i PAH ( wielopierścieniowy węglowodór aromatyczny ) zostało zbadane w wielu badaniach z niejednoznacznymi wynikami. Innym podejrzanym czynnikiem ryzyka jest długotrwałe stosowanie niesteroidowych leków przeciwzapalnych (NLPZ).
Wreszcie, badania wykazały, że kobiety, które przeszły histerektomię, mają ponad dwukrotnie większe ryzyko zachorowania na RCC niż kobiety, które tego nie zrobiły . Z drugiej strony wykazano, że umiarkowane spożycie alkoholu ma działanie ochronne.
Genetyka
Czynniki dziedziczne mają niewielki wpływ na indywidualną podatność, u bliskich krewnych osób z rakiem nerkowokomórkowym, u których ryzyko zachorowania jest dwu- do czterokrotnie większe. Inne genetycznie sprzężony warunki zwiększają ryzyko raka nerki, włączając dziedzicznego brodawkowatego raka nerki , dziedziczny leiomyomatosis , zespół Birt-Hogg-Dube , zespołem raka przytarczyc szczęką , rodzinną brodawkowatego tarczycy, raka , chorobę von Hippel-Lindau i anemii sierpowatej .
Jednak najważniejsza choroba wpływająca na ryzyko nie jest genetycznie powiązana – pacjenci z nabytą torbielowatością nerek wymagający dializy są 30 razy bardziej narażeni na rozwój RCC niż w populacji ogólnej.
Patofizjologia
Guz wywodzi się z komórek nabłonka proksymalnego kanalika nerkowego . Jest uważany za gruczolakoraka . Istnieją dwa podtypy: sporadyczny (czyli niedziedziczny) i dziedziczny. Oba takie podtypy są związane z mutacjami w krótkim ramieniu chromosomu 3 , przy czym implikowane geny są albo genami supresorowymi nowotworu ( VHL i TSC ) albo onkogenami (jak c-Met ).
Diagnoza
Pierwsze kroki podjęte w celu zdiagnozowania tego stanu to rozważenie oznak i objawów oraz historii medycznej (szczegółowy przegląd medyczny przeszłego stanu zdrowia) w celu oceny wszelkich czynników ryzyka. Na podstawie przedstawionych objawów można również rozważyć szereg badań biochemicznych (z wykorzystaniem próbek krwi i/lub moczu) jako część procesu przesiewowego w celu zapewnienia wystarczającej ilościowej analizy wszelkich różnic w elektrolitach , czynności nerek i wątroby oraz czasach krzepnięcia krwi . W badaniu fizykalnym palpacja brzucha może ujawnić obecność guza lub powiększenia narządu.
Chociaż choroba ta nie jest scharakteryzowana we wczesnych stadiach rozwoju nowotworu, ważne są rozważania oparte na różnych objawach klinicznych, a także oporności na promieniowanie i chemioterapię . Głównymi narzędziami diagnostycznymi do wykrywania raka nerkowokomórkowego są ultrasonografia , tomografia komputerowa (CT) i rezonans magnetyczny (MRI) nerek.
Klasyfikacja
Rak nerkowokomórkowy (RCC) nie jest pojedynczą jednostką, ale raczej zbiorem różnych typów guzów , z których każdy pochodzi z różnych części nefronu ( nabłonka lub kanalików nerkowych ) i ma odmienne cechy genetyczne, histologiczne , a dla niektórych zakres, fenotypy kliniczne.
| Klasyfikacja wspólnych podtypów histologicznych raka nerkowokomórkowego | |||
|---|---|---|---|
| Podtyp raka nerkowokomórkowego | Częstotliwość | Nieprawidłowości genetyczne | Charakterystyka |
|
Jasnokomórkowy rak nerkowokomórkowy (CRCCC) 
Na ogół komórki mają czystą cytoplazmę , są otoczone odrębną błoną komórkową i zawierają okrągłe i jednorodne jądra .
|
60–70% |
|
|
Rak brodawkowaty nerkowokomórkowy (PRCC)
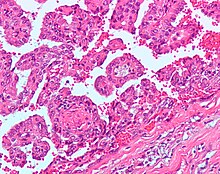
PRCC typu 1 składa się z brodawek pokrytych pojedynczą lub podwójną warstwą małych prostopadłościennych komórek ze skąpą cytoplazmą, a PRCC typu 2 składa się z brodawek pokrytych dużymi komórkami eozynofilowymi ułożonymi w sposób nieregularny lub pseudostratyfikowany .
|
10-15% |
|
|
Chromofobowy rak nerkowokomórkowy (ChRCC)

ChRCC składa się z komórek nowotworowych z obfitą cytoplazmą eozynofilową (komórki blade i komórki eozynofilowe z otoczką okołojądrową) i wykazują głównie strukturę litą .
|
3-5% |
|
|
| Cechy kliniczne, patologiczne i genetyczne rzadkich podtypów RCC uwzględnione w klasyfikacji patologii RCC 2004 WHO | ||||
|---|---|---|---|---|
| Podtyp RCC | Cechy kliniczne | Charakterystyka komórek/tkanek | Genetyka | Rokowanie |
| Wielokomorowy torbielowaty RCC |
|
Czysta cytoplazma , małe ciemne jądra | delecja 3p obserwowana w CCRCC |
|
| Rak przewodów zbiorczych Bellini |
|
Komórki nowotworowe o wysokim stopniu złośliwości z cytoplazmą eozynofilową | Wyniki zmienne: LOH na chromosomach 1q, 6p, 8p,9p, 13q, 19q32 i 21q; Amplifikacja c-erB2 związana z niekorzystnym wynikiem |
|
| Rak rdzeniasty |
|
Krwotok i martwica , komórki guza o wysokim stopniu złośliwości z cytoplazmą eozynofilową | Niezdefiniowane |
|
| Xp11.2 Rak translokacyjny |
|
|
Translokacja chromosomowa obejmująca gen TFE3 na Xp11.2 powodująca nadekspresję białka TFE3 |
|
| Śluzowy rak cewkowo-wrzecionowy |
|
Kanaliki, mucyna zewnątrzkomórkowa i komórki wrzecionowate | Niezdefiniowany; Odnotowano straty dotyczące chromosomów 1, 4, 6, 8, 9, 11, 13, 14, 15, 18, 22; Zmiany 3p i brak chromosomu 7 i 17 |
|
| Rak nerkowokomórkowy po neuroblastoma |
|
Komórki eozynofilowe z cechami onkocytoidalnymi (takie same jak CCRCC) | Niezdefiniowany; Zaobserwowano utratę wielu loci chromosomowych | Podobne do innych powszechnych podtypów RCC |
Kariotypowanie oparte na macierzach można wykorzystać do identyfikacji charakterystycznych aberracji chromosomowych w guzach nerek o trudnej morfologii. Kariotypowanie oparte na macierzach dobrze sprawdza się w przypadku guzów zatopionych w parafinie i nadaje się do rutynowego stosowania klinicznego. Zobacz także Wirtualny Kariotyp dla laboratoriów certyfikowanych przez CLIA, oferujących kariotypowanie oparte na macierzach guzów litych.
Klasyfikacja nowotworów układu moczowo-płciowego Światowej Organizacji Zdrowia (WHO) z 2004 r. obejmuje ponad 40 podtypów nowotworów nerek . Od czasu publikacji najnowszej iteracji klasyfikacji WHO w 2004 r. opisano kilka nowych podtypów guzów nerki:
- Jasnokomórkowy brodawkowaty rak nerkowokomórkowy i Jasnokomórkowy rak nerkowokomórkowy ze zrębem mięśni gładkich
- Rak śluzowo-cewkowy i wrzecionowatokomórkowy (MTSCC)
- Wielokomorowy torbielowaty rak jasnokomórkowy nerki
- Rak tubulocystyczny nerkowokomórkowy
- Rak nerkowokomórkowy podobny do tarczycy
- Nabyty rak nerkowokomórkowy związany z torbielowatością nerek
- Rak nerkowokomórkowy z translokacją t(6;11) (TFEB)
- Hybrydowy onkocytoma/chromofobowy rak nerkowokomórkowy
- Dziedziczna leiomiomatoza i rak nerkowokomórkowy (HLRCC)
Testy laboratoryjne
Badania laboratoryjne są zazwyczaj przeprowadzane, gdy u pacjenta występują oznaki i objawy, które mogą być charakterystyczne dla niewydolności nerek. Nie są one stosowane przede wszystkim do diagnozowania raka nerki, ze względu na jego bezobjawowy charakter i zwykle są wykrywane przypadkowo podczas testów na inne choroby, takie jak choroba pęcherzyka żółciowego . Innymi słowy, nowotwory te zwykle nie są wykrywane, ponieważ nie powodują bólu ani dyskomfortu, gdy zostaną wykryte. Analiza laboratoryjna może zapewnić ocenę ogólnego stanu zdrowia pacjenta i może dostarczyć informacji do określenia stopnia zaawansowania i stopnia przerzutów do innych części ciała (jeśli wykryto uszkodzenie nerek ) przed podaniem leczenia.
Badanie moczu
Obecność krwi w moczu jest częstym przypuszczalnym objawem raka nerkowokomórkowego. Hemoglobiny krwi powoduje, że mocz jest rdzawy, brązowe lub czerwono. Alternatywnie, analiza moczu może badać cukier , białko i bakterie, które mogą również służyć jako wskaźniki raka . Pełna morfologia krwi może również dostarczyć dodatkowych informacji dotyczących ciężkości i rozprzestrzeniania się nowotworu .
Całkowita liczba krwinek
CBC zapewnia ilościowy pomiar różnych komórek w próbce krwi pełnej od pacjenta. Takie komórki zbadane w tym teście obejmują krwinki czerwone ( erytrocyty ), krwinki białe ( leukocyty ) i płytki krwi ( trombocyty ). Powszechną oznaką raka nerkowokomórkowego jest niedokrwistość, w wyniku której pacjent wykazuje niedobór czerwonych krwinek. Testy CBC są niezbędne jako narzędzie przesiewowe do badania stanu zdrowia pacjenta przed operacją. Niezgodności z liczbą płytek krwi są również częste wśród tych pacjentów z rakiem i należy rozważyć dalsze badania krzepnięcia, w tym wskaźnik sedymentacji erytrocytów (OB), czas protrombinowy (PT), czas częściowej tromboplastyny po aktywacji (APTT).
Chemia krwi
Testy chemii krwi są przeprowadzane, jeśli podejrzewa się raka nerkowokomórkowego, ponieważ rak może podnieść poziom określonych substancji chemicznych we krwi. Na przykład stwierdzono, że enzymy wątrobowe , takie jak aminotransferaza asparaginianowa (AST) i aminotransferaza alaninowa (ALT) mają nienormalnie wysokie poziomy. Stopień zaawansowania nowotworu można również określić na podstawie nienormalnie podwyższonego poziomu wapnia, co sugeruje, że nowotwór mógł mieć przerzuty do kości. W takim przypadku lekarz powinien zostać poproszony o wykonanie tomografii komputerowej. Badania biochemiczne krwi oceniają również ogólną funkcję nerek i mogą pozwolić lekarzowi na podjęcie decyzji o dalszych badaniach radiologicznych.
Radiologia
Charakterystycznym wyglądem raka nerkowokomórkowego (RCC) jest lita zmiana nerkowa, która zaburza kontur nerek. Często będzie miał nieregularny lub zrazikowany brzeg i może być postrzegany jako guzek w dolnej części miednicy lub w okolicy brzucha. Tradycyjnie 85 do 90% litych zmian w nerkach okazuje się być rakiem nerkowokomórkowym, ale torbielowate masy nerkowe mogą być również spowodowane rakiem nerkowym. Jednak postępy metod diagnostycznych są w stanie przypadkowo zdiagnozować dużą część pacjentów ze zmianami w nerkach, które mogą wydawać się małe i łagodne. Dziesięć procent RCC będzie zawierało zwapnienia , a niektóre zawierają makroskopowy tłuszcz (prawdopodobnie z powodu inwazji i okrycia tłuszczu okołonerkowego). Decydowanie o łagodnym lub złośliwym charakterze guza nerkowego na podstawie jego zlokalizowanego rozmiaru jest problemem, ponieważ rak nerkowokomórkowy może mieć również charakter torbielowaty. Ponieważ istnieje kilka łagodnych zmian torbielowatych nerek (prosta torbiel nerki, torbiel krwotoczna nerki, wielokomorowy torbiel nerkowy , wielotorbielowatość nerek ), czasami radiologowi może być trudno odróżnić łagodną zmianę torbielowatą od złośliwej. Bośniacki system klasyfikacji zmian torbielowatych nerek klasyfikuje je na grupy łagodne i wymagające resekcji chirurgicznej na podstawie specyficznych cech obrazowania.
Głównymi badaniami obrazowymi wykonywanymi w celu identyfikacji raka nerkowokomórkowego są tomografia komputerowa miednicy i jamy brzusznej, badanie ultrasonograficzne nerek (ultrasonografia), rezonans magnetyczny, pielogram dożylny (IVP) czy angiografia nerek. Wśród tych głównych testów diagnostycznych, inne badania radiologiczne, takie jak urografia wydalnicza , tomografia emisyjna pozytonowa (PET), ultrasonografia , arteriografia , flebografia i skanowanie kości mogą być również stosowane w celu pomocy w ocenie zaawansowania mas nerkowych i różnicowaniu nie- nowotwory złośliwe z nowotworów złośliwych.
Tomografia komputerowa
Skanowanie tomografii komputerowej z kontrastem (CT) jest rutynowo stosowane do określenia zaawansowania raka nerkowokomórkowego w okolicy brzucha i miednicy . Skany CT mają potencjał do odróżnienia guzów litych od guzów torbielowatych i mogą dostarczyć informacji o lokalizacji, stadium lub rozprzestrzenianiu się raka na inne narządy pacjenta. Kluczowe części ludzkiego ciała, które są badane pod kątem przerzutów raka nerkowokomórkowego, mogą obejmować żyłę nerkową , węzeł chłonny i zajęcie żyły głównej dolnej . Według badań przeprowadzonych przez Sauk i wsp., wielodetektorowa charakterystyka obrazowania CT ma zastosowanie w diagnostyce pacjentów z jasnokomórkowym rakiem nerki poprzez zobrazowanie różnic między tymi komórkami na poziomie cytogenetycznym.
Ultradźwięk
Badanie ultrasonograficzne może być przydatne w ocenie wątpliwych bezobjawowych guzów nerki i zmian torbielowatych nerek, jeśli obrazowanie tomografii komputerowej jest niejednoznaczne. Ta bezpieczna i nieinwazyjna procedura radiologiczna wykorzystuje fale dźwiękowe o wysokiej częstotliwości do wygenerowania wewnętrznego obrazu ciała na monitorze komputera. Obraz generowany przez USG może pomóc w diagnozowaniu raka nerkowokomórkowego na podstawie różnic w odbiciu dźwięków na powierzchni narządów i nieprawidłowych masach tkanek. Zasadniczo badania ultradźwiękowe mogą określić, czy masa nerki jest głównie stała, czy wypełniona płynem.
Przezskórnej biopsji można przeprowadzić radiologa za pomocą ultradźwięków lub tomografii komputerowej do obsługi próbek guza, w celu postawienia diagnozy przez patologii . Nie jest to jednak rutynowo wykonywane, ponieważ przy występowaniu typowych cech obrazowych raka nerkowokomórkowego możliwość uzyskania błędnie ujemnego wyniku w połączeniu z ryzykiem powikłań medycznych dla pacjenta może sprawić, że będzie on niekorzystny z punktu widzenia stosunku ryzyka do korzyści. Jednak testy biopsyjne do analizy molekularnej w celu odróżnienia łagodnych od złośliwych guzów nerek są przedmiotem zainteresowania badawczego.
Rezonans magnetyczny
Obrazowanie metodą rezonansu magnetycznego (MRI) zapewnia obraz tkanek miękkich w ciele za pomocą fal radiowych i silnych magnesów. MRI można zastosować zamiast CT, jeśli pacjent wykazuje alergię na środki kontrastowe podawane do badania. Czasami przed badaniem MRI podaje się dożylnie kontrastujący materiał zwany gadolinem, aby uzyskać bardziej szczegółowy obraz. Pacjenci poddawani dializie lub z niewydolnością nerek powinni unikać tego kontrastowego materiału, ponieważ może on wywołać rzadkie, ale ciężkie działanie niepożądane znane jako nerkopochodne zwłóknienie układowe. Skan kości lub obrazowanie mózgu nie jest rutynowo wykonywane, chyba że objawy sugerują potencjalne przerzuty do tych obszarów. Należy również rozważyć badanie MRI w celu oceny rozrostu guza, który wyrósł w głównych naczyniach krwionośnych, w tym w żyle głównej w jamie brzusznej. MRI można wykorzystać do obserwacji możliwego rozprzestrzeniania się raka do mózgu lub rdzenia kręgowego, jeśli u pacjenta wystąpią objawy sugerujące, że może to mieć miejsce.
Pielogram dożylny
Pielogram dożylny (IVP) jest przydatną procedurą w wykrywaniu obecności nieprawidłowej masy nerek w drogach moczowych . Ta procedura polega na wstrzyknięciu kontrastowego barwnika w ramię pacjenta. Barwnik wędruje z krwioobiegu do nerek, który z czasem przechodzi do nerek i pęcherza moczowego. Ten test nie jest konieczny, jeśli przeprowadzono tomografię komputerową lub rezonans magnetyczny.
Angiografia nerek
Angiografia nerkowa wykorzystuje tę samą zasadę, co IVP, ponieważ ten typ promieniowania rentgenowskiego wykorzystuje również kontrastujący barwnik. To badanie radiologiczne jest ważne w diagnostyce raka nerkowokomórkowego jako pomoc w badaniu naczyń krwionośnych w nerkach. Ten test diagnostyczny opiera się na środku kontrastowym, który jest wstrzykiwany do tętnicy nerkowej, aby został wchłonięty przez komórki rakowe. Kontrastujący barwnik zapewnia wyraźniejszy zarys nieprawidłowo zorientowanych naczyń krwionośnych, które, jak się uważa, są związane z guzem. Jest to niezbędne dla chirurgów, ponieważ umożliwia mapowanie naczyń krwionośnych pacjenta przed operacją.
Inscenizacja
Stopień zaawansowania raka nerkowokomórkowego jest najważniejszym czynnikiem prognozującym jego rokowanie. Stopień zaawansowania może być zgodny z systemem stopniowania TNM , w którym rozmiar i rozległość guza (T), zajęcie węzłów chłonnych (N) i przerzuty (M) są klasyfikowane oddzielnie. Może również wykorzystywać ogólne grupowanie etapów w etapy I–IV, z rewizją AJCC z 1997 r. opisaną poniżej:
| Etap I | Guz o średnicy 7 cm (ok. 2,3⁄4 cala) lub mniejszy, ograniczony do nerki. Brak zajęcia węzłów chłonnych lub przerzutów do odległych narządów. |
| Etap II | Guz większy niż 7,0 cm, ale nadal ograniczony do nerki. Brak zajęcia węzłów chłonnych lub przerzutów do odległych narządów. |
|
Etap III dowolne z poniższych |
Guz dowolnej wielkości z zajęciem pobliskiego węzła chłonnego, ale bez przerzutów do odległych narządów. Guz w tym stadium może rozprzestrzeniać się lub nie do tkanki tłuszczowej wokół nerki, z lub bez rozprzestrzeniania się w dużych żyłach prowadzących od nerki do serca. |
| Guz z przerzutami do tkanki tłuszczowej wokół nerki i/lub do dużych żył prowadzących z nerki do serca, ale bez przerzutów do węzłów chłonnych lub innych narządów. | |
|
Etap IV którykolwiek z poniższych |
Guz, który rozprzestrzenił się bezpośrednio przez tkankę tłuszczową i tkankę przypominającą więzadło powięzi, która otacza nerkę. |
| Zajęcie więcej niż jednego węzła chłonnego w pobliżu nerki | |
| Zajęcie jakiegokolwiek węzła chłonnego nie w pobliżu nerki | |
| Przerzuty odległe, np. w płucach, kościach lub mózgu. |
W momencie rozpoznania 30% raków nerkowokomórkowych rozprzestrzeniło się do żyły nerkowej po tej samej stronie, a 5–10% do żyły głównej dolnej.
Histopatologia
Obraz gruboziarnisty i mikroskopowy raków nerkowokomórkowych jest bardzo zmienny. Rak nerkowokomórkowy może wykazywać zaczerwienione obszary, w których krwawiły naczynia krwionośne oraz cysty zawierające wodniste płyny. W ciele guza widoczne są duże naczynia krwionośne, których ściany składają się z komórek rakowych. Badanie zbiorcze często wykazuje żółtawy, wielopłatkowy guz w korze nerkowej , który często zawiera strefy martwicy , krwotoku i bliznowacenia . W kontekście mikroskopowym istnieją cztery główne histologiczne podtypy raka nerkowokomórkowego: jasnokomórkowy (konwencjonalny RCC, 75%), brodawkowaty (15%), chromofobowy (5%) i przewód zbiorczy (2%). Zmiany sarkomatoidalne (morfologia i wzory IHC naśladujące mięsaka, komórki wrzecionowate) można zaobserwować w obrębie każdego podtypu RCC i wiążą się z bardziej agresywnym przebiegiem klinicznym i gorszym rokowaniem. Pod mikroskopem świetlnym te komórki nowotworowe mogą wykazywać brodawki , kanaliki lub gniazda i są dość duże, nietypowe i wielokątne.
Ostatnie badania zwróciły uwagę na ścisły związek typu komórek rakowych z agresywnością choroby. Niektóre badania sugerują, że te komórki rakowe gromadzą glikogen i lipidy, ich cytoplazma wydaje się „czysta”, jądra pozostają w środku komórek, a błona komórkowa jest widoczna. Niektóre komórki mogą być mniejsze, z cytoplazmą eozynofilową, przypominającą normalne komórki kanalikowe. Zrąb jest zmniejszony, ale dobrze unaczyniony. Guz ściska otaczający miąższ , tworząc pseudotorebkę.
Najczęstszym typem komórek wykazywanym przez raka nerkowokomórkowego jest komórka jasna , której nazwa pochodzi od rozpuszczania się komórek o wysokiej zawartości lipidów w cytoplazmie. Uważa się, że przejrzyste komórki są najmniej podatne na rozprzestrzenianie się i zazwyczaj korzystniej reagują na leczenie. Jednak większość guzów zawiera mieszaninę komórek. Uważa się, że najbardziej agresywnym stadium raka nerki jest ten, w którym guz jest mieszany, zawierający zarówno komórki jasne, jak i ziarniste.
Rekomendowanym histologicznym schematem klasyfikacji RCC jest system Fuhrmana (1982), który jest oceną opartą na mikroskopowej morfologii nowotworu z hematoksyliną i eozyną (barwienie H&E). Ten system klasyfikuje raka nerkowokomórkowego w stopniach 1, 2, 3, 4 na podstawie cech jądra. Poniżej przedstawiono szczegóły systemu oceny Fuhrmana dla RCC:
| Poziom oceny | Charakterystyka jądrowa |
|---|---|
| Klasa I | Jądra wydają się okrągłe i jednolite, 10 μm; jąderka są niepozorne lub nieobecne. |
| Klasa II | Jądra mają nieregularny wygląd z oznakami tworzenia płatków, 15 μm; jąderka są oczywiste. |
| Klasa III | Jądra wydają się bardzo nieregularne, 20 μm; jąderka są duże i widoczne. |
| Klasa IV | Jądra wydają się dziwaczne i wielopłatkowe, 20 μm lub więcej; jąderka są widoczne. |
Uważa się, że stopień zaawansowania jądrowego jest jednym z najważniejszych czynników prognostycznych u pacjentów z rakiem nerkowokomórkowym. Jednak badanie Delahunta i in. (2007) wykazali, że klasyfikacja Fuhrmana jest idealna dla raka jasnokomórkowego, ale może nie być odpowiednia dla chromofobowych raków nerkowokomórkowych i że stopień zaawansowania raka (uzyskany za pomocą tomografii komputerowej) jest bardziej korzystnym predyktorem rokowania tej choroby. W odniesieniu do stopnia zaawansowania raka nerki w 1976 roku wprowadzono Heidelbergowski system klasyfikacji guzów nerki jako sposób pełniejszego skorelowania cech histopatologicznych ze stwierdzonymi defektami genetycznymi.
Zapobieganie
Ryzyko raka nerkowokomórkowego można zmniejszyć, utrzymując prawidłową masę ciała.
Kierownictwo

Rodzaj leczenia zależy od wielu czynników i osoby, z których niektóre obejmują stadium raka nerkowokomórkowego (narządy i części ciała dotknięte/niedotknięte), rodzaj raka nerkowokomórkowego, istniejące lub współistniejące schorzenia oraz ogólny stan zdrowia i wiek osoby. Każda forma leczenia wiąże się zarówno z ryzykiem, jak i korzyściami; pracownik służby zdrowia zapewni najlepsze opcje, które odpowiadają indywidualnym okolicznościom.
Jeśli rozprzestrzenił się poza nerki, często do węzłów chłonnych , płuc lub głównej żyły nerki, stosuje się wiele terapii, w tym zabiegi chirurgiczne i leki. RCC jest oporny na chemioterapię i radioterapię w większości przypadków, ale dobrze reaguje na immunoterapię interleukiną-2 lub interferonem alfa, terapię biologiczną lub terapię celowaną. We wczesnym stadium preferowanymi opcjami są krioterapia i zabieg chirurgiczny.
Aktywny nadzór
Aktywny nadzór lub „uważne oczekiwanie” staje się coraz bardziej powszechne, ponieważ wykrywane są małe masy nerek lub guzy, a także u starszego pokolenia, gdy operacja nie zawsze jest odpowiednia. Aktywny nadzór obejmuje wykonanie różnych procedur diagnostycznych, testów i obrazowania w celu monitorowania progresji RCC przed podjęciem bardziej ryzykownej opcji leczenia, takiej jak zabieg chirurgiczny. Jest to szczególnie przydatne u osób starszych, pacjentów ze współistniejącymi chorobami oraz u słabych kandydatów do operacji.
Chirurgia
W zależności od okoliczności najbardziej odpowiednie mogą być różne procedury.
Zalecanym leczeniem raka nerkowokomórkowego może być nefrektomia lub częściowa nefrektomia , chirurgiczne usunięcie całości lub części nerki. Może to obejmować niektóre z okolicznych narządów lub tkanek lub węzłów chłonnych. Jeśli rak występuje tylko w nerkach, co stanowi około 60% przypadków, można go wyleczyć w około 90% przypadków chirurgicznie .
Małe guzy nerek (< 4 cm) leczy się coraz częściej poprzez częściową nefrektomię, jeśli to możliwe. Większość z tych małych guzów nerkowych przejawia leniwe zachowanie biologiczne z doskonałym rokowaniem. Nefrektomię częściową oszczędzającą nerki stosuje się, gdy guz jest mały (średnica poniżej 4 cm) lub gdy pacjent ma inne problemy zdrowotne, takie jak cukrzyca lub nadciśnienie . Nefrektomia częściowa polega na usunięciu tylko uszkodzonej tkanki, oszczędzając resztę nerki, powięź Geroty i regionalne węzły chłonne. Pozwala to na większą ochronę nerek w porównaniu z radykalną nefrektomią, a to może mieć pozytywne długoterminowe korzyści zdrowotne. Większe i bardziej złożone guzy mogą być również leczone częściową nefrektomią przez chirurgów z dużym doświadczeniem w chirurgii nerek.
Nefrektomia chirurgiczna może być „radykalna”, jeśli w tym samym czasie usunie się całą zaatakowaną nerkę, w tym powięź Geroty , nadnercze, które znajduje się po tej samej stronie, co zaatakowana nerka, oraz regionalne zaotrzewnowe węzły chłonne. Ta metoda, choć ciężka, jest skuteczna. Ale nie zawsze jest to właściwe, ponieważ jest to poważna operacja, która wiąże się z ryzykiem powikłań zarówno w trakcie, jak i po operacji, i może mieć dłuższy czas powrotu do zdrowia. Należy zauważyć, że druga nerka musi być w pełni sprawna, a technikę tę stosuje się najczęściej, gdy duży guz występuje tylko w jednej nerce.
W przypadkach, gdy guz rozprzestrzenił się do żyły nerkowej, żyły głównej dolnej i prawdopodobnie do prawego przedsionka, tę część guza można również usunąć chirurgicznie. Gdy guz obejmuje żyłę główną dolną, ważne jest, aby sklasyfikować, które części żyły głównej są zajęte i odpowiednio zaplanować, ponieważ czasami całkowita resekcja będzie wymagać nacięcia w klatce piersiowej ze zwiększoną chorobowością. Z tego powodu dr Gaetano Ciancio zaadaptował techniki mobilizacji wątroby z przeszczepu wątroby, aby zająć się zakrzepicą pozawątrobową lub nawet nadwątrobową w żyle głównej dolnej związaną z nowotworami nerek. Dzięki tej technice cała dolna żyła brzuszna może zostać zmobilizowana. Ułatwia to dojenie guza poniżej głównych żył wątrobowych palcami chirurga, omijając potrzebę nacięcia piersiowo-brzusznego lub bypassu sercowo-płucnego . W przypadkach znanych przerzutów chirurgiczna resekcja nerki („nefrektomia cytoredukcyjna”) może poprawić przeżycie, jak również resekcja pojedynczej zmiany przerzutowej. Nerki są czasami embolizowane przed operacją, aby zminimalizować utratę krwi.
Chirurgia jest coraz częściej wykonywana technikami laparoskopowymi . Operacja ta, powszechnie określana jako chirurgia dziurki od klucza, nie ma dużych nacięć obserwowanych w klasycznie wykonywanej radykalnej lub częściowej nefrektomii, ale nadal skutecznie usuwa całą lub część nerki. Chirurgia laparoskopowa wiąże się z krótszym pobytem w szpitalu i szybszym czasem powrotu do zdrowia, ale nadal istnieje ryzyko związane z zabiegiem chirurgicznym. Mają one tę zaletę, że są mniejszym obciążeniem dla pacjenta, a przeżycie bez choroby jest porównywalne z przeżyciem otwartym. W przypadku niewielkich zmian egzofitycznych, które nie obejmują w dużym stopniu głównych naczyń lub układu moczowego, można wykonać częściową nefrektomię (określaną również jako „chirurgia oszczędzająca nefron”). Może to obejmować czasowe zatrzymanie dopływu krwi do nerki podczas usuwania masy, a także ochłodzenie nerek za pomocą lodu. Mannitol można również podawać w celu ograniczenia uszkodzenia nerek. Zwykle wykonuje się to przez otwarte nacięcie, chociaż mniejsze zmiany można wykonać laparoskopowo z pomocą robota lub bez niej.
Laparoskopowa krioterapia może być również wykonane na mniejszych zmian. Zazwyczaj biopsję wykonuje się w czasie leczenia. Ultrasonografia śródoperacyjna może pomóc w umieszczeniu sond zamrażających. Następnie przeprowadza się dwa cykle zamrażania/rozmrażania w celu zabicia komórek nowotworowych. Ponieważ guz nie został usunięty, obserwacja jest bardziej skomplikowana (patrz poniżej), a ogólny odsetek pacjentów wolnych od choroby nie jest tak dobry, jak uzyskany po usunięciu chirurgicznym.
Chirurgia choroby przerzutowej: Jeśli choroba przerzutowa jest obecna, leczenie chirurgiczne może nadal być realną opcją. Radykalna i częściowa nefrektomia nadal może wystąpić, aw niektórych przypadkach, jeśli przerzuty są małe, można je również usunąć chirurgicznie. Zależy to od etapu wzrostu i rozprzestrzenienia się choroby.
Przezskórne terapie ablacyjne
Terapie przezskórnej ablacji wykorzystują obrazowanie przez radiologów w leczeniu zlokalizowanych guzów, jeśli zabieg chirurgiczny nie jest dobrym rozwiązaniem. Chociaż zastosowanie laparoskopowych technik chirurgicznych do całkowitych nefrektomii zmniejszyło niektóre zagrożenia związane z operacją, w niektórych przypadkach zabieg chirurgiczny nadal nie będzie możliwy. Na przykład osoby starsze, osoby już cierpiące na ciężką dysfunkcję nerek lub osoby, które mają kilka chorób współistniejących , wszelkiego rodzaju operacje nie są uzasadnione.
Sonda jest umieszczana przez skórę i w guzie przy użyciu obrazowania w czasie rzeczywistym zarówno końcówki sondy, jak i guza za pomocą tomografii komputerowej , ultradźwięków lub nawet rezonansu magnetycznego , a następnie niszczenie guza ciepłem ( ablacja częstotliwościami radiowymi ) lub zimnem ( krioterapia ). Te metody są niekorzystne w porównaniu z tradycyjną chirurgią, ponieważ patologiczne potwierdzenie całkowitego zniszczenia guza nie jest możliwe. Dlatego też długoterminowa obserwacja ma kluczowe znaczenie dla oceny kompletności ablacji guza. Idealnie, ablacja przezskórna jest ograniczona do guzów mniejszych niż 3,5 cm i stanowi ukierunkowanie leczenia. Istnieją jednak przypadki, w których ablację można zastosować w przypadku większych guzów.
Dwa główne rodzaje technik ablacji stosowanych w raku nerkowokomórkowym to ablacja częstotliwościami radiowymi i krioablacja .
Ablacja częstotliwościami radiowymi wykorzystuje sondę elektrodową, która jest umieszczana w zaatakowanej tkance, aby wysłać fale radiowe do tkanki w celu wytworzenia ciepła poprzez tarcie cząsteczek wody. Ciepło niszczy tkankę nowotworową. Śmierć komórki zwykle następuje w ciągu kilku minut od wystawienia na działanie temperatury powyżej 50 °C.
Krioablacja obejmuje również wprowadzenie sondy do dotkniętego obszaru, jednak zamiast ciepła do zabicia guza stosuje się zimno. Sonda jest chłodzona bardzo zimnymi płynami chemicznymi. Temperatury zamarzania powodują obumieranie komórek nowotworowych, powodując odwodnienie osmotyczne , które wyciąga wodę z komórki, niszcząc enzym , organelle , błonę komórkową i zamrażając cytoplazmę .
Leki celowane
Nowotwory często rozwijają się w nieokiełznany sposób, ponieważ są w stanie uniknąć układu odpornościowego. Immunoterapia to metoda, która aktywuje układ odpornościowy człowieka i wykorzystuje go na swoją korzyść. Został opracowany po zaobserwowaniu, że w niektórych przypadkach nastąpiła spontaniczna regresja. Immunoterapia wykorzystuje to zjawisko i ma na celu budowanie odpowiedzi immunologicznej człowieka na komórki rakowe.
Inne leki celowane hamują czynniki wzrostu, które, jak wykazano, sprzyjają wzrostowi i rozprzestrzenianiu się guzów. Większość z tych leków została zatwierdzona w ciągu ostatnich dziesięciu lat. Te zabiegi to:
- Niwolumab
- Aksytynib
- Sunitynib
- Kabozantynib
- Ewerolimus
- Lenwatynib
- Pazopanib
- Bewacyzumab
- Sorafenib
- Tiwozanib
- Temsirolimus
- Interleukina-2 (IL-2) spowodowała „trwałe remisje” u niewielkiej liczby pacjentów, ale ze znaczną toksycznością.
- Interferon-α
U pacjentów z rakiem przerzutowym sunitynib prawdopodobnie powoduje większą progresję nowotworu niż pembrolizumab, aksytynib i awelumab. W porównaniu z pembrolizumabem i aksytynibem prawdopodobnie powoduje więcej zgonów, ale może nieznacznie zmniejszyć poważne działania niepożądane. W porównaniu z połączeniami immunoterapii (niwolumabem i ipilimumabem) sunitynib może prowadzić do większej progresji i poważnych skutków. Może być niewielka lub żadna różnica w progresji, przeżyciu i poważnych skutkach między pazopanibem a sunitibem.
Aktywność została również zgłoszona dla ipilimumabu, ale nie jest to zatwierdzony lek na raka nerki.
Oczekuje się, że w najbliższej przyszłości dostępnych będzie więcej leków, ponieważ obecnie prowadzi się kilka badań klinicznych dotyczących nowych terapii celowanych, w tym: atezolizumabu , varlilumabu , durwalumabu , awelumabu , LAG525 , MBG453 , TRC105 i savolitinibu .
Chemoterapia
Chemioterapia i radioterapia nie są tak skuteczne w przypadku RCC. RCC jest oporny w większości przypadków, ale wskaźnik powodzenia wynosi około 4–5%, ale często jest on krótkotrwały, a później rozwija się więcej guzów i narośli.
Terapia adjuwantowa i neoadjuwantowa
Terapia adjuwantowa , która odnosi się do terapii podawanej po pierwotnej operacji, nie okazała się korzystna w przypadku raka nerkowokomórkowego. Odwrotnie, terapia neoadjuwantowa jest stosowana przed zamierzonym leczeniem podstawowym lub głównym. W niektórych przypadkach wykazano, że terapia neoadjuwantowa zmniejsza rozmiar i stadium RCC, aby następnie umożliwić jego chirurgiczne usunięcie. Jest to nowa forma leczenia, a skuteczność tego podejścia jest wciąż oceniana w badaniach klinicznych .
Przerzut
Rak nerkowokomórkowy z przerzutami (mRCC) to rozprzestrzenianie się pierwotnego raka nerkowokomórkowego z nerki do innych narządów. 25-30% ludzi ma przerzuty do czasu zdiagnozowania raka nerkowokomórkowego. Ten wysoki odsetek tłumaczy się tym, że objawy kliniczne są na ogół łagodne do czasu progresji choroby do cięższego stanu. Najczęstszymi miejscami przerzutów są węzły chłonne, płuca, kości, wątroba i mózg. Jak to rozprzestrzenianie się wpływa na zaawansowanie choroby, a tym samym rokowanie, omówiono w rozdziale „Diagnoza” i „Prognoza”.
MRCC ma złe rokowania w porównaniu z innymi nowotworami, chociaż średni czas przeżycia wydłużył się w ciągu ostatnich kilku lat z powodu postępów w leczeniu. Średni czas przeżycia w 2008 r. dla przerzutowej postaci choroby wynosił mniej niż rok, a do 2013 r. poprawił się do średnio 22 miesięcy. Pomimo tej poprawy 5-letni wskaźnik przeżycia dla mRCC pozostaje poniżej 10%, a 20–25% chorych pozostaje nieodpowiadających na żadne terapie, aw tych przypadkach choroba postępuje szybko.
Dostępne metody leczenia RCC omówione w części „Leczenie” są również istotne dla przerzutowej postaci choroby. Opcje obejmują interleukinę-2, która jest standardową terapią zaawansowanego raka nerkowokomórkowego. Od 2007 do 2013 roku zatwierdzono siedem nowych metod leczenia mRCC (sunitynib, temsirolimus, bewacizumab, sorafenib, ewerolimus, pazopanib i aksytynib). Te nowe metody leczenia opierają się na fakcie, że raki nerkowokomórkowe są guzami bardzo naczyniowymi – zawierają dużą liczbę naczyń krwionośnych. Leki mają na celu zahamowanie wzrostu nowych naczyń krwionośnych w guzach, a tym samym spowolnienie wzrostu, aw niektórych przypadkach zmniejszenie wielkości guzów. Efekty uboczne są niestety dość powszechne w przypadku tych zabiegów i obejmują:
- Skutki żołądkowo-jelitowe – nudności, wymioty, biegunka, anoreksja
- Skutki oddechowe – kaszel, duszność (trudności w oddychaniu)
- Wpływ na układ sercowo-naczyniowy – nadciśnienie (wysokie ciśnienie krwi)
- Skutki neurologiczne – krwotok śródczaszkowy (krwawienie do mózgu), zakrzepica (zakrzepy krwi) w mózgu
- Wpływ na skórę i błony śluzowe – wysypki, zespół dłoniowo -podeszwowy , zapalenie jamy ustnej
- Supresja szpiku kostnego – powodująca zmniejszenie liczby białych krwinek, zwiększające ryzyko infekcji oraz niedokrwistości i zmniejszenia liczby płytek krwi
- Wpływ na nerki – upośledzona czynność nerek
- Zmęczenie.
Radioterapia i chemioterapia są częściej stosowane w przerzutowej postaci RCC w celu zwalczania wtórnych guzów kości, wątroby, mózgu i innych narządów. Chociaż nie są lecznicze, te metody leczenia zapewniają ulgę cierpiącym na objawy związane z rozprzestrzenianiem się nowotworów.
Rokowanie
Na rokowanie wpływa kilka czynników, w tym wielkość guza, stopień inwazji i przerzutów, typ histologiczny i stopień zaawansowania jądrowego. Stopień zaawansowania jest najważniejszym czynnikiem w przebiegu raka nerkowokomórkowego. Poniższe liczby są oparte na pacjentach zdiagnozowanych po raz pierwszy w 2001 i 2002 roku przez National Cancer Data Base:
| Scena | Opis | 5-letni wskaźnik przeżycia |
|---|---|---|
| i | Ograniczony do nerki | 81% |
| II | Przedłuż przez torebkę nerkową, ograniczony do powięzi Geroty | 74% |
| III | Uwzględnij żyłę nerkową lub wnękowe węzły chłonne | 53% |
| IV | Obejmuje guzy inwazyjne na sąsiednie narządy (z wyjątkiem nadnerczy) lub przerzuty odległe | 8% |
W koreańskim badaniu oszacowano, że ogólny 5-letni wskaźnik przeżycia specyficznego dla choroby wynosi 85%. W całości, jeśli choroba ogranicza się do nerki, tylko 20–30% rozwija chorobę przerzutową po nefrektomii. Bardziej szczegółowe podzbiory wykazują pięcioletni wskaźnik przeżycia wynoszący około 90-95% dla guzów mniejszych niż 4 cm. W przypadku większych guzów ograniczonych do nerki bez inwazji żylnej przeżywalność jest nadal stosunkowo dobra i wynosi 80–85%. W przypadku guzów, które rozciągają się przez torebkę nerkową i poza lokalne inwestycje powięziowe , przeżywalność zmniejsza się do blisko 60%. Czynniki takie jak ogólny stan zdrowia i kondycja lub nasilenie ich objawów mają wpływ na wskaźniki przeżycia. Na przykład u młodszych osób (w wieku 20–40 lat) rokowanie jest lepsze, pomimo występowania większej liczby objawów, prawdopodobnie z powodu mniejszej częstości rozprzestrzeniania się raka do węzłów chłonnych (stadium III).
Stopień histologiczny jest związany z agresywnością nowotworu i jest klasyfikowany w 4 stopniach, z których 1 ma najlepsze rokowanie (5-letnie przeżycie powyżej 89%), a 4 - najgorsze rokowanie (46% 5-letnich przeżyć).
U niektórych osób rak nerkowokomórkowy zostaje wykryty przed wystąpieniem objawów (przypadkowo) z powodu tomografii komputerowej (tomografii komputerowej) lub USG . Przypadkowo zdiagnozowany rak nerkowokomórkowy (brak objawów) różni się perspektywą od diagnozowanych po wystąpieniu objawów raka nerkowokomórkowego lub przerzutów. 5-letni wskaźnik przeżycia był wyższy w przypadku guzów incydentalnych niż objawowych: 85,3% w porównaniu z 62,5%. Zmiany przypadkowe były znacznie niższe niż te, które powodują objawy, ponieważ 62,1% pacjentów z incydentalnym rakiem nerkowokomórkowym obserwowano ze zmianami w stadium I, w porównaniu do 23% z objawowym rakiem nerkowokomórkowym.
Jeśli ma przerzuty do węzłów chłonnych, 5-letnie przeżycie wynosi około 5% do 15%. W przypadku przerzutowego raka nerkowokomórkowego czynniki, które mogą stanowić złe rokowanie, obejmują niską punktację stanu sprawności Karnofsky'ego (standardowy sposób pomiaru upośledzenia czynnościowego u pacjentów z rakiem), niski poziom hemoglobiny , wysoki poziom dehydrogenazy mleczanowej w surowicy oraz wysoki skorygowany poziom wapnia w surowicy. W przypadkach bez przerzutów algorytm punktacji Leibovicha może być stosowany do przewidywania pooperacyjnego progresji choroby.
Rak nerkowokomórkowy jest jednym z nowotworów najsilniej związanych z zespołami paranowotworowymi , najczęściej z powodu ektopowej produkcji hormonów przez guz. Leczenie tych powikłań RCC jest na ogół ograniczone do leczenia raka podstawowego.
Epidemiologia
Częstość występowania choroby różni się w zależności od czynników geograficznych, demograficznych i, w mniejszym stopniu, dziedzicznych. Istnieje kilka znanych czynników ryzyka, jednak znaczenie innych potencjalnych czynników ryzyka pozostaje bardziej kontrowersyjne. Zachorowalność na raka wzrastała na całym świecie w tempie około 2-3% na dekadę, aż do ostatnich kilku lat, kiedy liczba nowych przypadków ustabilizowała się.
Częstość występowania RCC różni się w zależności od płci, wieku, rasy i położenia geograficznego na całym świecie. Mężczyźni mają większą zachorowalność niż kobiety (około 1,6:1), a zdecydowana większość jest diagnozowana po 65 roku życia. Azjaci mają podobno znacznie niższą zapadalność na RCC niż biali i podczas gdy kraje afrykańskie mają najniższą zachorowalność, Afroamerykanie mają najwyższą zapadalność w populacji w Stanach Zjednoczonych. Kraje rozwinięte mają większą częstość występowania niż kraje rozwijające się, z najwyższymi wskaźnikami w Ameryce Północnej, Europie i Australii / Nowej Zelandii
Historia
Daniel Sennert poczynił pierwszą wzmiankę sugerującą powstawanie guza w nerce w swoim tekście Practicae Medicinae , opublikowanym po raz pierwszy w 1613 roku.
Miril opublikował najwcześniejszy jednoznaczny przypadek raka nerki w 1810 roku. Opisał przypadek Françoise Levelly, 35-letniej kobiety, która 6 kwietnia 1809 roku zgłosiła się do Brzeskiego Szpitala Miejskiego, przypuszczalnie w późnym okresie ciąży.
Koenig opublikował pierwszą klasyfikację guzów nerek opartą na morfologii makroskopowej w 1826 roku. Koenig podzielił guzy na formy włókniste, tłuszczakowate, grzybowe i rdzeniaste.
Kontrowersje dotyczące hipernerka
Po dokonaniu klasyfikacji guza badacze podjęli próbę zidentyfikowania tkanki, z której pochodzi rak nerki.
Patogeneza nerkowych nowotworów nabłonkowych był rozważany od dziesięcioleci. Debata została zainicjowana przez Paula Grawitza, kiedy w 1883 roku opublikował swoje obserwacje dotyczące morfologii małych, żółtych guzów nerek . Grawitz doszedł do wniosku, że tylko guzy pęcherzykowe pochodzą z nadnerczy , podczas gdy guzy brodawkowate pochodzą z tkanki nerek .
W 1893 roku Paul Sudeck zakwestionował teorię postulowaną przez Grawitza, publikując opisy guzów nerek, w których zidentyfikował nietypowe cechy w obrębie kanalików nerkowych i odnotował gradację tych nietypowych cech pomiędzy kanalikami a sąsiadującym nowotworem złośliwym . W 1894 roku Otto Lubarsch , który poparł teorię postulowaną przez Grawitza, ukuł termin guz nadnerczy , który został zmieniony na hipernefroma przez Felixa Victora Birch-Hirschfelda w celu opisania tych guzów.
Ostrą krytykę Grawitza przedstawił w 1908 r. Oskar Stoerk, który uważał, że nadnerczowe pochodzenie guzów nerek nie zostało udowodnione. Pomimo przekonujących argumentów przeciwko teorii wysuniętej przez Grawitza, w literaturze utrzymał się termin hipernerczak, z towarzyszącym mu konotacją nadnerczową.
Foot i Humphreys oraz Foote i in. wprowadził termin rak nerkowokomórkowy, aby podkreślić pochodzenie tych nowotworów z kanalików nerkowych . Ich nazwa została nieznacznie zmieniona przez Fettera na obecnie powszechnie akceptowany termin rak nerkowokomórkowy .
Przekonujące dowody na rozstrzygnięcie debaty przedstawili Oberling i in. w 1959, który badał ultrastrukturę czystych komórek z ośmiu raków nerki . Odkryli, że cytoplazma komórek nowotworowych zawiera liczne mitochondria oraz złogi glikogenu i tłuszczu. Zidentyfikowali błony cytoplazmatyczne umieszczone prostopadle na błonie podstawnej z rzadkimi komórkami zawierającymi mikrokosmki wzdłuż wolnych granic. Doszli do wniosku, że te cechy wskazują, że guzy powstały z komórek nabłonkowych kanalików nerkowych , ostatecznie rozstrzygając jeden z najbardziej dyskutowanych problemów w patologii guza .
Zobacz też
- Zespół Stauffera
- Hipoteza Knudsona
- Interleukina-2
- Rak nerki
- Rapamycyna
- Winblastyna
- Dysuria
- Interferon
Bibliografia
Zewnętrzne linki
| Klasyfikacja | |
|---|---|
| Zasoby zewnętrzne |