Steryd - Steroid

Steroid jest biologicznie aktywnym związkiem organicznym z czterema pierścieniami umieszczonymi w określonej konfiguracji cząsteczkowej . Steroidy pełnią dwie podstawowe funkcje biologiczne: jako ważne składniki błon komórkowych, które zmieniają płynność błon ; oraz jako cząsteczki sygnalizacyjne . Setki sterydów znajdują się w roślinach , zwierzętach i grzybach . Wszystkie sterydy są wytwarzane w komórkach ze steroli lanosterolu ( opistokonts ) lub cykloartenolu (rośliny). Lanosterolu i cykloartenol pochodzą z cyklizacji z triterpenowe skwalenu .
Struktura rdzenia steroidu zazwyczaj składa się z siedemnastu atomów węgla, połączonych w cztery „ skondensowane ” pierścienie: trzy sześcioczłonowe pierścienie cykloheksanowe (pierścienie A, B i C na pierwszej ilustracji) i jeden pięcioczłonowy pierścień cyklopentanowy (pierścień D) . Steroidy różnią się w zależności od grup funkcyjnych przyłączonych do tego czteropierścieniowego rdzenia i stanu utlenienia pierścieni. Sterole są formami steroidów z grupą hydroksylową w pozycji 3 i szkieletem pochodzącym z cholestanu . Steroidy można również bardziej radykalnie modyfikować, np. poprzez zmiany w strukturze pierścienia, na przykład przecięcie jednego z pierścieni. Pierścień tnący B wytwarza sekosteroidy, z których jednym jest witamina D 3 .
Przykłady obejmują lipidowego cholesterolu hormony płciowe estradiol i testosteron , i przeciwzapalne leki deksametazon .
Nomenklatura

Gonane , znany również jako steran lub cyklopentanoperhydrofenantren, najprostszy steroid i jądro wszystkich steroidów i steroli, składa się z siedemnastu atomów węgla w wiązaniach węgiel-węgiel tworzących cztery skondensowane pierścienie w trójwymiarowym kształcie . Trzy cykloheksan pierścienie (A, B i C, na pierwszej ilustracji) tworzą szkielet perhydro pochodną fenantren . Pierścień D ma strukturę cyklopentanową . Gdy obecne są dwie grupy metylowe i osiem węglowych łańcuchów bocznych (w C-17, jak pokazano dla cholesterolu), mówi się, że steroid ma szkielet cholestanowy. Dwie powszechne stereoizomeryczne postaci 5α i 5β steroidów istnieją z powodu różnic po stronie w dużej mierze płaskiego układu pierścieniowego, do którego przyłączony jest atom wodoru (H) przy węglu-5, co powoduje zmianę konformacji pierścienia A steroidu. Izomeryzacja w łańcuchu bocznym C-21 wytwarza równoległą serię związków, zwanych izosteroidami.
Przykładami struktur steroidowych są:
Testosteron , główny męski hormon płciowy i steryd anaboliczny
Kwas cholowy , A kwasu żółciowego , pokazując kwas karboksylowy i dodatkowe grupy hydroksylowe, często obecne
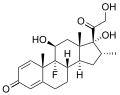
Deksametazon , syntetyczny lek kortykosteroidowy
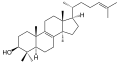
Lanosterol , biosyntetyczny prekursor sterydów zwierzęcych. Liczba węgli (30) wskazuje na jego klasyfikację triterpenoidową .
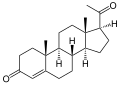
Progesteron , hormon steroidowy zaangażowany w żeński cykl menstruacyjny, ciążę i embriogenezę
Medrogestone , syntetyczny lek o działaniu podobnym do progesteronu
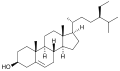
β-sitosterol , roślina lub fitosterol , z w pełni rozgałęzionym węglowodorowym łańcuchem bocznym przy C-17 i grupą hydroksylową przy C-3
Oprócz rozerwania pierścienia (rozszczepienia), ekspansji i skurczów (rozszczepianie i ponowne zamykanie do większych lub mniejszych pierścieni) - wszystkie odmiany w strukturze wiązania węgiel-węgiel - steroidy mogą się również różnić:
- w zamówieniach obligacji w pierścieniach,
- w liczbie grup metylowych przyłączonych do pierścienia (i, jeśli są obecne, na widocznym łańcuchu bocznym przy C17),
- w grupach funkcyjnych przyłączonych do pierścieni i łańcucha bocznego oraz
- w konfiguracji grup dołączonych do pierścieni i łańcuszka.
Na przykład, sterole, takie jak cholesterol i lanosterol, mają grupę hydroksylową przyłączoną w pozycji C-3, podczas gdy testosteron i progesteron mają karbonyl (podstawnik okso) w pozycji C-3; z nich, sam lanosterol ma dwie grupy metylowe w C-4, a cholesterol (z podwójnym wiązaniem C-5 do C-6) różni się od testosteronu i progesteronu (które mają podwójne wiązanie C-4 do C-5).

Cholesterol , prototypowy sterol zwierzęcy. Ten strukturalny lipid i kluczowy steroidowy prekursor biosyntezy .
|

5α- cholestan , wspólny rdzeń steroidowy
|
Rozmieszczenie gatunków i funkcja
U eukariontów sterydy znajdują się w grzybach, zwierzętach i roślinach.
Sterydy grzybicze
Steroidy grzybicze obejmują ergosterole , które biorą udział w utrzymaniu integralności błony komórkowej grzyba. Różne leki przeciwgrzybicze , takie jak amfoterycyna B i azolowe leki przeciwgrzybicze , wykorzystują te informacje do zabijania grzybów chorobotwórczych . Grzyby mogą zmieniać zawartość ergosterolu (np. poprzez utratę funkcji mutacje w enzymach ERG3 lub ERG6 , powodujące zubożenie ergosterolu lub mutacje, które zmniejszają zawartość ergosterolu), aby rozwinąć oporność na leki ukierunkowane na ergosterol. Ergosterol jest analogiczny do cholesterolu znajdującego się w błonach komórkowych zwierząt (w tym ludzi) lub fitosteroli znajdujących się w błonach komórkowych roślin. Wszystkie grzyby zawierają duże ilości ergosterolu, rzędu dziesiątek do setek miligramów na 100 gram suchej masy. Tlen jest niezbędny do syntezy ergosterolu w grzybach. Ergosterol odpowiada za zawartość witaminy D w grzybach; ergosterol jest chemicznie przekształcany w prowitaminę D2 pod wpływem światła ultrafioletowego . Prowitamina D2 spontanicznie tworzy witaminę D2. Jednak nie wszystkie grzyby wykorzystują ergosterol w swoich błonach komórkowych; na przykład patogenny gatunek grzyba Pneumocystis jirovecii nie ma, co ma istotne implikacje kliniczne (biorąc pod uwagę mechanizm działania wielu leków przeciwgrzybiczych). Na przykładzie grzyba Saccharomyces cerevisiae inne główne steroidy obejmują ergosta-5,7,22,24(28)-tetraen-3β-ol , zymosterol i lanosterol . S. cerevisiae wykorzystuje w swojej błonie komórkowej 5,6-dihydroergosterol zamiast ergosterolu.
Sterydy zwierzęce
Steroidy zwierzęce obejmują związki pochodzące od kręgowców i owadów , przy czym te ostatnie obejmują ekdysteroidy, takie jak ekdysteron (kontrolujący linienie u niektórych gatunków). Przykłady kręgowców obejmują hormony steroidowe i cholesterol; ten ostatni jest składnikiem strukturalnym błon komórkowych, który pomaga określić płynność błon komórkowych i jest głównym składnikiem płytki nazębnej (uczestniczącej w miażdżycy ). Hormony steroidowe obejmują:
- Hormony płciowe , które wpływają na różnice płci i wspomagają reprodukcję . Należą do nich androgeny , estrogeny i progestageny .
- Kortykosteroidy , w tym większość syntetycznych leków steroidowych, z naturalnych produktów klasach glukokortykoidy (które regulują wiele aspektów metabolizmu i funkcji układu immunologicznego ) i mineralokortykoidów (co pomaga w utrzymaniu objętości krwi i kontrolować nerkowego wydalania elektrolitów )
- Sterydy anaboliczne , naturalne i syntetyczne, które oddziałują z receptorami androgenowymi w celu zwiększenia syntezy mięśni i kości. W powszechnym użyciu termin „sterydy” często odnosi się do sterydów anabolicznych.
Sterydy roślinne
Steroidy roślinne obejmują alkaloidy steroidowe występujące w Solanaceae i Melanthiaceae (szczególnie rodzaj Veratrum ), glikozydy nasercowe , fitosterole i brassinosteroidy (w tym kilka hormonów roślinnych).
Prokariota
W prokariontach , biosyntetyczne drogi istnieją tetracyklicznego steroidowych (na przykład w ramach prątków ) - gdzie jego pochodzenie z eukariontów przypuszcza - a bardziej wspólnej jonem triterpinoid hopanoid ramy.
Rodzaje
Według funkcji
Główne klasy hormonów steroidowych , z wybitnymi członkami i przykładami powiązanych funkcji, to:
-
Kortykosteroidy :
-
Glikokortykosteroidy :
- Kortyzol , glikokortykoid, którego funkcje obejmują immunosupresję
-
Mineralokortykoidy :
- Aldosteron , mineralokortykoid, który pomaga regulować ciśnienie krwi poprzez równowagę wodno-elektrolitową
-
Glikokortykosteroidy :
-
Sterydy płciowe :
-
Progestageny :
- Progesteron , który reguluje cykliczne zmiany w endometrium w macicy i podtrzymuje ciążę
-
Androgeny :
- Testosteron , który przyczynia się do rozwoju i utrzymania męskich drugorzędowych cech płciowych
-
Estrogeny :
- Estradiol , który przyczynia się do rozwoju i utrzymania kobiecych drugorzędowych cech płciowych
-
Progestageny :
Dodatkowe klasy sterydów obejmują:
- Neurosteroidy, takie jak DHEA i allopregnanolon
- Aminosteroidowe leki blokujące przewodnictwo nerwowo-mięśniowe, takie jak bromek pankuronium
Jak również następująca klasa sekosteroidów (steroidy z otwartym pierścieniem):
- Formy witaminy D, takie jak ergokalcyferol , cholekalcyferol i kalcytriol
Według struktury
Nienaruszony system pierścieni
Sterydy można klasyfikować na podstawie ich składu chemicznego. Jeden przykład tego, jak MeSH przeprowadza tę klasyfikację, jest dostępny w katalogu Wikipedia MeSH. Przykłady tej klasyfikacji obejmują:
| Klasa | Przykład | Liczba atomów węgla |
|---|---|---|
| Cholestany | Cholesterol | 27 |
| Cholany | Kwas cholowy | 24 |
| Kobiety w ciąży | Progesteron | 21 |
| Androstany | Testosteron | 19 |
| Estranie | Estradiol | 18 |
Gonan (jądro steroidowe) jest macierzystą 17-węglową cząsteczką tetracyklicznego węglowodoru bez alkilowych łańcuchów bocznych.
Rozcięte, skurczone i rozszerzone pierścienie
Sekosteroidy (łac. seco , „do cięcia”) są podklasą związków steroidowych powstających, biosyntetycznie lub koncepcyjnie, z rozszczepienia (rozszczepienia) macierzystych pierścieni steroidowych (zwykle jednego z czterech). Główne podklasy sekosteroidów są definiowane przez steroidowe atomy węgla, w których nastąpiło to rozszczepienie. Na przykład, prototypowego secosteroid cholekalcyferolu , witamina D 3 (na rysunku), znajduje się w 9,10-secosteroid podklasy i jest otrzymywana w wyniku rozszczepiania atomach węgla C-9 i C-10 z B-steroidowego pierścienia; 5,6-sekosteroidy i 13,14-steroidy są podobne.
Norsteroidy ( nor- , L. norma ; „normalne” w chemii, wskazujące na usuwanie węgla) i homosteroidy (homo-, greckie homos ; „takie same”, wskazujące na dodanie węgla) są strukturalnymi podklasami steroidów powstałych w etapach biosyntezy. Były enzymatyczna obejmuje pierścieniowe rozszerzenia skurcz reakcji, a ta ostatnia jest realizowane ( biomimetically ) lub (częściej) poprzez zamknięcie pierścienia z alifatycznych prekursorów z (lub nawet mniej) atomów pierścienia, niż wyjściowy steroidów ramy.
Kombinacje tych zmian pierścienia są znane z natury. Na przykład owce, które pasą się na lilii kukurydzianej, spożywają cyklopaminę (pokazano) i weratraminę , dwie z podrodziny steroidów, w których pierścienie C i D są odpowiednio kurczone i rozszerzane poprzez biosyntetyczną migrację pierwotnego atomu C-13. Spożycie tych C-nor-D-homosteroids powoduje wady wrodzone u jagniąt: Cyclopia z cyclopamine i nóg deformacji od veratramine. Kolejny C-nor-D-homosteroid (nakiterpiozyna) jest wydalany przez okinawskie cyjanobakteriosgąbki . np. Terpios hoshinota , co prowadzi do śmiertelności koralowców z powodu choroby czarnego korala. Sterydy typu nakiterpiozyny są aktywne przeciwko szlakowi sygnałowemu obejmującemu białka wygładzone i hedgehog , szlaku, który jest nadaktywny w wielu nowotworach.
Znaczenie biologiczne
Steroidy i ich metabolity często działają jako cząsteczki sygnalizacyjne (najważniejszymi przykładami są hormony steroidowe), a steroidy i fosfolipidy są składnikami błon komórkowych . Sterydy, takie jak cholesterol, zmniejszają płynność błony . Podobnie jak lipidy , sterydy są wysoce skoncentrowanymi magazynami energii. Nie są to jednak zazwyczaj źródła energii; u ssaków są one normalnie metabolizowane i wydalane.
Sterydy odgrywają kluczową rolę w wielu chorobach, w tym w nowotworach złośliwych, takich jak rak prostaty , gdzie produkcja sterydów wewnątrz i na zewnątrz guza sprzyja agresywności komórek rakowych.
Biosynteza i metabolizm
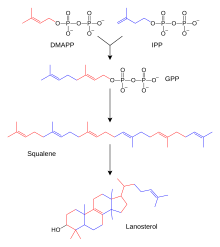
Setki steroidów występujących u zwierząt, grzybów i roślin wytwarza się z lanosterolu (u zwierząt i grzybów; patrz przykłady powyżej) lub cykloartenolu (u roślin). Lanosterolu i cykloartenol pochodzą z cyklizacji z triterpenoidów skwalen .
Biosynteza sterydów to ścieżka anaboliczna , która wytwarza steroidy z prostych prekursorów. U zwierząt przebiega unikalny szlak biosyntetyczny (w porównaniu z wieloma innymi organizmami ), co sprawia, że szlak ten jest powszechnym celem dla antybiotyków i innych leków przeciwinfekcyjnych. Metabolizm steroidów u ludzi jest również celem leków obniżających poziom cholesterolu, takich jak statyny.
U ludzi i innych zwierząt biosynteza steroidów przebiega w szlaku mewalonianu, który wykorzystuje acetylo-CoA jako elementy budulcowe pirofosforanu dimetyloallilu (DMAPP) i pirofosforanu izopentenylu (IPP). W kolejnych etapach DMPP i IPP łączą się, tworząc pirofosforan geranylu (GPP), który syntetyzuje steroid lanosterol. Modyfikacje lanosterolu w inne steroidy zaliczane są do przemian steroidogenezy.
Szlak mewalonianowy
Szlak mewalonianu (zwany również szlakiem reduktazy HMG-CoA) zaczyna się od acetylo-CoA i kończy na pirofosforanie dimetyloallilu (DMAPP) i pirofosforanie izopentenylu (IPP).
DMPP i IPP oddają jednostki izoprenowe , które są składane i modyfikowane w celu utworzenia terpenów i izoprenoidów (duża klasa lipidów, do której należą karotenoidy i tworzą największą klasę naturalnych produktów roślinnych . Tutaj jednostki izoprenowe są łączone w skwalen i sfałdowane). w zestaw pierścieni, aby wytworzyć lanosterol .Lanosterol można następnie przekształcić w inne steroidy, takie jak cholesterol i ergosterol .
Dwie klasy leków celują w szlak mewalonianowy : statyny (takie jak rosuwastatyna ), które są stosowane w celu obniżenia podwyższonego poziomu cholesterolu oraz bisfosfoniany (takie jak zoledronian ), które są stosowane w leczeniu wielu chorób zwyrodnieniowych kości.
Steroidogeneza
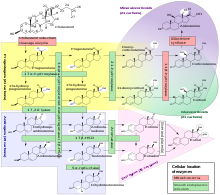
Steroidogeneza to proces biologiczny, w którym steroidy są generowane z cholesterolu i zamieniane w inne steroidy. Te ścieżki steroidogenezy różnić się między gatunkami. Jak wspomniano powyżej, główne klasy hormonów steroidowych (z ich znaczącymi składnikami i funkcjami) to progestogen , kortykosteroidy (kortykoidy), androgeny i estrogeny . Ludzka steroidogeneza tych klas zachodzi w kilku miejscach:
- Progestogeny są prekursorami wszystkich innych ludzkich sterydów, a wszystkie ludzkie tkanki, które produkują sterydy, muszą najpierw przekształcić cholesterol w pregnenolon . Ta konwersja jest etapem ograniczającym szybkość syntezy steroidów, który zachodzi wewnątrz mitochondrium odpowiedniej tkanki.
- Kortyzol, kortykosteron, aldosteron i testosteron są produkowane w korze nadnerczy .
- Estradiol, estron i progesteron powstają głównie w jajniku , estriol w łożysku podczas ciąży, a testosteron głównie w jądrach (część testosteronu jest również wytwarzana w korze nadnerczy).
- Estradiol jest przekształcany bezpośrednio z testosteronu (u mężczyzn) lub poprzez główny szlak DHEA – androstendion – estron i wtórnie poprzez testosteron (u kobiet).
- Wykazano, że komórki zrębowe wytwarzają steroidy w odpowiedzi na sygnalizację wytwarzaną przez komórki raka prostaty pozbawione androgenów .
- Niektóre neurony i glej w ośrodkowym układzie nerwowym (OUN) wyrażają enzymy niezbędne do lokalnej syntezy pregnenolonu, progesteronu, DHEA i DHEAS, de novo lub ze źródeł obwodowych.
| Seks | Hormon płciowy | Faza reprodukcyjna |
Tempo produkcji krwi |
Szybkość wydzielania gonad |
Wskaźnik klirensu metabolicznego |
Zakres referencyjny (poziomy w surowicy) | |
|---|---|---|---|---|---|---|---|
| Jednostki SI | Nie- SI jednostek | ||||||
| Mężczyźni | Androstendion |
–
|
2,8 mg/dzień | 1,6 mg/dzień | 2200 l/dzień | 2,8-7,3 nmol/L | 80–210 ng/dL |
| Testosteron |
–
|
6,5 mg/dzień | 6,2 mg/dzień | 950 l/dzień | 6,9–34,7 nmol/l | 200–1000 ng/dL | |
| Estrone |
–
|
150 μg/dzień | 110 μg/dzień | 2050 l/dzień | 37–250 pmol/l | 10–70 pg/ml | |
| Estradiol |
–
|
60 μg/dzień | 50 μg/dzień | 1600 l/dzień | <37–210 pmol/l | 10–57 pg/ml | |
| Siarczan estronu |
–
|
80 μg/dzień | Nieistotny | 167 l/dzień | 600–2500 pmol/l | 200–900 pg/ml | |
| Kobiety | Androstendion |
–
|
3,2 mg/dzień | 2,8 mg/dzień | 2000 l/dzień | 3,1–12,2 nmol/l | 89–350 ng/dL |
| Testosteron |
–
|
190 μg/dzień | 60 μg/dzień | 500 l/dzień | 0,7–2,8 nmol/l | 20–81 ng/dL | |
| Estrone | Faza folikularna | 110 μg/dzień | 80 μg/dzień | 2200 l/dzień | 110–400 pmol/l | 30–110 pg/ml | |
| Faza lutealna | 260 μg/dzień | 150 μg/dzień | 2200 l/dzień | 310–660 pmol/l | 80–180 pg/ml | ||
| Po menopauzie | 40 μg/dzień | Nieistotny | 1610 l/dzień | 22–230 pmol/l | 6–60 pg/ml | ||
| Estradiol | Faza folikularna | 90 μg/dzień | 80 μg/dzień | 1200 l/dzień | <37–360 pmol/l | 10-98 pg/ml | |
| Faza lutealna | 250 μg/dzień | 240 μg/dzień | 1200 l/dzień | 699–1250 pmol/l | 190–341 pg/ml | ||
| Po menopauzie | 6 μg/dzień | Nieistotny | 910 l/dzień | <37–140 pmol/l | 10-38 pg/ml | ||
| Siarczan estronu | Faza folikularna | 100 μg/dzień | Nieistotny | 146 l/dzień | 700–3600 pmol/l | 250–1300 pg/ml | |
| Faza lutealna | 180 μg/dzień | Nieistotny | 146 l/dzień | 1100–7300 pmol/l | 400–2600 pg/ml | ||
| Progesteron | Faza folikularna | 2 mg/dzień | 1,7 mg/dzień | 2100 l/dzień | 0,3–3 nmol/l | 0,1–0,9 ng/ml | |
| Faza lutealna | 25 mg/dzień | 24 mg/dzień | 2100 l/dzień | 19–45 nmol/l | 6–14 ng/ml | ||
|
Uwagi i źródła
Uwagi: „ Stężenie steroidu w krążeniu zależy od szybkości, z jaką jest on wydzielany z gruczołów, szybkości metabolizmu prekursora lub prehormonów do steroidu oraz szybkości, z jaką jest on ekstrahowany przez tkanki i metabolizowany. Szybkość wydzielania steroidu odnosi się do całkowitego wydzielania związku z gruczołu w jednostce czasu. Szybkość wydzielania oszacowano przez pobieranie próbek żylnych z gruczołu w czasie i odjęcie stężenia hormonów w tętnicach i żyłach obwodowych. Szybkość klirensu metabolicznego steroidu definiuje się jako objętość krwi, która została całkowicie oczyszczona z hormonu w jednostce czasu. Szybkość produkcji hormonu steroidowego odnosi się do wejścia do krwi związku ze wszystkich możliwych źródeł, w tym wydzielania z gruczołów i konwersji prohormony do sterydu będącego przedmiotem zainteresowania. W stanie stacjonarnym ilość hormonu wchodzącego do krwi ze wszystkich źródeł będzie równa tempu, w jakim jest cl ucha (wskaźnik klirensu metabolicznego) pomnożony przez stężenie we krwi (wskaźnik produkcji = tempo klirensu metabolicznego × stężenie). Jeśli jest niewielki udział metabolizmu prohormonów w krążącej puli sterydów, wtedy tempo produkcji będzie zbliżone do tempa wydzielania." Źródła: patrz szablon.
|
|||||||
Alternatywne ścieżki
W roślinach i bakteriach szlak niemewalonianowy wykorzystuje pirogronian i 3-fosforan gliceraldehydu jako substraty.
Podczas chorób mogą zostać wykorzystane szlaki inaczej nieistotne u zdrowych ludzi. Na przykład, w jednej z postaci wrodzonej nadnerczy rozrost niedobór 21-hydroksylazy enzymów szlaku prowadzi do nadmiaru 17a-hydroksyprogesteron (17-OHP) - jest patologiczna nadmiar 17-OHP z kolei można przekształcić do dihydrotestosteronu (DHT silnym androgenem) poprzez m.in. 17,20 Lyase (członek rodziny enzymów cytochromu P450 ), 5α-reduktazę i dehydrogenazę 3α-hydroksysteroidową .
Katabolizm i wydalanie
Steroidy są głównie utleniane przez enzymy oksydazy cytochromu P450 , takie jak CYP3A4 . Reakcje te wprowadzają tlen do pierścienia steroidowego, umożliwiając rozkład cholesterolu przez inne enzymy do kwasów żółciowych. Kwasy te mogą być następnie wydalane przez wydzielanie z wątroby wraz z żółcią . Ekspresja genu oksydazy może być podwyższona przez czujnik steroidów PXR, gdy występuje wysokie stężenie steroidów we krwi. Hormony steroidowe, pozbawione łańcucha bocznego cholesterolu i kwasów żółciowych, są zazwyczaj hydroksylowane w różnych pozycjach pierścienia lub utleniane w pozycji 17 , sprzężone z siarczanem lub kwasem glukuronowym i wydalane z moczem.
Izolacja, określenie struktury i metody analizy
Izolacja sterydowa , w zależności od kontekstu, to izolacja substancji chemicznej wymaganej do wyjaśnienia struktury chemicznej , chemii derywatyzacji lub degradacji, testów biologicznych i innych potrzeb badawczych (zwykle miligramy do gramów, ale często więcej lub izolacja „ilości analitycznych” substancja będąca przedmiotem zainteresowania (gdzie nacisk kładziony jest na identyfikację i ilościowe określenie substancji (na przykład w tkance lub płynie biologicznym). Wyizolowana ilość zależy od metody analitycznej, ale zazwyczaj jest mniejsza niż jeden mikrogram. Metody izolacji w celu osiągnięcia tych dwóch skale produktu są różne, ale obejmują ekstrakcję , wytrącanie, adsorpcję , chromatografię i krystalizację . W obu przypadkach wyizolowana substancja jest oczyszczana do chemicznej jednorodności; połączone metody rozdzielania i analityczne, takie jak LC-MS , są wybierane jako „ortogonalne „—osiągając ich separacje w oparciu o różne sposoby interakcji między substancją a macierzą izolującą — w celu wykrycia pojedynczego gatunku w czystej próbce. Określenie struktury odnosi się do metod określania struktury chemicznej wyizolowanego czystego steroidu przy użyciu ewoluującego szeregu metod chemicznych i fizycznych, które obejmują NMR i krystalografię małocząsteczkową . Metody analizy pokrywają się z obydwoma powyższymi obszarami, kładąc nacisk na metody analityczne do określenia, czy steroid występuje w mieszaninie i określenia jego ilości.
Synteza chemiczna
Mikrobiologiczne katabolizm z fitosteroli łańcuchów bocznych uzyskuje steroidów C-19, C-22, sterydów i 17-ketosteroidów (tj prekursory do kory hormonów i antykoncepcyjne ). Dodawanie i modyfikacja grup funkcyjnych ma kluczowe znaczenie przy wytwarzaniu szerokiej gamy leków dostępnych w ramach tej klasyfikacji chemicznej. Te modyfikacje przeprowadza się przy użyciu konwencjonalnych technik syntezy organicznej i/lub biotransformacji .
Prekursory
Półsynteza
Półsyntezy steroidów często rozpoczyna się od prekursorów, takich jak cholesterol , fitosterole , lub sapogeniny . Wysiłki Syntex , firmy zajmującej się meksykańskim handlem barbasco , wykorzystały Dioscorea mexicana do produkcji diosgeniny sapogeniny we wczesnych dniach przemysłu farmaceutycznego syntetycznych sterydów .
Całkowita synteza
Pewne hormony steroidowe są ekonomicznie uzyskać jedynie przez całkowitą syntezę z przemysłu petrochemicznego (na przykład 13- alkilowe steroidy). Na przykład, środek farmaceutyczny Norgestrel rozpoczyna się od metoksy -1- tetralonu , petrochemicznej pochodzącego z fenolem .
Nagrody naukowe
Za badania nad sterydami przyznano szereg Nagród Nobla , w tym:
- 1927 ( Chemia ) Heinrich Otto Wieland — Konstytucja kwasów żółciowych i steroli oraz ich związek z witaminami
- 1928 (Chemia) Adolf Otto Reinhold Windaus — Konstytucja steroli i ich związek z witaminami
- 1939 (Chemia) Adolf Butenandt i Leopold Ružička — Izolacja i badania strukturalne steroidowych hormonów płciowych oraz powiązane badania nad wyższymi terpenami
- 1950 ( fizjologia lub medycyna ) Edward Calvin Kendall , Tadeus Reichstein i Philip Hench -- Struktura i działanie biologiczne hormonów nadnerczy .
- 1965 (Chemia) Robert Burns Woodward — częściowo za syntezę cholesterolu, kortyzonu i lanosterolu
- 1969 (Chemia) Derek Barton i Odd Hassel — Rozwój koncepcji konformacji w chemii z podkreśleniem jądra steroidowego
- 1975 (Chemia) Vladimir Prelog — m.in. za opracowanie metod określania stereochemicznego przebiegu biosyntezy cholesterolu z kwasu mewalonowego przez skwalen
Zobacz też
Bibliografia
Bibliografia
- Russell CA (2005). „Chemia organiczna: produkty naturalne, sterydy”. W Russell CA, Roberts GK (red.). Historia chemiczna: recenzje najnowszej literatury . Cambridge: RSC Publ. Numer ISBN 978-0-85404-464-1.
- "Russell Marker Stworzenie meksykańskiego przemysłu hormonów steroidowych - punkt orientacyjny -" . Amerykańskie Towarzystwo Chemiczne. 1999.
- Lednicer D (2011). Chemia sterydów w skrócie . Hoboken: Wiley. doi : 10.1002/9780470973639 . Numer ISBN 978-0-470-66085-0. Zwięzła historia badań nad sterydami.
- Yoder RA, Johnston JN (grudzień 2005). „Studium przypadku w biomimetycznej syntezie całkowitej: karbocyklizacja poliolefin do terpenów i steroidów” . Recenzje chemiczne . 105 (12): 4730–56. doi : 10.1021/cr040623l . PMC 2575671 . PMID 16351060 .Przegląd historii syntezy steroidów, zwłaszcza biomimetycznych .
- Han TS, Walker BR, Arlt W, Ross RJ (luty 2014). „Leczenie i wyniki zdrowotne u dorosłych z wrodzonym przerostem nadnerczy”. Recenzje przyrody. Endokrynologia . 10 (2): 115-24. doi : 10.1038/nrendo.2013.239 . PMID 24342885 . S2CID 6090764 . Szlak steroidogenezy nadnerczy.
- Greep RO, wyd. (22 października 2013). „Kwasy korowe” . Najnowsze postępy w badaniach nad hormonami: Proceedings of the Laurentian Hormone Conference 1979 . Elsevier Nauka . s. 345-391. Numer ISBN 978-1-4832-1956-1.
- RZS Bowena (20 października 2001). „Steroidogeneza” . Patofizjologia układu hormonalnego . Uniwersytet Stanowy Kolorado. Zarchiwizowane z oryginału 28 lutego 2009 r.