Tamoksyfen - Tamoxifen
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Nolvadex, Genox, Tamifen, inne |
| Inne nazwy | TMX; ICI-46474 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a682414 |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Ustami |
| Klasa leków | Selektywny modulator receptora estrogenowego |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | ~100% |
| Wiązanie białek | >99% ( albumina ) |
| Metabolizm | Wątroba ( CYP3A4 , CYP2C9 , CYP2D6 ) |
| Metabolity | • N -Desmethyltamoxifen • endoksyfenu (4-hydroksy- N -desmethyltamoxifen) • Afimoxifene (4-hydroksytamoksyfen), • N , N -Didesmethyltamoxifen • Norendoxifen (4-hydroksy- N , N -didesmethyltamoxifen) • inne, koniugaty |
| Okres półtrwania eliminacji | 5–7 dni |
| Wydalanie |
Kał : 65% Mocz : 9% |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Ligand PDB | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.031.004 |
| Dane chemiczne i fizyczne | |
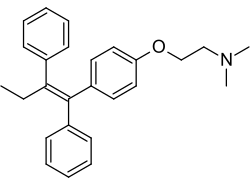
| Formuła | C 26 H 29 N O |
| Masa cząsteczkowa | 371,524 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Tamoksyfen , sprzedawany m.in. pod marką Nolvadex , jest selektywnym modulatorem receptora estrogenowego, stosowanym w profilaktyce raka piersi u kobiet oraz w leczeniu raka piersi u kobiet i mężczyzn. Jest również badany pod kątem innych rodzajów raka . Był używany w zespole Albrighta . Tamoksyfen jest zazwyczaj przyjmowany codziennie doustnie przez pięć lat w przypadku raka piersi.
Poważne skutki uboczne obejmują niewielki wzrost ryzyka raka macicy , udaru mózgu , problemów ze wzrokiem i zatorowości płucnej . Częste działania niepożądane obejmują nieregularne miesiączki , utratę wagi i uderzenia gorąca . Może zaszkodzić dziecku, jeśli zostanie zażyty w czasie ciąży lub karmienia piersią . Jest selektywnym modulatorem receptora estrogenowego (SERM) i działa poprzez zmniejszenie wzrostu komórek raka piersi. Należy do grupy związków trifenyloetylenowych .
Tamoksyfen został początkowo wyprodukowany w 1962 roku przez chemik Dorę Richardson. Znajduje się na Liście Leków Podstawowych Światowej Organizacji Zdrowia . Tamoksyfen jest dostępny jako lek generyczny . W 2018 roku był to 262. najczęściej przepisywany lek w Stanach Zjednoczonych, z ponad milionem recept.
Zastosowania medyczne
Bolesne miesiączkowanie
Tamoksyfen jest skutecznie stosowany w celu poprawy przepływu krwi, zmniejszenia kurczliwości macicy i bólu u pacjentek z bolesnym miesiączkowaniem.
Rak piersi
Tamoksyfen jest stosowany w leczeniu zarówno wczesnego, jak i zaawansowanego raka piersi z dodatnim receptorem estrogenowym (ER-dodatnim lub ER+) u kobiet przed i po menopauzie . Tamoksyfen zwiększa ryzyko krwawienia pomenopauzalnego , polipów endometrium , przerostu i raka endometrium ; stosowanie tamoksyfenu z systemem wewnątrzmacicznym uwalniającym lewonorgestrel może zwiększyć krwawienie z pochwy po 1 do 2 latach, ale w pewnym stopniu zmniejsza polipy i przerost endometrium, ale niekoniecznie raka endometrium. [137] Dodatkowo jest to najczęstsze leczenie hormonalne raka piersi u mężczyzn. Jest również zatwierdzony przez FDA do zapobiegania rakowi piersi u kobiet z wysokim ryzykiem zachorowania. Został on ponadto zatwierdzony do redukcji raka kontralateralnego (w przeciwległej piersi). Zaleca się stosowanie tamoksyfenu przez 10 lat.
W 2006 roku duże badanie kliniczne STAR wykazało, że raloksyfen jest również skuteczny w zmniejszaniu zachorowalności na raka piersi. Zaktualizowane wyniki po średnio 6,75 latach obserwacji wykazały, że raloksyfen zachowuje 76% skuteczności tamoksyfenu w zapobieganiu inwazyjnemu rakowi piersi, przy 45% mniej raków macicy i 25% mniej zakrzepów krwi u kobiet przyjmujących raloksyfen niż u kobiet przyjmujących tamoksyfen.
Bezpłodność
Tamoksyfen jest stosowany do indukcji owulacji w leczeniu niepłodności u kobiet z zaburzeniami bezowulacyjnymi . Podaje się go w trzecim do siódmym dniu kobiecego cyklu.
Tamoksyfen poprawia płodność u mężczyzn z niepłodnością poprzez odhamowanie osi podwzgórze-przysadka-gonady ( oś HPG) poprzez antagonizm ER, a tym samym zwiększenie wydzielania hormonu luteinizującego (LH) i hormonu folikulotropowego (FSH) oraz zwiększenie produkcji testosteronu w jądrach .
Ginekomastia
Tamoksyfen stosuje się w zapobieganiu i leczeniu ginekomastii . Jest przyjmowany jako środek zapobiegawczy w małych dawkach lub stosowany w przypadku wystąpienia jakichkolwiek objawów, takich jak bolesność lub nadwrażliwość sutków. Inne leki są przyjmowane w podobnych celach, takie jak klomifen i leki przeciwaromatyczne, które są stosowane w celu uniknięcia niepożądanych skutków związanych z hormonami.
Punkt czasowy kontynuacji |
Dawka tamoksyfenu | |||||
|---|---|---|---|---|---|---|
| Placebo | 1 mg/dzień | 2,5 mg/dzień | 5 mg/dzień | 10 mg/dzień | 20 mg/dzień | |
| 0 miesięcy |
–
|
|||||
| 6 miesięcy | 98% | 90% | 80% | 54% | 22% | 10% |
| 12 miesięcy | 99% | 95% | 84% | 56% | 38% | 19% |
| Uwagi: Zapobieganie objawom piersi – w szczególności ginekomastii i bólowi piersi – wywołanym przez monoterapię bikalutamidem w dawce 150 mg/dobę z tamoksyfenem u 282 mężczyzn z rakiem prostaty . Bikalutamid i tamoksyfen rozpoczęto w tym samym czasie (0 miesięcy). Poziomy estradiolu mieściły się w zakresie od około 22 do 47 pg/ml w leczonej grupie. Źródła: | ||||||
Wczesne dojrzewanie
Tamoksyfen jest przydatny w leczeniu obwodowego przedwczesnego dojrzewania płciowego , na przykład z powodu zespołu McCune-Albrighta , zarówno u dziewcząt, jak iu chłopców. Stwierdzono, że zmniejsza prędkość wzrostu i tempo dojrzewania kości u dziewcząt z przedwczesnym dojrzewaniem, a tym samym poprawia ostateczny wzrost u tych osób.
Dostępne formy
Tamoksyfen jest dostępny w postaci tabletki lub roztworu doustnego.
Przeciwwskazania
Tamoksyfen ma szereg przeciwwskazań , w tym znaną nadwrażliwość na tamoksyfen lub inne składniki, osoby przyjmujące jednocześnie leki przeciwzakrzepowe typu kumaryny oraz kobiety z żylną chorobą zakrzepowo-zatorową w wywiadzie ( zakrzepica żył głębokich lub zator tętnicy płucnej ).
Skutki uboczne
Raport z września 2009 r. Agencji ds. Badań i Jakości Opieki Zdrowotnej i Służby Zdrowia sugeruje, że tamoksyfen, raloksyfen i tibolon stosowane w leczeniu raka piersi znacznie zmniejszają ryzyko wystąpienia inwazyjnego raka piersi u kobiet w średnim i starszym wieku, ale także zwiększają ryzyko wystąpienia niepożądanych skutków ubocznych. .
Rak endometrium
Tamoksyfen jest selektywnym modulatorem receptora estrogenowego (SERM). Chociaż jest antagonistą w tkance piersi, działa jako częściowy agonista na endometrium i jest powiązany z rakiem endometrium u niektórych kobiet. Dlatego zmiany endometrium, w tym nowotwory, należą do działań niepożądanych tamoksyfenu. Z czasem ryzyko raka endometrium może wzrosnąć dwukrotnie, a nawet czterokrotnie, co jest powodem, dla którego tamoksyfen jest zwykle stosowany tylko przez pięć lat.
The American Cancer Society listy tamoksyfen jako znany czynnik rakotwórczy , stwierdzając, że zwiększa ryzyko niektórych rodzajów raka macicy przy jednoczesnym obniżeniu ryzyka nawrotu raka piersi.
Układ sercowo-naczyniowy i metaboliczny
Leczenie tamoksyfenem kobiet po menopauzie wiąże się z korzystnym wpływem na profile lipidowe surowicy. Jednak długoterminowe dane z badań klinicznych nie wykazały działania kardioprotekcyjnego. U niektórych kobiet tamoksyfen może powodować szybki wzrost stężenia trójglicerydów we krwi. Ponadto istnieje zwiększone ryzyko wystąpienia choroby zakrzepowo-zatorowej, zwłaszcza podczas i bezpośrednio po dużym zabiegu chirurgicznym lub w okresach bezruchu. Wykazano, że stosowanie tamoksyfenu nieznacznie zwiększa ryzyko zakrzepicy żył głębokich , zatorowości płucnej i udaru mózgu .
Toksyczność wątroby
Tamoksyfen był powiązany z wieloma przypadkami hepatotoksyczności . Doniesiono o kilku różnych odmianach hepatotoksyczności. Tamoksyfen może również wywołać niealkoholową stłuszczeniową chorobę wątroby u kobiet z otyłością i nadwagą (nie u kobiet o normalnej wadze) w średnim tempie 40% po roku stosowania 20 mg/dzień.
Przedawkować
Nie odnotowano przypadków ostrego przedawkowania tamoksyfenu u ludzi. W badaniach z różnymi dawkami , tamoksyfen podawano kobietom w bardzo dużych dawkach ( np . 300 mg/m 2 ) i stwierdzono , że powodował ostrą neurotoksyczność , w tym drżenie , hiperrefleksję , chwiejny chód i zawroty głowy . Objawy te wystąpiły w ciągu trzech do pięciu dni terapii i zniknęły w ciągu dwóch do pięciu dni od przerwania terapii. Nie zaobserwowano oznak trwałej neurotoksyczności. Wydłużenie odstępu QT obserwowano również przy bardzo dużych dawkach tamoksyfenu. Nie ma swoistego antidotum na przedawkowanie tamoksyfenu. Zamiast tego leczenie powinno opierać się na objawach .
Interakcje
Pacjenci z różnymi postaciami genu CYP2D6 mogą nie odnieść pełnych korzyści z tamoksyfenu z powodu zbyt wolnego metabolizmu proleku tamoksyfenu do jego aktywnych metabolitów. 18 października 2006 Podkomisja Farmakologii Klinicznej zaleciła zmianę oznaczenia tamoksyfenu w celu umieszczenia informacji o tym genie w ulotce dołączonej do opakowania. Pewne zmiany CYP2D6 u pacjentów z rakiem piersi prowadzą do gorszych wyników klinicznych leczenia tamoksyfenem. Dlatego też genotypowanie umożliwia identyfikację kobiet z tymi fenotypami CYP2D6, u których stosowanie tamoksyfenu wiąże się ze słabymi wynikami. Ostatnie badania wykazały, że 7-10% kobiet z rakiem piersi może nie otrzymać pełnych korzyści medycznych z przyjmowania tamoksyfenu ze względu na ich uwarunkowania genetyczne. Testy bezpieczeństwa leków DNA mogą badać wariacje DNA w CYP2D6 i inne ważne szlaki przetwarzania leków. Ponad 20% wszystkich stosowanych klinicznie leków jest metabolizowanych przez CYP2D6, a znajomość stanu CYP2D6 danej osoby może pomóc lekarzowi w wyborze leków w przyszłości. Inne biomarkery molekularne mogą być również wykorzystane do wybrania odpowiednich pacjentów, którzy mogą odnieść korzyści z tamoksyfenu.
Ostatnie badania sugerują, że przyjmowanie selektywnych inhibitorów wychwytu zwrotnego serotoniny (SSRI): paroksetyny (Paxil), fluoksetyny (Prozac) i sertraliny (Zoloft) może zmniejszać skuteczność tamoksyfenu, ponieważ leki te konkurują o enzym CYP2D6 niezbędny do metabolizowania tamoksyfenu w jego aktywne formy. Amerykańskie badanie zaprezentowane na dorocznym spotkaniu Amerykańskiego Towarzystwa Onkologii Klinicznej w 2009 r. wykazało, że po dwóch latach u 7,5% kobiet, które przyjmowały tylko tamoksyfen, wystąpił nawrót choroby, w porównaniu z 16%, które przyjmowały paroksetynę, fluoksetynę lub sertralinę, leki uważane za najsilniejsze inhibitory CYP2D6. Ta różnica przekłada się na 120% wzrost ryzyka nawrotu raka piersi. Pacjenci przyjmujący SSRI; Celexa ( citalopram ), Lexapro ( escitalopram ) i Luvox ( fluwoksamina ) nie miały zwiększonego ryzyka nawrotu, ze względu na brak konkurencyjnego metabolizmu enzymu CYP2D6. Nowsze badanie wykazało wyraźniejsze i silniejsze działanie paroksetyny w powodowaniu najgorszych wyników. Pacjenci leczeni zarówno paroksetyną, jak i tamoksyfenem mają o 67% zwiększone ryzyko zgonu z powodu raka piersi, od 24% do 91%, w zależności od czasu trwania jednoczesnego podawania.
Tamoksyfen wchodzi w interakcje z niektórymi innymi antyestrogenami . Inhibitor aromatazy aminoglutetimid indukuje metabolizm tamoksyfenu. Odwrotnie, inhibitor aromatazy letrozol nie wpływa na metabolizm tamoksyfenu. Jednak tamoksyfen indukuje metabolizm letrozolu i znacznie obniża jego stężenia.
Farmakologia
Farmakodynamika
Selektywne działanie modulatora receptora estrogenowego

Tamoksyfen działa jako selektywny modulator receptora estrogenowego (SERM), albo w postaci częściowego agonisty z receptorem estrogenowym (ER). Ma mieszane działanie estrogenne i antyestrogenne , a profil działania różni się w zależności od tkanki . Na przykład tamoksyfen ma głównie działanie antyestrogenne na piersi, ale przede wszystkim działanie estrogenowe na macicę i wątrobę . W tkance sutka tamoksyfen działa jako antagonista ER , przez co hamowana jest transkrypcja genów odpowiadających na estrogen. Korzystnym skutkiem ubocznym tamoksyfenu jest to, że zapobiega utracie kości, działając jako agonista ER (tj. naśladując działanie estrogenu) w tym typie komórek. Dlatego hamując osteoklasty , zapobiega osteoporozie . Kiedy tamoksyfen został wprowadzony jako lek, sądzono, że będzie działał jako antagonista ER we wszystkich tkankach, w tym w kościach, dlatego obawiano się, że przyczyni się do osteoporozy. Było zatem bardzo zaskakujące, że klinicznie zaobserwowano odwrotny efekt. Stąd selektywne tkankowe działanie tamoksyfenu bezpośrednio doprowadziło do sformułowania koncepcji SERM.
| Lek | Pierś | Kość | Wątroba | Macica | Pochwa | Mózg | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Lipidy | Koagulacja | SHBG | IGF-1 | Uderzenia gorąca | Gonadotropiny | |||||||||
| Estradiol | + | + | + | + | + | + | + | + | + | + | ||||
| "Idealny SERM" | – | + | + | ± | ± | ± | – | + | + | ± | ||||
| Bazedoksyfen | – | + | + | + | + | ? | – | ± | – | ? | ||||
| Klomifen | – | + | + | ? | + | + | – | ? | – | ± | ||||
| Lazofoksyfen | – | + | + | + | ? | ? | ± | ± | – | ? | ||||
| Ospemifen | – | + | + | + | + | + | ± | ± | – | ± | ||||
| Raloksyfen | – | + | + | + | + | + | ± | – | – | ± | ||||
| Tamoksyfen | – | + | + | + | + | + | + | – | – | ± | ||||
| Toremifen | – | + | + | + | + | + | + | – | – | ± | ||||
| Efekt: + = Estrogenny / agonistyczny . ± = Mieszany lub neutralny. – = Antyestrogenne / antagonistyczne . Uwaga: SERM generalnie zwiększają poziom gonadotropin u mężczyzn z hipogonadyzmem i eugonadyzmem, a także kobiet przed menopauzą (antyestrogenne), ale obniżają poziom gonadotropin u kobiet po menopauzie (estrogenne). Źródła: Zobacz szablon. | ||||||||||||||
Tamoksyfen jest długo działającym SERM, z retencją jądrową kompleksu ER-tamoksyfen (lub metabolitu) przez ponad 48 godzin. Ma stosunkowo niewielkie powinowactwo do samego ER, a zamiast tego działa jako prolek do aktywnych metabolitów , takich jak endoksyfenu (4-hydroksy- N -desmethyltamoxifen) i afimoxifene (4-hydroksytamoksyfen, 4-OHT). Te metabolity mają około 30 do 100 razy większe powinowactwo do ER niż sam tamoksyfen. W jednym badaniu tamoksyfen miał 7% i 6% powinowactwa estradiolu odpowiednio do ERα i ERβ , podczas gdy afimoksyfen miał 178% i 338% powinowactwa estradiolu odpowiednio do ERα i ERβ. Stąd afimoksyfen wykazywał 25-krotnie wyższe powinowactwo do ERα i 56-krotnie wyższe powinowactwo do ERβ niż tamoksyfen. Siły działania antyestrogenowego endoksyfenu i afimoksyfenu są bardzo podobne. Jednak endoksyfen występuje w znacznie wyższych stężeniach niż afimoksyfen i obecnie uważa się, że jest główną aktywną formą tamoksyfenu w organizmie.
Tamoksyfen wiąże się kompetycyjnie z ER (w stosunku do endogennego agonisty estrogenu) w komórkach nowotworowych i innych docelowych tkankach, tworząc kompleks jądrowy, który zmniejsza syntezę DNA i hamuje działanie estrogenów. Jest to środek niesteroidowy o silnych właściwościach antyestrogenowych, który konkuruje z estrogenem o miejsca wiązania w piersiach i innych tkankach. Tamoksyfen powoduje, że komórki pozostają w G 0 i G 1 fazach cyklu komórkowego . Ponieważ zapobiega podziałowi komórek (przed)rakowych, ale nie powoduje śmierci komórki, tamoksyfen jest raczej cytostatyczny niż cytobójczy. Tamoksyfen wiąże się z ER, kompleks ER/tamoksyfen rekrutuje inne białka znane jako korepresory , a następnie kompleks wiąże się z DNA, aby modulować ekspresję genów. Niektóre z tych białek obejmują NCoR i SMRT . Działanie tamoksyfenu może być regulowane przez szereg różnych zmiennych, w tym czynniki wzrostu. Tamoksyfen musi blokować białka czynnika wzrostu, takie jak ErbB2/HER2, ponieważ wykazano, że wysoki poziom ErbB2 występuje w rakach opornych na tamoksyfen. Wydaje się, że tamoksyfen do pełnego działania przeciwnowotworowego wymaga białka PAX2 . W obecności wysokiej ekspresji PAX2 kompleks tamoksyfen/ER jest zdolny do tłumienia ekspresji proproliferacyjnego białka ERBB2 . W przeciwieństwie do tego, gdy ekspresja AIB-1 jest wyższa niż PAX2, kompleks tamoksyfen/ER reguluje w górę ekspresję ERBB2, powodując stymulację wzrostu raka sutka.
Tamoksyfen jest antigonadotropic w menopauzie kobiet i częściowo hamuje poziomy gonadotropin , hormonu luteinizującego (LH) i hormon folikulotropowy (FSH) w tych kobiet. Ma jednak progonadotropic efekty w okresie przed menopauzą kobiet i zwiększa estrogen poziom przez 6-krotnie w nich. Ze względu na naturę tamoksyfenu jako konkurencyjnego liganda ER, ten wzrost poziomów estrogenu może zakłócać antyestrogenną skuteczność tamoksyfenu. Efekty tamoksyfenu na raka piersi, Ki-67 ekspresji , globuliny wiążącej hormony płciowe (SHBG) w surowicy, a poziom IGF-1 w osoczu są zależne od dawki całej dawki w zakresie 1 mg do 20 mg / dziennie u kobiet z rakiem sutka. Stwierdzono, że tamoksyfen obniża poziom insulinopodobnego czynnika wzrostu 1 (IGF-1) o 17 do 38% u kobiet i mężczyzn. Tłumienie produkcji IGF-1 w wątrobie jest dobrze znanym działaniem estrogenów i SERM. Dawka 10 mg/dzień tamoksyfenu jest prawie tak samo skuteczna jak dawka 20 mg/dzień w hamowaniu poziomów IGF-1.
Inne czynności
Afimoxifene jest agonistą o sprzężonego z białkiem G receptora estrogenu (GPER) o względnie niskim powinowactwie . Jego powinowactwo do receptora mieści się w zakresie od 100 do 1000 nM, w stosunku do 3 do 6 nM dla estradiolu.
Oprócz swojej aktywności jako SERM, afimoksyfen wiąże się zarówno z receptorem estrogenopodobnym β, jak i receptorem estrogenowym γ i jest antagonistą receptora związanego z estrogenem γ (ERRγ).
Stwierdzono, że norendoksyfen (4-hydroksy- N , N- didesmetylotamoksyfen), inny aktywny metabolit tamoksyfenu, działa jako silny kompetycyjny inhibitor aromatazy ( IC 50 = 90 nM), a także może być zaangażowany w działanie przeciwestrogenowe tamoksyfenu.
Oprócz swojej aktywności jako SERM, tamoksyfen jest silnym i selektywnym inhibitorem kinazy białkowej C i jest pod tym względem aktywny w stężeniach terapeutycznych. Uważa się , że to działanie leży u podstaw skuteczności tamoksyfenu w leczeniu choroby afektywnej dwubiegunowej .
Tamoksyfen jest inhibitorem glikoproteiny P .
Farmakokinetyka
Wchłanianie
Tamoksyfen jest szybko i intensywnie wchłaniany z jelit po podaniu doustnym . Doustna biodostępność tamoksyfenu wynosi około 100%, co sugeruje minimalnym stopniu metabolizmowi pierwszego przejścia w jelicie i wątrobie . Po spożyciu szczytowe stężenie tamoksyfenu występuje po trzech do siedmiu godzinach. Poziomy stanu stacjonarnego tamoksyfenu są osiągane zazwyczaj po 3 do 4 tygodniach, ale prawdopodobnie do 16 tygodni codziennego podawania. Poziomy stanu stacjonarnego afimoksyfenu są osiągane po 8 tygodniach codziennego podawania tamoksyfenu. Maksymalne poziomy tamoksyfenu po pojedynczej dawce doustnej 40 mg wynosiły 65 ng/ml, a poziomy w stanie stacjonarnym przy 20 mg/dobę wynosiły 310 ng/ml. Poziomy tamoksyfenu wykazują wyraźną zależność od dawki w zakresie dawek od 1 do 20 mg/dzień. Poziomy endoksyfenu są około 5 do 10 razy wyższe niż poziomy afimoksyfenu, z dużą zmiennością międzyosobniczą . Stężenia endoksyfenu zgłaszano jako 10,8 do 15,9 ng/ml w stanie stacjonarnym u osób z normalnym metabolizmem CYP2D6 podczas leczenia tamoksyfenem w dawce 20 mg/dobę. Najliczniejszymi metabolitami tamoksyfenu pod względem stężeń w krążeniu są N- desmetylotamoksyfen , N , N- didesmetylotamoksyfen , ( Z )-endoksyfen i N - tlenek tamoksyfenu .
Dystrybucja
Objętość dystrybucji tamoksyfenu wynosi od 50 do 60 l / kg, a jego prześwit został oszacowany jako 1,2 do 5,1 l / godzinę. Wysokie stężenia tamoksyfenu stwierdzono w piersi , macicy , wątrobie, nerkach , płucach , trzustce i jajnikach zwierząt i ludzi. Stwierdzono, że stężenie tamoksyfenu w macicy jest 2-3-krotnie wyższe niż w układzie krążenia, a w piersiach 10-krotnie wyższe niż w układzie krążenia. Białka osocza tamoksyfenu i afimoxifene jest większa niż 99%. Większość tamoksyfenu wiąże się z albuminą . Sama albumina wiąże 98,8% tamoksyfenu, podczas gdy inne białka osocza nie są w dużym stopniu zaangażowane.
Metabolizm
| Pogarszać | Średnie stężenia w osoczu |
Wpływ na ER / powinowactwo do ER a |
|---|---|---|
| Tamoksyfen | 190–420 nmol/l | Słaby antagonista / 2% |
| N- Desmetylotamoksyfen | 280–800 nmol/l | Słaby antagonista / 1% |
| N , N- Desmetylotamoksyfen | 90–120 nmol/l | Słaby antagonista |
| Endoksyfen | 14–130 nmol/l | Silny antagonista / równy afimoksyfenowi |
| Afimoksyfen | 3–17 nmol/l b | Silny antagonista / 188% |
| α-hydroksytamoksyfen | 1 nmol/L | Nic |
| 3,4-Dihydroksytamoksyfen | ? | Słaby antagonista / wysokie powinowactwo |
| N- tlenek tamoksyfenu | 15–24 nmol/l | Słaby antagonista c |
| Przypisy: a = Estradiol wynosi 100%. b = Jedno badanie wykazało znacznie wyższe stężenie (67 nmol/l). c = Może być spowodowane redukcją do tamoksyfenu. | ||
Tamoksyfen jest prolekiem i jest metabolizowany w wątrobie przez izoformy cytochromu P450 CYP3A4 , CYP2C9 i CYP2D6 do aktywnych metabolitów, takich jak endoksyfen (4-hydroksy- N- desmetylotamoksyfen) i afimoksyfen (4-hydroksytamoksyfen). Przekształcenie tamoksyfenu przez N- demetylację do N- desmetylotamoksyfenu , który jest katalizowany głównie przez CYP3A4 i CYP3A5 , odpowiada za około 92% metabolizmu tamoksyfenu. Odwrotnie, 4-hydroksylacja tamoksyfenu do afimoksyfenu odpowiada tylko za około 7% metabolizmu tamoksyfenu. Po utworzeniu N- desmetylotamoksyfen jest utleniany do kilku innych metabolitów, z których najważniejszym jest endoksyfen. Inny aktywny metabolit, norendoksyfen (4-hydroksy- N , N- didesmetylotamoksyfen), powstaje poprzez N- demetylację endoksyfenu lub 4-hydroksylację N , N- didesmetylotamoksyfenu . Tamoksyfen i jego metabolity ulegają koniugacji , w tym glukuronidacji i siarczanowaniu . Tamoksyfen może hamować swój własny metabolizm.
Eliminacja
Tamoksyfen ma długi okres półtrwania w fazie eliminacji, zwykle od 5 do 7 dni, w zakresie od 4 do 11 dni. Podobnie okres półtrwania afimoksyfenu wynosi 14 dni. Odwrotnie, okres półtrwania endoksyfenu wynosi od 50 do 70 godzin (2-3 dni). Długie okresy półtrwania tamoksyfenu i afimoksyfenu przypisuje się ich silnemu wiązaniu z białkami osocza oraz recyrkulacji jelitowo-wątrobowej . Po przerwaniu leczenia poziomy tamoksyfenu i jego metabolitów utrzymują się w krążeniu przez co najmniej 6 tygodni. Tamoksyfen jest wydalany z żółcią i wydalany z kałem , natomiast niewielkie ilości wydalane są z moczem .
Chemia
Tamoksyfen jest niesteroidowym SERM z rodziny trifenyloetylenów i wywodzi się strukturalnie z estrogenów typu dietylostilbestrolu i antyestrogenów, takich jak chlorotrianizen i etamoksytriphetol . Początkowo zsyntetyzowano klomifen , a następnie opracowano tamoksyfen. Tamoksyfen jest strukturalnie blisko spokrewniony z innymi trifenyloetylenami, takimi jak klomifen, nafoksydyna , ospemifen , toremifen i wiele innych. Inne SERM, takie jak raloksyfen , są strukturalnie różne od tamoksyfenu i innych trifenyloetylenów.
Historia
Pod koniec lat pięćdziesiątych firmy farmaceutyczne aktywnie badały nowo odkrytą klasę związków antyestrogenowych w nadziei na opracowanie pigułki antykoncepcyjnej „dzień po”. Arthur L Walpole był endokrynologiem reprodukcyjnym, który kierował takim zespołem w laboratoriach badawczych Alderley Park w ICI Pharmaceuticals. To właśnie tam w 1962 roku chemik Dora Richardson po raz pierwszy zsyntetyzowała tamoksyfen, znany wówczas jako ICI-46 474, kiedy szukała pochodnych trifenyloetylenu do projektu pigułki antykoncepcyjnej, nad którym pracował jej zespół.
Związek ten został pierwotnie stworzony do działania jako inhibitor estrogenu, ale zamiast tego stwierdzono, że stymuluje owulację u uczestniczek próby testowania leków. Walpole i jego koledzy złożyli patent w Wielkiej Brytanii na ten związek w 1962 roku, ale ochrona patentowa na ten związek była wielokrotnie odmawiana w USA aż do lat 80. XX wieku. Tamoksyfen ostatecznie uzyskał dopuszczenie do obrotu jako lek na niepłodność, ale ta klasa związków nigdy nie okazała się przydatna w antykoncepcji u ludzi. Związek między estrogenem a rakiem piersi był znany od wielu lat, ale leczenie raka nie było wówczas priorytetem korporacji, a osobiste interesy Walpole'a były ważne dla utrzymania poparcia dla tego związku przy życiu w obliczu tego i braku ochrony patentowej . Dopiero gdy Walpole zagroził odejściem ze stanowiska, korporacja zdecydowała się zezwolić na próby i testy Tamoxifenu jako leku, który mógłby być stosowany w leczeniu raka piersi. Bez wysiłków Walpole'a w obronie pracy, którą wykonał jego zespół w odkryciu potencjalnie rewolucyjnego źródła leczenia raka piersi, Tamoxifen mógłby stać się odrzuconym lub niedostatecznie zbadanym pomysłem. Zespół Walpole'a składał się z Dory Richardson i GA Snowa, którzy pracowali nad chemiczną częścią projektu, oraz GE Pageta i JK Walleya, którzy koncentrowali się głównie na stronie biologicznej.
Tamoksyfen jest jednym z trzech leków w protokole antyangiogenetycznym opracowanym przez dr Judah Folkman , badacza ze Szpitala Dziecięcego w Harvard Medical School w Bostonie. Folkman odkrył w latach 70., że angiogeneza – wzrost nowych naczyń krwionośnych – odgrywa znaczącą rolę w rozwoju raka. Od czasu jego odkrycia rozwinęła się zupełnie nowa dziedzina badań nad rakiem. Badania kliniczne inhibitorów angiogenezy trwają od 1992 roku z użyciem wielu różnych leków. Naukowcy z Harvardu opracowali specyficzny protokół dla golden retrievera o imieniu Navy, który był wolny od raka po otrzymaniu przepisanego koktajlu celekoksybu , doksycykliny i tamoksyfenu – leczenie później stało się znane jako Protokół Marynarki Wojennej. Ponadto wykazano, że samo leczenie tamoksyfenem ma działanie antyangiogenetyczne w zwierzęcych modelach raka, które wydają się być, przynajmniej częściowo, niezależne od właściwości antagonisty ER tamoksyfenu.
Inne antyestrogeny, takie jak etamoksytriphetol (MER-25) i klomifen (MRL-41), zostały ocenione pod kątem leczenia raka piersi i okazały się skuteczne przed tamoksyfenem, ale były nękane problemami z toksycznością . Pierwsze badanie kliniczne tamoksyfenu odbyło się w Christie Hospital w 1971 roku i wykazało przekonujący efekt w zaawansowanym raku piersi, niemniej jednak program rozwoju ICI był bliski zakończenia, gdy został przejrzany w 1972 roku. W niepublikowanym artykule z pierwszych dni Podczas badania Dora Richardson udokumentowała podekscytowanie swojego zespołu działaniem tamoksyfenu w przeciwdziałaniu problemom z niepłodnością oraz wczesnymi pozytywnymi skutkami stwierdzonymi u pacjentów z rakiem piersi. Niestety praca ta nie została dobrze przyjęta przez wszystkich, ponieważ zespół miał szukać pigułki antykoncepcyjnej. Dalszy rozwój Tamoxifenu mógł być wzmocniony przez drugie badanie kliniczne przeprowadzone przez Harolda WC Ward w Queen Elizabeth Hospital w Birmingham . Badanie Warda wykazało bardziej definitywną odpowiedź na lek w wyższej dawce. Walpole mógł również pomóc przekonać firmę do wprowadzenia tamoksyfenu na raka piersi w późnym stadium w 1973 roku. Odegrał również kluczową rolę w finansowaniu V. Craiga Jordana do pracy nad tamoksyfenem. W 1972 roku ICI Pharmaceuticals Division z powodów finansowych zrezygnowało z opracowywania tamoksyfenu. Lek został następnie wynaleziony na nowo z nieudanego środka antykoncepcyjnego, aby stać się tamoksyfenem, złotym standardem w leczeniu uzupełniającym raka piersi i pionierskim lekiem w zapobieganiu chemioterapii kobietom wysokiego ryzyka. Dwie książki, Estrogen Action, Selective Estrogen Receptor Modulators and Women's Health (Imperial College Press 2013) oraz Tamoxifen Pioneering Medicine in Breast Cancer (Springer 2013) opowiadają tę historię.
| Antyestrogen | Dawkowanie | Rok (lata) | Odsetek odpowiedzi | Toksyczność |
|---|---|---|---|---|
| Etamoksytriphetol | 500-4500 mg/dzień | 1960 | 25% | Ostre epizody psychotyczne |
| Klomifen | 100–300 mg/dzień | 1964-1974 | 34% | Obawy przed zaćmą |
| Nafoksydyna | 180–240 mg/dzień | 1976 | 31% | Zaćma , rybia łuska , światłowstręt |
| Tamoksyfen | 20-40 mg/dzień | 1971-1973 | 31% | Przemijająca małopłytkowość |
| Przypisy: a = „Szczególną zaletą tego leku jest niska częstość występowania uciążliwych skutków ubocznych (25).” „Skutki uboczne były zwykle błahe (26).” Źródła: | ||||
W 1980 r. opublikowano pierwsze badanie wykazujące, że tamoksyfen podawany w połączeniu z chemioterapią poprawia przeżywalność chorych na wczesnego raka piersi. W zaawansowanej chorobie tamoksyfen jest obecnie uznawany za skuteczny tylko u pacjentów z ER+, ale we wczesnych badaniach nie wybrano pacjentów z ER+, a do połowy lat osiemdziesiątych obraz badań klinicznych nie wykazywał większych korzyści dla tamoksyfenu. Niemniej jednak tamoksyfen miał stosunkowo łagodny profil działań niepożądanych i kontynuowano wiele dużych badań.
Farmakologia SERM została odkryta, zdefiniowana i rozszyfrowana w latach 80. Opisano strategię kliniczną, która doprowadziła do stworzenia SERM jako grupy leków wielofunkcyjnych, mających na celu leczenie lub zapobieganie wielu stanom u kobiet po menopauzie, np. osteoporozie i rakowi piersi . Ta historia jest opowiedziana w: V. Craig Jordan, wyd. 2013. „Działanie estrogenów, selektywne modulatory receptorów estrogenowych i zdrowie kobiet” Imperial College Press, Singapur.
Wczesna sprzedaż tamoksyfenu zarówno w Wielkiej Brytanii, jak i Stanach Zjednoczonych znacznie przekroczyła pierwotne szacunki ICI, ale mimo to podczas corocznego przeglądu portfolio członkowie zarządu ICI nadal twierdzili, że „nie było rynku na raka”, pozostawiając marketingowy sukces leku polegać na na jej wyniki kliniczne oraz zainteresowanie klinicystów i naukowców. Niedługo potem Dora Richardson opublikowała historię Tamoxifenu, która, co nietypowe dla tego rodzaju papieru, zawierała osobiste relacje i listy od pacjentów, którzy przypisywali swoje uzdrowienie temu narkotykowi. Jest to oddanie głosu pacjentom chorym na raka za pomocą Tamoxifenu, a tym samym wspieranie go naprzód, uzasadniając to zarówno moralnie, jak i naukowo korporacjom.
Dopiero w 1998 roku metaanaliza przeprowadzonej przez grupę Early Breast Cancer Trialists' Collaborative Group z siedzibą w Oxfordzie wykazała definitywnie, że tamoksyfen był skuteczny we wczesnym stadium raka piersi.
Społeczeństwo i kultura
Nazwy marek
Tamoxifen jest sprzedawany pod markami Nolvadex i Soltamox oraz pod wieloma innymi markami na całym świecie.
Ekonomia
Globalna sprzedaż tamoksyfenu w 2001 roku wyniosła około 1,02 miliarda dolarów. Od wygaśnięcia patentu w 2002 roku jest powszechnie dostępny jako lek generyczny na całym świecie. W 2004 roku tamoksyfen był najlepiej sprzedającym się na świecie lekiem hormonalnym do leczenia raka piersi.
Badania
W zespole McCune-Albrighta (MAS) tamoksyfen był stosowany w leczeniu przedwczesnego dojrzewania i jego konsekwencji. Zaobserwowano, że tamoksyfen zmniejsza szybkie dojrzewanie kości, które jest wynikiem nadmiernej ilości estrogenów i zmiany przewidywanego wzrostu dorosłego (PAH). Te same efekty zaobserwowano również u niskich chłopców w okresie dojrzewania. Jednak jedno badanie in vitro w 2007 r., a później badanie in vivo w 2008 r. wykazało, że tamoksyfen indukuje apoptozę chondrocytów w płytce wzrostowej, obniża poziom insulinopodobnego czynnika wzrostu 1 (IGF-1) w surowicy i powoduje trwałe opóźnienie podłużnego i korowego wzrost kości u młodych samców szczurów, co skłoniło naukowców do wyrażenia zaniepokojenia podawaniem tamoksyfenu rosnącym osobnikom.
Tamoksyfen badano w leczeniu rzadkich stanów włóknienia przestrzeni zaotrzewnowej i idiopatycznego stwardniającego zapalenia krezki . Został również zaproponowany jako część planu leczenia zapalenia tarczycy Riedla .
Tamoksyfen jest używany jako narzędzie badawcze do wywołania specyficznej tkankowo ekspresji genów w wielu konstruktach warunkowej ekspresji u genetycznie zmodyfikowanych zwierząt, w tym w wersji techniki rekombinacji Cre-Lox . Chociaż jest szeroko stosowany w badaniach transgenicznych, silne działanie anaboliczne Tamoxifenu na kości może dezorientować to podejście, szczególnie w odniesieniu do konstruktów ukierunkowanych na kości.
Tamoksyfen może być skuteczny w leczeniu manii u osób z chorobą afektywną dwubiegunową . Uważa się, że jest to spowodowane blokadą kinazy białkowej C (PKC), enzymu regulującego aktywność neuronów w mózgu . Naukowcy uważają, że PKC jest nadaktywna podczas manii u pacjentów z chorobą afektywną dwubiegunową. We wrześniu 2019 r. endoksyfen , główny aktywny metabolit tamoksyfenu o 4-krotnie silniejszym hamowaniu PKC, był w badaniach klinicznych III fazy dotyczących zaburzeń afektywnych dwubiegunowych.
Bibliografia
Dalsza lektura
- Dziekan L (2014). „Terapia tamoksyfenem i genotyp CYP2D6” . W Pratt VM, McLeod HL, Rubinstein WS i in. (wyd.). Podsumowania Genetyki Medycznej . Narodowe Centrum Informacji Biotechnologicznej (NCBI). PMID 28520357 . Identyfikator regału: NBK247013.
Zewnętrzne linki
- „Tamoksyfen” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Cytrynian tamoksyfenu” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Cytrynian tamoksyfenu” . Narodowy Instytut Raka . 5 października 2006 r.

