Tryptamina - Tryptamine

|
|
|
|
| Nazwy | |
|---|---|
|
Preferowana nazwa IUPAC
2-( 1H -indol-3-ilo)etan-1-amina |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CHEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.000.464 |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 10 H 12 N 2 | |
| Masa cząsteczkowa | 160,220 g·mol -1 |
| Wygląd zewnętrzny | krystaliczny proszek o barwie od białej do pomarańczowej |
| Temperatura topnienia | 113-116˚C |
| Temperatura wrzenia | 137 ° C (279 ° F; 410 K) (0,15 mmHg) |
| znikoma rozpuszczalność w wodzie | |
| Zagrożenia | |
| Temperatura zapłonu | 185˚C |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
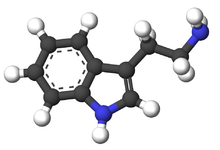
Tryptamina jest metabolitem indolaminy aminokwasu egzogennego, tryptofanu . Strukturę chemiczną określa indol ─ skondensowany pierścień benzenowy i pirolowy oraz grupa 2-aminoetylowa przy trzecim węglu. Struktura tryptaminy jest wspólną cechą niektórych aminergicznych neuromodulatorów, w tym melatoniny , serotoniny , bufoteniny i pochodnych psychedelicznych, takich jak dimetylotryptamina (DMT), psilocybina , psylocyna i inne . Wykazano, że tryptamina aktywuje śladowe receptory związane z aminami wyrażane w mózgu ssaków i reguluje aktywność układów dopaminergicznych , serotoninergicznych i glutaminianergicznych . W jelitach, bakterie symbiotyczne konwersji diety tryptofanu tryptaminy, która aktywuje 5-HT 4 receptory i reguluje motoryki przewodu pokarmowego. Opracowano wiele leków pochodnych tryptaminy do leczenia migreny , podczas gdy receptory związane z aminami śladowymi są badane jako potencjalny cel leczenia zaburzeń neuropsychiatrycznych.
Aby zapoznać się z listą pochodnych tryptaminy, zobacz: Lista podstawionych tryptamin .
Zdarzenia naturalne
Aby zapoznać się z listą roślin, grzybów i zwierząt zawierających tryptaminy, patrz Lista roślin psychoaktywnych i Lista naturalnie występujących tryptamin .
Mózg ssaków
Endogenne poziomy tryptaminy w mózgu ssaków wynoszą mniej niż 100 ng na gram tkanki. Jednak podwyższone poziomy amin śladowych zaobserwowano u pacjentów z pewnymi zaburzeniami neuropsychiatrycznymi, takimi jak depresja dwubiegunowa i schizofrenia .
Mikrobiom jelitowy ssaków
Tryptamina jest stosunkowo obfita w jelitach i kale ludzi i gryzoni. Bakterie komensalne , w tym Ruminococcus gnavus i Clostridium sporogenes w przewodzie pokarmowym , posiadają enzym dekarboksylazę tryptofanu , który pomaga w konwersji tryptofanu z diety do tryptaminy. Tryptaminy jest ligandem dla typu nabłonka jelita 4 serotoniny (5-HT 4 ) receptorów i reguluje pokarmowego elektrolitu równowagi przez okrężnicy wydzielin.
Metabolizm
Biosynteza
Aby uzyskać tryptaminę in vivo , dekarboksylaza tryptofanowa usuwa grupę kwasu karboksylowego na węglu α tryptofanu . Syntetyczne modyfikacje tryptaminy mogą wytwarzać serotoninę i melatoninę ; jednak szlaki te nie występują naturalnie jako główny szlak syntezy endogennych neuroprzekaźników.
Katabolizm
Oksydazy monoaminowe A i B są głównymi enzymami biorącymi udział w metabolizmie tryptaminy do produkcji indolo-3-acetaldehydu , jednak nie jest jasne, która izoforma jest specyficzna dla degradacji tryptaminy.
Mechanizmy działania i efekty biologiczne
Neuromodulacja
Tryptamina może słabo aktywować śladowy receptor związany z aminami , TAAR1 (hTAAR1 u ludzi). W ograniczonych badaniach uznano tryptaminę za śladowy neuromodulator zdolny do regulowania aktywności odpowiedzi komórek nerwowych bez wiązania się z powiązanymi receptorami postsynaptycznymi.
hTAAR1
hTAAR1 jest stymulującym receptorem sprzężonym z białkiem G (GPCR), który ulega słabej ekspresji w przedziale wewnątrzkomórkowym zarówno neuronów pre-, jak i postsynaptycznych. Tryptaminy i innych agonistów hTAAR1 może zwiększyć neuronalnych przez hamowanie recyklingu neurotransmitera przez cAMP zależnej od fosforylacji z transportera ponownego wychwytu monoaminy . Mechanizm ten zwiększa ilość neuroprzekaźnika w szczelinie synaptycznej, a następnie zwiększa wiązanie receptora postsynaptycznego i aktywację neuronów. Odwrotnie, gdy hTAAR1 są kolokalizowane ze sprzężonymi z białkiem G rektyfikującymi do wewnątrz kanałami potasowymi (GIRK), aktywacja receptora zmniejsza odpalanie neuronów poprzez ułatwianie hiperpolaryzacji błony poprzez wypływ jonów potasu. Równowaga między aktywnością hamującą i pobudzającą aktywacji hTAAR1 podkreśla rolę tryptaminy w regulacji aktywności neuronalnej.
Aktywacja hTAAR1 jest badana jako nowa metoda leczenia depresji, uzależnień i schizofrenii. hTAAR1 jest wyrażany głównie w strukturach mózgu związanych z układami dopaminowymi, takimi jak brzuszny obszar nakrywki (VTA) i układy serotoninowe w grzbietowych jądrach szwu (DRN). Ponadto, gen hTAAR1 jest zlokalizowana w 6q23.2 na ludzkim chromosomie, który jest podatność locus zaburzeń nastroju i schizofrenii. Aktywacja TAAR1 sugeruje potencjalne nowe leczenie zaburzeń neuropsychiatrycznych, ponieważ agoniści TAAR1 wywołują działanie przeciwdepresyjne, zwiększają funkcje poznawcze , zmniejszają stres i działają przeciwuzależnieniowo.
Ruchliwość przewodu pokarmowego
Tryptamina wytwarzana przez bakterie mutualistyczne w jelicie ludzkim aktywuje GPCR serotoniny wszechobecnie wyrażane wzdłuż nabłonka okrężnicy. Po tryptaminy wiązania aktywowanego 5-HT 4 , poddaje receptor zmiany konformacyjne, co pozwala na G s podjednostki alfa do wymiany PKB dla GTP i jej uwolnienie z 5-przeprowadzeniu HT 4 receptora i βγ podjednostkę. G związaną z GTP y aktywuje cyklazy adenylanowej , która katalizuje konwersję ATP do cyklicznego monofosforanu adenozyny (cAMP). cAMP otwiera kanały jonów chlorkowych i potasowych, aby napędzać wydzielanie elektrolitów w okrężnicy i promować ruchliwość jelit.
Farmakodynamika
| Tryptamina | Ludzkie TAAR1 | Mysz TAAR1 | Szczur TAAR | |||
|---|---|---|---|---|---|---|
| WE 50 | K i | WE 50 | K i | WE 50 | K i | |
| Tryptamina | 21 | Nie dotyczy | 2,7 | 1,4 | 0,41 | 0,13 |
| Serotonina | >50 | Nie dotyczy | >50 | Nie dotyczy | 5.2 | Nie dotyczy |
| psylocyna | >30 | Nie dotyczy | 2,7 | 17 | 0,92 | 1,4 |
| DMT | >10 | Nie dotyczy | 1.2 | 3,3 | 1,5 | 22 |
|
EC 50 i K I wartości w mikromolarnym (uM). EC 50 odzwierciedla kwotę
tryptaminy wymaganej do wywołania 50% maksymalnej odpowiedzi TAAR1. Mniejszy K i wartość, tym silniejsze tryptaminy wiąże do receptora. |
||||||
Leki na bazie tryptaminy
| Narkotyk | Mechanizm | Leczenie | Efekt | Struktura |
|---|---|---|---|---|
| Sumatryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Rizatryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Zolmitryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Almotryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Eletryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Frowatryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu | |
| Naratryptan | agonista 5-HT 1B i 5-HT 1D | Migrenowe bóle głowy | Zwężenie naczyń krwionośnych mózgu |
Zobacz też
- Tryptofan
- Podstawione tryptaminy
- Aminy śladowe
- Agonista receptora serotoninowego
- Receptor 1 . związany z ludzkimi śladowymi aminami
- Neuromodulacja
Bibliografia
Zewnętrzne linki
- Najczęściej zadawane pytania dotyczące tryptaminy
- Halucynogeny i Świadomość Tryptaminy
- Tryptamind Psychoactives , strona referencyjna na temat tryptaminy i innych środków psychoaktywnych.
- Wpis tryptaminy (T) w TiHKAL • info










