Wygięta geometria molekularna - Bent molecular geometry
| Wygięta geometria molekularna | |
|---|---|
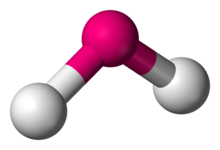 | |
| Przykłady | H 2 O , SO 2 |
| Grupa punktów | C 2v |
| Numer koordynacyjny | 2 |
| Kąt (y) wiązania | 90 ° <θ <120 ° |
| μ (biegunowość) | > 0 |

W chemii , cząsteczki z niewspółliniowe układ dwóch sąsiednich wiązań ma budowa kątowa , znany również jako kątowe lub w kształcie litery V . Niektóre atomy, takie jak tlen, prawie zawsze ustawiają swoje dwa (lub więcej) wiązania kowalencyjne w niekoliniowych kierunkach ze względu na ich konfigurację elektronową . Woda (H 2 O) jest przykładem wygiętej cząsteczki, a także jej analogów . Kąt wiązania między dwoma atomami wodoru wynosi około 104,45 °. Nieliniową geometrię często obserwuje się w przypadku innych triatomicznych cząsteczek i jonów zawierających tylko główne elementy grupy, których wybitnymi przykładami są dwutlenek azotu (NO 2 ), dichlorek siarki (SCl 2 ) i metylen (CH 2 ).
Ta geometria jest prawie zawsze zgodna z teorią VSEPR , która zwykle wyjaśnia niekoliniowość atomów w obecności pojedynczych par . Istnieje kilka wariantów zginania, z których najczęstszym jest AX 2 E 2, w którym dwa wiązania kowalencyjne i dwie samotne pary centralnego atomu (A) tworzą kompletną 8-elektronową powłokę . Mają centralne kąty od 104 ° do 109,5 °, przy czym ten ostatni jest zgodny z uproszczoną teorią, która przewiduje tetraedryczną symetrię czterech orbitali zhybrydyzowanych sp 3 . Najczęstsze rzeczywiste kąty to 105 °, 107 ° i 109 °: różnią się one ze względu na różne właściwości atomów peryferyjnych (X).
Inne przypadki również doświadczają hybrydyzacji orbitalnej , ale w różnym stopniu. Cząsteczki AX 2 E 1 , takie jak SnCl 2 , mają tylko jedną samotną parę i środkowy kąt około 120 ° (środek i dwa wierzchołki trójkąta równobocznego ). Mają trzy orbitale sp 2 . Istnieją również hybrydyzowane sd związki AX 2 metali przejściowych bez wolnych par: mają one środkowy kąt około 90 ° i są również klasyfikowane jako wygięte.
