Stany spinowe (d elektronów) - Spin states (d electrons)
Stany spinu podczas opisywania kompleksów koordynacyjnych metali przejściowych odnoszą się do potencjalnych konfiguracji spinów elektronów d centralnego metalu. W wielu przypadkach te stany spinowe różnią się między konfiguracjami wysokospinowymi i niskospinowymi . Konfiguracje te można zrozumieć za pomocą dwóch głównych modeli stosowanych do opisu kompleksów koordynacyjnych; teoria pola krystalicznego i teoria pola ligandów , która jest bardziej zaawansowaną wersją opartą na teorii orbitali molekularnych .
Wysoka rotacja kontra niska rotacja
Kompleksy oktaedryczne
Rozszczepienie Δ z d orbitali odgrywa ważną rolę w stanie spinu elektronowego kompleksu koordynacyjnego. Na Δ wpływają trzy czynniki: okres (wiersz w układzie okresowym) jonu metalu, ładunek jonu metalu i natężenie pola ligandów kompleksu, zgodnie z opisem serii spektrochemicznej . Jedynie kompleksy oktaedryczne metali przejściowych pierwszego rzędu przyjmują stany wysokospinowe.
W celu rozszczepienia niskiej wirowania występuje, koszt energetyczny umieszczenie elektron do już zajęte pojedynczo orbitalnej musi być mniejszy niż koszt wprowadzania dodatkowych elektronów w e g orbitalnej na kosztach energii hemibursztynianu. Jeśli energia wymagana do pary dwóch elektronów jest większe niż koszt energii wprowadzania elektronu w e g , Δ, podział występuje wysoki wirowania.
Jeśli odległość między orbitalami jest duża, to orbitale o niższej energii są całkowicie wypełnione przed zaludnieniem orbitali wyższych zgodnie z zasadą Aufbau . Kompleksy takie jak ten nazywane są „niskospinowymi”, ponieważ wypełnienie orbity dopasowuje elektrony i zmniejsza całkowity spin elektronów. Jeśli odległość między orbitalami jest wystarczająco mała, łatwiej jest umieścić elektrony na orbitalach o wyższej energii niż dwa na ten sam orbital niskoenergetyczny, ze względu na odpychanie wynikające z dopasowania dwóch elektronów na tym samym orbicie. Tak więc jeden elektron jest umieszczany na każdym z pięciu orbitali d, zanim nastąpi jakiekolwiek parowanie zgodnie z regułą Hunda, co skutkuje tak zwanym kompleksem „wysokospinowym”. Kompleksy takie jak ten nazywane są „wysokospinowymi”, ponieważ wypełnienie górnej orbity pozwala uniknąć dopasowań między elektronami o przeciwnym spinie.
Ładunek centrum metalicznego odgrywa rolę w polu ligandowym i rozszczepieniu Δ. Im wyższy stopień utlenienia metalu, tym silniejsze jest tworzone pole ligandowe. W przypadku, gdy istnieją dwa metale o tej samej konfiguracji elektronów d, ten o wyższym stopniu utlenienia z większym prawdopodobieństwem będzie miał niski spin niż ten o niższym stopniu utlenienia. Na przykład, Fe 2+ i Co 3+ są oba d 6 ; jednak wyższy ładunek Co 3+ tworzy silniejsze pole ligandowe niż Fe 2+ . Wszystkie inne czynniki są równe, Fe 2+ ma większą rotację niż Co 3+ .
Ligandy wpływają również na wielkość rozszczepienia Δ orbitali d zgodnie z ich natężeniem pola, jak opisano w szeregach spektrochemicznych . Ligandy silnego pola, takie jak CN - i CO, zwiększają rozszczepienie i są bardziej prawdopodobne, że będą niskospinowe. Ligandy o słabym polu, takie jak I - i Br - powodują mniejsze rozszczepienie Δ i są bardziej prawdopodobne, że będą wysokospinowe.
Niektóre kompleksy oktaedryczne wykazują skrzyżowanie spinowe , gdzie stany wysokiego i niskiego spinu występują w równowadze dynamicznej.
Kompleksy tetraedryczne
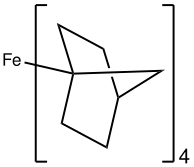
Energia rozszczepienia Δ dla tetraedrycznych kompleksów metali (cztery ligandy), Δtet jest mniejsza niż dla kompleksu oktaedrycznego. W konsekwencji, tetraedryczne kompleksy są prawie zawsze wysokospinowe Przykłady niskospinowych kompleksów tetraedrycznych obejmują Fe(2-norbornyl) 4 , [Co(4-norbornyl) 4 ] + oraz kompleks nitrozylowy Cr(NO)( (N(tms) 2 ) ) 3 .
Kwadratowe kompleksy płaskie
Wiele d 8 kompleksy metali pierwszego rzędu istnieje w czworościennej lub kwadratową płaską geometrię. W niektórych przypadkach te geometrie istnieją w mierzalnej równowadze. Na przykład, dichlorobis(trifenylofosfino)nikiel(II) został wykrystalizowany zarówno w tetraedrycznej, jak i kwadratowej geometrii płaskiej.
Teoria pola liganda a teoria pola kryształu
Jeśli chodzi o rozszczepienie orbitalne d, teoria pola ligandów (LFT) i teoria pola krystalicznego (CFT) dają podobne wyniki. CFT to starszy, prostszy model, który traktuje ligandy jako ładunki punktowe. LFT jest bardziej chemiczny, podkreśla wiązanie kowalencyjne i wyraźnie uwzględnia wiązanie pi.
Systemy wysokospinowe i niskospinowe
W przypadku kompleksów oktaedrycznych, kwestia wysokiego spinu w stosunku do niskiego spinu pojawia się najpierw dla d 4 , ponieważ ma więcej niż 3 elektrony do wypełnienia niewiążących orbitali d zgodnie z teorią pola ligandów lub ustabilizowanych orbitali d zgodnie z kryształem podział pól.
Wszystkie kompleksy metali drugiego i trzeciego rzędu są niskospinowe.
- d 4
- Oktaedryczne wysokospinowe: 4 niesparowane elektrony, paramagnetyczne , substytucyjnie labilne. Zawiera Cr 2+ . Wiele kompleksów przypisanych jako Cr(II) to jednak Cr(III) ze zredukowanymi ligandami .), Mn3+ .
- Oktaedryczne niskospinowe: 2 niesparowane elektrony, paramagnetyczne , substytucyjnie obojętne. Obejmuje Cr 2+ , Mn 3+ .
- d 5
- Oktaedryczne wysokospinowe: 5 niesparowanych elektronów, paramagnetyczne , substytucyjnie labilne. Zawiera Fe 3+ , Mn 2+ . Przykład: Tris(acetyloacetoniano)żelazo(III) .
- Oktaedryczny niskospinowy: 1 niesparowany elektron, paramagnetyczny , substytucyjnie obojętny. Zawiera Fe 3+ . Przykład: [Fe(CN) 6 ] 3- .
- d 6
- Oktaedryczne wysokospinowe: 4 niesparowane elektrony, paramagnetyczne , substytucyjnie labilne. Obejmuje Fe 2+ , Co 3+ . Przykłady: [Fe (H 2 O) 6 ] 2+ [COF 6 ] 3- .
- Oktaedryczny niskospinowy: brak niesparowanych elektronów, diamagnetyczny , substytucyjnie obojętny. Zawiera Fe 2+ , Ni 4+ . Przykład: [Co(NH 3 ) 6 ] 3+ .
- d 7
- Oktaedryczne wysokospinowe: 3 niesparowane elektrony, paramagnetyczne , substytucyjnie labilne. Zawiera Co 2+ , Ni 3+ .
- Oktaedryczny niskospinowy:1 niesparowany elektron, paramagnetyczny , substytucyjnie labilny. Zawiera Co 2+ , Ni 3+ . Przykład: [Co(NH 3 ) 6 ] 2+ .
- d 8
- Oktaedryczne wysokospinowe: 2 niesparowane elektrony, paramagnetyczne , substytucyjnie labilne. Zawiera Ni 2+ . Przykład: [Ni (NH 3 ) 6 ] 2+ .
- Tetraedryczne wysokospinowe: 2 niesparowane elektrony, paramagnetyczne , substytucyjnie labilne. Zawiera Ni 2+ . Przykład: [NiCl 4 ] 2 .
- Kwadratowe płaskie niskospinowe: brak niesparowanych elektronów, diamagnetyczne , substytucyjnie obojętne. Zawiera Ni 2+ . Przykład: [Ni(CN) 4 ] 2- .
promienie jonowe
Stan spinowy kompleksu wpływa na promień jonowy atomu . Dla danej liczby elektronów d kompleksy wysokospinowe są większe.
d 4
- Wysoki spin oktaedryczny: Cr 2+ , 64.5 pm .
- Niski spin ośmiościenny: Mn 3+ , 58 po południu.
- d 5
- Wysoki spin oktaedryczny: Fe 3+ , promień jonowy wynosi 64,5 pm.
- Oktaedryczny niski spin: Fe 3+ , promień jonowy wynosi 55 pm.
- d 6
- Oktaedryczny wysoki spin: Fe 2+ , promień jonowy wynosi 78 pm, promień jonowy Co 3+ 61 pm.
- Oktaedralny niski spin: zawiera promień jonów Fe 2+ 62 pm, promień jonów Co 3+ 54,5 pm, promień jonów Ni 4+ 48 pm.
- d 7
- Oktaedryczny wysoki spin: promień jonów Co 2+ 74,5 μm, promień jonów Ni 3+ 60 μm .
- Oktaedryczny niski spin: promień jonów Co 2+ 65 pm, promień jonów Ni 3+ 56 pm.
- d 8
- Oktaedryczny wysoki spin: promień jonów Ni 2+ 69 pm.
- Kwadratowe płaskie niskospinowe: promień jonów Ni 2+ 49 pm.
Kursy wymiany Ligandów
Na ogół szybkości dysocjacji ligandów z kompleksów o niskim spinie są niższe niż szybkości dysocjacji z kompleksów o wysokim spinie. W przypadku kompleksów ośmiościennych, elektrony w e g poziomy są zabezpieczone wiązania w stosunku do wiązania metal-ligand. Słynne "inercyjne" kompleksy wymiany to oktaedryczne kompleksy jonów metali d 3 i niskospinowych d 6 , zilustrowane odpowiednio przez Cr 3+ i Co 3+ .