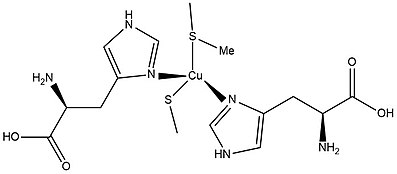
Białko miedzi - Copper protein
Białka miedzi to białka zawierające jeden lub więcej jonów miedzi jako grupy prostetyczne . Białka miedzi znajdują się we wszystkich formach życia oddychającego powietrzem. Białka te są zwykle związane z przeniesieniem elektronów z udziałem tlenu (O 2 ) lub bez niego . Niektóre organizmy wykorzystują nawet białka miedzi do przenoszenia tlenu zamiast białek żelaza. Znaczącymi białkami miedzi u ludzi jest oksydaza cytochromu c (cco). Enzym cco pośredniczy w kontrolowanym spalaniu, które wytwarza ATP .
Klasy
Centra metaliczne w białkach miedzi można podzielić na kilka typów:
- Centra miedzi typu I (T1Cu) charakteryzują się pojedynczym atomem miedzi koordynowanym przez dwie reszty histydyny i resztę cysteiny w strukturze trygonalnej planarnej oraz zmienny ligand osiowy . W białkach T1Cu klasy I (np. amicyjanina , plastocyjanina i pseudoazuryna) ligandem aksjalnym jest siarka metioniny , natomiast aminokwasy inne niż metionina (np. glutamina ) powodują powstanie białek miedzi T1Cu klasy II. Azurins zawierają trzeci rodzaj centrów T1Cu: oprócz metioniny w jednym położeniu osiowym, zawierają drugi osiowy ligand (ą grupę karbonylową z glicyny pozostałości). Białka zawierające T1Cu są zwykle nazywane „cupredoksynami” i wykazują podobne trójwymiarowe struktury, stosunkowo wysokie potencjały redukujące (> 250 mV) i silną absorpcję w pobliżu 600 nm (ze względu na przeniesienie ładunku S → Cu ), co zwykle powoduje kolor niebieski. Cupredoksyny są zatem często nazywane „niebieskimi białkami miedzi”. Może to być mylące, ponieważ niektóre centra T1Cu również absorbują około 460 nm i dlatego są zielone. W badaniach spektroskopowych EPR centra T1Cu wykazują małe, nadsubtelne rozszczepienia w równoległym obszarze widma (w porównaniu do zwykłych związków koordynacyjnych miedzi).
- Centra miedzi typu II (T2Cu) wykazują kwadratową płaską koordynację przez ligandy N lub N/O . Wykazują osiowe widmo EPR z nadsubtelnym rozszczepieniem miedzi w obszarze równoległym, podobnym do obserwowanego w zwykłych związkach koordynacyjnych miedzi. Ponieważ nie występuje ligacja siarki, widma optyczne tych centrów nie mają charakterystycznych cech. Ośrodki T2Cu występują w enzymach , gdzie pomagają w utlenianiu lub utlenianiu.
- Centra miedzi typu III (T3Cu) składają się z pary centrów miedzi, z których każde koordynowane jest przez trzy reszty histydynowe. Białka te nie wykazują sygnału EPR z powodu silnego sprzężenia antyferromagnetycznego (tj. parowania spinów) między dwoma jonami metalu S = 1/2 z powodu ich kowalencyjnego nakładania się z ligandem mostkującym . Ośrodki te są obecne w niektórych oksydazach i białkach transportujących tlen (np. hemocyjaninie i tyrozynazie ).
- Dwujądrzaste centra miedzi i stopów miedzi ( A ) znajdują się w cytochromu c oksydazy i azotu, tlenku reduktazy ( EC 1.7.99.6 ). Dwa atomy miedzi są koordynowane przez dwie histydyny, jedną metioninę, tlenowy karbonylowy szkielet białka i dwie mostkujące reszty cysteiny.
- Centra miedzi (Cu B B ) znajdują się w cytochromu c oksydazy . Atom miedzi jest koordynowany przez trzy histydyny w trójkątnej geometrii piramidy.
- Czterojądrowe centrum miedzi Z (Cu Z ) znajduje się w reduktazie podtlenku azotu. Cztery atomy miedzi są koordynowane przez siedem reszt histydynowych i połączone mostkiem przez atom siarki.
Niebieskie białka miedzi
Niebieskie białka miedzi zawdzięczają swoją nazwę intensywnemu niebieskiemu zabarwieniu ( Cu(II) ). Niebieskie białko miedzi często nazywane jest „ białkiem księżyca ”, co oznacza, że białko może pełnić więcej niż jedną funkcję. Służą one jako środki przenoszenia elektronów, z miejscem aktywnym przemieszczającym się między Cu(I) i Cu(II). Cu 2+ w stanie utlenionym może przyjąć jeden elektron, tworząc Cu 1+ w zredukowanym białku. Geometria centrum Cu ma duży wpływ na jego właściwości redoks. Zniekształcenie Jahna-Tellera nie dotyczy niebieskich białek miedzi, ponieważ miejsce miedzi ma niską symetrię, która nie wspiera degeneracji w rozgałęzieniu d-oczodołu. Brak dużych zmian reorganizacyjnych zwiększa tempo ich przenoszenia elektronów. Miejsce aktywne białka niebieskiej miedzi typu I. Dwie 2-histydyny, 1 metionina i 1 cysteina obecne w sferze koordynacji. Przykładami białka niebieskiej miedzi typu I są plastocyjanina , azuryna i reduktaza azotynowa, hemocyjanina i tyrozynaza .
Struktura niebieskich białek miedzi typu I centrów miedziowych
Białka Blue Copper, klasa białek miedzi typu 1, to małe białka zawierające fałd miedziowy i pojedynczy jon miedzi typu I koordynowany przez dwa N-donory histydyny , S-donor tiolanu cysteiny i S-donor tioeteru metioniny . W stanie utlenionym jon Cu +2 będzie tworzył koordynację trygonalną dwupiramidową lub czworościenną. Białka miedzi typu 1 są identyfikowane jako niebieskie białka miedzi ze względu na przeniesienie ładunku liganda do metalu intensywne pasmo przy długości fali 600 nm, które nadaje charakterystyczny ciemnoniebieski kolor obecny w widmie absorpcji elektronów.
Struktura białkowa białka miedzi typu 1, amicyjanina , jest zbudowana z fałd polipeptydowych, które są powszechnie spotykane w strukturze kanapkowej niebieskich białek miedziowych β. Struktura jest bardzo podobna do plastocyjaniny i azuryny, ponieważ są one również identyfikowane jako białka miedzi typu 1. Są one również podobne do siebie ze względu na geometrię miejsca miedzi w każdym białku miedzi. Białkowa azuryna ma trygonalną dwupiramidową geometrię z podłużnymi osiowymi ligandami glicyny i metoinionowej siarki. Plastocyjaniny posiadają dodatkowy metioninowy ligand siarkowy w pozycji osiowej. Główną różnicą każdego białka miedzi jest to, że każde białko ma inną liczbę i rodzaj ligandu skoordynowanego z centrum miedzi.
Struktura elektronowa kompleksów miedzi typu I białka niebieskiej miedzi
Silne wiązanie pomiędzy jonami miedzi i siarki cysteiny umożliwia niezwiązanego elektronu na cysteinę siarki być obecny zarówno na niskie / wirowania, stan jonów miedzi, d x 2 -d Y 2 orbitalny i p-orbitalnym z siarka cysteinowa. Większość kompleksów miedzi (II) wykazuje efekt Jahna-Tellera, gdy kompleks tworzy tetragonalne zniekształcenie złożonej geometrii oktaedrycznej . W przypadku niebieskich białek miedzi powstanie zniekształcony kompleks czworościenny z powodu silnego równikowego ligandu cysteinowego i słabego aksjalnego ligandu metioninowego. Dwa obojętne ligandy histydynowe są pozycjonowane przez ligand białkowy, więc geometria jest zniekształcona czworościenna. To spowoduje, że nie będą w stanie idealnie koordynować jako czworościenne lub kwadratowe.
Zmiany spektralne wraz z temperaturą
Obniżenie temperatury może zmienić przejścia. Intensywną absorbancję przy około 16000 cm- 1 charakteryzowała cecha absorpcyjna miedzi niebieskiej. Istniało drugie pasmo cech o niższej energii z umiarkowaną intensywnością absorpcji. Dane dotyczące absorpcji spolaryzowanych kryształów sygnału na plastocyjaninie wykazały, że oba pasma mają ten sam stosunek polaryzacji, co związane z wiązaniem Cu(II)-S(Cys). Wyjaśnia to, że normalny kompleks miedziowy ma wysokoenergetyczną sigma i niskoenergetyczne słabe wiązania π. Jednak w przypadku niebieskiego białka miedzi mają sigma o niskiej energii i słabe wiązania π o wysokiej energii, ponieważ intensywność CT odzwierciedla nakładanie się orbitali donorowych i akceptorowych w procesie CT. Wymaga to, 3D (x 2 -y 2 ) orbitalnej niebieskiego miejscu miedzi być tak zorientowany, że jego płaty przepoławiać Cu-S (Cys) wiązania, dając dominującą gatunku nakładania się siarkę bezpośrednio. Wreszcie, natura funkcji falowej stanu podstawowego białka niebieskiej miedzi jest bogata w widmo absorpcji elektronów.
Koordynacja metalowa sfery wewnętrznej i zewnętrznej
Wiązania jonów cysteinowo-siarkowo-miedziowych (II) mieszczą się w zakresie od 2,6 do 3,2 Å. W postaci zredukowanej, CuI , struktury białkowe są nadal tworzone z wiązaniami wydłużonymi o 0,1 Å lub mniej. dzięki utlenionym i zredukowanym strukturom białkowym można je nakładać. W przypadku amicyjaniny istnieje wyjątek, ponieważ histydyna jest poddawana ligacji i nie jest związana z jodkiem miedzi. W Azurin The cysteina 112 tiolanu przyjmuje wiązań wodorowych ze szkieletu amidowej asparaginy 47 i fenyloalaniny 114 i histydyny 46 przekazuje wiązania wodorowego ze szkieletem karbonylowej Asparagine10. Cysteine84 tiolanowy z plastocyjaniny przyjmuje wiązania wodorowego ze szkieletem amidowej, asparaginy 38 i Histidine37 wchodzą mocno w interakcje ze szkieletem karbonylowej Alanina 33 i słabiej ze szkieletem karbonylowej leucyny 5, glicyna 34 i szkieletem amidowej Phenylalanine35.
Białko Niebieskiej Miedzi "Stan brzuszny"
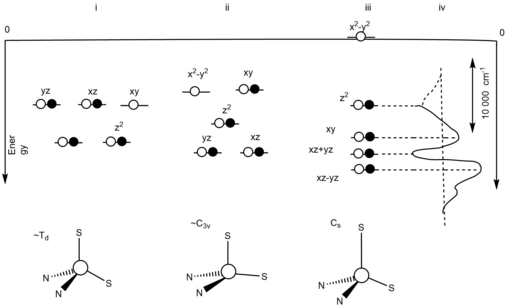
Degeneracja orbitalna jest usuwana z powodu asymetrycznego pola ligandów. Na asymetryczne pole ligandów wpływa silny ekwatorialny ligand cysteinowy i słaby aksjalny ligand metioninowy. Reorganizacja stanu utlenionego Cu +2 w miejscu aktywnym białka miedzi w kolorze niebieskim będzie zminimalizowana ze względu na fakt, że w stanie utlenionym Cu +2 efekt Jahna-Tellera będzie nieskuteczny. Na rysunku 2 przedstawiono diagram poziomów energii, który pokazuje trzy różne idealne geometrie i ich stany zdegenerowane. (I) przedstawia schemat poziom energii o czworościennej strukturze geometrycznej z T 2 zdegenerowanego stanu podstawowego. Wynika to ze zniekształceń Jahna-Tellera spowodowanych utlenianiem. (ii) stanowi wykres poziomu energię C 3V strukturze symetrycznej o 2 E stanie zdegenerowany gruntu. Wynikało to z wydłużenia wiązania tioeterowego w miejscu redukcji niebieskiego białka miedzi. Niesparowane elektrony prowadzą do efektu Jahna-Tellera. (iii) przedstawia diagram poziomów energetycznych stanów podstawowych, które nie są na równym poziomie. To pokazuje, że nie występuje efekt Jahna-Tellera. Wynika to z silnych interakcji donorów równikowych i słabych donorów osiowych. (iv) reprezentuje różnicę odległości między d xy i d x 2 −y 2 .