Cyclospora cayetanensis - Cyclospora cayetanensis
| Cyclospora cayetanensis | |
|---|---|

|
|
| Oocysty Cyclospora cayetanensis | |
| Klasyfikacja naukowa | |
| Domena: | |
| (nierankingowe): | |
| (nierankingowe): | |
| Gromada: | |
| Klasa: | |
| Podklasa: | |
| Zamówienie: | |
| Podrząd: | |
| Rodzina: | |
| Rodzaj: | |
| Gatunki: |
C. cayetanensis
|
| Nazwa dwumianowa | |
|
Cyclospora cayetanensis Ortega, Gilman & Sterling, 1994
|
|
Cyclospora cayetanensis jest kokcydiozą, która wywołuje u ludzi i prawdopodobnie innych naczelnych chorobę biegunkową zwaną cyklosporiozą . Pierwotnie zgłaszany jako nowy patogen prawdopodobnie kokcydia w latach 80. XX wieku i opisany na początku lat 90., był praktycznie nieznany w krajach rozwiniętych, dopóki świadomość nie wzrosła z powodu kilku epidemii związanych z importowanymi produktami skażonymi odchodami. Od tego czasu C. cayetanensis stała się endemiczną przyczyną biegunki w krajach tropikalnych oraz przyczyną biegunki podróżnych i zakażeń przenoszonych przez żywność w krajach rozwiniętych. Gatunek ten został zaliczony do rodzaju Cyclospora ze względu na kulisty kształt sporocyst. Specyficzna nazwa odnosi się do Uniwersytetu Cayetano Heredia w Limie w Peru, gdzie wykonano wczesne prace epidemiologiczne i taksonomiczne.
Historia
Pierwszy opublikowany raport dotyczący Cyclospora cayetanensis u ludzi wydaje się być autorstwa Ashforda (1979), który znalazł niezidentyfikowaną kokcydię podobną do Isospory w odchodach trzech osobników w Papui w Nowej Gwinei. Fotomikrografie w artykule ukazują organizm morfologicznie identyczny z organizmem widzianym obecnie. Później Narango i wsp. (1989) opisali, co może być tym samym organizmem od kilku Peruwiańczyków z przewlekłą biegunką i nazwali organizm podobny do Cryptosporidium muris . Inni badacze uważali, że niesporulowane oocysty wydają się być bardziej podobne do sinic , a nazwa „ciało podobne do cyjanobakterii ” lub CLB stała się powszechna w literaturze (czasami autorzy używali również terminu „ciało przypominające kokcydiozę” lub CLB). Ostatecznie Ortega i wsp. (1992) opublikowali abstrakcyjne doniesienie, że zarodnikowali i usunęli oocysty, co doprowadziło do umieszczenia pasożyta w rodzaju Cyclospora . W tym czasie stworzyli również nazwę Cyclospora cayetanensis . Ponieważ jednak w streszczeniu nie przedstawiono żadnych informacji morfologicznych, C. cayetanensis stał się technicznie nomen nudum (nazwany gatunek bez opisu). Chociaż Ortega i wsp. (1993) później opublikowali dodatkowe szczegóły dotyczące tego kokcydiana, pełny opis morfologiczny nie został opublikowany w celu potwierdzenia nazwy aż do 1994 roku. Tak więc prawidłowa nazwa tego pasożyta to Cyclospora cayetanensis Ortega, Gilman i Sterling, 1994, a etymologia nomen triviale wywodzi się z Uniwersytetu Cayetano Heredia w Limie w Peru. W tym dwuletnim okresie, kiedy C. cayetanensis był nomen nudum , każdy, kto chciałby opublikować pełny opis morfologiczny i zmienić nazwę, miałby do tego prawo.
Charakteryzacja
Cyclospora cayetanensis jest apikompleksem , tworzącym cysty pierwotniakiem kokcydiów, który wywołuje samoograniczającą się biegunkę. Jeśli chodzi o morfologię, ma kuliste oocysty o średnicy od 7,5 do 10 μm, które mają również ściankę o grubości 50 nm z zewnętrzną powłoką przypominającą nitkę, którą niektórzy badacze nazwali zmarszczką. Wzór oocysty to O.2.2, ponieważ jedna oocysta zawiera dwie sporocysty, a każda sporocysta zawiera dwa sporozoity.
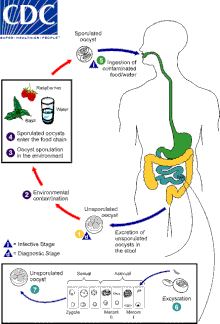
Jedynymi potwierdzonymi żywicielami C. cayetanensis są ludzie. Pierwotniak przeżywa swój cykl życiowy wewnątrzkomórkowo w komórkach nabłonka żywiciela i przewodzie pokarmowym . Infekcja jest przenoszona drogą fekalno-ustną i rozpoczyna się, gdy osoba połknie oocysty w pokarmie lub wodzie zanieczyszczonej kałem. Różne substancje chemiczne w przewodzie pokarmowym żywiciela powodują, że oocysty wydzielają się i uwalniają sporozoity ; ogólnie obserwuje się dwa na oocystę. Po tym, jak sporozoity zaatakują komórki nabłonka, przechodzą merogonię , formę rozmnażania bezpłciowego , w wyniku której powstaje wiele merozoitów potomnych. Te komórki potomne mogą albo infekować nowe komórki gospodarza i zainicjować kolejną rundę merogonii, albo podjąć ścieżkę seksualną poprzez gametogonię : merozoity córki stają się męskimi makrogamontami - które tworzą wiele mikrogamet - i żeńskimi makrogamontami. Po zapłodnieniu poprzez fuzję męskich mikrogamet z samicami makrogamontów zygota dojrzewa do oocysty i rozrywa komórkę żywiciela, skąd jest wydalana ze stolcem . Przekazywane oocysty nie są jednak bezpośrednio zakaźne. Sporulacja może trwać od jednego do kilku tygodni, co oznacza, że przenoszenie się z osoby na osobę nie jest prawdopodobnym problemem. To odróżnia C. cayetanensis od Cryptosporidium parvum - blisko spokrewnionego organizmu wywołującego podobną chorobę - ponieważ oocysty C. parvum są zakaźne natychmiast po uwolnieniu od żywiciela.
Objawy
C. cayetanensis powoduje zapalenie żołądka i jelit , przy czym zakres choroby zależy od wieku, stanu żywiciela i wielkości dawki zakaźnej. Objawy obejmują „wodnistą biegunkę, utratę apetytu, utratę masy ciała, wzdęcia i skurcze brzucha, zwiększone wzdęcia , nudności , zmęczenie i niską gorączkę ”, chociaż w cięższych przypadkach można to nasilić przez wymioty, znaczną utratę masy ciała, nadmierną biegunkę i bóle mięśni. Zwykle u pacjentów z uporczywą wodnistą biegunką utrzymującą się przez kilka dni można podejrzewać, że jest nosicielem choroby, zwłaszcza jeśli podróżowali do regionu, w którym pierwotniak występuje endemicznie. Okres inkubacji u żywiciela wynosi zwykle około tygodnia, a choroba może trwać sześć tygodni, zanim samo się ograniczy. Jeśli nie jest leczone, choroba może nawrócić. Cięższe postacie choroby mogą wystąpić u pacjentów z obniżoną odpornością , takich jak chorzy na AIDS . Cyklosporioza u ludzi jest klinicznie podobna do kryptosporydiozy , izosporiozy , lambliozy i mikrosporydiozy ze względu na podobne cechy kliniczne. Zespół grypopodobny z bólami mięśni i stawów może poprzedzać wystąpienie biegunki. Gorączka jest niskiego stopnia i jest niezwykła. Występuje umiarkowane do ciężkiego odwodnienie, kompensacyjna tachykardia , skurczowe ciśnienie tętnicze (SBP <90 mmHg) i może wystąpić zmniejszenie turgoru skóry . Ale łagodna infekcja powoduje niewiele objawów klinicznych lub nie powoduje ich wcale. Układ odpornościowy może determinować pojawienie się objawów; to znaczy od stadium objawowego do bezobjawowego zależy od oporności układu odpornościowego.
Czynniki ryzyka
Osoby mieszkające lub podróżujące na rozwijających się obszarach tropikalnych lub subtropikalnych mogą być narażone na zwiększone ryzyko zarażenia się C. cayetanensis , ponieważ występuje tam endemicznie. Infekcje w regionach endemicznych zwykle wykazują wyraźną sezonowość, która jest słabo poznana, podczas gdy epidemie w Ameryce Północnej występują najczęściej późną wiosną i latem, co koreluje ze zwiększonym importem produktów z tropików. Spożywanie jedzenia lub wody podczas wizyty w krajach rozwijających się jest dobrze udokumentowanym sposobem wywoływania biegunki podróżnych. Podróżni są często ostrzegani przed takimi działaniami, ale ponad 70 procent niektórych produktów konsumowanych w Stanach Zjednoczonych jest importowanych z krajów rozwijających się, co umożliwia wystąpienie „biegunki podróżnych” bez podróży międzynarodowych. Ponieważ oocysty są wydalane z kałem zarażonych osób, a następnie muszą dojrzewać w środowisku 2–14 dni, zanim staną się zakaźne, jest mało prawdopodobne, aby dana osoba zaraziła się bezpośrednio od innej osoby, na przykład osoby mającej kontakt z żywnością.
Uznanie
Rozpoznanie C. cayetanensis może być bardzo trudne ze względu na niewielkie rozmiary, środowisko wewnątrzkomórkowe i niezdolność do prawidłowego przyjmowania wielu przebarwień histologicznych . Do tej pory opracowano cztery metody pozytywnej diagnozy pierwotniaka: mikroskopowe wykrywanie oocyst w próbkach kału; odzyskiwanie oocyst w próbkach z biopsji płynu jelitowego / jelita cienkiego; wykazanie sporulacji oocyst; i amplifikację DNA C. cayetanensis w reakcji łańcuchowej polimerazy (PCR) . Ponieważ wykrywanie jest tak trudne, jeden wynik negatywny nie powinien pomijać możliwości wystąpienia C. cayetanensis : należy również rozważyć testy obejmujące świeże próbki kału w ciągu następnych kilku dni.
Z wyjątkiem amplifikacji PCR, po odzyskaniu próbki, w której podejrzewa się oocysty, przeprowadza się standardowe testy w celu identyfikacji C. cayetanensis . Testy te obejmują mikroskopię z kontrastem fazowym w celu sprawdzenia opisanych wcześniej sferycznych oocyst, zmodyfikowane barwienie kwasoodporne w celu sprawdzenia zmiennego barwienia (od bladego do czerwonego) oraz autofluorescencję w świetle UV . Uzyskanie tych oocyst jest zwykle wyzwaniem, chociaż ostatnie badania pokazują łatwiejsze metody ich uzyskiwania. W niedawnych badaniach dotyczących różnych technik stosowanych w badaniach kału do identyfikacji oocyst, wirowanie próbki kału w roztworze sacharozy, a następnie przeniesienie niewielkiej ilości na szkiełko okazało się niezwykle skuteczne - zarówno w przypadku znalezionych oocyst, jak i względnej łatwości porodu. w wykrywaniu oocyst C. cayetanensis : w rzeczywistości w artykule stwierdzono, że uzyskanych próbek dodatnich stanowiło około 84%.
W przeszłości C. cayetanensis mylono z innymi zakażeniami pierwotniakami, najczęściej błędnie identyfikowanymi jako Cryptosporidium parvum . Można jednak zauważyć kilka różnic między nimi, aby zapewnić właściwą diagnozę. Różnice te obejmują: różnicę wielkości - C. parvum jest mniejsza; odmienne wyniki od zmodyfikowanego barwienia kwasoodpornego - C. parvum ma stałe zabarwienie na czerwono, podczas gdy C. cayetanensis wykazuje zmienne zabarwienie; oraz autofluorescencja w świetle UV - wykazuje to C. cayetanensis , podczas gdy C. parvum nie.
Przypadki zakażenia C. cayetanensis często pozostają niewyjaśnione, częściowo z powodu trudności związanych z badaniami epidemiologicznymi takich przypadków i brakiem metod genotypowania. Niedawne próby lepszej charakterystyki genotypowania obejmują typowanie sekwencji multilocus w oparciu o markery mikrosatelitarne i polimorfizmy pojedynczych nukleotydów (SNP) markerów jądrowych.
Leczenie
Większość ludzi, którzy mają zdrowy układ odpornościowy, wyzdrowieje bez leczenia. Nieleczona choroba może trwać od kilku dni do miesiąca lub dłużej. Objawy mogą wydawać się ustępować, a następnie powracać raz lub więcej razy (nawrót). Leki przeciwbiegunkowe mogą pomóc zmniejszyć biegunkę, ale przed przyjęciem leku należy skonsultować się z lekarzem. Osoby, które są w złym stanie zdrowia lub mają osłabiony układ odpornościowy, mogą być bardziej narażone na ciężką lub długotrwałą chorobę. Do tej pory najskuteczniejszym lekiem do leczenia pierwotniaka jest siedmiodniowy cykl doustnego trimetoprimu-sulfametoksazolu (TMP-SMX). Skutki leku obejmują znaczące skrócenie czasu trwania wydalania oocyst, ustąpienie biegunki i ujemny wynik na obecność oocyst próbek kału w ciągu dwóch do trzech dni. TMP-SMX jest klasyfikowany w kategorii C w czasie ciąży, co oznacza, że mogą wystąpić potencjalne działania niepożądane (takie jak teratogenne, embriobójcze lub inne) i należy je podawać tylko wtedy, gdy potencjalna korzyść znacznie przewyższa ryzyko. Leku należy unikać w najbliższym czasie, ponieważ istnieje wysoki potencjał hiperbilirubinemii i kernicterusu u noworodków. Dodatkowo TMP-SMX może przenikać do mleka matki, co jest zgodne z normami zdrowych noworodków urodzonych o czasie, ale należy tego unikać u wcześniaków, chorych, zestresowanych lub z żółtaczką. Do tej pory nie odkryto wysoce alternatywnego schematu antybiotykowego dla pacjentów z alergią na sulfonamidy.
Zapobieganie
Żadna szczepionka przeciwko temu patogenowi nie jest dostępna. Ponieważ zakażenie następuje poprzez skażoną kałem żywność i wodę w środowiskach endemicznych, zaproponowano kilka prostych rozwiązań w celu zapobiegania infekcjom C. cayetanensis . Najprościej jest ostrzec podróżnych, aby nie odwiedzali regionów, w których pierwotniak występuje endemicznie (ogólnie rzecz biorąc, regiony tropikalne i subtropikalne, w których warunki sanitarne są słabe, takie jak Peru, Brazylia i Haiti), zwłaszcza gdy pora roku jest najlepsza do rozprzestrzeniania się: podróżni również powinni należy pamiętać, że traktowanie wody lub żywności chlorem lub jodem jest mało prawdopodobne, aby zabić oocysty Cyclospora . Ponadto lepsze praktyki zdrowotne w pierwotnym środowisku rolniczym - takie jak upewnienie się, że systemy podlewania produktów nie ciągną wody, która ma dostęp do ludzkich odchodów. Dodatkowo, stosowanie systemów filtrujących, takich jak 1 mikronowy system filtracji absolutnego węgla, zmniejszy obecność Cyclospory , drastycznie zmniejszając częstość rozprzestrzeniania się tego pasożyta. Szanse na zakażenie Cyclosporą i wieloma innymi patogenami przenoszonymi przez żywność można znacznie zmniejszyć, dokładnie myjąc owoce i warzywa w czystej wodzie przed spożyciem. Jednak samo mycie żywności nie usuwa 100% obecnych oocyst.
Cyclospora i maliny
Badanie przeprowadzone na próbkach kału pracowników farmy malinowej wykazało wyższą częstość występowania oocyst Cyclospora w ich próbkach w porównaniu z innymi ludźmi w okolicy. Może to być spowodowane tym, że Cyclospora spp. są wysoce odporne na środki dezynfekujące powszechnie stosowane przez pracowników do celów higienicznych oraz przetwórstwa żywności i wody. Ta odporność jest prawdopodobnie zwiększona przez większe powinowactwo wiązania niektórych świeżych produktów. Drobne, przypominające włosy wypustki na malinach ułatwiają uwięzienie lepkich oocyst na ich powierzchni w porównaniu z innymi owocami, takimi jak jeżyny. Kontrast pomiędzy powierzchnią maliny (po lewej) i jeżyny (po prawej), widziany za pomocą skaningowego mikroskopu elektronowego: Zwróć uwagę na nierówną powierzchnię maliny, wraz ze szczelinami i włoskami.
Wybuch w Stanach Zjednoczonych w 2013 roku
Co najmniej 285 osób w 11 stanach zostało dotkniętych chorobą do 26 lipca 2013 r. Według amerykańskiego Centrum Kontroli i Zapobiegania Chorobom (CDC) dokładna przyczyna wybuchu nie została jeszcze zidentyfikowana . Większość przypadków była zlokalizowana na Środkowym Zachodzie , 138 zgłoszonych przypadków w stanie Iowa i 70 w Nebrasce . Inne stany dotknięte problemem to: Teksas , Floryda , Georgia , Wisconsin , Connecticut , Illinois , Kansas , Minnesota , New Jersey i Ohio .
Według stanu na 29 lipca 2013 roku, CDC poinformowało, że 373 osoby w 15 stanach zostały dotknięte epidemią. Do tej pory hospitalizowano 21 pacjentów z trzech stanów, bez zgłoszonych zgonów. Nie zidentyfikowano żadnego źródła pożywienia, ale urzędnicy ds. Zdrowia w Iowa - stan zgłaszający większość przypadków - powiedzieli, że podejrzewają importowane warzywa.
30 lipca 2013 roku Departament Zdrowia i Opieki Społecznej stanu Nebraska oraz Departament Zdrowia stanu Iowa ogłosiły, że pakowana sałatka z sieci restauracji jest wektorem choroby pasożyta. Jednak CDC i Amerykańska Agencja ds.Żywności i Leków (FDA) nadal oceniają informacje z innych stanów, aby sprawdzić, czy wyniki mają zastosowanie do tamtejszych chorób.
W aktualizacji z 1 sierpnia 2013 r. CDC zgłosiło 397 przypadków, podczas gdy Iowa i Teksas dodały kolejne 22. To spowodowało, że nieoficjalna liczba przypadków wzrosła do ponad 400 przypadków. Ponadto Luizjana zgłosiła swój pierwszy przypadek, zwiększając całkowitą liczbę dotkniętych stanów do 16.
W dniu 3 sierpnia 2013 r. CNN poinformowało, że epidemię można przypisać pakowanej sałatce serwowanej w restauracjach Olive Garden i Red Lobster, które zostały wyprodukowane przez Taylor Farms de Mexico .
W dniu 15 sierpnia 2013 r. CDC zgłosiło dziewięć kolejnych infekcji Cyclospora , zwiększając liczbę przypadków do 548. Liczba dotkniętych stanów pozostała na poziomie 19, ale CDC stwierdziło, że nie wszystkie przypadki były powiązane z wybuchem epidemii w Iowa i Nebrasce do zanieczyszczonej mieszanki sałat z Meksyku.
19 sierpnia 2013 r. CDC zgłosiło 10 kolejnych przypadków Cyclospory , podnosząc nieoficjalną liczbę do ponad 600. Tennessee również zgłosiło swój pierwszy przypadek, zwiększając liczbę stanów dotkniętych do 20. CDC nadal ostrzega, że czy przypadki we wszystkich stanach są związane z epidemiami w Iowa i Nebrasce, nie jest jasne.
Na dzień 27 sierpnia 2013 r. Pochodzenie epidemii nadal pozostawało tajemnicą. FDA stwierdziła, że nie wykryła żadnych naruszeń bezpieczeństwa żywności w fabryce sałat Taylor Farms de Mexico w Meksyku, które byłyby powiązane z niektórymi chorobami.
Wybuch epidemii w Teksasie w 2015 roku
W oświadczeniu FDA, CDC cytuje: „obecnie (w lipcu 2015 r.) W Stanach Zjednoczonych trwa kolejny wybuch cyklosporii, w którym zarówno Departament Stanu Służby Zdrowia Teksasu, jak i Departament Usług Zdrowotnych Wisconsin i Departament Stanu Wisconsin Rolnictwo, handel i ochrona konsumentów zidentyfikowały kolendrę z meksykańskiego stanu Puebla jako podejrzany nośnik w odniesieniu do oddzielnych grup chorób. " W zeszłym roku w Teksasie odnotowano 200 przypadków, z których niektóre były związane z kolendrą z regionu Puebla.
Wybuch epidemii w Teksasie w 2016 roku
Urzędnicy ds. Zdrowia powiedzieli, że w czterech głównych hrabstwach północnego Teksasu potwierdzono ponad tuzin przypadków cyklosporii, a źródłem była prawdopodobnie skażona żywność. Departament Stanu Służby Zdrowia Teksasu podał w środę, że pasożyt został znaleziony w hrabstwach Dallas, Tarrant, Collin i Denton i że pochodzenie mogło być powiązane ze świeżym produktem.
Urzędnicy hrabstwa powiedzieli NBC 5, że odnotowano cztery przypadki w hrabstwie Dallas, trzy w hrabstwie Collin, cztery w hrabstwie Denton i siedem w hrabstwie Tarrant. Sprawy hrabstwa Denton i co najmniej cztery przypadki hrabstwa Tarrant niedawno wyjechały poza granice kraju, co stawia pod znakiem zapytania miejsce pochodzenia.
W całym stanie odnotowano obecnie 66 potwierdzonych przypadków cyklosporii - chociaż źródła infekcji nie zostały potwierdzone. U większości ludzi objawy nie były poważne. „Ale dla tych, którzy są bardzo młodzi i starszych, lub tych, którzy mają osłabiony układ odpornościowy, ta choroba może powodować poważne problemy” - powiedział dr Khang Tran, główny lekarz w Centrum Medycznym w Plano. W ostatnich latach, 2012–2015, ogniska cyklospory były związane ze świeżą kolendrą importowaną z Puebla w Meksyku. Od lata 2015 roku Urząd ds. Żywności i Leków wprowadził zakaz importu z tego regionu w okresie od kwietnia do sierpnia.
2018 Epidemia warzyw na Środkowym Zachodzie Del Monte
Del Monte wycofał zapakowane tace warzywne Del Monte Fresh Produce, które zawierały brokuły, marchew, kalafior, paluszki selera i dip koperkowy, od niektórych sprzedawców detalicznych, w tym Kwik Trip i Peapod, zgodnie z danymi CDC. Mieszkańcy czterech stanów - Iowa, Michigan, Minnesota i Wisconsin zachorowali na Cyclospora .
2018 Epidemia sałatek McDonald's na Środkowym Zachodzie
McDonald's przestał sprzedawać sałatki dostarczane przez Fresh Express w około 3000 miejsc w całym kraju, głównie w środkowo - zachodnich Stanach Zjednoczonych z powodu wielostanowiskowej epidemii pasożytów, która wywołała chorobę u 551 osób wywołanych przez Cyclosporę .
2020 Środkowy zachód wybuchu epidemii sałatek ogrodowych w workach
W czerwcu 2020 roku CDC i inne organy regulacyjne rozpoczęły badanie wybuchu cyklosporyozy w środkowo-zachodnich Stanach Zjednoczonych, związanego z zapakowaną mieszanką sałat. W dniu 27 czerwca 2020 r. Fresh Express ogłosił dobrowolne wycofanie ponad 91 produktów sałatkowych Fresh Express i marek własnych.
| Rok | Liczba przypadków | Częstość występowania |
|---|---|---|
| 2015 | 316 | |
| 2014 * | 200 | 0,7 |
| 2013 * | 351 | 1.3 |
| 2012 * | 44 | 0,2 |
| 2011 * | 14 | 0,1 |
| 2010 | 9 | 0.0 |
| 2009 | 10 | 0.0 |
| 2008 | 6 | 0.0 |
| 2007 | 2 | 0.0 |
| 2006 | 1 | 0.0 |
| 2005 | 1 | 0.0 |
| 2004 | 4 | 0.0 |
| 2003 | 1 | 0.0 |
| 2002 | 1 | 0.0 |
| 2001 | 0 | 0.0 |
IR = współczynnik zachorowalności na 100 000
* współczynniki zapadalności są oparte na prognozowanych danych spisowych uzyskanych z DSHS Center for Health Statistics.
Amerykańskie ogniska cyklosporii przenoszone przez żywność: 2000–2014
Ogniska cyklosporii przenoszone przez żywność zgłaszano w Stanach Zjednoczonych od połowy lat 90. XX wieku i wiązano je z różnymi rodzajami importowanych świeżych produktów, w tym malinami, bazylią, groszkiem śnieżnym, sałatą mesclun i kolendrą; do tej pory nie stwierdzono związku z żadnym produktem mrożonym komercyjnie. Amerykańskie ogniska cyklosporizy przenoszone przez żywność, które wystąpiły przed 2000 r., Zostały podsumowane wcześniej, podobnie jak główne udokumentowane epidemie w 2013 i 2014 r . Ogniska przenoszone przez żywność w okresie 15 lat 2000–2014 podsumowano w tabeli. Tabela zawiera informacje o 31 zgłoszonych ogniskach cyklosporii przenoszonych przez żywność, które wystąpiły w Stanach Zjednoczonych w latach 2000–2014; całkowita liczba spraw wyniosła 1562. W latach 2003, 2007 ani 2010 nie zgłoszono żadnych ognisk. Ogółem zgłaszano średnio dwa ogniska rocznie, z medianą 20 przypadków na ognisko (zakres od 3 do 582 przypadków). Chociaż ogniska występowały w ciągu 8 różnych miesięcy (od grudnia do lipca), szczytowymi miesiącami były maj, czerwiec i lipiec. Jak wskazano w tabeli, w przypadku 15 z 31 ognisk choroby zidentyfikowano nośnik pokarmowy zakażenia.
Podsumowanie ognisk cyklosporyozy przenoszonej przez żywność w USA w latach 2000–2014
| Rok (y) * | Miesięcy)* | Jurysdykcja * | Liczba przypadków † | Nośnik i źródło żywności, jeśli zidentyfikowano ‡ |
|---|---|---|---|---|
| 2000 | Może | Gruzja | 19 | Maliny i / lub jeżyny (podejrzewa się) |
| 2000 | czerwiec | Pensylwania | 54 | Maliny |
| 2001 | Styczeń luty | Floryda | 39 | |
| 2001 | styczeń | Nowy Jork | 3 | |
| 2001–02 | Grudzień styczeń | Vermont | 22 | Maliny (prawdopodobnie) |
| 2002 | Kwiecień maj | Massachusetts | 8 | |
| 2002 | czerwiec | Nowy Jork | 14 | |
| 2004 | luty | Teksas | 38 | |
| 2004 | luty | Illinois | 57 | Bazylia (prawdopodobnie) |
| 2004 | Może | Tennessee | 12 | |
| 2004 | Maj czerwiec | Pensylwania | 96 | Groszek śnieżny z Gwatemali |
| 2005 | Marzec maj | Floryda | 582 ¶ | Bazylia z Peru |
| 2005 | Może | Karolina Południowa | 6 | |
| 2005 | kwiecień | Massachusetts | 58 | |
| 2005 | Może | Massachusetts | 16 | |
| 2005 | czerwiec | Connecticut | 30 | Bazylia (podejrzewana) |
| 2006 | czerwiec | Minnesota | 14 | |
| 2006 | czerwiec | Nowy Jork | 20 | |
| 2006 | lipiec | Gruzja | 3 | |
| 2008 | Marsz | Wisconsin | 4 | Groszek cukrowy (prawdopodobnie) |
| 2008 | lipiec | Kalifornia | 45 ¶ | Maliny i / lub jeżyny (prawdopodobnie) |
| 2009 | czerwiec | Dystrykt Kolumbii | 34 | |
| 2011 | czerwiec | Floryda | 12 | |
| 2011 | lipiec | Gruzja | 100 | |
| 2012 | Czerwiec lipiec | Teksas | 16 | |
| 2013 ** | czerwiec | Iowa i Nebraska | 161 | Mieszanka sałat w workach z Meksyku |
| 2013 ** | Czerwiec lipiec | Teksas | 38 | Cilantro z Meksyku |
| 2013 | lipiec | Wisconsin | 8 | Sałatka Jagodowa (podejrzewana) |
| 2014 | czerwiec | Michigan | 14 | |
| 2014 †† | Czerwiec lipiec | Teksas | 26 | Cilantro z Meksyku |
| 2014 | lipiec | Karolina Południowa | 13 |
* Wpisy w pierwszych trzech kolumnach odnoszą się do znanych lub prawdopodobnych lat, miesięcy i jurysdykcji, w których wystąpiło narażenie na cyklosporę .
** Dodatkowe informacje można znaleźć w podsumowaniu informacji o dochodzeniach w sprawie epidemii w 2013 r . Do celów niniejszej tabeli miesiąc (-y) narażenia i liczba przypadków są ograniczone do tych, które są wyraźnie powiązane w dochodzeniach z produktem żywnościowym określonym w ostatniej kolumnie.
† Podane liczby przypadków obejmują potwierdzone laboratoryjnie i prawdopodobne przypadki cyklosporii. Z definicji każde ognisko obejmowało co najmniej dwa powiązane przypadki, z których co najmniej jeden został potwierdzony laboratoryjnie.
‡ Pojazd spożywczy jest określony tylko wtedy, gdy w dochodzeniu w sprawie epidemii zidentyfikowano pojedynczy składnik lub towar.
¶ Nie uwzględniono przypadków, które miały miejsce u podróżujących z Kanady do Stanów Zjednoczonych.
†† Aby uzyskać dodatkową perspektywę, zobacz podsumowanie informacji o dochodzeniach w sprawie epidemii w 2014 r . Do celów niniejszej tabeli miesiące narażenia i liczba przypadków ogniska w Teksasie są ograniczone do tych, które są wyraźnie powiązane w dochodzeniach z produktem żywnościowym określonym w ostatniej kolumnie.
Bibliografia
- Türk M, Türker M, Ak M, Karaayak B, Kaya T (marzec 2004). „Cyklosporioza związana z biegunką u immunokompetentnego pacjenta w Turcji” . J. Med. Microbiol . 53 (Pt 3): 255–7. doi : 10,1099 / jmm.0.45531-0 . PMID 14970253 .
- Kimura K, Kumar Rai S, Takemasa K i wsp. (Wrzesień 2004). „Porównanie trzech mikroskopowych technik diagnostycznych Cyclospora cayetanensis ”. FEMS Microbiol. Lett . 238 (1): 263–6. doi : 10.1016 / j.femsle.2004.07.045 . PMID 15336431 .
- Mansfield LS, Gajadhar AA (grudzień 2004). „ Cyclospora cayetanensis , pasożyt kokcydia przenoszony przez żywność i wodę”. Weterynarz. Parasitol . 126 (1–2): 73–90. doi : 10.1016 / j.vetpar.2004.09.011 . PMID 15567580 .
- Yu JR, Sohn WM (październik 2003). „Przypadek cyklosporyozy u ludzi powodującej biegunkę podróżnika po wizycie w Indonezji” . J. Korean Med. Sci . 18 (5): 738–41. doi : 10.3346 / jkms.2003.18.5.738 . PMC 3055112 . PMID 14555830 .