Zwijanie wewnątrznaczyniowe - Endovascular coiling
| Zwijanie wewnątrznaczyniowe | |
|---|---|
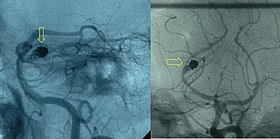 Arteriogram po embolizacji przedstawiający zwinięty tętniak (wskazany żółtymi strzałkami) tętnicy tylnej mózgu z resztkowym workiem tętniaka.
| |
| Inne nazwy | Embolizacja wewnątrznaczyniowa |
| Specjalność | Neuroradiologia interwencyjna |
Zawijanie wewnątrznaczyniowe to wewnątrznaczyniowe leczenie tętniaków wewnątrzczaszkowych i krwawienia w całym ciele. Procedura zmniejsza krążenie krwi w tętniaku za pomocą odłączanych mikrochirurgicznych drutów platynowych, z klinicystą wprowadzającym jeden lub więcej do tętniaka, dopóki nie zostanie ustalone, że przepływ krwi już nie występuje w przestrzeni. Jest to jeden z dwóch głównych sposobów leczenia tętniaków mózgu, drugim jest chirurgiczne obcinanie . Klipowanie jest alternatywą dla stentowania krwawienia.
Zastosowania medyczne
Zwijanie wewnątrznaczyniowe jest stosowane w leczeniu tętniaków mózgu . Głównym celem jest zapobieganie pękaniu tętniaków niepękniętych oraz zapobieganie ponownemu krwawieniu w tętniakach pękniętych poprzez ograniczenie krążenia krwi do przestrzeni tętniaka. Klinicznie zaleca się, aby gęstość upakowania wynosiła 20-30% lub więcej objętości tętniaka, co zwykle wymaga zastosowania wielu przewodów. Większe objętości mogą być trudne ze względu na delikatną naturę tętniaka; W przypadku tej procedury częstość pęknięć śródoperacyjnych wynosi aż 7,6%. W pękniętych tętniakach zwijanie wykonuje się szybko po pęknięciu ze względu na wysokie ryzyko ponownego krwawienia w ciągu pierwszych kilku tygodni po początkowym pęknięciu. Najodpowiedniejsi do wewnątrznaczyniowego zwijania są pacjenci z tętniakami o małym rozmiarze szyi (najlepiej <4 mm), średnicy światła <25 mm oraz ci, którzy różnią się od naczynia macierzystego. Większe tętniaki podlegają zagęszczeniu cewek, zarówno ze względu na mniejszą gęstość upakowania (potrzeba większej liczby cewek), jak i zwiększony przepływ krwi. Zagęszczanie kręgów czyni je nieodpowiednimi, ponieważ nie są w stanie powstrzymać przepływu krwi. Jednak postęp technologiczny umożliwił również zwijanie wielu innych tętniaków.
Wyniki
W wielu badaniach kwestionowano skuteczność zwijania wewnątrznaczyniowego w porównaniu z bardziej tradycyjnym przycinaniem chirurgicznym. Większość obaw dotyczy możliwości późniejszego krwawienia lub innej rekanalizacji. Ze względu na mniej inwazyjny charakter zwijanie wewnątrznaczyniowe zwykle charakteryzuje się szybszym czasem powrotu do zdrowia niż przycinanie chirurgiczne, przy czym w jednym badaniu stwierdzono znaczne zmniejszenie prawdopodobieństwa zgonu lub uzależnienia w porównaniu z populacją neurochirurgiczną. Częstość powikłań związanych z zwijaniem jest również ogólnie niższa niż w przypadku mikrochirurgii (odpowiednio 11,7% i 17,6% w przypadku zwijania i mikrochirurgii). Mimo to udokumentowano, że międzyoperacyjne współczynniki zerwania w zwijaniu sięgają nawet 7,6%. Stwierdzono, że wyniki kliniczne są podobne po dwumiesięcznym i rocznym okresie obserwacji między zwijaniem a neurochirurgią.
Zgłaszane częstości nawrotów są dość zróżnicowane, przy czym częstość nawrotów tętniaków wynosi od 20 do 50% w ciągu jednego roku od zwinięcia, a częstość nawrotów wzrasta z czasem. Wyniki te są podobne do tych, które wcześniej opisywały inne grupy endowaskularne. Inne badania kwestionowały, czy nowe cewki matrycowe działają lepiej niż same cewki platynowe.
Międzynarodowy Tętniak Trial podpajęczynówkowe testowano skuteczność wewnątrznaczyniowego nawijania przeciwko tradycyjnej mikro-chirurgiczne przycinania. Badanie początkowo przyniosło bardzo korzystne wyniki dla zwijania, jednak jego wyniki i metodologia zostały skrytykowane. Od czasu opublikowania badania w 2002 r. i ponownie w 2005 r. niektóre badania wykazały wyższy odsetek nawrotów po zwijaniu, podczas gdy inne wykazały, że nie ma jednoznacznej zgody co do tego, która procedura jest preferowana.
Zagrożenia
Ryzyko zwinięcia wewnątrznaczyniowego obejmuje udar mózgu , pęknięcie tętniaka podczas zabiegu oraz nawrót i pęknięcie tętniaka po zabiegu. Dodatkowo u niektórych pacjentów zwijanie może nie być skuteczne. Na ogół zwijanie wykonuje się tylko wtedy, gdy ryzyko pęknięcia tętniaka jest wyższe niż ryzyko samego zabiegu.
Podobnie jak u pacjentów poddawanych zabiegom neurochirurgicznym, zwijanie powoduje wzrost spoczynkowego wydatku energetycznego, aczkolwiek w nieco mniejszym tempie niż ich odpowiednik neurochirurgiczny. Może to prowadzić do niedożywienia, jeśli nie zostaną podjęte kroki w celu zrekompensowania zwiększonego tempa metabolizmu.
Mechanizm
Zabieg działa poprzez promowanie krzepnięcia krwi ( zakrzepicy ) w tętniaku, ostatecznie odcinając go od przepływu krwi. Osiąga się to poprzez zmniejszenie ilości przepływu krwi wchodzącej do tętniaka, zwiększenie czasu przebywania krwi (a tym samym obniżenie prędkości) w przestrzeni tętniaka i zmniejszenie naprężenia ścinającego ściany tętniaka. Ta zmiana przepływu krwi lub hemodynamiki ostatecznie zależy od kilku czynników, w tym:
- typ tętniaka (bezpośrednio na tętnicy macierzystej lub na rozwidleniu tętnicy)
- pozycja tętniaka (względny kąt tętniaka do zbliżającego się przepływu krwi)
- gęstość upakowania cewki
- kąt krzywizny naczynia macierzystego
- rozmiar szyjki tętniaka
Chociaż czynniki te mają kluczowe znaczenie dla powodzenia zabiegu, zakrzepica ostatecznie zależy od procesów biologicznych, a zwijanie zapewnia tylko odpowiednie warunki do zajścia procesu i, miejmy nadzieję, zamknięcie tętniaka.
Procedura
Zawijanie wewnątrznaczyniowe jest zwykle wykonywane przez neuroradiologa interwencyjnego lub neurochirurga w znieczuleniu ogólnym. Cały zabieg wykonywany jest pod kontrolą obrazowania fluoroskopowego . Cewnik prowadzący wprowadzany jest przez tętnicę udową i wprowadzany do miejsca w pobliżu tętniaka, po czym wykonuje się angiografię w celu zlokalizowania i oceny tętniaka. Następnie do tętniaka wprowadza się mikrocewnik.
Zabieg wykorzystuje rozłączne cewki wykonane z platyny, które wprowadza się do tętniaka za pomocą mikrocewnika. Dostępne są różne cewki, w tym cewki odłączane Guglielmi (GDC), które są platynowe, cewki Matrix, które są pokryte biopolimerem oraz cewki powlekane hydrożelem. Cewki są również dostępne w różnych średnicach, długościach i przekrojach. Cewka jest najpierw umieszczana wzdłuż ściany tętniaka, aby utworzyć ramkę, a następnie rdzeń jest wypełniany większą liczbą cewek. Można również zastosować szereg coraz mniejszych cewek. Sukces jest określany przez wstrzyknięcie barwnika kontrastowego do tętnicy macierzystej i jakościowe określenie, czy barwnik wpływa do przestrzeni tętniaka podczas fluoroskopii. Jeśli nie obserwuje się przepływu, procedurę uważa się za zakończoną. W przypadku tętniaków z szeroką szyjką można zastosować stent .
Historia
Zwijanie wewnątrznaczyniowe powstało w wyniku syntezy szeregu innowacji, które miały miejsce w latach 1970-1990 w dziedzinie elektroniki, neurochirurgii i radiologii interwencyjnej . Chociaż sama procedura była i nadal jest porównywana do chirurgicznego obcinania, rozwój koncepcji i procedury sprawił, że stała się ona złotym standardem w wielu ośrodkach.
Wypełnianie przedziału wewnątrznaczyniowego
Pierwsza udokumentowana technika wykorzystania metalowych cewek do wywoływania zakrzepicy została dokonana przez Mullana w 1974 roku. Miedziane cewki zostały wprowadzone do olbrzymiego tętniaka poprzez zewnętrzne nakłucie ściany tętniaka poprzez kraniotomię. Pięciu pacjentów zmarło, a dziesięciu miało zadowalający proces. Nie zyskała popularności ze względu na wymagany specjalistyczny sprzęt, a ponadto technikę nieodpowiednią dla wielu typów tętniaków. Później, w 1980 r., Alksne i Smith opracowali podobne techniki, wykorzystując żelazo zawieszone w metakrylanie metylu u ograniczonej grupy pacjentów. Nie było zgonów w 22 kolejnych przypadkach o niskiej zachorowalności. Ta technika również nie zyskała przyczepności ze względu na postępy w przycinaniu.
Podejścia wewnątrznaczyniowe
Aby uniknąć metod inwazyjnych, wczesne interwencje wewnątrznaczyniowe obejmowały zastosowanie odłączalnych i nieodłączalnych cewników balonowych w celu zamknięcia tętniaka przy jednoczesnym zachowaniu tętnicy macierzystej . Pomimo innowacyjnego podejścia często stwierdzano, że tętniaki przystosowują się do kształtu samego balonu, co skutkuje częstszymi przypadkami pękania tętniaka. Procedura ta została uznana za „niekontrolowaną” ze względu na wysoką zachorowalność i śmiertelność, ale wykazała, że dostęp wewnątrznaczyniowy był wykonalny w przypadku wielu tętniaków. W 1989 Hilal i wsp. zastosowali spirale wewnątrznaczyniowe, ale były to krótkie, sztywne spirale, które nie zapewniały żadnej kontroli, zapobiegając gęstej upakowania tętniaka. Później zastosowano sterowane systemy mikroprzewodników.
Odłączany system cewek
W 1983 roku po raz pierwszy opisano zastosowanie zakrzepicy indukowanej elektrycznie w tętniakach wewnątrzczaszkowych. Elektroda ze stali nierdzewnej dostarczała do tętniaka dodatni prąd, aby stymulować elektrozakrzepicę. Osiągnięto minimalną okluzję, ale naukowcy odkryli, że erozja elektrody spowodowana elektrolizą byłaby przydatna jako system oderwania. Odłączane cewki zostały zbudowane z platynowej cewki przylutowanej do drutu doprowadzającego ze stali nierdzewnej, po raz pierwszy opisanego w 1991 przez Guglielmi et al. W połączeniu z kontrolowanym systemem mikroprowadnicowym można wprowadzić wiele cewek, aby w pełni zapakować tętniak.
Badania
Biorąc pod uwagę złożoność modelowania układu naczyniowego, wiele badań poświęcono modelowaniu hemodynamiki tętniaka przed i po interwencji. Techniki, takie jak prędkość obrazowania cząstek (PIV) i obliczeniowa dynamika płynów / analiza elementów skończonych (CFD/FEA) przyniosły wyniki, które wpłynęły na kierunek badań, ale do tej pory żaden model nie był w stanie uwzględnić wszystkich obecnych czynników. Do zalet metody badawczej in silico należy elastyczność doboru zmiennych, ale jedno badanie porównawcze wykazało, że symulacje mają tendencję do nadmiernego podkreślania wyników w porównaniu z PIV i są bardziej korzystne dla trendów niż dokładne wartości.
Obrazy medyczne, w szczególności angiografia CT , mogą być wykorzystywane do generowania rekonstrukcji 3D anatomii specyficznej dla pacjenta. W połączeniu z CFD/FEA, hemodynamikę można oszacować w symulacjach specyficznych dla pacjenta, dając klinicyście większe narzędzia prognostyczne do planowania chirurgicznego i oceny wyników, aby jak najlepiej promować tworzenie skrzepliny. Jednak większość modeli komputerowych wykorzystuje wiele założeń dla uproszczenia, w tym sztywne ściany (nieelastyczne) dla unaczynienia, zastępowanie ośrodka porowatego w miejsce fizycznych reprezentacji cewek i stokesa Naviera dla zachowania płynu. Jednak wraz ze wzrostem mocy obliczeniowej opracowywane są nowe modele predykcyjne, w tym algorytmy do symulacji zachowania cewki in vivo.


