Chlorek żelaza(II) - Iron(II) chloride
 Struktura bezwodnego chlorku żelaza (
Fe, Cl)
|
|||
|
|||
| Nazwy | |||
|---|---|---|---|
|
Nazwy IUPAC
Chlorek
żelaza (II) Dichlorek żelaza |
|||
| Inne nazwy
Chlorek żelazawy
Rokühnite |
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| CZEBI | |||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.028.949 |
||
| Numer WE | |||
|
Identyfikator klienta PubChem
|
|||
| Numer RTECS | |||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| FeCl 2 | |||
| Masa cząsteczkowa | 126.751 g/mol (bezwodny) 198,8102 g/mol (tetrahydrat) |
||
| Wygląd | Brązowe ciało stałe (bezwodne) Bladozielone ciało stałe (di-tetrahydrat) |
||
| Gęstość | 3,16 g / cm 3 (bezwodna) 2,39 g / cm 3 (dwuwodzian) 1,93 g / cm 3 (tetrahydrat) |
||
| Temperatura topnienia | 677 °C (1251 °F; 950 K) (bezwodny) 120 °C (dihydrat) 105 °C (tetrahydrat) |
||
| Temperatura wrzenia | 1,023 °C (1873 °F; 1,296 K) (bezwodny) | ||
| 64,4 g/100 ml (10 °C), 68,5 g/100 ml (20 °C), 105,7 g/100 ml (100 °C) |
|||
| Rozpuszczalność w THF | Rozpuszczalny | ||
| log P | -0,15 | ||
| +14 750 x 10 -6 cm 3 / mol | |||
| Struktura | |||
| Jednoskośny | |||
| Oktaedry w Fe | |||
| Farmakologia | |||
| B03AA05 ( KTO ) | |||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | MSDS chlorku żelaza (II) | ||
| NFPA 704 (ognisty diament) | |||
| NIOSH (limity ekspozycji dla zdrowia w USA): | |||
|
REL (zalecane)
|
TWA 1 mg/m 3 | ||
| Związki pokrewne | |||
|
Inne aniony
|
Fluorek żelaza(II) Bromek żelaza(II) Jodek żelaza(II) |
||
|
Inne kationy
|
Chlorek kobaltu(II) Chlorek manganu(II) Chlorek miedzi(II) |
||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Chlorek żelaza (II) , znany także jako chlorek żelazawy , jest związek chemiczny o wzorze FeCl 2 . Jest to paramagnetyczne ciało stałe o wysokiej temperaturze topnienia. Mieszanka jest biała, ale typowe próbki są często białawe. FeCl 2 krystalizuje z wody w postaci zielonkawego tetrahydratu , który jest formą najczęściej spotykaną w handlu i laboratorium. Jest też dwuwodzian. Związek jest dobrze rozpuszczalny w wodzie, dając jasnozielone roztwory.
Produkcja
Uwodnione postaci chlorku żelaza są generowane przez obróbkę odpadów z produkcji stali, z kwasu solnego . Takie roztwory są określane jako „zużyty kwas” lub „płyn marynujący”, zwłaszcza gdy kwas solny nie jest całkowicie zużyty:
- Fe + 2 HCl → FeCl 2 + H 2
Zużyty kwas wymaga oczyszczenia, jeśli zostanie usunięty. Chlorek żelazawy jest używany do produkcji chlorku żelazowego. Do regeneracji kwasu solnego można również użyć chlorku żelazawego. Jest to również produkt uboczny produkcji tytanu, ponieważ niektóre rudy tytanu zawierają żelazo.
Bezwodny FeCl 2
Chlorek żelazawy wytwarza się przez dodanie proszku żelaza do roztworu kwasu solnego w metanolu. Reakcja ta daje solwat metanolowy dichlorku, który po ogrzaniu w próżni w temperaturze około 160 ° C przekształca się w bezwodnym FeCl 2 . Reakcja netto jest pokazana:
- Fe + 2 HCl → FeCl 2 + H 2
FeBr 2 i Fel 2 można wytwarzać analogicznie.
Alternatywna synteza bezwodnego chlorku żelaza jest zmniejszenie FeCl 3 z chlorobenzenem :
- 2 FeCl 3 + C 6 H 5 Cl → 2 FeCl 2 + C 6 H 4 Cl 2 + HCl
W jednym z dwóch klasycznych syntezy ferrocenu , Wilkinson generowane FeCl 2 in situ przez comproportionation FeCl 3 z proszkiem żelaza w tetrahydrofuranie (THF). Chlorek żelazowy rozkłada się do chlorku żelazawego w wysokich temperaturach.
Hydraty
Dihydrat, FeCl 2 (H 2 O) 2 , krystalizuje się z stężonym kwasem solnym. Dihydrat jest polimerem koordynacyjnym . Każde centrum Fe jest koordynowane przez cztery podwójnie mostkujące ligandy chlorkowe . Oktaedron jest uzupełniony parą wzajemnie trans aquo ligandów .
Reakcje
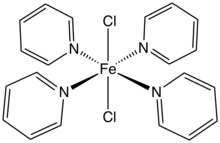
FeCl 2 i jego wodziany tworzą kompleksy z wielu ligandów. Na przykład, roztwory hydratów reagują z dwoma równoważnikami molowymi [(C 2 H 5 ) 4 N] CI z wytworzeniem soli, [(C 2 H 5 ) 4 N] 2 [FeCl 4 ].
Bezwodny FeCl 2 , który jest rozpuszczalny w THF, jest standardowym prekursorem w syntezie metaloorganicznej. FeCl 2 stosuje się w celu wytworzenia kompleksów NHC in situ przez reakcje sprzęgania krzyżowego .
Aplikacje
W przeciwieństwie do pokrewnego siarczanu żelazawego i chlorku żelazowego, chlorek żelazawy ma niewiele zastosowań komercyjnych. Oprócz zastosowania w laboratoryjnej syntezie kompleksów żelaza, chlorek żelaza służy jako czynnik koagulujący i flokulujący w oczyszczaniu ścieków , zwłaszcza odpadów zawierających chromiany lub siarczki . Służy do kontroli zapachów w oczyszczaniu ścieków. Jest używany jako prekursor do wytwarzania różnych gatunków hematytu, które można stosować w różnych pigmentach. Jest prekursorem uwodnionych tlenków żelaza(III), które są pigmentami magnetycznymi. FeCl 2 znajduje zastosowanie jako odczynnik w syntezie organicznej .
Naturalne występowanie
Lawrencyt , (Fe,Ni)Cl 2 , jest naturalnym odpowiednikiem i typowym (choć rzadko występującym) minerałem meteorytowym. Naturalną formą dihydratu jest rokühnite - bardzo rzadki minerał. Pokrewne, ale bardziej złożone (w szczególności zasadowe lub uwodnione) minerały to hibbingit , droninoit i kuliginit .