Heksachlorocykloheksan - Hexachlorocyclohexane
Heksachlorocykloheksan ( HCH ), C
6h
6Cl
6, to dowolny z kilku polichlorowcowanych związków organicznych składający się z sześciowęglowego pierścienia z jednym chlorem i jednym wodorem przyłączonym do każdego węgla. Struktura ta ma dziewięć stereoizomerów (osiem diastereoizomerów , z których jeden ma dwa enancjomery ), różniących się stereochemią poszczególnych podstawników chloru w cykloheksanie . Czasami jest błędnie nazywany „ sześciochlorkiem benzenu ” (BHC). Wykorzystano je jako modele do analizy wpływu różnych położeń geometrycznych dużych atomów z wiązaniami dipolarnymi na stabilność konformacji cykloheksanu . Izomery są w różnym stopniu trującymi, pestycydowymi i trwałymi zanieczyszczeniami organicznymi .
Heksachlorocykloheksan poddano dimeryzacji, aby wyprodukować Mirex , zakazany pestycyd.
Typowe formy to:
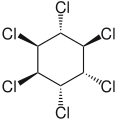
- alfa- heksachlorocykloheksan , α-HCH lub α-BHC ( CAS RN : 319-84-6 ), optycznie czynny izomer
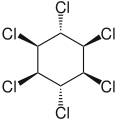
- beta- heksachlorocykloheksan , β-HCH lub β-BHC (CAS RN: 319-85-7 )
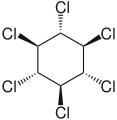
- gamma- heksachlorocykloheksan, γ-HCH, γ-BHC lub lindan (CAS RN: 58-89-9 ), najbardziej owadobójczy izomer
- delta- heksachlorocykloheksan, δ-HCH lub δ-BHC (CAS RN: 319-86-8 )
- techniczny heksachlorocykloheksan, t-HCH lub t-BHC (CAS RN: 608-73-1 ), mieszanina izomerów
α-Heksachlorocykloheksan, lewoskrętny enancjomer
γ-Heksachlorocykloheksan, lindan
Chlorowanie benzenu pod elektrofilowe aromatyczne podstawienie warunkach (Cl 2 / FeCI 3 lub C 2 / AlCl 3 ) wytwarza chlorobenzen . Ponieważ monochloro-odwodornianie dezaktywuje cząsteczkę przed dalszymi reakcjami elektrofilowymi, reakcję można zatrzymać przy podstawieniu jednego atomu chloru.
- Chlorowanie elektrofilowe: C 6 H 6 + Cl 2 → C 6 H 5 Cl + HCl
W przeciwieństwie do tego, chlorowanie benzenu pod addycja rodnika warunkach (Cl 2 , H ν ( photochlorination ) lub Cl 2 , Δ wysokiej P ) otrzymuje się izomery heksachlorocykloheksan po trzech kolejnych etapach rodników dichlorowania. Zachodzi raczej dodawanie niż substytucja , ze względu na bardzo wysoką energię dysocjacji wiązania C–H (112 kcal/mol), która nie sprzyja abstrakcji atomu wodoru. Dodanie Cl 2 niszczy aromatyczność pierścienia benzenowego, a dodanie dwóch kolejnych cząsteczek Cl 2 jest szybkie w porównaniu z pierwszą. W związku z tym z tej reakcji można wyizolować tylko trzykrotnie chlorowany produkt.
- Addycja rodnikowa: C 6 H 6 + 3Cl 2 → C 6 H 6 Cl 6
Izomery heksachlorocykloheksanu z więcej niż jednym atomem chloru na węgiel to:
- 1,1,2,3,4,5-heksachlorocykloheksan
- 1,1,2,3,4,6-heksachlorocykloheksan
- 1,1,2,3,5,6-heksachlorocykloheksan
- 1,1,2,2,3,4-heksachlorocykloheksan
- 1,1,2,2,3,5-heksachlorocykloheksan
- 1,1,2,2,3,6-heksachlorocykloheksan
- 1,1,2,2,4,5-heksachlorocykloheksan
- 1,1,2,3,3,4-heksachlorocykloheksan
- 1,1,2,3,3,5-heksachlorocykloheksan
- 1,1,2,3,4,4-heksachlorocykloheksan
- 1,1,3,3,5,5-heksachlorocykloheksan
- 1,1,2,4,4,5-heksachlorocykloheksan
- 1,1,2,4,4,6-heksachlorocykloheksan
- 1,1,2,4,5,5-heksachlorocykloheksan
- 1,1,2,5,6,6-heksachlorocykloheksan
- 1,1,2,2,3,3-heksachlorocykloheksan
- 1,1,2,2,4,4-heksachlorocykloheksan
- 1,1,3,3,5,5-heksachlorocykloheksan