Prosty pierścień aromatyczny - Simple aromatic ring
Proste pierścienie aromatyczne , znane również jako proste areny lub proste związki aromatyczne , to aromatyczne związki organiczne, które składają się tylko ze sprzężonego płaskiego układu pierścieniowego. Wiele prostych pierścieni aromatycznych ma trywialne nazwy. Zwykle występują jako podstruktury bardziej złożonych cząsteczek („ podstawione związki aromatyczne”). Typowymi prostymi związkami aromatycznymi są benzen , indol i pirydyna .
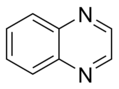
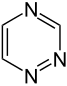
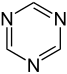
Proste pierścienie aromatyczne mogą być heterocykliczne, jeśli zawierają atomy pierścieniowe niewęglowe , na przykład tlen , azot lub siarkę . Mogą być monocykliczne, jak w benzenie, bicykliczne, jak w naftalenie lub policykliczne, jak w antracenie . Proste monocykliczne pierścienie aromatyczne to zwykle pięcioczłonowe pierścienie, takie jak pirol lub sześcioczłonowe pierścienie, takie jak pirydyna . Skondensowane / skondensowane pierścienie aromatyczne składają się z monocyklicznych pierścieni, które mają wspólne wiązania.
Heterocykliczne pierścienie aromatyczne
|
|||||||||||||||||||||||||||||||||||||||||||||||||
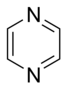
Pierścienie aromatyczne zawierające azot (N) można rozdzielić na zasadowe pierścienie aromatyczne, które są łatwo protonowane i tworzą aromatyczne kationy i sole (np. Pirydyniowe ) oraz niezasadowe pierścienie aromatyczne.
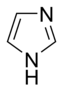
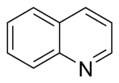
- W podstawowych pierścieni aromatycznych The wolną parę z elektronów nie jest częścią układu aromatycznego i rozciąga się w płaszczyźnie pierścienia. Ta samotna para jest odpowiedzialna za zasadowość tych zasad azotowych , podobnie jak atom azotu w aminach . W tych związkach atom azotu nie jest połączony z atomem wodoru. Przykładami podstawowych pierścieni aromatycznych są pirydyna lub chinolina . Kilka pierścieni zawiera zarówno zasadowe, jak i niezasadowe atomy azotu, np. Imidazol i puryna .
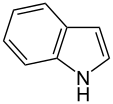
- W pierścieniach niezasadowych samotna para elektronów atomu azotu jest zdelokalizowana i uczestniczy w aromatycznym układzie pi-elektronów. W tych związkach atom azotu jest połączony z atomem wodoru. Przykładami niezasadowych pierścieni aromatycznych zawierających azot są pirol i indol .
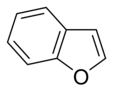
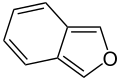
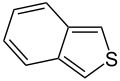
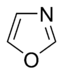
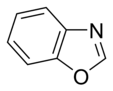
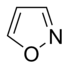
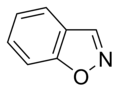
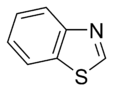
W pierścieniach aromatycznych zawierających tlen i siarkę jedna z par elektronów heteroatomów uczestniczy w układzie aromatycznym (podobnie jak pierścienie niezasadowe zawierające azot), podczas gdy druga wolna para rozciąga się w płaszczyźnie pierścienia ( podobne do pierścieni zawierających pierwotny azot).
Kryteria aromatyczności
- Cząsteczka musi być cykliczna.
- Każdy atom w pierścieniu musi mieć zajęty orbital p , który zachodzi na orbitale p po obu stronach (całkowicie sprzężone ).
- Cząsteczka musi być płaska.
- Musi zawierać nieparzystą liczbę par elektronów pi; musi spełniać regułę Hückela : (4n + 2) pi elektronów, gdzie n jest liczbą całkowitą zaczynającą się od zera.
Natomiast cząsteczki z elektronami 4n pi są antyaromatyczne .