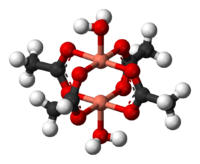
Octan miedzi(II) - Copper(II) acetate
 Octan miedzi(II) częściowo sproszkowany
|
|
 Małe kryształy octanu miedzi(II)
|
|
 Kryształy octanu miedzi(II) na drucie miedzianym
|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
Tetra- μ 2 -acetatodiaquadicopper (II),
|
|
| Inne nazwy
Miedź (II), octanu metylu
octan miedziowy octan miedzi Verdigris |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.005.049 |
| Numer WE | |
|
Identyfikator klienta PubChem
|
|
| UNII | |
| Numer ONZ | 3077 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| Cu(CH 3 COO) 2 | |
| Masa cząsteczkowa | 181,63 g/mol (bezwodny) 199,65 g/mol (hydrat) |
| Wygląd zewnętrzny | Ciemnozielone krystaliczne ciało stałe |
| Zapach | Bezwonny (hydrat) |
| Gęstość | 1,882 g / cm 3 (wodzian) |
| Temperatura topnienia | Nieokreślony(135-by 中文wikipedia) |
| Temperatura wrzenia | 240 ° C (464° F; 513 K) |
|
Hydrat : 7,2 g/100 ml (zimna woda) 20 g/100 ml (gorąca woda) |
|
| Rozpuszczalność | Rozpuszczalny w alkoholu Słabo rozpuszczalny w eterze i glicerolu |
|
Współczynnik załamania ( n D )
|
1,545 (hydrat) |
| Struktura | |
| Jednoskośny | |
| Zagrożenia | |
| Arkusz danych dotyczących bezpieczeństwa | Karta Charakterystyki Piekarza |
| Piktogramy GHS |
   
|
| Hasło ostrzegawcze GHS | Zagrożenie |
| H301 , H302 , H311 , H314 , H318 , H400 , H410 , H411 , H412 | |
| P260 , P264 , P270 , P273 , P280 , P301+310 , P301+312 , P301+330+331 , P302+352 , P303+361+353 , P304+340 , P305+351+338 , P310 , P312 , P321 , P322 , P330 , P361 , P363 , P391 , P405 , P501 | |
| NFPA 704 (ognisty diament) | |
| Temperatura zapłonu | Nie palne |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
710 mg/kg doustnie szczur |
| NIOSH (limity ekspozycji dla zdrowia w USA): | |
|
PEL (dopuszczalne)
|
TWA 1 mg/m 3 (jako Cu) |
|
REL (zalecane)
|
TWA 1 mg/m 3 (jako Cu) |
|
IDLH (Bezpośrednie niebezpieczeństwo)
|
TWA 100 mg/m 3 (jako Cu) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Octan miedzi(II) , zwany również octanem miedzi , jest związkiem chemicznym o wzorze Cu (OAc) 2 gdzie AcO − to octan ( CH
3WSPÓŁ−
2). Uwodniony pochodna Cu 2 (OAc) 4 (H 2 O) 2 , który zawiera jedną cząsteczkę wody na każdy atom miedzi, jest dostępna w handlu. Bezwodny miedzi (ll) jest ciemnozielone krystaliczne ciało stałe, podczas gdy Cu 2 (OAc) 4 (H 2 O) 2 jest bardziej niebiesko-zielony. Od czasów starożytnych jako fungicydy i zielone pigmenty stosowano octany miedzi w jakiejś formie . Obecnie octany miedzi są używane jako odczynniki do syntezy różnych związków nieorganicznych i organicznych . Octan miedzi, jak wszystkie związki miedzi, emituje w płomieniu niebiesko-zieloną poświatę . Hoganit mineralny jest naturalnie występującą formą octanu miedzi(II). Pokrewnym minerałem, również zawierającym wapń, jest pacyt. Oba są bardzo rzadkie.
Struktura
Hydrat octanu miedzi przyjmuje strukturę koła łopatkowego widoczną również dla pokrewnych tetraoctanów Rh(II) i Cr(II). Jeden atom tlenu na każdym octanie jest związany z jednym atomem miedzi przy 1,97 Å (197 pm ). Sferę koordynacyjną dopełniają dwa ligandy wodne o odległościach Cu–O 2,20 Å (220 pm). Dwa atomy miedzi są oddzielone tylko 2,62 Å (262 pm), co jest bliskie separacji Cu-Cu w metalicznej miedzi. Dwa centra miedzi Interact w wyniku spadku zdolności momentu magnetycznego tak, że w temperaturze poniżej 90 K, Cu 2 (OAc) 4 (H 2 O) 2 jest zasadniczo diamagnetycznego. Cu 2 (OAc) 4 (H 2 O) 2 był krytycznym krokiem w rozwoju nowoczesnych teorii sprzężenia wymiany antyferromagnetycznej , które przypisują jego zachowanie diamagnetyczne w niskich temperaturach zniesieniu dwóch przeciwstawnych spinów na sąsiednich atomach miedzi.
Synteza
Octan miedzi(II) wytwarza się przemysłowo przez ogrzewanie wodorotlenku miedzi(II) lub zasadowego węglanu miedzi(II) z kwasem octowym .
Związki pokrewne
Ogrzewanie mieszaniny bezwodnego octanu miedzi(II) i miedzi metalicznej daje octan miedzi(I) :
- Cu + Cu(OAc) 2 → 2 CuOAc
W przeciwieństwie do pochodnej miedzi(II), octan miedzi(I) jest bezbarwny i diamagnetyczny.
„Zasadowy octan miedzi” wytwarza się przez zobojętnienie wodnego roztworu octanu miedzi(II). Zasadowy octan jest słabo rozpuszczalny. Materiał ten jest składnikiem patyny , niebiesko-zielonej substancji, która tworzy się na miedzi podczas długiej ekspozycji na atmosferę.
Zastosowania w syntezie chemicznej
Octan miedzi(II) znalazł zastosowanie jako środek utleniający w syntezach organicznych. W reakcji Eglintona Cu 2 (OAc) 4 jest używany do sprzęgania terminalnych alkinów w celu uzyskania 1,3- diynu :
- Cu 2 (OAc) 4 + 2 RC≡CH → 2 CuOAc + RC≡C−C≡CR + 2 HOAc
Reakcja przebiega za pośrednictwem acetylenków miedzi(I) , które są następnie utleniane przez octan miedzi(II), uwalniając rodnik acetylenkowy. Pokrewną reakcją z udziałem acetylenków miedzi jest synteza ynamin , terminalnych alkinów z grupami aminowymi, przy użyciu Cu 2 (OAc) 4 . Jest on używany do hydroaminowania z akrylonitrylu .
Jest również środkiem utleniającym w teście Barfoeda .
Reaguje z trójtlenkiem arsenu, tworząc acetoarsenit miedzi, silny środek owadobójczy i grzybobójczy zwany zielenią paryską .
Zewnętrzne linki
- Copper.org – Inne związki miedzi 5 lutego 2006
- Infoplease.com – Paryż zielony 6 lutego 2006
- Verdigris – historia i synteza 6 lutego 2006
- Australijski – Krajowy Spis Zanieczyszczeń 8 sierpnia 2016 r.
- USA NIH National Center for Biotechnology Information 8 sierpnia 2016 r.
Bibliografia
- ^ Trimble, RF (1976). „Monohydrat octanu miedzi (II) - błędna temperatura topnienia”. Journal of Chemical Education . 53 (6): 397. Kod bib : 1976JChEd..53..397T . doi : 10.1021/ed053p397 .
- ^ a b c Kieszonkowy przewodnik NIOSH po zagrożeniach chemicznych. „#0150” . Narodowy Instytut Bezpieczeństwa i Higieny Pracy (NIOSH).
- ^ „Zarchiwizowana kopia” (PDF) . Zarchiwizowane z oryginału (PDF) dnia 2011-09-28 . Źródło 2011-06-14 .CS1 maint: zarchiwizowana kopia jako tytuł ( link )
- ^ B Richardson H. Wayne. „Związki miedzi”. Encyklopedia Chemii Przemysłowej Ullmanna . Weinheim: Wiley-VCH.
- ^ Musumeci, Antoni; Mróz, Ray L. (2007-05-01). „Spektroskopowe i termoanalityczne badanie mineralnego hoganitu” . Spectrochimica Acta Część A: Spektroskopia molekularna i biomolekularna . 67 (1): 48–57. Kod Bib : 2007AcSpA..67...48M . doi : 10.1016/j.saa.2006.05.037 . ISSN 1386-1425 . PMID 17321784 .
- ^ B Hibbs, DE; Kolitsch, U.; Leverett, P.; Sharpe'a, JL; Williams, PA (czerwiec 2002). „Hoganit i paceit, dwa nowe minerały octanowe z kopalni Potosi, Broken Hill, Australia” . Magazyn mineralogiczny . 66 (3): 459–464. Kod Bib : 2002MinM...66..459H . doi : 10.1180/0026461026630042 . ISSN 0026-461X . S2CID 97116531 .
- ^ https://www.mindat.org/min-10918.html
- ^ https://www.ima-mineralogy.org/Minlist.htm
- ^ Van Niekerk, JN; Schöning, FRL (1953). „Dowody rentgenowskie dla wiązań metal-metal w octanie miedzi i chromu”. Natura . 171 (4340): 36-37. Kod bib : 1953Natur.171...36V . doi : 10.1038/171036a0 . S2CID 4292992 .
- ^ Wells, AF (1984). Strukturalna Chemia Nieorganiczna . Oxford: Clarendon Press.
- ^ Catterick, J.; Thornton, P. (1977). „Struktury i właściwości fizyczne wielopierścieniowych karboksylanów” . Przysł. Inorg. Chem. Radiochem . Postępy w chemii nieorganicznej i radiochemii. 20 : 291-362. doi : 10.1016/s0065-2792(08)60041-2 . Numer ISBN 9780120236206.
- ^ van Niekerk, JN; Schoening, FRL (1953-03-10). „Nowy typ kompleksu miedzi występujący w strukturze krystalicznej octanu miedzi, Cu2(CH3COO)4.2H2O” . Acta Crystallographica . 6 (3): 227–232. doi : 10.1107/S0365110X53000715 . ISSN 0365-110X .
- ^ Meester, Patrice de; Fletcher, Steven R.; Skapski, Andrzej C. (1973-01-01). „Wyrafinowana struktura krystaliczna tetra-µ-acetato-bisaquodicopper(II)” . Journal of the Chemical Society, Dalton Transactions (23): 2575-2578. doi : 10.1039/DT9730002575 . ISSN 1364-5447 .
- ^ Brązowy, GM; Chidambaram, R. (1973-11-15). „Monohydrat dwujądrowego octanu miedzi(II): ponowne określenie struktury za pomocą analizy dyfrakcyjnej neutronów” . Acta Crystallographica Sekcja B Krystalografia strukturalna i chemia kryształów . 29 (11): 2393-2403. doi : 10.1107/S0567740873006758 . ISSN 0567-7408 .
- ^ Carlin, RL (1986). Magnetochemia . Berlin: Springer. s. 77-82. Numer ISBN 978-3642707353.
- ^ Kirchner, SJ; Fernando, Q. (1980). Octan miedzi(I) . Inorg. Syntezator. Syntezy nieorganiczne. 20 . s. 53–55. doi : 10.1002/9780470132517.ch16 . Numer ISBN 9780470132517.
- ^ Parafia, EJ; Kizito, SA (2001). „Octan miedzi (I)”. Encyklopedia odczynników do syntezy organicznej . John Wiley & Synowie. doi : 10.1002/047084289X.rc193 . Numer ISBN 0471936235.
- ^ Stöckel, K.; Sondheimer, F. „[18] Annulen” . Syntezy organiczne . 54 : 1. doi : 10.15227/orgsyn.054.0001 .; Tom zbiorowy , 6 , s. 68
- ^ Campbell, ID; Eglinton, G. "Difenylodiacetylen" . Syntezy organiczne . 45 : 39. doi : 10.15227/orgsyn.045.0039 .; Tom zbiorowy , 5 , s. 517
- ^ Vogel, P.; Srogl, J. (2005). „Octan miedzi (II)”. Encyklopedia odczynników do syntezy organicznej EROS . John Wiley & Synowie. doi : 10.1002/047084289X.rc194.pub2 . Numer ISBN 978-0-470-84289-8..
- ^ Heininger, SA „3-( o- chloroanilino) propionitryl” . Syntezy organiczne . 38 : 14. doi : 10.15227/orgsyn.038.0014 .; Tom zbiorowy , 4 , s. 146