Związek cykliczny - Cyclic compound
Cykliczny (lub związek pierścień ), jest to określenie dla związku w dziedzinie chemii , w których jeden lub więcej atomów w serii związku jest połączony, tworząc pierścień . Pierścienie mogą różnić się wielkością od trzech do wielu atomów i obejmują przykłady, w których wszystkie atomy są węglem (tj. są karbocyklami ), żaden z atomów nie jest węglem (nieorganiczne związki cykliczne) lub w których obecne są zarówno atomy węgla, jak i niewęglowe ( związki heterocykliczne ). W zależności od wielkości pierścienia, kolejności wiązań poszczególnych wiązań między atomami pierścienia i ich rozmieszczenia w pierścieniach, związki karbocykliczne i heterocykliczne mogą być aromatyczne lub niearomatyczne; w tym ostatnim przypadku mogą one różnić się od pełnego nasycenia do różnej liczby wiązań wielokrotnych między atomami pierścienia. Ze względu na ogromną różnorodność, na którą pozwala w połączeniu wartościowości wspólnych atomów i ich zdolność do tworzenia pierścieni, liczba możliwych struktur cyklicznych, nawet niewielkich rozmiarów (np. < 17 atomów ogółem), liczy się w wielu miliardach.
- Przykłady związków cyklicznych: W pełni węglowe (karbocykliczne) i bardziej złożone naturalne związki cykliczne.
Ingenol , złożony, terpenoidowy produkt naturalny , spokrewniony z paklitakselem , ale prostszy niż następujący, który wykazuje złożoną strukturę pierścieniową obejmującą 3-, 5- i 7-członowe niearomatyczne , karbocykliczne pierścienie.
Cykloalkany , najprostsze karbocykle , w tym cyklopropan , cyklobutan , cyklopentan i cykloheksan . Zauważ, że gdzie indziej używany jest skrót z chemii organicznej, w którym atomy wodoru są wywnioskowane jako obecne, aby wypełnić wartościowość węgla wynoszącą 4 (zamiast ich wyraźnie pokazać).
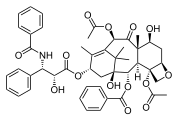
Paklitaksel , kolejny złożony terpenoid pochodzenia roślinnego , również produkt naturalny, wykazujący złożoną strukturę wielopierścieniową obejmującą pierścienie 4-, 6- i 8-członowe (karbocykliczne i heterocykliczne , aromatyczne i niearomatyczne).
Dodając do ich złożoności i liczby, zamykanie atomów w pierścienie może blokować poszczególne atomy z wyraźną substytucją (przez grupy funkcyjne ) tak, że uzyskuje się stereochemię i chiralność związku, w tym pewne przejawy, które są unikalne dla pierścieni (np. izomery konfiguracyjne ). Ponadto, w zależności od rozmiaru pierścienia, trójwymiarowe kształty poszczególnych struktur cyklicznych – zwykle pierścieni składających się z pięciu atomów i większych – mogą się zmieniać i przekształcać w taki sposób, że widoczna jest izomeria konformacyjna . Rzeczywiście, rozwój tej ważnej koncepcji chemicznej powstał historycznie w odniesieniu do związków cyklicznych. Wreszcie, związki cykliczne, z powodu unikalnych kształtów, reaktywności, właściwości i bioaktywności , które wywołują, stanowią większość wszystkich cząsteczek zaangażowanych w biochemię, strukturę i funkcję żywych organizmów oraz w molekułach stworzonych przez człowieka, takich jak leki, pestycydy itp.
Wprowadzenie strukturalne
Związek cykliczny lub związek pierścieniowy to związek, w którym co najmniej niektóre jego atomy są połączone tworząc pierścień. Pierścienie różnią się wielkością od trzech do kilkudziesięciu, a nawet setek atomów. Przykłady związków pierścieniowych łatwo obejmują przypadki, w których:
- wszystkie atomy to węgiel (tj. są karbocyklami ),
- żaden z atomów nie jest węglem (nieorganiczne związki cykliczne) lub gdzie
- obecne są zarówno atomy węgla, jak i nie-węglowe ( związki heterocykliczne ).
Zwykłe atomy mogą (w wyniku ich wartościowości ) tworzyć różną liczbę wiązań, a wiele powszechnych atomów łatwo tworzy pierścienie. Ponadto, w zależności od wielkości pierścienia, kolejności wiązań poszczególnych wiązań między atomami pierścienia i ich rozmieszczenia w pierścieniach, związki cykliczne mogą być aromatyczne lub niearomatyczne; w przypadku niearomatycznych związków cyklicznych mogą one różnić się od pełnego nasycenia do różnej liczby wiązań wielokrotnych. Jako konsekwencja konstytucyjnej zmienności, która jest termodynamicznie możliwa w strukturach cyklicznych, liczba możliwych struktur cyklicznych, nawet niewielkich rozmiarów (np. <17 atomów) liczy się w wielu miliardach.
Co więcej, zamknięcie atomów w pierścienie może zablokować określoną grupę funkcyjną – podstawione atomy w miejscu, co skutkuje powiązaniem ze związkiem stereochemii i chiralności , w tym pewnych objawów charakterystycznych dla pierścieni (np. izomery konfiguracyjne ); Ponadto, w zależności od rozmiaru pierścienia, trójwymiarowe kształty poszczególnych struktur cyklicznych — zazwyczaj pierścienie złożone z pięciu atomów i większe — mogą się zmieniać i przekształcać w taki sposób, że prezentowana jest izomeria konformacyjna .
Nomenklatura
Nomenklatura IUPAC ma rozbudowane zasady obejmujące nazewnictwo struktur cyklicznych, zarówno jako struktury rdzeniowe, jak i jako podstawniki dołączone do struktur alicyklicznych . Termin makrocykl jest stosowany, gdy związek zawierający pierścień ma pierścień składający się z 12 lub więcej atomów. Termin policykliczny jest używany, gdy w jednej cząsteczce pojawia się więcej niż jeden pierścień. Naftalen jest formalnie związkiem policyklicznym, ale bardziej konkretnie jest określany jako związek bicykliczny. Kilka przykładów struktur makrocyklicznych i policyklicznych podano w końcowej galerii poniżej.
Atomy wchodzące w skład struktury pierścieniowej nazywane są atomami pierścieniowymi.
Carbocykle
Zdecydowana większość związków cyklicznych to związki organiczne , a spośród nich znacząca i koncepcyjnie ważna część składa się z pierścieni zbudowanych wyłącznie z atomów węgla (tj. są to karbocykle).
Nieorganiczne związki cykliczne
Atomy nieorganiczne również tworzą związki cykliczne. Przykłady obejmują siarkę , krzem (np. w silanach ), fosfor (np. w wariantach fosfanów i kwasu fosforowego ) oraz bor (np. w kwasie triborowym). Gdy węgiel w benzenie jest „zastępowany” innymi pierwiastkami, np. borabenzenem , silabenzenem , germanabenzenem , stannabenzenem i fosforem , aromatyczność zostaje zachowana, a zatem aromatyczne nieorganiczne związki cykliczne są znane i dobrze scharakteryzowane.
Związki heterocykliczne
Związki cykliczne, które zawierają zarówno atomy węgla, jak i atomy niewęglowe, są określane jako ( związki heterocykliczne ); alternatywnie nazwa może odnosić się do nieorganicznych związków cyklicznych, takich jak siloksany i borazyny, które mają w swoich pierścieniach więcej niż jeden typ atomu. Nomenklatura Hantzscha-Widmana jest zalecana przez IUPAC do nazewnictwa heterocykli, ale wiele popularnych nazw pozostaje w regularnym użyciu.
Aromatyczność
Związki cykliczne mogą, ale nie muszą, wykazywać aromatyczności ; benzen jest przykładem aromatycznego związku cyklicznego, podczas gdy cykloheksan jest niearomatyczny. W chemii organicznej termin aromatyczność jest używany do opisania cyklicznej (w kształcie pierścienia), płaskiej (płaskiej) cząsteczki, która wykazuje niezwykłą stabilność w porównaniu z innymi geometrycznymi lub łącznymi układami tego samego zestawu atomów. Ze względu na ich stabilność bardzo trudno jest spowodować rozerwanie cząsteczek aromatycznych i reakcję z innymi substancjami. Związki organiczne, które nie są aromatyczne, są klasyfikowane jako związki alifatyczne – mogą być cykliczne, ale tylko pierścienie aromatyczne mają szczególną stabilność (niska reaktywność).
Ponieważ jeden z najczęściej spotykanych układów aromatycznych związków w chemii organicznej oparty jest na pochodnych prototypowego związku aromatycznego benzenu (węglowodór aromatyczny powszechnie występujący w ropie naftowej i jej destylatach), słowo „aromatyczny” jest czasami używane w odniesieniu do pochodnych benzenu , i tak to zostało po raz pierwszy zdefiniowane. Niemniej jednak istnieje wiele niebenzenowych związków aromatycznych. Na przykład w organizmach żywych najpowszechniejszymi pierścieniami aromatycznymi są zasady dwupierścieniowe w RNA i DNA. Grupa funkcyjna lub inny podstawnik, który jest aromatyczny, nazywana jest grupą arylową.
Najwcześniejsze użycie terminu „aromatyczny” było w artykule Augusta Wilhelma Hofmanna z 1855 roku. Hofmann użył tego terminu dla klasy związków benzenu, z których wiele ma zapachy (aromaty), w przeciwieństwie do czystych węglowodorów nasyconych. Obecnie nie ma ogólnego związku między aromatycznością jako właściwością chemiczną a właściwościami węchowymi takich związków (jak pachną), chociaż w 1855 roku, zanim zrozumiano strukturę benzenu lub związków organicznych, chemicy tacy jak Hofmann zaczęli rozumieć, że Cząsteczki roślinne, takie jak terpeny, mają właściwości chemiczne, które dziś uznajemy za podobne do nienasyconych węglowodorów ropopochodnych, takich jak benzen.
Jeśli chodzi o elektronową naturę cząsteczki, aromatyczność opisuje sprzężony system często złożony z naprzemiennych pojedynczych i podwójnych wiązań w pierścieniu. Ta konfiguracja pozwala na delokalizację elektronów w układzie pi cząsteczki wokół pierścienia, zwiększając stabilność cząsteczki. Cząsteczka nie może być reprezentowana przez jedną strukturę, ale raczej hybrydę rezonansową różnych struktur, na przykład dwie struktury rezonansowe benzenu. Cząsteczek tych nie można znaleźć w żadnej z tych reprezentacji, z dłuższymi wiązaniami pojedynczymi w jednym miejscu i krótszymi wiązaniami podwójnymi w innym (patrz Teoria poniżej). Cząsteczka wykazuje raczej długości wiązań pomiędzy wiązaniami pojedynczymi i podwójnymi. Ten powszechnie spotykany model pierścieni aromatycznych, a mianowicie pomysł, że benzen powstał z sześcioczłonowego pierścienia węglowego z naprzemiennymi wiązaniami pojedynczymi i podwójnymi (cykloheksatrien), został opracowany przez Augusta Kekulé (patrz rozdział Historia poniżej). Model dla benzenu składa się z dwóch form rezonansowych, co odpowiada wiązaniom podwójnym i pojedynczym, które nakładają się, tworząc sześć wiązań półtora. Benzen jest bardziej stabilną cząsteczką, niż można by oczekiwać bez uwzględnienia delokalizacji ładunku.
Proste, monocykliczne przykłady
Oto przykłady prostych i aromatycznych karbocykli, nieorganicznych związków cyklicznych i heterocykli:
- Proste związki monocykliczne: przykłady karbocykliczne, nieorganiczne i heterocykliczne (aromatyczne i niearomatyczne).
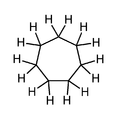
Cykloheptan , prosty 7-członowy związek karbocykliczny, pokazano wodory metylenowe (niearomatyczne).
Benzen , 6-członowy związek karbocykliczny. pokazano wodory metinu i 6 elektronów pokazanych jako zdelokalizowane poprzez narysowanie koła (aromatyczne).
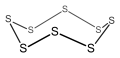
Cyklo - oktasiarka , 8-członowy nieorganiczny związek cykliczny (niearomatyczny).
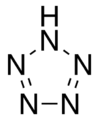
Pentazol , 5-członowy nieorganiczny związek cykliczny (aromatyczny).
Pirydyna , 6-członowy związek heterocykliczny, z implikowanymi atomami wodoru metyny , nie pokazanymi i zdelokalizowanymi elektronami π, pokazanymi jako wiązania dyskretne (aromatyczne).
Stereochemia
Zamknięcie atomów w pierścienie może blokować poszczególne atomy z wyraźną substytucją grupami funkcyjnymi tak, że wynikiem jest stereochemia i chiralność związku, w tym pewne przejawy, które są unikalne dla pierścieni (np. izomery konfiguracyjne ).
Izomeria konformacyjna
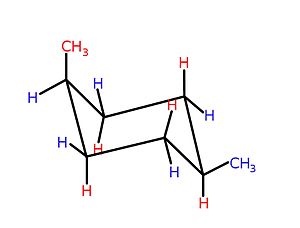
W zależności od rozmiaru pierścienia, trójwymiarowe kształty poszczególnych struktur cyklicznych — zazwyczaj pierścienie o 5 atomach i większych — mogą się zmieniać i przekształcać w taki sposób, że jest wyświetlana izomeria konformacyjna . Rzeczywiście, rozwój tej ważnej koncepcji chemicznej nastąpił historycznie w odniesieniu do związków cyklicznych. Na przykład cykloheksany — sześcioczłonowe karbocykle bez wiązań podwójnych, do których mogą być dołączone różne podstawniki, patrz zdjęcie — wyświetlają równowagę między dwiema konformacjami, krzesłem i łodzią, jak pokazano na obrazku.
Krzesło konformacja jest preferowanym konfiguracji, ponieważ w tej konformacji, na zawadę szczepem , szczepem spychając i odkształcenia kątowego , które są możliwe w innym przypadku są zminimalizowane. Która z możliwych konformacji krzesełkowych przeważa w cykloheksanach zawierających jeden lub więcej podstawników, zależy od podstawników i ich umiejscowienia na pierścieniu; Ogólnie, „przestrzenne” podstawniki-te grupy o dużej objętości , lub grup, które są w inny sposób w swoim odpychające interakcje -prefer zajmować położenie równikowego. Przykładem oddziaływań w cząsteczce, które prowadziłyby do odkształcenia sterycznego , prowadzącego do przesunięcia równowagi z łodzi na krzesło, jest oddziaływanie między dwiema grupami metylowymi w cis -1,4-dimetylocykloheksanie. W tej cząsteczce dwie grupy metylowe znajdują się w przeciwnych pozycjach pierścienia (1,4-), a ich stereochemia cis rzutuje obie te grupy w stronę tej samej strony pierścienia. Stąd, jeśli zostaną zmuszone do formy łodzi o wyższej energii, te grupy metylowe pozostają w kontakcie sterycznym, odpychają się nawzajem i kierują równowagę w kierunku konformacji krzesła.
Makrocykle
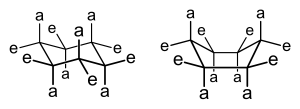
Termin makrocykl jest używany dla związków mających pierścienie z 8 lub więcej atomami. Makrocykle mogą być w pełni karbocykliczne, heterocykliczne, ale mające ograniczone heteroatomy (np. w laktonach i laktamach ) lub być bogate w heteroatomy i wykazywać znaczącą symetrię (np. w przypadku chelatujących makrocykli). Makrocykle mogą uzyskać dostęp do wielu stabilnych konformacji , z preferencją przebywania w konformacjach, które minimalizują transpierścieniowe oddziaływania niezwiązane w obrębie pierścienia (np. krzesło i krzesło-łodzi są bardziej stabilne niż konformacja łódź-łodzi dla cyklooktanu, ze względu na przedstawione interakcje pokazanymi łukami). Pierścienie średnie (8-11 atomów) są najbardziej obciążone, z energią odkształcenia w zakresie 9-13 (kcal/mol), a analizę czynników ważnych w konformacjach większych makrocykli można modelować za pomocą konformacji pierścienia średniego. Analiza konformacyjna pierścieni o nieparzystym członie sugeruje, że mają one tendencję do przebywania w mniej symetrycznych formach z mniejszymi różnicami energii między stabilnymi konformacjami.

Podstawowe zastosowania struktur cyklicznych
Ze względu na unikalne kształty, reaktywności, właściwości i bioaktywności , które wywołują, związki cykliczne stanowią największą większość wszystkich cząsteczek zaangażowanych w biochemię, strukturę i funkcję żywych organizmów oraz w molekułach wytworzonych przez człowieka (np. leki, herbicydy itp.), za pomocą których człowiek próbuje sprawować kontrolę nad przyrodą i systemami biologicznymi.
Przykłady złożone i policykliczne
Poniżej przedstawiono przykłady związków cyklicznych wykazujących bardziej złożone układy pierścieniowe i cechy stereochemiczne:
- Złożone związki cykliczne: Przykłady makrocykliczne i policykliczne
Naftalen , technicznie policykliczny, a dokładniej bicykliczny związek, z kółkami pokazującymi delokalizację elektronów π (aromatycznych).
Dekalina (dekahydronaftalen), w pełni nasycona pochodna naftalenu , ukazująca dwie stereochemie możliwe do „połączenia” dwóch pierścieni i jak wpływa to na kształty dostępne dla tego bicyklicznego związku (niearomatycznego).
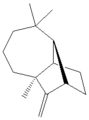
Longifolen , naturalny produkt terpenowy i przykład cząsteczki trójpierścieniowej (niearomatycznej).
Paklitaksel , policykliczny produkt naturalny z tricyklicznym rdzeniem: z heterocyklicznym, 4-członowym pierścieniem D, skondensowanym z kolejnymi 6- i 8-członowymi pierścieniami karbocyklicznymi (A/C i B) (niearomatycznymi) oraz z trzema dalszymi bocznymi pierścieniami fenyl -rings na jego "ogon", oraz dołączony do C-2 (ang Ph, d. 6 H 5 ; aromatyczne).
Reprezentacyjny trójwymiarowy kształt przyjęty przez paklitaksel , dzięki unikalnej, cyklicznej strukturze.
Cholesterol , inny naturalny produkt terpenowy, w szczególności steroid , klasa cząsteczek tetracyklicznych (niearomatycznych).
Benzo[a]piren , związek pentacykliczny, zarówno naturalny, jak i wytworzony przez człowieka, oraz zdelokalizowane elektrony π pokazane jako wiązania dyskretne (aromatyczne).
Pagodane , złożony, wysoce symetryczny, wytworzony przez człowieka związek policykliczny (niearomatyczny).
Brevetoksyna A , naturalny produkt z dziesięcioma pierścieniami, wszystkie skondensowane i wszystkie heterocykliczne oraz toksyczny składnik związany z organizmami odpowiedzialnymi za czerwone przypływy . Grupa R po prawej odnosi się do jednego z kilku możliwych czterowęglowych łańcuchów bocznych (patrz główny artykuł dotyczący Brevetoksyny ; niearomatyczny).
Reakcje syntetyczne zmieniające pierścienie
Ważne ogólne reakcje na tworzenie pierścieni
Istnieje wiele wyspecjalizowanych reakcji, których zastosowanie polega wyłącznie na tworzeniu pierścieni i zostaną one omówione poniżej. Oprócz tego istnieje szeroka gama ogólnych reakcji organicznych, które historycznie miały kluczowe znaczenie dla rozwoju, po pierwsze, zrozumienia koncepcji chemii pierścieni, a po drugie, niezawodnych procedur wytwarzania struktur pierścieniowych z wysoką wydajnością i ze zdefiniowaną orientacja podstawników pierścieniowych (tj. zdefiniowana stereochemia ). Te ogólne reakcje obejmują:
- kondensacja acyloiny ;
- Utleniania anodowe ; oraz
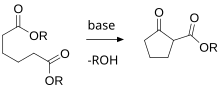
- kondensacji Dieckmann stosowanego do tworzenia pierścienia.
Reakcje zamknięcia pierścienia
W chemii organicznej różne syntetyczne procedury są szczególnie przydatne do zamykania pierścieni karbocyklicznych i innych; są to tak zwane reakcje zamykania pierścienia . Przykłady obejmują:
- trimeryzacja alkinów ;
- Bergman cyklizacja ;
- się reakcji Dielsa-Aldera i inne cykloaddycji niepożądane;
- cyklizacji Nazarov ;
- różne cyklizacje rodnikowe ;
- reakcje metatezy z zamknięciem pierścienia , które można również wykorzystać do osiągnięcia określonego typu polimeryzacji ;
- syntezy duży pierścień Ruzicka ; oraz
- Wenker syntezy z azyrydyny .
Reakcje otwarcia pierścienia
Różnorodne dalsze procedury syntetyczne są szczególnie przydatne w otwieraniu pierścieni karbocyklicznych i innych, na ogół zawierających podwójne wiązanie lub inną „obsługę” grupy funkcyjnej w celu ułatwienia chemii; są to tak zwane reakcje otwarcia pierścienia . Przykłady obejmują:
- metateza z otwarciem pierścienia , która może być również wykorzystana do osiągnięcia określonego typu polimeryzacji .
Reakcje rozszerzania i kurczenia pierścienia
Reakcje rozszerzania i kurczenia pierścieni są powszechne w syntezie organicznej i często spotykane w reakcjach okołocyklicznych . Rozszerzenia i skurcze pierścienia mogą obejmować wstawienie grupy funkcyjnej, tak jak w przypadku utleniania Baeyera-Villigera cyklicznych ketonów, przegrupowania cyklicznych karbocykli, jak widać w wewnątrzcząsteczkowych reakcjach Dielsa-Aldera lub załamanie lub przegrupowanie związków bicyklicznych jako kilka przykładów.
Zobacz też
Bibliografia
- ^ Marzec Jerry (1985), Zaawansowana chemia organiczna: reakcje, mechanizmy i struktura (3rd ed.), New York: Wiley, ISBN 0-471-85472-7
- ^ Halduc, I. (1961). „Klasyfikacja nieorganicznych związków cyklicznych”. Czasopismo Chemii Strukturalnej . 2 (3): 350-8. doi : 10.1007/BF01141802 . S2CID 93804259 .
- ^ Reymond, Jean-Louis (2015). "Projekt Chemicznej Kosmosu" . Rachunki z badań chemicznych . 48 (3): 722–30. doi : 10.1021/ar500432k . PMID 25687211 .
- ^ B c d e f g h William Reusch (2010). „Stereoizomery część I” w wirtualnym podręczniku chemii organicznej. Uniwersytet Stanowy Michigan . Źródło 7 kwietnia 2015 .
- ^ a b Nadal, W. Clark; Galynker, Igor (1981). „Chemiczne konsekwencje konformacji w związkach makrocyklicznych”. Czworościan . 37 (23): 3981-96. doi : 10.1016/S0040-4020(01)93273-9 .
-
^ B J.D. Dunitz (1968). JD Dunitz i JA Ibers (red.). Perspektywy w chemii strukturalnej . Tom. 2. Nowy Jork: Wiley. s. 1-70.
|volume=ma dodatkowy tekst ( pomoc ) - ^ Morris, Christopher G .; Prasa akademicka (1992). Akademicki Słownik Nauki i Techniki . Profesjonalne wydawnictwa z Zatoki Perskiej. P. 120. Numer ISBN 9780122004001.
- ^ Eliel, EL, Wilen, SH i Mander, LS ( 1994 ) Stereochemia związków organicznych, John Wiley and Sons, Inc., Nowy Jork.
- ^ Anet, FAL; św. Jakuba M.; Henrichsa, premiera; Cheng, AK; Krane, J.; Wong, L. (1974). „Analiza konformacyjna ketonów średniopierścieniowych”. Czworościan . 30 (12): 1629–37. doi : 10.1016/S0040-4020(01)90685-4 .
- ^ Löwe, J; Li, H; Downing, KH; Nogales, E (2001). „Wyrafinowana struktura αβ-tubuliny w rozdzielczości 3,5 Å” . Czasopismo Biologii Molekularnej . 313 (5): 1045–57. doi : 10.1006/jmbi.2001.5077 . PMID 11700061 .
Dalsza lektura
- Jürgen-Hinrich Fuhrhop & Gustav Penzlin, 1986, „Synteza organiczna: koncepcje, metody, materiały wyjściowe”, Weinheim, BW, DEU:VCH, ISBN 0895732467 , patrz [1] , dostęp 19 czerwca 2015.
- Michael B. Smith & Jerry marzec 2007, „March's Advanced Organic Chemistry: Reactions, Mechanisms and Structure”, wyd. 6, Nowy Jork, NY, USA: Wiley & Sons, ISBN 0470084944 , patrz [2] , dostęp 19 czerwca 2015.
- Francis A. Carey i Richard J. Sundberg, 2006, „Tytuł Zaawansowana Chemia Organiczna: Część A: Struktura i Mechanizmy”, wyd. 4, Nowy Jork, NY, USA: Springer Science & Business Media, ISBN 0306468565 , patrz [3] , dostęp 19 czerwca 2015 r.
- Michael B. Smith, 2011, „Organic Chemistry: An Acid-Base Approach”, Boca Raton, FL, USA: CRC Press, ISBN 1420079212 , patrz [4] , dostęp 19 czerwca 2015. [Może nie być najbardziej potrzebnym materiałem do tego artykuł, ale znacząca treść tutaj jest dostępna online.]
- Jonathan Clayden, Nick Greeves & Stuart Warren, 2012, „Chemia organiczna”, Oxford, Oxon, GBR: Oxford University Press, ISBN 0199270295 , patrz [5] , dostęp 19 czerwca 2015.
- László Kürti & Barbara Czakó, 2005, „Strategic Applications of Named Reactions in Organic Synthesis: Background and Detail Mechanisms, Amsterdam, NH, NLD: Elsevier Academic Press, 2005ISBN 0124297854, patrz [6] , dostęp 19 czerwca 2015 r.
Zewnętrzne linki
- Policykliczne + związki w amerykańskiej National Library of Medicine Medical Subject Headings (MeSH)
- Macrocyclic + Compounds w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)