Chlorek indu (III) - Indium(III) chloride
|
|
| Nazwy | |
|---|---|
| Inne nazwy
Chlorek
indu Trichlorek indu |
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChemSpider | |
| Karta informacyjna ECHA |
100.030.027 |
| Numer WE | |
|
PubChem CID
|
|
| Numer RTECS | |
| UNII | |
| Numer ONZ | 3260 |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| InCl 3 | |
| Masa cząsteczkowa | 221,18 g / mol |
| Wygląd | białe płatki |
| Gęstość | 3,46 g / cm 3 |
| Temperatura topnienia | 586 ° C (1087 ° F, 859 K) |
| Temperatura wrzenia | 800 ° C (1470 ° F; 1070 K) |
| 195 g / 100 ml, egzotermiczny | |
| Rozpuszczalność w innych rozpuszczalnikach | THF , etanol |
| Struktura | |
| Jednoskośny , MS16 | |
| C12 / m1, nr 12 | |
| Zagrożenia | |
| Główne zagrożenia | Żrący |
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna karta charakterystyki |
| Piktogramy GHS |
 
|
| Hasło ostrzegawcze GHS | Niebezpieczeństwo |
| H302 , H314 | |
| P260 , P303 + 361 + 353 , P305 + 351 + 338 , P301 + 330 + 331 , P405 , P501 | |
| NFPA 704 (ognisty diament) | |
| Związki pokrewne | |
|
Inne aniony
|
Fluorek indu (III) Bromek indu (III) Jodek indu (III) |
|
Inne kationy
|
Chlorek glinu Trichlorek galu Chlorek talu (III) |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Chlorek indu (III) jest związek chemiczny o wzorze W Cl 3 . Sól ta jest białym, płatkowatym ciałem stałym, mającym zastosowanie w syntezie organicznej jako kwas Lewisa . Jest również najlepiej dostępną rozpuszczalną pochodną indu.
Synteza i struktura
Będąc metalem stosunkowo elektrododatnim, ind szybko reaguje z chlorem, tworząc trichlorek. Trichlorek indu jest bardzo dobrze rozpuszczalny i rozpływający się. Opisano syntezę z użyciem ogniwa elektrochemicznego w mieszanym roztworze metanolu i benzenu .
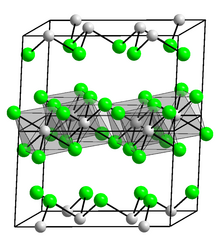
Jak AlCl 3 i TlCl 3 , w tym 3 krystalizuje w postaci struktury warstwowej składającej się z gęstego upakowania układu chlorek, zawierającego warstwy octahedrally skoordynowane W (III), Centers, struktura podobna do obserwowanej w YCL 3 . W przeciwieństwie do tego, GaCl 3 krystalizuje w postaci dimerów zawierających Ga 2 Cl 6 . Stopiony InCl 3 przewodzi prąd, podczas gdy AlCl 3 nie przekształca się w dimer molekularny Al 2 Cl 6 .
Reakcje
InCl 3 jest kwasem Lewisa i tworzy kompleksy z ligandami dawcy , L, InCl 3 L, InCl 3 L 2 , InCl 3 L 3 . Na przykład z jonem chlorkowym tworzy tetraedryczny InCl 4 - , trygonalny bipiramidalny InCl 5 2− i oktaedryczny InCl 6 3− .
W eterze dietylowym roztworze, w tym 3 reaguje z wodorek litowo , LiH, aby utworzyć . Ten niestabilny związek rozkłada się w temperaturze poniżej 0 ° C, poddaje się reakcji in situ, w syntezie organicznej, ponieważ środek redukujący i przygotowanie trzeciorzędowe aminy i fosfiny kompleksy INH 3 .
Trimetyloindium , InMe 3 , można wytworzyć w reakcji InCl 3 w roztworze eteru dietylowego albo z odczynnikiem Grignarda, albo z metylolitem , LiMe. Trietylindium można przygotować w podobny sposób, ale z odczynnikiem Grignarda EtMgBr.
InCl 3 reaguje z metalem indu w wysokiej temperaturze, tworząc chlorki indu o niższej wartościowości w 5 Cl 9 , In 2 Cl 3 i InCl.
Katalizator w chemii
Chlorek indu jest kwasowym katalizatorem Lewisa w reakcjach organicznych, takich jak acylowanie Friedela-Craftsa i reakcje Dielsa-Aldera . Jako przykład tego ostatniego, reakcja przebiega w temperaturze pokojowej , przy obciążeniu 1% molowym katalizatora w mieszaninie rozpuszczalników acetonitryl- woda. Pierwszym krokiem jest kondensacja Knoevenagela między kwasem barbiturowym i aldehydem; drugi etap jest odwrotna elektronów żądanie Dielsa-Aldera , która jest wieloskładnikowy reakcji z N, N'-dimetylo kwasu barbiturowego , benzaldehydu i octan winylu eter . W przypadku katalizatora, podana wydajność chemiczna wynosi 90%, a procent izomeru trans 70%. Bez dodanego katalizatora wydajność spada do 65% przy 50% produkcie trans.







