Siarczan potasu - Potassium sulfate
 Arcanite
|
|
|
|
| Nazwy | |
|---|---|
| Inne nazwy
Siarczan potasu
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Karta informacyjna ECHA |
100.029.013 |
| Numer E. | E515 (i) (regulatory kwasowości, ...) |
| KEGG | |
|
PubChem CID
|
|
| Numer RTECS | |
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| K 2 SO 4 | |
| Masa cząsteczkowa | 174,259 g / mol |
| Wygląd | Białe ciało stałe |
| Zapach | bezwonny |
| Gęstość | 2,66 g / cm 3 |
| Temperatura topnienia | 1069 ° C (1956 ° F; 1342 K) |
| Temperatura wrzenia | 1689 ° C (3072 ° K; 1962 K) |
| 111 g / l (20 ° C) 120 g / l (25 ° C) 240 g / l (100 ° C) |
|
| Rozpuszczalność | słabo rozpuszczalny w glicerolu nierozpuszczalny w acetonie , alkoholu , CS 2 |
| -67,0 · 10-6 cm 3 / mol | |
|
Współczynnik załamania ( n D )
|
1.495 |
| Struktura | |
| rombowy | |
| Zagrożenia | |
| Główne zagrożenia | Drażniący |
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna karta charakterystyki |
| Zwroty R (nieaktualne) | R22 |
| Zwroty S (nieaktualne) | S36 |
| Temperatura zapłonu | Nie palne |
| Dawka lub stężenie śmiertelne (LD, LC): | |
|
LD 50 ( mediana dawki )
|
6600 mg / kg (doustnie, szczur) |
| Związki pokrewne | |
|
Inne aniony
|
Potasu selenian potasu tellurate |
|
Inne kationy
|
Siarczan litu Siarczan sodu Siarczan rubidu Siarczan cezu |
|
Związki pokrewne
|
Wodorosiarczan potasu Siarczyn potasu Wodorosiarczyn potasu Nadsiarczan potasu |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referencje Infobox | |
Siarczan potasu (USA) lub siarczan potasu (Wielka Brytania), zwany także siarczanem potasu (SOP), arkanitem lub archaicznie potasem siarki , jest związkiem nieorganicznym o wzorze K 2 SO 4 , rozpuszczalnym w wodzie białym ciałem stałym. Jest powszechnie stosowany w nawozach , dostarczając zarówno potasu, jak i siarki .
Historia
Siarczan potasu (K 2 SO 4 ) jest znany od początku XIV wieku. Został zbadany przez Glaubera , Boyle'a i Tacheniusa. W XVII wieku nazwano go arcanuni lub sal duplicatum , ponieważ było to połączenie soli kwaśnej z solą alkaliczną . Był również znany jako witrioliczny kamień nazębny i sól Glasera lub sal polychrestum Glaseri od nazwiska chemika farmaceutycznego Christophera Glasera, który go przygotował i użył w medycynie.
Znany jako arcanum duplicatum ("double secret") lub panacea duplicata w medycynie przednowoczesnej , został przygotowany z pozostałości ( caput mortuum ) pozostałej po produkcji aqua fortis (kwas azotowy, HNO 3 ) z azotanu potasu, KNO 3 ) i olej witriolu (kwas siarkowy, H 2 SO 4 ) w procesie Glaubera :
- 2 KNO 3 + H 2 SO 4 → 2 HNO 3 + K 2 SO 4
Pozostałość rozpuszczono w gorącej wodzie, przesączono i odparowano do naskórka. Następnie pozostawiono do krystalizacji. Był stosowany jako środek moczopędny i potowy .
Według Chambersa Cyclopedia , przepis został zakupiony za pięćset talarów przez Karola Fryderyka, księcia Holstein-Gottorp . Schroder, lekarz księcia, napisał cuda o jego wielkich zastosowaniach w przypadkach hipochondrii , utrzymujących się i przejściowych gorączkach , kamieniach, szkorbut i nie tylko.
Zasoby naturalne
Forma mineralna siarczanu potasu, arkanitu , jest stosunkowo rzadka. Naturalne zasoby siarczanu potasu to minerały bogate w sól Stassfurt . Są to kokrystalizacje siarczanu potasu i siarczanów magnezu , wapnia i sodu .
Istotne minerały to:
- Kainit , KMg (SO 4 ) · Cl · 3H 2 O
- Schönit (obecnie znany jako pikromeryt), K 2 SO 4 · MgSO 4 · 6H 2 O
- Leonit , K 2 SO 4 · MgSO 4 · 4H 2 O
- Langbeinit , K 2 Mg 2 (SO 4 ) 3
- Aftitalit (wcześniej znany jako glaseryt), K 3 Na (SO 4 ) 2
- Polihalit , K 2 SO 4 · MgSO 4 · 2CaSO 4 · 2H 2 O
Siarczan potasu można oddzielić od niektórych z tych minerałów, takich jak kainit, ponieważ odpowiadająca mu sól jest słabiej rozpuszczalna w wodzie.
Kizeryt , MgSO 4 · H 2 O, można łączyć z roztworem chlorku potasu w celu wytworzenia siarczanu potasu.
Produkcja
Około 1,5 miliona ton wyprodukowano w 1985 roku, zwykle w reakcji chlorku potasu z kwasem siarkowym , analogicznie do procesu produkcji siarczanu sodu z Mannheima . Proces obejmuje pośrednie tworzenie się wodorosiarczanu potasu , egzotermiczną reakcję, która zachodzi w temperaturze pokojowej:
- KCl + H 2 SO 4 → HCl + KHSO 4
Drugi etap procesu jest endotermiczny i wymaga wkładu energii:
- KCl + KHSO 4 → HCl + K 2 SO 4
Struktura i właściwości
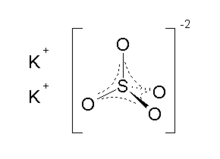
Znane są dwie formy krystaliczne. Rombowa β-K 2 SO 4 jest postacią powszechną, ale powyżej 583 ° C przekształca się w α-K 2 SO 4 . Struktury te są złożone, chociaż siarczan przyjmuje typową geometrię czworościenną.
W przeciwieństwie do siarczanu sodu nie tworzy hydratu . Sól krystalizuje jako podwójne sześcioboczne piramidy, klasyfikowane jako rombowe. Są przezroczyste, bardzo twarde i mają gorzki, słony smak. Sól jest rozpuszczalna w wodzie, ale nierozpuszczalna w roztworach wodorotlenku potasu ( sp. Gr. 1,35) lub w absolutnym etanolu .
Gdy siarczan potasu jest podgrzewany w wodzie i poddawany wirowaniu w zlewce, kryształy tworzą wieloramienną strukturę spiralną po pozostawieniu do osiadania.
Używa
Dominującym zastosowaniem siarczanu potasu jest nawóz . K 2 SO 4 nie zawiera chlorków, które mogą być szkodliwe dla niektórych upraw. Siarczan potasu jest preferowany dla tych upraw, które obejmują tytoń oraz niektóre owoce i warzywa. Uprawy, które są mniej wrażliwe, mogą nadal wymagać siarczanu potasu dla optymalnego wzrostu, jeśli gleba gromadzi chlorki z wody do nawadniania.
Sól surowa jest również sporadycznie wykorzystywana do produkcji szkła. Siarczan potasu jest również używany jako reduktor płomienia w ładunkach miotających artylerii . Redukuje błysk wylotowy , odblask i nadciśnienie podmuchowe.
Czasami jest używany jako alternatywny środek do piaskowania, podobny do sody w oczyszczaniu sodą, ponieważ jest twardszy i podobnie rozpuszczalny w wodzie.
Siarczan potasu może być również stosowany w pirotechnice w połączeniu z azotanem potasu w celu wytworzenia fioletowego płomienia .
Reakcje
Zakwaszenie
Wodorosiarczan potasu (znany również jako wodorosiarczan potasu), KHSO 4 , jest łatwo wytwarzany w reakcji K 2 SO 4 z kwasem siarkowym . Tworzy rombowe piramidy , które topią się w temperaturze 197 ° C (387 ° F). Rozpuszcza się w trzech częściach wody o temperaturze 0 ° C (32 ° F). Roztwór zachowuje się tak, jakby jego dwa kongenery , K 2 SO 4 i H 2 SO 4 , były obecne obok siebie niezwiązane; nadmiar etanolu wytrąca normalny siarczan (z niewielką ilością wodorosiarczanu) z pozostałym nadmiarem kwasu.
Zachowanie stopionej suchej soli jest podobne po podgrzaniu do kilkuset stopni; działa na krzemiany , tytaniany itp. w taki sam sposób, jak kwas siarkowy podgrzany powyżej swojej naturalnej temperatury wrzenia. Dlatego jest często stosowany w chemii analitycznej jako środek rozsadzający. Aby uzyskać informacje na temat innych soli zawierających siarczany, zobacz siarczan .



