Pseudorabie - Pseudorabies
| Suid alfaherpeswirus 1 | |
|---|---|
|
Klasyfikacja wirusów |
|
| (bez rankingu): | Wirus |
| Królestwo : | Duplodnaviria |
| Królestwo: | Heunggongvirae |
| Gromada: | Peploviricota |
| Klasa: | Herviviricetes |
| Zamówienie: | Herpesvirale |
| Rodzina: | Herpesviridae |
| Rodzaj: | Varicellowirus |
| Gatunek: |
Suid alfaherpeswirus 1
|
| Synonimy | |
|
|
Choroba Aujeszky'ego , w Stanach Zjednoczonych zwana wścieklizną rzekomą , jest chorobą wirusową świń, która ma charakter endemiczny w większości krajów świata. Jest to spowodowane przez Suid herpesvirus 1 (SuHV-1). Choroba Aujeszky'ego jest uważana za najważniejszą pod względem gospodarczym chorobę wirusową świń na obszarach, gdzie klasyczny pomór świń ( hog cholera ) został zwalczony. Inne ssaki , takie jak bydło , owce , kozy , koty , psy i szopy są również podatne. Choroba jest zwykle śmiertelna u tych gatunków zwierząt.
Badania nad SuHV-1 u świń są pionierem w zwalczaniu chorób zwierząt za pomocą genetycznie zmodyfikowanych szczepionek. SuHV-1 jest obecnie wykorzystywany w badaniach modelowych podstawowych procesów podczas litycznej infekcji herpeswirusem oraz do odkrywania molekularnych mechanizmów neurotropizmu herpeswirusa .
Historia
1902, A węgierski weterynarii , Aladár Aujeszky'ego wykazał nowe czynnika zakaźnego u psa, wołu, i kota, i pokazały, że przyczyną tej samej choroby u świń, królików . W kolejnych dziesięcioleciach zakażenie stwierdzono w kilku krajach europejskich, zwłaszcza u bydła, gdzie charakterystycznym objawem jest miejscowy intensywny świąd (swędzenie). A w Stanach Zjednoczonych uznano, że dobrze znana choroba bydła zwana „szalonym swędzeniem” jest w rzeczywistości chorobą Aujeszkyego.
Przegląd chorób
Wirus rozprzestrzenia się w ślinie i wydzielinie nosowej świń zakażonych drogą oddechową. Może również wystąpić aerozolizacja wirusa i przenoszenie przez formy . Wirus może potencjalnie przetrwać siedem godzin w wilgotnym powietrzu, a w wodzie studziennej do siedmiu godzin, w zielonej trawie, glebie i kale do dwóch dni, w zanieczyszczonej paszy do trzech dni, a w ściółka ze słomy do czterech dni.
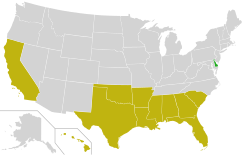
Diagnozę stawia się głównie poprzez izolację wirusa w kulturach tkankowych lub testy ELISA lub PCR. Dostępne są szczepionki dla świń ( kody ATCvet : QI09AA01 ( WHO ) inaktywowane, QI09AD01 ( WHO ) żywe, plus różne kombinacje). Zakażenie zostało wyeliminowane w wielu krajach europejskich. W Stanach Zjednoczonych populację świń domowych w 2004 r. uznano za wolną od choroby Aujeszky'ego, chociaż infekcja nadal występuje w populacjach zdziczałych świń.
Objawy kliniczne
Infekcja dróg oddechowych jest zwykle bezobjawowa u świń w wieku powyżej 2 miesięcy, ale może powodować poronienia, wysoką śmiertelność prosiąt, kaszel, kichanie, gorączkę, zaparcia, depresję, drgawki, ataksję , krążenie i nadmierne ślinienie się u prosiąt i dojrzałych świń. Śmiertelność prosiąt w wieku poniżej jednego miesiąca jest bliska 100%, ale jest mniejsza niż 10% u świń w wieku od jednego do sześciu miesięcy. Świnie w ciąży mogą wchłonąć swoje mioty lub rodzić zmumifikowane, martwo urodzone lub osłabione prosięta. U bydła (patrz następna sekcja) objawy obejmują intensywne swędzenie, po którym następują objawy neurologiczne i śmierć. U psów objawy obejmują intensywne swędzenie, porażenie szczęki i gardła , wycie i śmierć. Każdy zarażony żywiciel wtórny na ogół żyje tylko od dwóch do trzech dni.
Wydaje się, że infekcje narządów płciowych były powszechne przez większą część XX wieku w wielu krajach europejskich w stadach trzody chlewnej, gdzie knury z ośrodków knurowych były wykorzystywane do naturalnej obsługi loch lub loszek. Ta manifestacja choroby zawsze była bezobjawowa u zakażonych świń, a obecność infekcji na farmie została wykryta tylko z powodu przypadków u bydła wykazujących świąd na zadzie (infekcja pochwy, patrz poniżej).
U podatnych zwierząt innych niż świnie infekcja jest zwykle śmiertelna, a dotknięte nią zwierzęta najczęściej wykazują intensywny świąd w obszarze skóry. Świąd w chorobie Aujeszky'ego jest uważany za wrażenie fantomowe, ponieważ nigdy nie znaleziono wirusa w miejscu świądu.
Patogeniczność i zjadliwość SuHV-1
Epidemiologia choroby Aujeszkyego różni się w zależności od patogenności lub zjadliwości danego szczepu wirusa. Najlepiej ilustruje to rozwój ciężkości choroby w Danii, gdzie import świń był zakazany przez dziesięciolecia aż do 1972 roku. kraju, głównie przez handel zwierzętami. Pod koniec lat 70. rozwinęły się bardziej zjadliwe szczepy. Choroba u świń stała się znacznie poważniejsza, epidemie chorób układu oddechowego u bydła gwałtownie wzrosły, a infekcja rozprzestrzeniła się drogą powietrzną na inne stada świń. Wyższa zjadliwość tych szczepów wirusa była związana z pewną zdolnością do tworzenia syncytiów (fuzji komórek) w hodowlach tkankowych (syncytialne szczepy wirusa). Kompleksowe analizy wzorów fragmentów restrykcyjnych DNA wirusa udokumentowały, że bardziej zjadliwe szczepy nie zostały wprowadzone z zagranicy, ale rozwinęły się w dwóch etapach z oryginalnych duńskich szczepów. Korelację między wysoką zjadliwością szczepów wirusa a powstawaniem syncycjów w hodowlach tkankowych potwierdzono badaniami izolatów z innych krajów. Ten drugi krok w rozwoju ciężkości choroby w Danii spowodował decyzję o jej zwalczeniu. Wszystkie nowe epidemie po zwalczeniu rdzennej infekcji do końca 1985 r. były spowodowane przez obce, wysoce zjadliwe szczepy syncytium, wprowadzone drogą transmisyjną drogą powietrzną z Niemiec.
W skrócie, SuHV-1 rozprzestrzenia się drogą płciową lub drogą oddechową. Stwierdzono, że szczepy narządów płciowych są niesyncytalne. Szczepy oddechowe mogą mieć stosunkowo niską lub wysoką zjadliwość. W Europie stwierdzono, że szczepy syncytium są wysoce zjadliwe.
Epidemiologia
Populacje dzików lub zdziczałych świń ( Sus scrofa ) w USA powszechnie zarażają się wirusem i rozprzestrzeniają go na całym swoim zasięgu. Śmiertelność jest najwyższa u młodych prosiąt. Ciężarne lochy często przerywają po zakażeniu. W przeciwnym razie zdrowi dorośli mężczyźni (knury) są zazwyczaj utajonymi nosicielami, to znaczy, że są nosicielami i przenoszą wirusa bez oznak lub niepełnosprawności.
Świnie (zarówno domowe, jak i dzikie) są zwykłymi rezerwuarami tego wirusa, chociaż ma on wpływ na inne gatunki. Choroba Aujeszky'ego została zgłoszona u innych ssaków, w tym niedźwiedzi brunatnych i czarnych , panter florydzkich , szopów praczy , kojotów i jeleni białoogonowych. W większości przypadków kontakt ze świniami lub produktami wieprzowymi był znany lub podejrzewany. Ogniska gatunków futer hodowlanych w Europie ( norki i lisy ) są związane z karmieniem skażonymi produktami wieprzowymi. Wiele innych gatunków może zostać zarażonych eksperymentalnie. Ludzie nie są potencjalnymi gospodarzami.
Stwierdzono, że bydło jest zakażone drogą oddechową lub pochwową ( pominięto przypadki jatrogenne ). Pierwotne zakażenie błon śluzowych górnych dróg oddechowych wiąże się ze świądem głowy, natomiast zakażenie płuc prowadzi do świądu klatki piersiowej. Stwierdzono, że zakażenie pochwy bydła, które regularnie wykazuje świąd tylnych kończyn, jest związane z równoczesnym zakażeniem narządów płciowych u świń na tym samym terenie, a badania wykazały, że zakażenie pochwy bydła było przenoszone drogą płciową przez człowieka z zakażonych macior . Zakażenie narządów płciowych w stadach świń jest ściśle skorelowane z wykorzystaniem knurów z ośrodków knurowych do naturalnej obsługi loch.
Przenoszenie
Choroba Aujeszkyego jest wysoce zaraźliwa. Powszechnie uważa się, że infekcja przenosi się między świniami poprzez kontakt nos-nos, ponieważ wirus występuje głównie w okolicach nosa i jamy ustnej. Temu poglądowi przeczą jednak wyniki badań epidemiologicznych, według których decydujące rozprzestrzenienie się w stadach następuje przez wielometrowe prądy powietrza. W związku z tym stwierdzono, że ryzyko przeniesienia wysoce zjadliwych szczepów wirusa drogą powietrzną z ostro zakażonych stad do innych stad świń jest bardzo wysokie. Stwierdzono, że zakażenie przenoszone jest na odległość wielu kilometrów. W przeciwnym razie infekcja jest najczęściej przenoszona na stada przez wprowadzenie świń zarażonych ostro lub latentnie. Odnośnie przenoszenia na bydło, patrz sekcja powyżej.
Zapobieganie
Chociaż nie jest dostępne żadne specyficzne leczenie ostrego zakażenia SuHV-1, szczepienie może złagodzić objawy kliniczne u świń w określonym wieku. Zazwyczaj zaleca się masowe szczepienie wszystkich świń w gospodarstwie zmodyfikowaną szczepionką z żywym wirusem. Donosowe szczepienie loch i nowonarodzonych prosiąt w wieku od jednego do siedmiu dni, a następnie szczepienie domięśniowe (IM) wszystkich innych świń na terenie obiektu, pomaga zmniejszyć wydalanie wirusa i poprawić przeżywalność. Zmodyfikowany żywy wirus replikuje się w miejscu wstrzyknięcia iw regionalnych węzłach chłonnych. Wirus szczepionkowy jest wydalany w tak niskich ilościach, że przenoszenie śluzu na inne zwierzęta jest minimalne. W szczepionkach z delecją genową usunięto również gen kinazy tymidynowej; w ten sposób wirus nie może infekować i replikować się w neuronach. Stada hodowlane zaleca się szczepić co kwartał, a tuczniki powinny być szczepione po zmniejszeniu poziomu przeciwciał matczynych. Regularne szczepienia zapewniają doskonałą kontrolę choroby. W celu zwalczania wtórnych patogenów bakteryjnych zaleca się równoczesną antybiotykoterapię w postaci paszy i iniekcji domięśniowej.
Zastosowania w neuronauce
SuHV-1 może być wykorzystywany do analizy obwodów nerwowych w ośrodkowym układzie nerwowym (OUN). W tym celu atenuowany (mniej zjadliwy) szczep Bartha SuHV-1 jest powszechnie stosowany i jest wykorzystywany jako transneuronalny znacznik wsteczny i wsteczny . W kierunku wstecznym, SuHV-1-Bartha jest transportowany do ciała komórki neuronalnej poprzez swój akson, gdzie ulega replikacji i dyspersji w cytoplazmie i drzewie dendrytycznym. SuHV-1-Bartha uwalniany przez synapsę jest w stanie przejść przez synapsę, aby zainfekować zakończenia aksonów synaptycznie połączonych neuronów, tym samym propagując wirusa; jednak zakres, w jakim może również wystąpić niesynaptyczny transport transneuronalny, jest niepewny. Stosując badania czasowe i/lub genetycznie zmodyfikowane szczepy SuHV-1-Bartha, można zidentyfikować neurony drugiego, trzeciego i wyższego rzędu w sieci neuronowej będącej przedmiotem zainteresowania.
