Wydzielina - Secretion
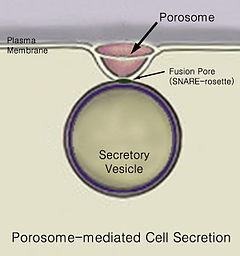
Wydzielanie to przemieszczanie się materiału z jednego punktu do drugiego, np. substancji chemicznej wydzielanej z komórki lub gruczołu . Natomiast wydalanie to usuwanie pewnych substancji lub produktów odpadowych z komórki lub organizmu. Klasyczny mechanizm sekrecji komórkowej odbywa się poprzez portale wydzielnicze w błonie komórkowej komórek zwane porosomami . Porosomy są trwałą strukturą lipoproteinową w kształcie miseczki w błonie komórkowej komórki, w której pęcherzyki wydzielnicze przejściowo łączą się i łączą, aby uwolnić wewnątrzpęcherzykową zawartość z komórki.
Wydzielanie w gatunkach bakterii oznacza transport lub translokację cząsteczek efektorowych, na przykład: białek , enzymów lub toksyn (takich jak toksyna cholery w bakteriach chorobotwórczych, na przykład Vibrio cholerae ) z wnętrza ( cytoplazmy lub cytozolu ) komórki bakteryjnej na jej zewnątrz. Wydzielanie jest bardzo ważnym mechanizmem w funkcjonowaniu i działaniu bakterii w ich naturalnym środowisku dla adaptacji i przetrwania.
W komórkach eukariotycznych
Mechanizm
Eukariotycznych komórek , w tym komórek ludzkich , mają bardzo rozwiniętą proces wydzielania. Białka skierowane na zewnątrz są syntetyzowane przez rybosomy podłączone do szorstkiej retikulum endoplazmatycznego (ER). Podczas syntezy białka te przemieszczają się do światła ER , gdzie są glikozylowane i gdzie białka opiekuńcze wspomagają fałdowanie białek . Nieprawidłowo sfałdowane białka są zwykle tutaj identyfikowane i podlegają retrotranslokacji przez degradację związaną z ER do cytozolu , gdzie są degradowane przez proteasom . Te pęcherzyki zawierające odpowiednio złożone białka, a następnie wprowadzić do aparatu Golgiego .
W aparacie Golgiego glikozylacja białek jest modyfikowana i mogą wystąpić dalsze modyfikacje potranslacyjne , w tym rozszczepienie i funkcjonalizacja. Te białka są następnie przemieszczane do pęcherzyków wydzielniczych, które przemieszczają się wzdłuż cytoszkieletu na krawędzi komórki. Więcej modyfikacji może nastąpić w pęcherzykach wydzielniczych (na przykład insulina jest odcinana od proinsuliny w pęcherzykach wydzielniczych).
Ostatecznie dochodzi do fuzji pęcherzyków z błoną komórkową w strukturze zwanej porosomem , w procesie zwanym egzocytozą , wyrzucającym jego zawartość z otoczenia komórki.
Utrzymuje się ścisłą kontrolę biochemiczną nad tą sekwencją stosując gradient pH : pH cytozolu wynosi 7,4, pH ER wynosi 7,0, a cis-golgi ma pH 6,5. Pęcherzyki wydzielnicze mają pH w zakresie od 5,0 do 6,0; niektóre pęcherzyki wydzielnicze ewoluują w lizosomy o pH 4,8.
Wydzielina nieklasyczna
Istnieje wiele białek, takich jak FGF1 (aFGF), FGF2 (bFGF), interleukina-1 (IL1) itp., które nie mają sekwencji sygnałowej. Nie używają klasycznej ścieżki ER-Golgi. Są one wydzielane różnymi nieklasycznymi szlakami.
Opisano co najmniej cztery nieklasyczne (niekonwencjonalne) szlaki sekrecji białek. Obejmują one 1) bezpośrednią translokację białek przez błonę plazmatyczną prawdopodobnie przez transportery błonowe, 2) tworzenie się pęcherzyków , 3) sekrecję lizosomalną i 4) uwalnianie przez egzosomy pochodzące z ciał wielopęcherzykowych. Ponadto białka mogą być uwalniane z komórek przez mechaniczne lub fizjologiczne zranienie oraz przez nie powodujące śmierci, przemijające pory onkotyczne w błonie plazmatycznej indukowane przez przemycie komórek pożywką lub buforami bez surowicy.
W tkankach ludzkich
Wiele typów ludzkich komórek ma zdolność bycia komórkami wydzielniczymi. Mają dobrze rozwiniętą retikulum endoplazmatyczne , a do pełnienia tej funkcji aparat Golgiego . Tkanki wytwarzające wydzieliny obejmują przewód pokarmowy wydzielający enzymy trawienne i kwas żołądkowy , płuca wydzielające środki powierzchniowo czynne oraz gruczoły łojowe wydzielające łój w celu nawilżenia skóry i włosów. Gruczoły Meiboma w powiece wydzielają meibum, aby nawilżyć i chronić oko.
W bakteriach Gram-ujemnych
Wydzielina nie jest unikalna dla eukariontów – występuje również w bakteriach i archeonach. Transportery typu kasety wiążącej ATP (ABC) są wspólne dla trzech domen życia. Niektóre wydzielane białka są translokowane przez błonę cytoplazmatyczną przez translokon SecYEG , jeden z dwóch systemów translokacji, który wymaga obecności N-końcowego peptydu sygnałowego na wydzielanym białku. Inne są translokowane przez błonę cytoplazmatyczną przez szlak translokacji bliźniaczej argininy (Tat). Bakterie Gram-ujemne mają dwie błony, co sprawia, że sekrecja jest bardziej złożona topologicznie. W bakteriach Gram-ujemnych istnieje co najmniej sześć wyspecjalizowanych systemów wydzielniczych. Wiele białek sekrecyjnych ma szczególne znaczenie w patogenezie bakterii.
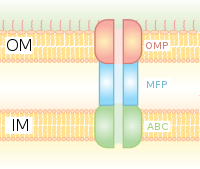
System wydzielniczy typu I (T1SS lub TOSS)
Wydzielanie typu I jest systemem wydzielniczym zależnym od białek opiekuńczych, wykorzystującym klastry genów Hly i Tol. Proces rozpoczyna się, gdy sekwencja liderowa białka, które ma być wydzielane, jest rozpoznawana przez HlyA i wiąże HlyB na błonie. Ta sekwencja sygnałowa jest wyjątkowo specyficzna dla transportera ABC. Kompleks HlyAB stymuluje HlyD, który zaczyna się rozwijać i dociera do błony zewnętrznej, gdzie TolC rozpoznaje cząsteczkę końcową lub sygnał na HlyD. HlyD rekrutuje TolC do błony wewnętrznej, a HlyA jest wydalany na zewnątrz błony zewnętrznej przez kanał białkowy o długim tunelu.
Układ wydzielniczy typu I transportuje różne cząsteczki, od jonów, leków, po białka o różnej wielkości (20 – 900 kDa). Wydzielane cząsteczki różnią się wielkością od małej kolicyny V z peptydu Escherichia coli (10 kDa) do białka adhezyjnego komórek Pseudomonas fluorescens LapA o masie 520 kDa. Najlepiej scharakteryzowane są toksyny RTX i lipazy. Wydzielanie typu I bierze również udział w eksporcie substratów niebiałkowych, takich jak cykliczne β-glukany i polisacharydy.
System wydzielniczy typu II (T2SS)
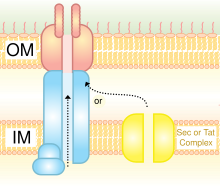
Białka wydzielane przez system typu II lub główną końcową gałąź ogólnego szlaku sekrecyjnego zależą od systemu Sec lub Tat dla początkowego transportu do peryplazmy . Tam przechodzą przez błonę zewnętrzną przez multimeryczny (12-14 podjednostek) kompleks białek sekretyny tworzących pory. Oprócz białka sekretyny na cały aparat sekrecyjny składa się 10–15 innych białek błony wewnętrznej i zewnętrznej, z których wiele ma jeszcze nieznaną funkcję. Pilusy Gram-ujemne typu IV wykorzystują zmodyfikowaną wersję systemu typu II do ich biogenezy, aw niektórych przypadkach pewne białka są wspólne dla kompleksu pilusa i systemu typu II w obrębie jednego gatunku bakterii.
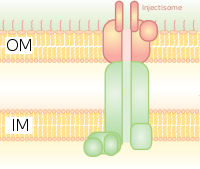
System wydzielniczy typu III (T3SS lub TTSS)
Jest homologiczny z ciałem podstawowym w wiciach bakteryjnych. Jest jak molekularna strzykawka, za pomocą której bakteria (np. niektóre typy Salmonella , Shigella , Yersinia , Vibrio ) może wstrzykiwać białka do komórek eukariotycznych. Niskie stężenie Ca 2+ w cytozolu otwiera bramkę regulującą T3SS. Jeden z takich mechanizmów wykrywania niskiego stężenia wapnia został zilustrowany przez antygen lcrV (Low Calcium Response) wykorzystywany przez Yersinia pestis , który jest stosowany do wykrywania niskich stężeń wapnia i wywołuje przyłączanie T3SS. System Hrp w patogenach roślinnych wstrzykuje do roślin harpiny i białka efektorowe patogenów poprzez podobne mechanizmy. Ten system wydzielniczy został po raz pierwszy odkryty w Yersinia pestis i wykazał, że toksyny można wstrzykiwać bezpośrednio z cytoplazmy bakteryjnej do cytoplazmy komórek gospodarza, a nie po prostu wydzielać do środowiska zewnątrzkomórkowego.
System wydzielniczy typu IV (T4SS lub TFSS)
| T4SS | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 System wydzielniczy typu IV
| |||||||||
| Identyfikatory | |||||||||
| Symbol | T4SS | ||||||||
| Pfam | PF07996 | ||||||||
| InterPro | IPR012991 | ||||||||
| SCOP2 | 1gl7 / zakres / SUPFAM | ||||||||
| TCDB | 3.A.7 | ||||||||
| Nadrodzina OPM | 215 | ||||||||
| Białko OPM | 3jqo | ||||||||
| |||||||||
Jest homologiczny do maszynerii koniugacji bakterii, koniugacyjnych pilusów . Jest zdolny do transportu zarówno DNA, jak i białek. Została odkryta w Agrobacterium tumefaciens , która wykorzystuje ten system do wprowadzenia części T-DNA plazmidu Ti do rośliny żywiciela, co z kolei powoduje, że zaatakowany obszar rozwija się w galas koronowy (guz). Helicobacter pylori wykorzystuje system wydzielniczy typu IV do dostarczania CagA do komórek nabłonka żołądka, co jest związane z karcynogenezą żołądka. Bordetella pertussis , czynnik wywołujący krztusiec, częściowo wydziela toksynę krztuśca przez układ typu IV. Legionella pneumophila , czynnik powodujący legionelozy (legionellozie) wykorzystuje układ wydzielniczy IVB , znany jako icm / kropki ( I Ntra C ellular m ultiplication / d efect w O rganelle t rafficking geny) systemem, translokacji liczne białka efektorowe do swojego eukariotycznego gospodarza. Prototypowym układem wydzielniczym typu IVA jest kompleks VirB Agrobacterium tumefaciens .
Członkowie białek z tej rodziny są składnikami układu wydzielniczego typu IV. Pośredniczą w wewnątrzkomórkowym przenoszeniu makrocząsteczek w mechanizmie rodowo podobnym do mechanizmu koniugacji bakterii .
Funkcjonować
W skrócie, system sekrecyjny typu IV (T4SS) to ogólny mechanizm, dzięki któremu komórki bakteryjne wydzielają lub pobierają makrocząsteczki. Ich dokładny mechanizm pozostaje nieznany. T4SS jest kodowany na Gram-ujemnych elementach skoniugowanych bakterii. T4SS to kompleksy obejmujące otoczkę komórkową lub innymi słowy 11–13 białek rdzeniowych, które tworzą kanał, przez który DNA i białka mogą przemieszczać się z cytoplazmy komórki dawcy do cytoplazmy komórki dawcy. komórka odbiorcy. Dodatkowo T4SS wydziela również białka czynnika wirulencji bezpośrednio do komórek gospodarza, a także pobiera DNA z pożywki podczas naturalnej transformacji , co świadczy o wszechstronności tego makromolekularnego aparatu sekrecyjnego.
Struktura
Jak pokazano na powyższym rysunku, TraC składa się w szczególności z wiązki trzech helis i luźnego wyrostka kulistego.
Interakcje
T4SS ma dwa białka efektorowe: po pierwsze ATS-1, co oznacza translokowany substrat 1 Anaplasma, a po drugie AnkA , co oznacza białko A zawierające domenę powtórzeń ankirynowych. Dodatkowo białka sprzęgające T4SS to VirD4, które wiążą się z VirE2.
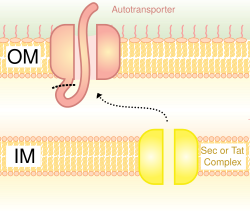
System wydzielniczy typu V (T5SS)
Nazywany również systemem autotransportera, sekrecja typu V polega na wykorzystaniu systemu Sec do przejścia przez błonę wewnętrzną. Białka korzystające z tego szlaku mają zdolność tworzenia beczki beta z końcem C, która wstawia się do błony zewnętrznej, umożliwiając reszcie peptydu (domenie pasażera) dotarcie na zewnątrz komórki. Często autotransportery są rozszczepiane, pozostawiając domenę beta-beczki w błonie zewnętrznej i uwalniając domenę pasażera. Niektórzy badacze uważają, że pozostałości autotransporterów dały początek porynom, które tworzą podobne struktury beta-beczki. Typowym przykładem autotransportera, który wykorzystuje ten system wydzielania jest Trimeric Autotransporter Adhesins .
System wydzielniczy typu VI (T6SS)
Systemy wydzielnicze typu VI zostały pierwotnie zidentyfikowane w 2006 roku przez grupę Johna Mekalanosa z Harvard Medical School (Boston, USA) w dwóch patogenach bakteryjnych, Vibrio cholerae i Pseudomonas aeruginosa . Zostały one zidentyfikowane, gdy mutacje w genach Hcp i VrgG w Vibrio Cholerae doprowadziły do zmniejszenia zjadliwości i patogenności. Od tego czasu układy wydzielnicze typu VI wykryto w jednej czwartej wszystkich genomów proteobakteryjnych, w tym w patogenach zwierzęcych, roślinnych, ludzkich, a także w bakteriach glebowych, środowiskowych i morskich. Podczas gdy większość wczesnych badań wydzielania typu VI skupiała się na jego roli w patogenezie organizmów wyższych, nowsze badania sugerowały szerszą fizjologiczną rolę w obronie przed prostymi drapieżnikami eukariotycznymi i jego rolę w interakcjach międzybakteryjnych. Klastry genów układu wydzielniczego typu VI zawierają od 15 do ponad 20 genów, z których dwa, Hcp i VgrG, okazały się prawie powszechnie wydzielanymi substratami układu. Analiza strukturalna tych i innych białek w tym systemie wykazuje uderzające podobieństwo do kolca ogonowego faga T4 i uważa się, że aktywność systemu funkcjonalnie przypomina infekcję faga.
Uwalnianie pęcherzyków błony zewnętrznej
Oprócz zastosowania wymienionych powyżej kompleksów wielobiałkowych, bakterie Gram-ujemne posiadają inną metodę uwalniania materiału: tworzenie pęcherzyków błony zewnętrznej bakterii . Części błony zewnętrznej ściskają się, tworząc nanoskalowe sferyczne struktury wykonane z bogatej w lipopolisacharydy dwuwarstwy lipidowej zawierającej materiały peryplazmatyczne i są wykorzystywane do przemieszczania pęcherzyków błonowych w celu manipulowania środowiskiem lub inwazji na styku gospodarz-patogen . Stwierdzono, że pęcherzyki wielu gatunków bakterii zawierają czynniki wirulencji, niektóre mają działanie immunomodulujące, a niektóre mogą bezpośrednio przylegać i odurzać komórki gospodarza. wykazano, że uwalnianie pęcherzyków jest ogólną odpowiedzią na warunki stresowe, proces ładowania białek ładunkowych wydaje się być selektywny.
Wydzielina w bakteriach Gram-dodatnich
W przypadku niektórych gatunków Staphylococcus i Streptococcus dodatkowy układ wydzielniczy obsługuje eksport wysoce powtarzalnych glikoprotein adhezyjnych.
Zobacz też
- Bakteryjne białko efektorowe
- Bakteryjne pęcherzyki błony zewnętrznej
- Interfejs gospodarz-patogen
- Handel pęcherzykami błonowymi
- Secretomics
- Białka sekrecyjne
- Stan wydawcy
Bibliografia
Dalsza lektura
- Alberts B, Johnson A, Lewis J, Raff M, Roberts K, Walter P, wyd. (2002). „Szukaj: Wydzielanie” . Biologia molekularna komórki (4 wyd.). Nowy Jork: Garland Science. Numer ISBN 978-0-8153-3218-3.
- Białe D (2000). Fizjologia i biochemia prokariontów (wyd. 2). Oxford University Press. Numer ISBN 978-0-19-512579-5.
- Avon D. "Strona główna" . Komórki żyją! .
Zewnętrzne linki
- Wydzieliny w Narodowej Bibliotece Medycyny USA Medical Subject Headings (MeSH)
- T5SS / ilustracja autotransportera w Uni Münster