Współczynnik transkrypcji II H - Transcription factor II H
| ogólny czynnik transkrypcyjny IIH, polipeptyd 1, 62 kDa | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | GTF2H1 | ||||||
| Alt. symbolika | BTF2 | ||||||
| Gen NCBI | 2965 | ||||||
| HGNC | 4655 | ||||||
| OMIM | 189972 | ||||||
| RefSeq | NM_005316 | ||||||
| UniProt | P32780 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 11 p15.1-p14 | ||||||
| |||||||
| ogólny czynnik transkrypcyjny IIH, polipeptyd 2, 44kDa | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | GTF2H2 | ||||||
| Alt. symbolika | BTF2, TFIIH, BTF2P44, T-BTF2P44 | ||||||
| Gen NCBI | 2966 | ||||||
| HGNC | 4656 | ||||||
| OMIM | 601748 | ||||||
| RefSeq | NM_001515 | ||||||
| UniProt | Q13888 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 5 q12.2-13.3 | ||||||
| |||||||
| ogólny czynnik transkrypcyjny IIH, polipeptyd 3, 34 kDa | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | GTF2H3 | ||||||
| Alt. symbolika | BTF2, TFIIH | ||||||
| Gen NCBI | 2967 | ||||||
| HGNC | 4657 | ||||||
| OMIM | 601750 | ||||||
| RefSeq | NM_001516 | ||||||
| UniProt | Q13889 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 12 kwartałów 24.31 | ||||||
| |||||||
Ludzki czynnik transkrypcyjny II ( czynnik transkrypcyjny II H ; TFIIH ) jest ważnym kompleksem białkowym , odgrywającym rolę w transkrypcji różnych genów kodujących białka i szlakach naprawy DNA poprzez wycinanie nukleotydów (NER). TFIIH po raz pierwszy ujrzał światło dzienne w 1989 roku, kiedy ogólny czynnik transkrypcyjny-δ lub podstawowy czynnik transkrypcyjny 2 został scharakteryzowany jako niezbędny czynnik transkrypcyjny in vitro. Ten czynnik został również wyizolowany z drożdży i ostatecznie nazwany jako TFIIH w 1992 roku.
TFIIH składa się z dziesięciu podjednostek, z których 7 ( ERCC2 /XPD, ERCC3 /XPB, GTF2H1 / p62 , GTF2H4 /p52, GTF2H2 /p44, GTF2H3 /p34 i GTF2H5 /TTDA) tworzą rdzeń. Subkompleks kinazy aktywującej cyklinę ( CDK7 , MAT1 i cyklina H) jest połączony z rdzeniem przez białko XPD. Dwie z podjednostek, ERCC2 /XPD i ERCC3/ XPB , wykazują aktywność helikazy i ATPazy i pomagają w tworzeniu bańki transkrypcyjnej . W probówce te podjednostki są wymagane do transkrypcji tylko wtedy, gdy matryca DNA nie została jeszcze zdenaturowana lub jest superskręcona .
Dwie inne podjednostki TFIIH , CDK7 i cyklina H , fosforylują aminokwasy seryny na C-końcowej domenie polimerazy II RNA i prawdopodobnie inne białka biorące udział w cyklu komórkowym . Oprócz istotnej funkcji w inicjacji transkrypcji, TFIIH bierze również udział w naprawie przez wycinanie nukleotydów .
Historia TFIIH
Zanim TFIIH go zidentyfikował, miał kilka nazw: ten czynnik po raz pierwszy w 1989 wyizolowany z wątroby szczura znany wówczas jako czynnik transkrypcyjny delta to także, wyizolowany z komórki rakowej znanej wówczas jako podstawowy czynnik transkrypcyjny 2, również wyizolowany z drożdży znany czynnik transkrypcyjny B. Wreszcie w 1992 roku znany jako TFIIH.
Struktura TFIIH
TFIIH to złożony z dziesięciu podjednostek; siedem z tych podjednostek stanowi „rdzeń”, podczas gdy trzy zawierają dysocjowalny moduł „CAK” (CDK Activating Kinase). Rdzeń składa się z podjednostek XPB, XPD, p62 , p52 , p44, p34 i p8, podczas gdy CAK składa się z CDK7 , cykliny H i MAT1 .
Funkcje
Ogólna funkcja TFIIH:
- Inicjacja transkrypcji genu kodującego białko.
- Naprawa nukleotydów DNA.
(NER)TFIIH jest ogólnym czynnikiem transkrypcyjnym, który rekrutuje RNA Pol II do promotorów genów. Działa jak helikaza, która rozwija DNA. Odwija również DNA po rozpoznaniu uszkodzenia DNA przez szlak globalnej naprawy genomu (GGR) lub szlak naprawy sprzężonej z transkrypcją (TCR) NER. Oczyszczony TFIIH odgrywa rolę w zatrzymaniu dalszej syntezy RNA poprzez aktywację enzymu a-amanityny.
Trichotiodystrofia
Mutacja w genach ERCC3 / XPB , ERCC2 / XPD lub TTDA przyczyną trichotiodystrofia , stan charakteryzujący się nadwrażliwości , rybia łuska , łamliwych włosów i paznokci, upośledzeniem umysłowym, zmniejszenie płodności i / lub niskiego wzrostu.
Choroba
Wiadomo, że polimorfizmy genetyczne genów kodujących podjednostki TFIIH są związane ze zwiększoną podatnością na raka w wielu tkankach, np.; tkanka skóry, tkanka piersi i tkanka płuc. Mutacje w podjednostkach (takich jak XPD i XPB) mogą prowadzić do różnych chorób, w tym xeroderma pigmentosum (XP) lub XP w połączeniu z zespołem Cockayne'a . Oprócz zmian genetycznych, białka kodowane przez wirusy są również skierowane na TFIIH.
Naprawa DNA
TFIIH uczestniczy w naprawie przez wycinanie nukleotydów (NER) poprzez otwarcie podwójnej helisy DNA po początkowym rozpoznaniu uszkodzenia. NER to wieloetapowa ścieżka, która usuwa szeroki zakres różnych uszkodzeń, które zniekształcają normalne parowanie zasad, w tym duże uszkodzenia chemiczne i uszkodzenia wywołane promieniowaniem UV. Osoby z defektami mutacji w genach określających składniki białkowe, które katalizują szlak NER, w tym składniki TFIIH, często wykazują cechy przedwczesnego starzenia (patrz teoria starzenia się uszkodzeń DNA ).
Inhibitory
Ostatnio doniesiono, że silne, bioaktywne produkty naturalne, takie jak tryptolid, które hamują transkrypcję ssaków poprzez hamowanie podjednostki XPB ogólnego czynnika transkrypcyjnego TFIIH, stanowią koniugat glukozy do celowania w niedotlenione komórki rakowe ze zwiększoną ekspresją transportera glukozy.
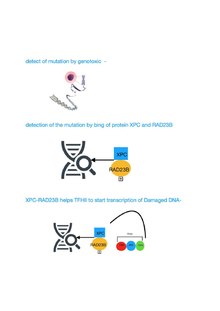
Mechanizm naprawy uszkodzonej sekwencji DNA przez TFIIH
Bibliografia
Zewnętrzne linki
- Transkrypcja + czynnik + TFIIH w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)