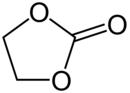
Węglan etylenu - Ethylene carbonate
|
|
|||
| Nazwy | |||
|---|---|---|---|
|
Preferowana nazwa IUPAC
1,3-dioksolan-2-on |
|||
| Inne nazwy
węglan glikolu etylenowego
|
|||
| Identyfikatory | |||
|
Model 3D ( JSmol )
|
|||
| ChemSpider | |||
| Karta informacyjna ECHA |
100.002.283 |
||
|
Identyfikator klienta PubChem
|
|||
| UNII | |||
|
Pulpit nawigacyjny CompTox ( EPA )
|
|||
|
|||
|
|||
| Nieruchomości | |||
| C 3 H 4 O 3 | |||
| Masa cząsteczkowa | 88,062 g·mol -1 | ||
| Wygląd zewnętrzny | Ciało stałe o barwie białej do żółtej | ||
| Gęstość | 1,3210 g / cm 3 | ||
| Temperatura topnienia | 34 do 37 ° C (93 do 99 ° F; 307 do 310 K) | ||
| Temperatura wrzenia | 243,0 °C (469,4 °F; 516,1 K) | ||
| Rozpuszczalny | |||
| Zagrożenia | |||
| Arkusz danych dotyczących bezpieczeństwa | Zewnętrzna Karta Charakterystyki | ||
|
Klasyfikacja UE (DSD) (nieaktualna)
|
Drażniący ( XI ) | ||
| Zwroty R (nieaktualne) | R41 | ||
| Zwroty S (nieaktualne) | S26 S39 | ||
| Temperatura zapłonu | 150 ° C (302 ° F; 423 K) | ||
| 465 ° C (869 ° F; 738 K) | |||
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|||
|
|
|||
| Referencje do infoboksu | |||
Węglan etylenu (czasami skrótem EC ) jest związkiem organicznym o wzorze (CH 2 O) 2 CO. Jest ona klasyfikowana jako cykliczny ester węglanowy z glikolu etylenowego i kwasu węglowego . W temperaturze pokojowej (25°C) węglan etylenu jest przezroczystym, krystalicznym ciałem stałym, praktycznie bezwonny i bezbarwny, w pewnym stopniu rozpuszczalny w wodzie. W stanie ciekłym (tt 34-37°C) jest to bezbarwna, bezwonna ciecz.
Produkcja i reakcje
Węglan etylenu wytwarza się w reakcji tlenku etylenu i dwutlenku węgla . Reakcja jest katalizowana przez różne kationy i kompleksy:
- (CH 2 ) 2 O + CO 2 → (CH 2 O) 2 CO
W laboratorium węglan etylenu można również wytworzyć w reakcji mocznika i glikolu etylenowego przy użyciu tlenku cynku jako katalizatora w temperaturze 150°C i pod ciśnieniem 3 kPa:
- (NH 2 ) 2 CO + HO-CH 2 CH 2 - OH → (CH 2 O) 2 CO + 2 NH 3
Węglan etylenu (i węglan propylenu ) może być przekształcony do węglanu dimetylu (przydatnego rozpuszczalnika, z łagodnym środkiem metylującym ) poprzez transestryfikację w metanolu :
- C 2 H 4 CO 3 + 2 CH 3 OH → CH 3 OCO 2 CH 3 + HOC 2 H 4 OH
Węglan dimetylu można również wytworzyć poprzez transestryfikację węglanu etylenu i metanolu, katalizowaną przez materiały grafitowego azotku węgla (gC 3 N 4) o dużej powierzchni (termicznie eksfoliowany) . Ta metoda zmniejsza ryzyko zanieczyszczenia metalem lub halogenkiem i może zapewnić wydajność do 60% w temperaturze 393 K.
Węglan dimetylu sam może być podobnie transestryfikowany do węglanu difenylu , substytut fosgenu :
- CH 3 OCO 2 CH 3 + 2 PhOH → PhOCO 2 Ph + 2 MeOH
Aplikacje
Węglan etylenu jest stosowany jako rozpuszczalnik polarny o cząsteczkowym momencie dipolowym 4,9 D , tylko o 0,1 D niższym niż węglan propylenu .
Może być stosowany jako składnik elektrolitów o wysokiej przenikalności elektrycznej w bateriach litowych i litowo-jonowych . Inne składniki, takie jak węglan dietylu, węglan etylu metylu, węglan dimetylu i octan metylu można dodawać do tych elektrolitów w celu zmniejszenia lepkości i temperatury topnienia .
Typowy akumulator sodowy z interkalacją wykorzystuje elektrolit składający się z: węglanu fluoroetylenu (FEC) (99%), metalicznego Na (99,9%) i 1,0 M roztworów nadchloranu sodu (NaClO4) w węglanie etylenu i węglanie dietylu (EC/DEC) , klasa baterii 1:1 v/v%, zmieszana z FEC (10% wagowo). Tam, gdzie stosuje się mieszaninę węglanów etylenu i dietylu, podczas gdy fluorowane węglany zapewniają wyższe potencjały do 2 woltów.
Węglan etylenu jest również używany jako plastyfikator oraz jako prekursor węglanu winylenu , który jest używany w polimerach i syntezie organicznej .
Chlorek oksalilu jest wytwarzany komercyjnie z węglanu etylenu. Fotochlorowanie daje węglan tetrachloroetylenu:
- C 2 H 4 O 2 CO + 4 Cl 2 → C 2 Cl 4 O 2 CO + 4 HCl
Tetrachlorek jest degradowany do chlorku oksalilu przez katalizatory aminowe.
- C 2 Cl 4 O 2 CO → C 2 O 2 Cl 2 + COCl 2
Zobacz też
Zewnętrzne linki
Bibliografia
- ^ "CID 7303 - Podsumowanie związku PubChem" . pubchem.ncbi.nlm.nih.gov . Źródło 2008-03-15 .
- ^ Wpis do katalogu JEFFSOL ETYLENE CARBONATE na www.huntsman.com. Dostęp 18.02.2010.
- ^ B Buysch Hans-Josef (2012). „Estry węgla”. Encyklopedia Chemii Przemysłowej Ullmanna . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a05_197 .
- ^ Comerford, James W.; Ingram, Ian DV; Północ, Michael; Wu, Xiao (2015). „Zrównoważone katalizatory na bazie metali do syntezy cyklicznych węglanów zawierających pięcioczłonowe pierścienie”. Zielona Chemia . 17 (4): 1966-1987. doi : 10.1039/C4GC01719F .
- ^ Bhalchandra M. Bhanage; Shinichiro Fujita (2003). „Transestryfikacja mocznika i glikolu etylenowego do węglanu etylenu jako ważny krok w syntezie węglanu dimetylu na bazie mocznika”. Zielona Chemia . 5 (4): 429–432. doi : 10.1039/b304182d .
- ^ Gan, Yu-Lin; Hu, Xiao-Qian; Wen, Lin-Zhi; Xu, Jie; Xue, Bing (24.02.2020). „Bezmetalowa synteza węglanu dimetylu poprzez transestryfikację węglanu etylenu katalizowaną grafitowymi materiałami azotku węgla” . Nowy Czasopismo Chemii . 44 (8): 3215–3223. doi : 10.1039/C9NJ04530A . ISSN 1369-9261 . S2CID 213404364 .
- ^ Ralph P. Seward; Ernesta C. Vieira (1958). „Stałe dielektryczne węglanu etylenu i roztworów węglanu etylenu w wodzie, metanolu, benzenie i węglanie propylenu”. J. Fiz. Chem . 62 (1): 127–128. doi : 10.1021/j150559a041 .
- ^ Richard Payne; Ignacego E. Theodorou (1972). „Właściwości dielektryczne i relaksacja w węglanie etylenu i węglanie propylenu”. J. Fiz. Chem . 76 (20): 2892–2900. doi : 10.1021/j100664a019 .
- ^ ER Logan; JR Dahn (2018). „Badanie właściwości fizycznych elektrolitów akumulatorów litowo-jonowych zawierających estry”. J. Elektrochem. Soc . 165 (2): A21–A30. doi : 10.1149/2.0271802jes . OSTI 1469344 .
- ^ Youssef powiedział, powiedział; Kalisvaart, W. Peter; Olsen, Brian; Luber, Eryk; Buriak, Jillian (13.07.2020). „Stabilizacja anod cynowych w akumulatorach sodowo-jonowych przez stopienie z krzemem” . figshare . doi : 10.26434/chemrxiv.12642956.v1 . Pobrano 2021-02-24 .
- ^ Pfoertner, Karl-Heinz (2000). "Fotochemia". Encyklopedia Chemii Przemysłowej Ullmanna . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a19_573 .