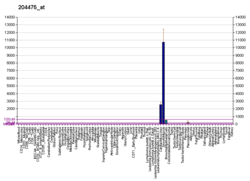
MMP1 - MMP1
Metaloproteinaza macierzy 1 (MMP-1) znana również jako kolagenaza śródmiąższowa i kolagenaza fibroblastów jest enzymem, który u ludzi jest kodowany przez gen MMP1 . Gen jest częścią klastra genów MMP, które lokalizują się na chromosomie 11q22.3. MMP-1 była pierwszą kolagenazą kręgowców, zarówno oczyszczoną do jednorodności jako białko, jak i sklonowaną jako cDNA. MMP-1 ma szacunkową masę cząsteczkową 54 kDa.
Cechy konstrukcyjne
MMP-1 ma strukturę archetypową składającą się z predomeny , prodomeny , domeny katalitycznej, regionu łącznikowego i domeny podobnej do hemopeksyny . Pierwotna struktura MMP-1 została po raz pierwszy opublikowana przez Goldberg, GI, et al. Obecnie stosowane są dwie główne nomenklatury struktury pierwszorzędowej, pierwotna, od której pierwszy aminokwas zaczyna się od peptydu sygnałowego, a druga, w której pierwszy aminokwas zaczyna liczyć od prodomeny (nomenklatura proenzymów).
Domena katalityczna
Domeny Katalityczne MMP mają bardzo podobne właściwości, mając ogólny kształt spłaszczonej elipsoidy o średnicy ~40 Å. Pomimo podobieństwa domen katalitycznych MMP, ten wpis skupi się tylko na cechach strukturalnych domeny katalitycznej MMP-1.
Ogólna charakterystyka strukturalna
Domena katalityczna MMP-1 składa się z pięciu silnie skręconych nici β (sI-sV), trzech helis α (hA-hC) i łącznie ośmiu pętli, zawierających łącznie pięć jonów metali, trzy Ca 2+ oraz dwa Zn 2+ , z których jeden pełni rolę katalityczną.
Domena katalityczna (CAT) MMP-1 zaczyna się od F100 (nieskrócony CAT) jako pierwszego aminokwasu pętli N-końcowej domeny CAT. Pierwsza opublikowana struktura rentgenowska domeny CAT była reprezentatywna dla skróconej postaci tej domeny, w której pierwszych 7 aminokwasów nie występuje.
Po początkowej pętli sekwencje następują do pierwszego i najdłuższego arkusza β (sI). Druga pętla poprzedza dużą „amfipatyczną α-helisę” (hA), która rozciąga się wzdłużnie na miejsce białka. Nici β sII i sIII następują po rozdzieleniu odpowiednimi pętlami, przy czym pętla 4 jest powszechnie określana jako „krótka pętla” łącząca sII z sIII. Po nici sIII sekwencja spotyka się z „podwójną pętlą w kształcie litery S”, która ma pierwszorzędne znaczenie dla struktury peptydu i aktywności katalitycznej (patrz dalej), ponieważ rozciąga się do strony szczeliny „wybrzuszenie”, kontynuując do jedynej antyrównoległej nici β sIV, który ma pierwszorzędne znaczenie dla wiązania substratów peptydowych lub inhibitorów poprzez tworzenie wiązania wodorowego łańcucha głównego . Po sIV pętla Gln186-Gly192 i β-nić sV są odpowiedzialne za udział wielu ligandów w kilku jonach metali obecnych w białku (czytaj dalej). Duża otwarta pętla podąża za sV, która okazała się ważna w specyficzności substratowej w rodzinie MMP. Określony region (183)RWTNNFREY (191) został zidentyfikowany jako krytyczny segment metaloproteinazy macierzy 1 dla ekspresji aktywności kolagenolitycznej. Na C-końcowej części domeny CAT hB α-helisa, znana jako „helisa miejsca aktywnego” obejmuje część „sekwencji konsensusowej wiążącej cynk” HEXXHXXGXXH, która jest charakterystyczna dla nadrodziny Metzincin . α-helisa hB kończy się nagle w Gly225, gdzie zaczyna się ostatnia pętla domeny. Ta ostatnia pętla zawiera „pętlę specyficzności”, która jest najkrótsza w rodzinie MMP. Domena katalityczna kończy się na Gly261 z α-helisą hC.
Funkcjonować
MMP biorą udział w rozpadzie macierzy zewnątrzkomórkowej w normalnych procesach fizjologicznych, takich jak rozwój embrionalny, reprodukcja i przebudowa tkanek, a także w procesach chorobowych, takich jak zapalenie stawów i przerzuty. W szczególności MMP-1 rozkłada kolageny śródmiąższowe typu I, II i III.

Indukcja metaloproteinazy macierzy 1 w rogówce szczura przez cyprofloksacynę , ofloksacynę i lewofloksacynę (b,c,d) w porównaniu ze sztucznymi łzami (a). Reviglio i wsp., 2003.
|
Rozporządzenie
Siła mechaniczna może zwiększyć ekspresję MMP1 w ludzkich komórkach więzadła ozębnej.
Interakcje
Wykazano, że MMP1 oddziałuje z CD49b .
Bibliografia
Dalsza lektura
- Krane SM (1995). „Czy kolagenaza (metaloproteinaza macierzy 1) jest niezbędna do przebudowy kości i innych tkanek łącznych?”. Clin. Ortopedia. Wzgl. Res. (313): 47-53. PMID 7641497 .
- Massova I, Kotra LP, Fridman R, Mobashery S (1998). „Metaloproteinazy macierzy: struktury, ewolucja i dywersyfikacja”. FASEB J . 12 (25n26): 1075–95. CiteSeerX 10.1.1.31.3959 . doi : 10.1142/S0217984998001256 . PMID 9737711 .
- Nagase H, Woessner JF (1999). „Metaloproteinazy macierzowe” . J. Biol. Chem . 274 (31): 21491-4. doi : 10.1074/jbc.274.31.21491 . PMID 10419448 .
- Okada Y, Hashimoto G (2001). „[Degradacja macierzy zewnątrzkomórkowej przez metaloproteinazy macierzy i niszczenie stawów]”. Seikagaku . 73 (11): 1309–21. PMID 11831026 .
- Seiki M (2003). „Metaloproteinaza macierzy błonowej typu 1: kluczowy enzym do inwazji nowotworu”. Rak Lett . 194 (1): 1–11. doi : 10.1016/S0304-3835(02)00699-7 . PMID 12706853 .
- Golubkov VS, Strongin AY (2007). „Onkogeneza sterowana proteolizą” . Cykl komórkowy . 6 (2): 147-50. doi : 10.4161/cc.6.2.3706 . PMID 17245132 .
Zewnętrzne linki
- Merops bazy danych online peptydaz i ich inhibitorów: M10.001
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : P03956 (kolagenaza śródmiąższowa) w PDBe-KB .