Budezonid/formoterol - Budesonide/formoterol
 | |
| Kombinacja | |
|---|---|
| Budezonid | Glikokortykosteroidy |
| Formoterol | Długo działający agonista receptorów beta-adrenergicznych |
| Dane kliniczne | |
| Nazwy handlowe | Symbicort, DuoResp Spiromax, BiResp Spiromax, inne |
| AHFS / Drugs.com | Profesjonalne fakty dotyczące leków |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Inhalacja |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Identyfikatory | |
| Numer CAS | |
| KEGG | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Dane chemiczne i fizyczne | |
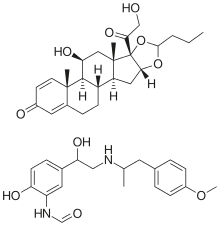
| Formuła | C 44 H 58 N 2 O 10 |
| Masa cząsteczkowa | 774.952 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Budezonid/formoterol , sprzedawany m.in. pod marką Symbicort , jest lekiem złożonym o ustalonej dawce, stosowanym w leczeniu astmy lub przewlekłej obturacyjnej choroby płuc (POChP). Zawiera budezonid , steroid i formoterol , długo działający beta 2 -mimetyk (LABA). Monografia produktu nie uzasadnia jego zastosowania w nagłym pogorszeniu lub leczeniu czynnego skurczu oskrzeli . Jednak przegląd literatury z 2020 r. potwierdza takie zastosowanie. Jest używany przez wdychanie leku .
Częste (≥1/100 do <1/10) działania niepożądane obejmują kandydozę , ból głowy , drżenie , kołatanie serca , podrażnienie gardła, kaszel i dysfonię . Zapalenie płuc jest częstym działaniem niepożądanym u osób z POChP i udokumentowano inne, mniej częste działania niepożądane. Istniały obawy, że składnik LABA zwiększa ryzyko zgonu u dzieci z astmą, jednak obawy te zostały usunięte w 2017 roku. Dlatego ta kombinacja jest zalecana tylko u tych, którzy nie są kontrolowani za pomocą samego wziewnego steroidu . Istnieją wstępne dowody na to, że typowe dawki steroidów wziewnych i LABA są bezpieczne w ciąży. Zarówno formoterol, jak i budezonid przenikają do mleka matki.
Budezonid/formoterol został dopuszczony do użytku medycznego w Stanach Zjednoczonych w 2006 roku. Znajduje się on na Liście Leków Podstawowych Światowej Organizacji Zdrowia , najbezpieczniejszych i najskuteczniejszych leków potrzebnych w systemie opieki zdrowotnej . W 2019 roku był to 57. najczęściej przepisywany lek w Stanach Zjednoczonych, z ponad 12 milionami recept.
Zastosowania medyczne
Utrzymanie
Wykazano skuteczność budezonidu/formoterolu w zapobieganiu atakom astmy. Nie jest jasne, czy budezonid/formoterol różni się od flutikazonu i salmeterolu w przewlekłej astmie.
Zaostrzenie
Połączenie jest zatwierdzone w Stanach Zjednoczonych tylko jako lek podtrzymujący w astmie i przewlekłej obturacyjnej chorobie płuc (POChP). Jednak przegląd literatury z 2020 r. potwierdza stosowanie w razie potrzeby podczas ostrego pogorszenia u osób z łagodną chorobą oraz jako leczenie podtrzymujące, po którym następują dodatkowe dawki podczas pogorszenia.
Stosowanie zarówno w leczeniu podtrzymującym, jak i w razie potrzeby jest również znane jako pojedyncza terapia podtrzymująca i doraźna (SMART) i jest leczeniem o ugruntowanej pozycji. Wykazano, że zmniejsza zaostrzenia astmy, które wymagają doustnych kortykosteroidów, wizyty w szpitalu są lepsze niż same wziewne kortykosteroidy podtrzymujące w wyższej dawce lub wziewny kortykosteroid w tej samej lub wyższej dawce z długo działającym lekiem rozszerzającym oskrzela (LABA)), z krótko działającym lek rozszerzający oskrzela (SABA) jako lek doraźny. Potrzebne są dalsze badania z zastosowaniem budezonidu/formoterolu SMART u dzieci.
Skutki uboczne
Często (do 1 na 10 osób)
- Łagodne podrażnienie gardła
- Kaszel
- Chrypka
- Kandydoza jamy ustnej (pleśniawki. znacznie mniej prawdopodobne, jeśli pacjent wypłukuje usta wodą po inhalacjach)
- Bół głowy
Często łagodne i zwykle ustępują w miarę dalszego stosowania leku:
Niezbyt często (do 1 na 100 osób)
- Uczucie niepokoju, zdenerwowania lub pobudzenia
- Zakłócony sen
- Zawroty głowy
- Mdłości
- Tachykardia (szybkie tętno)
- Zasinienie skóry
- Skurcze mięśni
Rzadko (do 1 na 1000 osób)
- Wysypka
- Swędzenie
- Skurcz oskrzeli (napięcie mięśni dróg oddechowych powodujące świszczący oddech natychmiast po zastosowaniu leku, które jest prawdopodobnie oznaką reakcji alergicznej i powinno być natychmiast skonsultowane z lekarzem)
- Hipokaliemia (niski poziom potasu we krwi)
- arytmia serca
Bardzo rzadko (do 1 na 10 000 osób)
- Depresja
- Zmiany w zachowaniu, szczególnie u dzieci
- Ból w klatce piersiowej lub ucisk w klatce piersiowej
- Wzrost poziomu glukozy we krwi
- Zmiany smakowe, takie jak nieprzyjemny smak w ustach
- Zmiany ciśnienia krwi
Inne
Przy wysokich dawkach przez długi czas.
- Zmniejszona gęstość mineralna kości, powodująca osteoporozę
- Zaćma
- Jaskra
- Spowolnione tempo wzrostu u dzieci i młodzieży
- Dysfunkcja nadnerczy , która wpływa na produkcję różnych hormonów
Reakcja alergiczna
- Obrzęk naczynioruchowy (obrzęk twarzy, ust, języka i/lub gardła. Trudności w połykaniu. Pokrzywka. Trudności w oddychaniu. Uczucie omdlenia)
- Skurcz oskrzeli (nagły ostry świszczący oddech lub duszność natychmiast po zastosowaniu leku. Pacjent powinien natychmiast zastosować lek doraźny).
Społeczeństwo i kultura
Dawki
Symbicort w Stanach Zjednoczonych jest inhalatorem z odmierzaną dawką i jest dostępny w wersjach 160/4,5 mcg i 80/4,5 mcg na jedną dawkę.
W Unii Europejskiej, Australii, Kanadzie, Izraelu, Arabii Saudyjskiej i innych krajach połączenie jest dostępne jako inhalator suchego proszku w następujących dawkach: 50/3 (40/2,25), 100/3 (80/2,25), 100/6 (80/4,5), 200/6 (160/4,5) i 400/12 (320/9), gdzie większa liczba to dawka budezonidu na dawkę (w mikrogramach ), a mniejsza dawka formoterolu (również w mikrogramów).
Rynek
Formuła budezonidu/formoterolu została wprowadzona w Szwecji w 2000 roku. Została dopuszczona do użytku w Stanach Zjednoczonych w lipcu 2006 roku. Obecnie jest dopuszczona do stosowania w co najmniej 70 krajach, przynosząc globalną sprzedaż przekraczającą 1 miliard USD w 2005 roku, a obecnie około 3,7 miliarda dolarów rocznie.
Budezonid/formoterol został dopuszczony do stosowania w Unii Europejskiej w kwietniu 2014 r.
Istnieje kilka patentów związanych z lekiem; niektóre z nich już wygasły. Początkowo był sprzedawany przez firmę AstraZeneca .
Bibliografia
Zewnętrzne linki
- „Mieszanka budezonidu z formoterolem” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Inhalacja doustna budesonidem” . MedlinePlus .
- "Formoterol Inhalacja Doustna" . MedlinePlus .


