Kwas klawulanowy - Clavulanic acid
 | |
 | |
| Dane kliniczne | |
|---|---|
| Wymowa | / ˌ K L ae v J ʊ l ć n ɪ K / |
| AHFS / Drugs.com | Międzynarodowe nazwy leków |
Kategoria ciąży |
|
| Drogi administracji |
Ustne, IV |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | "Dobrze przyswajalny" |
| Metabolizm | Wątrobowy (rozległy) |
| Okres półtrwania eliminacji | 1 godzina |
| Wydalanie | Nerki (30–40%) |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.055.500 |
| Dane chemiczne i fizyczne | |
| Formuła | C 8 H 9 N O 5 |
| Masa cząsteczkowa | 199,162 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Kwas klawulanowy jest lekiem β-laktamowym , działającym jako działający na zasadzie mechanizmu inhibitora β-laktamazy . Chociaż sam w sobie nie jest skuteczny jako antybiotyk , w połączeniu z antybiotykami z grupy penicylin może przezwyciężyć oporność na antybiotyki u bakterii wydzielających β-laktamazę , która w przeciwnym razie inaktywuje większość penicylin.
W swoich najczęstszych preparatach klawulanian potasu (kwas klawulanowy jako sól potasu) łączy się z:
- amoksycylina ( co- amoksyklaw, nazwy handlowe Augmentin, Tyclav, Clavamox ( weterynaryjne ), Synulox ( weterynaryjne ) i inne)
- tikarcylina ( co-ticarclav , nazwa handlowa Timentin)
Kwas klawulanowy został opatentowany w 1974 roku.
Zastosowania medyczne
Amoksycylina kwas klawulanowy jest lekiem pierwszego rzutu w przypadku wielu rodzajów infekcji, w tym infekcji zatok i infekcji dróg moczowych, w tym odmiedniczkowego zapalenia nerek . Wynika to częściowo z jego skuteczności wobec bakterii Gram-dodatnich, które są trudniejsze do kontrolowania niż bakterie Gram-ujemne za pomocą antybiotyków chemioterapeutycznych.
Niekorzystne skutki
Stosowanie kwasu klawulanowego z penicylinami wiąże się ze zwiększoną częstością występowania żółtaczki cholestatycznej i ostrego zapalenia wątroby podczas leczenia lub krótko po nim. Powiązana żółtaczka zwykle ustępuje samoistnie i bardzo rzadko prowadzi do zgonu.
PL Komisja Bezpieczeństwa Leków (CSM) zaleca, aby obróbce, takiej jak amoksycylina / preparatów kwas klawulanowy są zarezerwowane dla zakażenia bakteryjne, które mogą być powodowane przez szczepy β-laktamazy wytwarzania amoksycyliny ścieranie, a obróbka nie powinna przekraczać 14 dni.
Alergia odnotowano.
Źródła
Nazwa pochodzi od szczepów Streptomyces clavuligerus , które wytwarzają kwas klawulanowy.
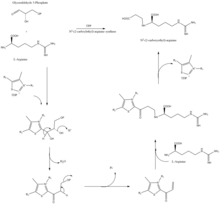
Biosynteza
Β-laktamu jak struktura kwasu klawulanowego wygląda strukturalnie podobne do penicyliny , ale w biosyntezie tej cząsteczki polega na innej drodze biochemicznej. Kwas klawulanowy jest wytwarzany przez bakterię Streptomyces clavuligerus przy użyciu 3-fosforanu aldehydu glicerynowego i L- argininy jako materiałów wyjściowych. Chociaż każdy z produktów pośrednich szlaku jest znany, dokładny mechanizm wszystkich reakcji enzymatycznych nie jest w pełni zrozumiały. Sposób obejmuje przede wszystkim 3 enzymów: clavaminate syntazy , β-laktamu syntetazy i N 2 - (2-karboksyetylo) -L-argininy (CEA) syntazy . Syntaza klawaminianowa jest oksygenazą niehemową zależną od żelaza i α-keto-glutaranu i jest kodowana przez orf5 zgrupowania genów kwasu klawulanowego . Specyficzny mechanizm działania tego enzymu nie jest w pełni poznany, ale enzym ten reguluje 3 etapy ogólnej syntezy kwasu klawulanowego. Wszystkie 3 etapy zachodzą w tym samym regionie katalitycznego, zawierającego żelazo centrum reakcyjnego, ale nie występują kolejno i wpływają na różne obszary struktury kwasu klawulanowego.
Syntetaza β-laktamowa jest białkiem o masie 54,5 kDa, które jest kodowane przez orf3 klastra genów kwasu klawulanowego i wykazuje podobieństwo do syntazy asparaginy – enzymów klasy B. Dokładny mechanizm działania tego enzymu w syntezie β-laktamu nie został udowodniony, ale uważa się, że występuje w koordynacji z syntazą CEA i ATP .
Syntaza CEA jest białkiem 60,9 kDA i jest pierwszym genem znalezionym w klastrze genów biosyntezy kwasu klawulanowego, kodowanym przez orf2 klastra genów kwasu klawulanowego. Specyficzny mechanizm działania tego enzymu jest wciąż badany; wiadomo jednak, że enzym ten ma zdolność sprzęgania 3-fosforanu aldehydu glicerynowego z L-argininą w obecności difosforanu tiaminy (TDP lub pirofosforan tiaminy ), który jest pierwszym etapem biosyntezy kwasu klawulanowego.
Historia
Kwas klawulanowy został odkryty w latach 1974-75 przez brytyjskich naukowców pracujących w firmie farmaceutycznej Beecham z bakterii Streptomyces clavuligerus . Po kilku próbach Beecham w końcu złożył wniosek o ochronę patentową w USA na lek w 1981 roku, a patenty USA 4,525,352, 4,529,720 i 4,560,552 zostały przyznane w 1985 roku.
Kwas klawulanowy ma znikomą samoistną aktywność przeciwdrobnoustrojową, pomimo wspólnego pierścienia β-laktamowego, który jest charakterystyczny dla antybiotyków β-laktamowych . Jednak podobieństwo w budowie chemicznej pozwala cząsteczce na interakcję z enzymem β-laktamazy wydzielanym przez niektóre bakterie w celu nadania oporności na antybiotyki β-laktamowe.
Kwas klawulanowy jest inhibitorem samobójstw , wiążącym się kowalencyjnie z resztą seryny w miejscu aktywnym β-laktamazy. To przebudowuje cząsteczkę kwasu klawulanowego, tworząc znacznie bardziej reaktywne formy, które atakują inny aminokwas w miejscu aktywnym, trwale go dezaktywując, a tym samym dezaktywując enzym.
To hamowanie przywraca przeciwdrobnoustrojowe działanie antybiotyków β-laktamowych przeciwko bakteriom opornym na wydzielanie laktamazy. Mimo to pojawiły się pewne szczepy bakteryjne, które są odporne nawet na takie kombinacje.