Fibrylina 1 - Fibrillin 1
Fibrylina-1 to białko, które u ludzi jest kodowane przez gen FBN1 zlokalizowany na chromosomie 15.
FBN1 jest gen 230 kb z 65 kodujących egzonów kodujących 2871 aminokwas długo probiałko nazwie profibrillin który jest proteolitycznie odcinany w pobliżu jej C-końcu w wyniku działania enzymu furyna konwertaza aby dać fibryliny-1, członek fibryliny rodziny i 140-aminokwasowy hormon długobiałkowy aspzyn .
Fibrylina-1 jest dużą glikoproteiną macierzy zewnątrzkomórkowej, która służy jako składnik strukturalny 10-12 nm mikrowłókien wiążących wapń . Te mikrowłókna zapewniają wsparcie strukturalne w elastycznej i nieelastycznej tkance łącznej w całym ciele.
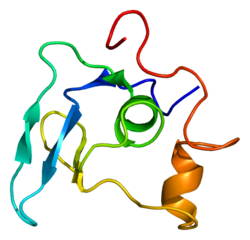
Struktura
Sekwencja fibryliny-1 obejmuje 47 sześciocysteinowych domen podobnych do EGF , 7 ośmiocysteinowych domen homologicznych z utajonym białkiem wiążącym TGF-beta i region bogaty w prolinę .
Rozwój sercowo-naczyniowy płodu
Gen FBN-1 bierze udział w różnych programach rozwoju embrionalnego. Mikrofibryle wykonane z fibryliny-1 przyczyniają się do tworzenia struktur elastycznych i nieelastycznych. Tworzenie elastycznych włókien w zastawkach serca i aorcie wymaga zaangażowania zarówno FBN-1, jak i FBN-2. Wykazano, że zarówno FBN-1, jak i FBN-2 wraz z innymi składnikami włókien elastycznych ulegają ekspresji w embrionalnych zastawkach półksiężycowatych już w 4 tygodniu ciąży. Te cząsteczki oddziałują, tworząc elastyczne włókna w warstwie komorowej zastawek półksiężycowatych. Fibrylina-1 i fibrylina-2 są również kluczowe dla rozwoju włókien elastycznych w aorcie. Podczas gdy ekspresja fibryliny-2 znacznie spada po rozwoju płodowym, ekspresja fibryliny-1 utrzymuje się w wieku dorosłym. Potwierdza to pogląd, że fibrylina-2 dyktuje rozwój wczesnych włókien elastycznych, podczas gdy fibrylina-1 zapewnia wsparcie strukturalne dojrzałych włókien elastycznych.
W przypadku wystąpienia mutacji w genach FBN-1 lub FBN-2, w wyniku uszkodzenia macierzy zewnątrzkomórkowej mogą powstać znaczne deformacje. Zespół Marfana jest chorobą wrodzoną, która wynika z mutacji w genie FBN-1. Prowadzi to do malformacji, a następnie osłabienia mikrowłókien w ciele pacjenta, w tym struktur układu sercowo-naczyniowego. Osłabione włókna elastyczne spowodują pogorszenie trwałości i rozciągliwości zastawek serca i aorty. Stanowi to wyjaśnienie tętniaków aorty i wypadania zastawek, które są powszechnie związane z zespołem Marfana.
Zespół Marfana
Zespół Marfana (MFS) to autosomalne dominujące zaburzenie, które atakuje tkankę łączną układów organizmu, takich jak oczy, układ sercowo-naczyniowy, układ kostny, skóra, układ płucny i opona twarda. MFS dotyka około 1 na 5000 osób. MFS nie jest łatwą do zdiagnozowania patologią z systemem punktacji zwanym tabelą nozologiczną Gandawy, a nie testem jednocząsteczkowym. Aby zdiagnozować osoby z MFS, które nie miały historii rodzinnej, muszą być spełnione dwa kryteria. Po pierwsze, dwa różne główne układy narządów muszą być zaatakowane, a po drugie, trzeci układ narządów musi być zaangażowany.
MFS zwykle występuje w wyniku mutacji „De Novo” i skutkuje u osobnika fenotypowo przejawiającym długie i cienkie kończyny i kończyny, zakrzywione kręgosłupy zwykle powodujące skoliozę piersiową, nadmiernie giętkie stawy, klatkę piersiową lejkowatą, odwarstwienie siatkówki i zapadniętą klatkę piersiową. Mutacje „De Novo” prowadzące do ciężkiego MFS mają wysoką oczekiwaną śmiertelność noworodków. Klasyczne objawy MFS zwykle stają się zauważalne w okresie dojrzewania lub w późniejszym życiu; rzadko rozwija się we wcześniejszych etapach życia. Najczęstszą manifestacją skórną MFS są rozstępy rozstępowe, w których prążki skórne są czerwone, fioletowe, a następnie białe. Naskórek skóry jest cienki i spłaszczony, a grubość górnej warstwy ochronnej skóry jest zmniejszona. Ta manifestacja histologicznie charakteryzuje się prostymi, cienkimi wiązkami kolagenu ułożonymi równolegle do skóry i włókien elastycznych. Włókna elastyczne są gęstsze w górnej części skóry właściwej, a poniżej tej strefy występuje miejscowy brak włókien elastycznych. Pomiędzy granicami rozstępów i skóry występują czasem poskręcane, połamane, siateczkowate włókna sprężyste. Objawy te są odpowiedzialne za wygląd skóry przypominający pajęczyny u pacjentów z MFS.
Zarządzanie MFS polega na operowaniu osoby poprzez operację na otwartym sercu. Postępowanie w MFS obejmuje standardowe implikacje, takie jak poradnictwo dotyczące stylu życia w celu zmniejszenia i ograniczenia aktywności fizycznej, profilaktyka endoprotezowa, seryjne obrazowanie aorty, leki β-adrenolityczne w celu ochrony aorty i profilaktyczna wymiana korzenia aorty. Zaleca się, aby dorośli dotknięci MFS zmniejszyli stres emocjonalny i fizyczny oraz zmienili sporty o dużym wysiłku, takie jak sztuki walki, piłka nożna, koszykówka itp., na ćwiczenia izotoniczne, o niewielkim wpływie, takie jak pływanie, jazda na rowerze lub jogging, gdzie tętno wynosi około < 110 uderzeń na minutę. Dzieci powinny również przestrzegać podobnych wytycznych, aby zapewnić prawidłowe leczenie MFS.
MFS jest spowodowane mutacją w genie „FBN1” umiejscowionym na chromosomie 15q21.1, co skutkuje zdekonstruowaną formą fibryliny-1. Fibrillin-1 to 350-kDa, 2871-aminokwasowa, bogata w cystynę glikoproteina, która jest odpowiedzialna za połączenie elastyny z elastycznymi włóknami tkanki łącznej w macierzy zewnątrzkomórkowej (ECM). Kruchość tkanki łącznej zwykle powoduje tętniaki aorty, ponieważ ściana nie jest w stanie wytrzymać ciśnienia wewnątrz światła. Defekty fibryliny-1 skutkują podwyższonymi poziomami TGF-β, które bezpośrednio korelują z MFS.
Rola TGF-β w ekspresji zespołu Marfana
TGF-β jest parakrynnym białkiem regulatorowym odpowiedzialnym za przetwarzanie embrionalne, wzrost komórek, indukcję apoptozy oraz wzmaga produkcję kolagenu i przebudowę ECM. U osoby bez MFS białko TGF-β jest wydzielane z komórki w celu stymulowania wytwarzania PAI-1 i fosforylacji Smad2. Białko TGF-β wiąże się z białkiem związanym z latencją (LAP) na właściwościach końca N i jednym z trzech utajonych białek wiążących TGF-β (LTBP1, 3 lub 4), tworząc mały kompleks utajony (SLC). Następnie SLC wiąże się pozakomórkowo z utajonym białkiem wiążącym TGF-β (LTBP) tworząc duży utajony kompleks (LLC), który zawiera aktywną cytokinę. LLC przyłącza się do mikrofibryli Fibryliny-1 poprzez LTBP, umożliwiając zachowanie nieaktywnego TGF-β [6]. TGF-β może być aktywowany jedynie poprzez szereg mechanizmów regulowanych; utrzymanie prawidłowego funkcjonowania w rozwoju embrionalnym. Mutacje w fibrylinie-1 powodują podwyższone poziomy TGF-β w przestrzeni EC z powodu niezdolności LLC do przyłączenia się do mikrofibryli i braku wytwarzania utajonych form. TGF-β tworzy kompleks ze swoimi receptorami dimerowymi, aby zainicjować kaskadę fosforylacji. Ta fosforylacja może powodować awarie, takie jak tętniak aorty i wypadanie zastawek.
Objawy kliniczne MFS, takie jak poszerzenie korzenia aorty, rozedma płuc, zmiany zastawki przedsionkowo-komorowej i miopatia mięśni szkieletowych, są indukowane przez zmienioną aktywację i sygnalizację TGF-β. Objawy specyficzne dla aorty są ściśle związane z nadmierną sygnalizacją TGF-β w ścianie korzenia aorty. Antagonizm TGF-β poprzez ogólnoustrojowe podawanie przeciwciała neutralizującego TGF-β (NAb) zapobiegał rozwojowi patologii aorty związanych z MDS, a dokładniej zmianom w ścianie aorty i postępującym poszerzeniu aorty. Antagonizm TGF-β również dodatkowo redukował objawy MFS, gdzie pomagał w regeneracji mięśni, architekturze i sile, przegrodach pęcherzyków płucnych i morfologii zastawki mitralnej.
LLC, której nie można usunąć z ECM, jest bardziej podatna na aktywację w sposób zależny od proteazy lub niezależny. MMP2 i MMP9 są wybranymi aktywatorami i ligandami TGF-β i znajdują się na wyższych poziomach w tkankach pacjentów dotkniętych MFS. TGF-β w postaci złożonej i wolnej może przenikać do krążenia dzięki zmutowanej sekwestracji ECM i zwiększonej aktywacji LLC.
Mutacje w genie „FBN1”
''FBN-1'' jest genem o wielkości około 200 kb i składa się z dużej sekwencji kodującej podzielonej na 65 eksonów zlokalizowanych na chromosomie 15. Ten gen koduje białko fibryliny-1. Fibrylina-1 jest dużą, bogatą w cysteinę glikoproteiną o wielkości około 350 kDa, złożoną głównie z tandemicznie powtarzających się domen modułów podobnych do naskórkowego czynnika wzrostu (EGF). Domeny te są homologiczne do modułu naskórkowego czynnika wzrostu wiążącego wapń (motywy podobne do cbEGF) i odrębnych modułów 8-cysteinowych tworzących elastyczną i nieelastyczną tkankę. Te elastyczne i nieelastyczne tkanki są wiązkami mikrofibrylarnymi, heteropolimerami zarówno fibryliny-1, jak i fibryliny-2. Elastogeneza to proces biologiczny, w którym mikrofibryle i włókna elastyczne są samoorganizujące się poprzez zorganizowane osadzanie przez kilka makrocząsteczek. Spolimeryzowane fibryliny można scharakteryzować poprzez ich strukturę mikrowłókien „kulki na nitce”; dając początek sieci mikrowłókienkowej poprzez boczną komunikację poszczególnych polimerów i składników strukturalnych.
Mutacje fibryliny-1 są głównym zmutowanym białkiem powodującym MFS. Ta mutacja zwykle zaburza łączenie mikrowłókien, powodując mechanizm dominujący-negatywny
Mutacje mogą obejmować:
- Mutacje typu missense spowodowane przez podstawienia pojedynczych zasad, takie jak cysteina lub te związane z wiązaniem wapnia w fibrylinie-1.
- Przedwczesne terminacje spowodowane przez nonsensowne mutacje lub przesunięcia ramki.
- Mutacje w obrębie egzonowego miejsca splotu umożliwiające wstawianie lub usuwanie z powodu tworzenia tajemniczych miejsc splotu.
- Zmiany bazy miejsca splicingu firmy Intronic prowadzące do alternatywnego splicingu i pomijania lub usuwania egzonów w ramce.
Połączenie czterech typów mutacji powoduje nieprawidłową ekspresję fibryliny-1. Nie ma korelacji między fenotypem a genotypem na poziomie molekularnym
Znane są mutacje genu FBN-1 w sześciu loci chromosomowych, TAAD1 przy 5q13-14, FAA1 przy 11q23-24, TAAD2 przy 3p24-25, TAAD3 przy 15q24-26, TAAD4 przy 10q23-24 i MYH11 przy 16p12-13 być wyzwalaczami MFS. Te loci mają tendencję do posiadania genów, które są zaangażowane w funkcję naczyń. Gen MYH11 jest odpowiedzialny za łańcuch ciężki miozyny mięśni gładkich, a ACTA2 w loci TAAD4 koduje alfa-aktynę mięśni gładkich.
Niesynonimiczna zmiana aminokwasowa wpływająca na konserwowaną cysteinę domeny podobnej do CaB-EGF, kodowanej przez ekson 13 genu FBN1 może spowodować rozwój MFS. Wyższa częstotliwość i nasilenie MFS występuje, gdy występują nieprawidłowe podstawienia w wiązaniach dwusiarczkowych C1-C2 lub C3-C4, dlatego prawidłowa lokalizacja cysteiny i wiązania dwusiarczkowe w tych loci mają kluczowe znaczenie dla integralności strukturalnej. Mutacje w genie FBN1 skutkujące nieprawidłowym wiązaniem w wiązaniu dwusiarczkowym C5-C6 na ogół powodują MFS o mniejszym nasileniu. Skoncentrowane mutacje domeny CaB-EGF wzdłuż polipeptydu FBN1 wpływają na fenotyp nasilenia MFS. Zlokalizowane mutacje substytucji substytucji cysteiny w C538P na eksonie 13, C570R na eksonie 14 lub C587Y na eksonie 15 powodują objawy MFS związane z oczami, w szczególności ektopia lentis. Same mikrofibryle mogą wspierać obciążenie hemodynamiczne w układach krążenia bezkręgowców i mniejszych kręgowców. Elastyna i rozwój systemu ECM zintegrowanego z otaczającym VSMC są potrzebne do prawidłowego funkcjonowania wyższych kręgowców. Fibrylina-1 nie jest niezbędna do stabilizacji jednostki elastycznej, ale zamiast tego do tworzenia mikrofibryli. Regulacja w górę aktywiny A działa w połączeniu z cząsteczkami sygnalizacyjnymi Fibrillin-1 i TGF-β w celu wytworzenia odpowiedzi fibroproliferacyjnej. Indukcja CYR61 działa również, aby wspierać adhezję komórek i regulować przebudowę macierzy i ma fundamentalne znaczenie w tworzeniu dużych naczyń i ich integralności.
Powszechne warianty w FBN1 mogą mieć również wpływ na gen i ludzkie fenotypy. Na przykład powszechny wariant w populacjach peruwiańskich (E1297G) może spowodować zmniejszenie wzrostu o 2,2 cm.
Znaczenie kliniczne
Mutacje w FBN1 genu są związane z zespołem Marfana i jego wariantu zespołu Marfanoid-progeroid, lipodystrofia , autosomalna dominująca zespół weilla-marchesaniego , samodzielnie zwichnięcie soczewki , MASS fenotyp oraz zespół shprintzena-goldberga .
Mutacje w FBN1 i FBN2 są związane z młodzieńczą skoliozą idiopatyczną .
Objawy kliniczne MFS, takie jak poszerzenie korzenia aorty, rozedma płuc, zmiany zastawki przedsionkowo-komorowej i miopatia mięśni szkieletowych, są indukowane przez zmienioną aktywację i sygnalizację TGF-β. Objawy specyficzne dla aorty są ściśle związane z nadmierną sygnalizacją TGF-β w ścianie korzenia aorty. Antagonizm TGF-β poprzez ogólnoustrojowe podawanie przeciwciała neutralizującego TGF-β (NAb) zapobiegał rozwojowi patologii aorty związanych z MDS, a dokładniej zmianom w ścianie aorty i postępującym poszerzeniu aorty. Antagonizm TGF-β również dodatkowo redukował objawy MFS, gdzie pomagał w regeneracji mięśni, architekturze i sile, przegrodach pęcherzyków płucnych i morfologii zastawki mitralnej.
Losartan
Losartan jest blokerem receptora angiotensyny II typu 1 (AT1), o którym wiadomo, że antagonizuje sygnalizację TGF-β poprzez hamowanie ekspresji i aktywacji TGF-β. Losartan może działać niezależnie lub z terapią β-adrenolitykami w celu zmniejszenia szybkości zmian średnicy korzenia aorty w patologii MFS.
Zobacz też
Uwagi
Bibliografia
Dalsza lektura
- Hayward C, Brock DJ (1998). „Mutacje fibryliny-1 w zespole Marfana i innych fibrynopatiach typu 1”. Mutacja ludzka . 10 (6): 415–23. doi : 10.1002/(SICI)1098-1004(1997)10:6<415::AID-HUMU1>3.0.CO;2-C . PMID 9401003 .
- Robinson PN, Godfrey M (styczeń 2000). „Genetyka molekularna zespołu Marfana i pokrewnych mikrofibrylopatii” . Dziennik Genetyki Medycznej . 37 (1): 9–25. doi : 10.1136/jmg.37.1.9 . PMC 1734449 . PMID 10633129 .
- Handford PA (grudzień 2000). „Fibrylina-1, białko wiążące wapń macierzy zewnątrzkomórkowej” . Biochimica et Biophysica Acta (BBA) - Badania nad komórkami molekularnymi . 1498 (2-3): 84-90. doi : 10.1016/s0167-4889(00)00085-9 . PMID 11108952 .
- Robinson PN, Booms P, Katzke S, Ladewig M, Neumann L, Palz M, Pregla R, Tiecke F, Rosenberg T (wrzesień 2002). „Mutacje FBN1 i korelacji genotyp-fenotyp w zespole Marfana i pokrewnych fibrynopatii”. Mutacja ludzka . 20 (3): 153-61. doi : 10.1002/humu.10113 . PMID 12203987 .
- Adès LC, Holman KJ, Brett MS, Edwards MJ, Bennetts B (kwiecień 2004). „Fenotypy Ectopia lentis i gen FBN1”. American Journal of Medical Genetics. Część A . 126A (3): 284-9. doi : 10.1002/ajmg.a.20605 . PMID 15054843 .
- Milewicz DM, Dietz HC, Miller DC (marzec 2005). „Leczenie choroby aorty u pacjentów z zespołem Marfana” . Obieg . 111 (11): e150-7. doi : 10.1161/01.CIR.0000155243.70456.F4 . PMID 15781745 .
- Boileau C, Jondeau G, Mizuguchi T, Matsumoto N (maj 2005). „Genetyka molekularna zespołu Marfana”. Aktualna opinia w kardiologii . 20 (3): 194–200. doi : 10.1097/01.hco.0000162398.21972.cd . PMID 15861007 .
- Whiteman P, Hutchinson S, Handford PA (2006). „Nieprawidłowe fałdowanie fibryliny-1 i choroba”. Przeciwutleniacze i sygnalizacja redoks . 8 (3–4): 338–46. doi : 10.1089/ars.2006.8.338 . PMID 16677079 .
Zewnętrzne linki
- GeneReviews/NCBI/NIH/UW wpis dotyczący zespołu Marfana
- Przegląd wszystkich informacji strukturalnych dostępnych w PDB dla UniProt : P35555 (Fibrillin-1) w PDBe-KB .