Syntaza tromboksanu-A - Thromboxane-A synthase
Syntaza tromboksanu A 1 (płytka, cytochrom P450, rodzina 5, podrodzina A) , znana również jako TBXAS1 , jest enzymem cytochromu P450, który u ludzi jest kodowany przez gen TBXAS1 .
Funkcjonować
Ten gen koduje członka nadrodziny enzymów cytochromu P450. W cytochromu P450 białka są monooksygenazy które katalizują wiele reakcji zaangażowane w metabolizm leku i syntezy cholesterolu, hormonów i innych lipidów. Jednak to białko jest uważane za członka nadrodziny cytochromów P450 na podstawie podobieństwa sekwencji, a nie podobieństwa funkcjonalnego. To białko błony retikulum endoplazmatycznego katalizuje konwersję prostaglandyny H 2 do tromboksanu 2 , silny zwężający naczynia krwionośne oraz induktor agregacji płytek krwi , a także 12 Hydroxyheptadecatrienoic kwasu (czyli 12- ( S ) -hydroksy-5 Z , 8, e , 10 Kwas E- heptadekatrienowy lub 12-HHT ) agonista receptorów leukotrienu B4 (tj. Receptory BLT2 ) i mediator niektórych działań receptorów BLT2 . Enzym odgrywa rolę w kilku procesach patofizjologicznych, w tym w hemostazie, chorobach sercowo-naczyniowych i udarze. Gen wyraża dwa warianty transkryptu.
Inhibitory
Inhibitory syntazy tromboksanu są stosowane jako leki przeciwpłytkowe . Ifetroban jest silnym i wybiórczym antagonistą receptora tromboksanu. Dipirydamol jest również antagonistą tego receptora, ale ma również różne inne mechanizmy działania przeciwpłytkowego. Pikotamid działa zarówno jako inhibitor syntazy tromboksanu, jak i jako antagonista receptora tromboksanu .
Struktura
Ludzka syntaza tromboksanu A (TXA) jest białkiem cytochromu P450 o masie 60 kDa z 533 aminokwasami i grupą prostetyczną hemu . Enzym ten, zakotwiczony w retikulum endoplazmatycznym, znajduje się w płytkach krwi, monocytach i kilku innych typach komórek. Koniec NH2 zawiera dwa hydrofobowe segmenty, których struktura drugorzędowa jest uważana za helikalną. Dowody sugerują, że peptydy służą jako kotwica błonowa dla enzymu. Ponadto badanie klonów cDNA, które umożliwiły techniki reakcji łańcuchowej polimerazy, pozwoliło na dalsze wyjaśnienie pierwotnej struktury syntazy TXA. Podobnie jak inni członkowie rodziny cytochromów P450, syntaza TXA ma grupę hemu skoordynowaną z grupą tiolanową reszty cysteiny, a konkretnie cysteiną 480. Badania mutagenezy, w których dokonano podstawień w tej pozycji, spowodowały utratę aktywności katalitycznej i minimalne wiązanie hemu. Inne reszty, które miały podobne wyniki, to W133, R478, N110 i R413. Reszty te, znajdujące się w pobliżu grup propionianowych hemu lub dystalnej powierzchni hemu, są również ważne dla właściwej integracji hemu z apoproteiną. Niestety, naukowcy stwierdzili, że uzyskanie struktury krystalicznej syntazy TXA jest trudne ze względu na wymóg ekstrakcji z membrany do obróbki detergentem, ale do stworzenia struktury 3D wykorzystali modelowanie homologii. Jeden model pokazał dwie domeny, domenę bogatą w alfa-helisę i domenę bogatą w arkusz beta. Stwierdzono, że hem był wciśnięty pomiędzy helisy I i L.
Mechanizm
Tromboksan A (TXA) pochodzi z cząsteczki prostaglandyny H2 (PGH2). PGH2 zawiera stosunkowo słabe wiązanie epidioksy i znany jest możliwy mechanizm obejmujący homolityczne rozszczepienie epiditlenku i przegrupowanie do TXA. Grupa hemu w miejscu aktywnym syntazy TXA odgrywa ważną rolę w tym mechanizmie. Badania kinetyki zatrzymanego przepływu z analogiem substratu i rekombinowaną syntazą TXA wykazały, że wiązanie substratu zachodzi w dwóch etapach. Najpierw następuje szybkie początkowe wiązanie z białkiem, a następnie ligacja z żelazem hemowym. W pierwszym etapie mechanizmu żelazo hemowe koordynuje się z tlenem endonadtlenku C-9. Bierze udział w homolitycznym rozszczepieniu wiązania OO w endonadtlenku, co stanowi etap ograniczający szybkość, i ulega zmianie w stanie redoks z Fe (III) na Fe (IV). Wolny rodnik tlenowy tworzy się na C-11, a ten związek pośredni ulega rozszczepieniu pierścienia. Z wolnym rodnikiem teraz w C-12, żelazo hem utlenia następnie ten rodnik do karbokokacji. Cząsteczka jest teraz gotowa do tworzenia pierścienia wewnątrzcząsteczkowego. Ujemnie naładowany tlen atakuje karbonyl, a elektrony z jednego z podwójnych wiązań są przyciągane do karbokationu, zamykając w ten sposób pierścień.
Znaczenie biologiczne
Utrzymanie równowagi między prostacyklinami i tromboksanami jest ważne w organizmie, zwłaszcza, że te dwa eikozanoidy mają przeciwstawne działanie. W katalizowaniu syntezy tromboksanów, syntaza TXA bierze udział w szlaku przepływu, który może modulować ilość wytwarzanego tromboksanu. Ta kontrola staje się ważnym czynnikiem w wielu procesach, takich jak regulacja ciśnienia krwi, krzepnięcie i reakcje zapalne. Uważa się, że rozregulowanie syntazy TXA i brak równowagi w stosunku prostacykliny do tromboksanu są przyczyną wielu stanów patologicznych, takich jak nadciśnienie płucne . Ponieważ tromboksany odgrywają rolę w zwężaniu naczyń i agregacji płytek krwi, ich dominacja może zaburzać homeostazę naczyń i powodować zakrzepowe zdarzenia naczyniowe. Co więcej, znaczenie tromboksanów i ich syntezy w homeostazie naczyniowej ilustrują odkrycia, że pacjenci, u których płytki krwi nie reagowały na TXA, wykazywali defekty hemostatyczne, a niedobór produkcji płytek krwi prowadził do zaburzeń krzepnięcia.
Ponadto stwierdzono, że ekspresja syntazy TXA może mieć kluczowe znaczenie dla rozwoju i progresji raka. Ogólny wzrost TXA syntazy ekspresję zaobserwowano w wielu różnych nowotworów, takich jak brodawkowatego raka tarczycy , raka prostaty i rak nerki . Komórki rakowe są znane z nieograniczonego potencjału replikacji komórek i postawiono hipotezę, że zmiany w profilu eikozanoidów wpływają na wzrost raka. Badania doprowadziły do wniosku, że syntaza TXA przyczynia się do szeregu szlaków przeżycia nowotworu, w tym wzrostu, hamowania apoptozy , angiogenezy i przerzutów .
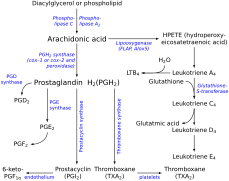
Ścieżka
Zobacz też
Bibliografia
Dalsza lektura
- Shen RF, Tai HH (1998). „Tromboksany: syntaza i receptory”. J. Biomed. Sci . 5 (3): 153–172. doi : 10.1007 / BF02253465 . PMID 9678486 .
- Smith G, Stubbins MJ, Harries LW, Wolf CR (1999). „Genetyka molekularna nadrodziny monooksygenazy cytochromu P450 człowieka”. Xenobiotica . 28 (12): 1129–1165. doi : 10.1080 / 004982598238868 . PMID 9890157 .
- Wang LH, Kulmacz RJ (2003). „Syntaza tromboksanu: budowa i funkcja białka i genu”. Prostaglandyny Inne Lipid Mediat . 68–69: 409–422. doi : 10.1016 / S0090-6980 (02) 00045-X . PMID 12432933 .
- Itoh S, Yanagimoto T, Tagawa S i wsp. (1992). „Organizacja genomu genów związanych z ludzkim płodem specyficznym dla P-450IIIA7 (cytochrom P-450HFLa) i interakcja regulacyjnego czynnika transkrypcji z jego elementem DNA w regionie flankującym 5 '”. Biochim. Biophys. Acta . 1130 (2): 133–8. doi : 10.1016 / 0167-4781 (92) 90520-a . PMID 1562592 .
- Yokoyama C, Miyata A, Ihara H i wsp. (1991). „Klonowanie molekularne syntazy tromboksanu A ludzkich płytek krwi”. Biochem. Biophys. Res. Commun . 178 (3): 1479–1484. doi : 10.1016 / 0006-291X (91) 91060-P . PMID 1714723 .
- Ohashi K, Ruan KH, Kulmacz RJ i wsp. (1992). „Podstawowa struktura ludzkiej syntazy tromboksanowej określona na podstawie sekwencji cDNA”. J. Biol. Chem . 267 (2): 789–93. PMID 1730669 .
- Jones DA, Fitzpatrick FA, Malcolm KC (1991). „Synteza tromboksanu A2 w ludzkich komórkach erytroleukemii”. Biochem. Biophys. Res. Commun . 180 (1): 8–14. doi : 10.1016 / S0006-291X (05) 81247-1 . PMID 1930241 .
- Wang LH, Ohashi K, Wu KK (1991). „Izolacja częściowego komplementarnego DNA kodującego ludzką syntazę tromboksanu”. Biochem. Biophys. Res. Commun . 177 (1): 286–291. doi : 10.1016 / 0006-291X (91) 91980-Q . PMID 2043115 .
- Nüsing R, Schneider-Voss S., Ullrich V (1990). „Oczyszczanie immunopowinowactwa ludzkiej syntazy tromboksanu”. Łuk. Biochem. Biophys . 280 (2): 325–330. doi : 10.1016 / 0003-9861 (90) 90337-X . PMID 2195994 .
- Mestel F, Oetliker O, Beck E i wsp. (1980). „Poważne krwawienie związane z wadliwą syntetazą tromboksanu” . Lancet . 1 (8160): 157. doi : 10.1016 / S0140-6736 (80) 90642-X . PMID 6101498 . S2CID 29803926 .
- Miyata A, Yokoyama C, Ihara H i wsp. (1994). „Charakterystyka ludzkiego genu (TBXAS1) kodującego syntazę tromboksanu”. Eur. J. Biochem . 224 (2): 273–279. doi : 10.1111 / j.1432-1033.1994.00273.x . PMID 7925341 .
- Wang LH, Tazawa R, Lang AQ, Wu KK (1995). „Alternatywne składanie mRNA ludzkiej syntazy tromboksanu”. Łuk. Biochem. Biophys . 315 (2): 273–278. doi : 10.1006 / abbi.1994.1500 . PMID 7986068 .
- Maruyama K., Sugano S (1994). „Oligo-capping: prosta metoda zastąpienia struktury czapeczki w eukariotycznych mRNA oligorybonukleotydami”. Gene . 138 (1–2): 171–174. doi : 10,1016 / 0378-1119 (94) 90802-8 . PMID 8125298 .
- Lee KD, Baek SJ, Shen RF (1994). „Klonowanie i charakterystyka promotora genu ludzkiej syntazy tromboksanu”. Biochem. Biophys. Res. Commun . 201 (1): 379–387. doi : 10.1006 / bbrc.1994.1712 . PMID 8198598 .
- Chase MB, Baek SJ, Purtell DC i wsp. (1993). „Mapowanie ludzkiego genu syntazy tromboksanu (TBXAS1) do chromosomu 7q34-q35 przez dwukolorową fluorescencyjną hybrydyzację in situ”. Genomics . 16 (3): 771–773. doi : 10.1006 / geno.1993.1264 . PMID 8325653 .
- Ruan KH, Wang LH, Wu KK, Kulmacz RJ (1993). „Topologia końca aminowego syntazy tromboksanu w retikulum endoplazmatycznym”. J. Biol. Chem . 268 (26): 19483–90. PMID 8366093 .
- Tazawa R, Green ED, Ohashi K i wsp. (1996). „Charakterystyka całej struktury genomu ludzkiego genu syntazy tromboksanu i analiza funkcjonalna jego promotora”. Łuk. Biochem. Biophys . 334 (2): 349–356. doi : 10.1006 / abbi.1996.0464 . PMID 8900410 .
- Baek SJ, Lee KD, Shen RF (1996). „Struktura genomu i polimorfizm ludzkiego genu kodującego syntazę tromboksanu”. Gene . 173 (2): 251–256. doi : 10.1016 / 0378-1119 (95) 00881-0 . PMID 8964509 .
- Suzuki Y, Yoshitomo-Nakagawa K, Maruyama K i wsp. (1997). „Konstrukcja i charakterystyka biblioteki cDNA wzbogaconej o pełnej długości i wzbogaconej na 5'-końcach”. Gene . 200 (1–2): 149–156. doi : 10.1016 / S0378-1119 (97) 00411-3 . PMID 9373149 .
Linki zewnętrzne
- Tromboxane-A + Synthase w US National Library of Medicine Medical Subject Headings (MeSH)