Kwas liponowy - Lipoic acid
|
|
|
|

|
|
| Nazwy | |
|---|---|
|
Nazwa IUPAC
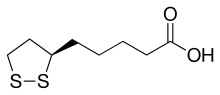
Kwas ( R )-5-(1,2-ditiolan-3-ylo)pentanowy
|
|
| Inne nazwy
Kwas α-liponowy; Kwas alfa liponowy; Kwas tioktanowy; Kwas 6,8-ditiooktanowy
|
|
| Identyfikatory | |
|
Model 3D ( JSmol )
|
|
| CZEBI | |
| CHEMBL | |
| ChemSpider | |
| DrugBank | |
| Karta informacyjna ECHA |
100,012,793 |
| KEGG | |
| Siatka | Liponowy+kwas |
|
Identyfikator klienta PubChem
|
|
| UNII | |
|
Pulpit nawigacyjny CompTox ( EPA )
|
|
|
|
|
|
| Nieruchomości | |
| C 8 H 14 O 2 S 2 | |
| Masa cząsteczkowa | 206.32 g·mol -1 |
| Wygląd zewnętrzny | Żółte igiełkowate kryształy |
| Temperatura topnienia | 60–62 ° C (140–144 ° F; 333–335 K) |
| Bardzo słabo rozpuszczalny (0,24 g/L) | |
| Rozpuszczalność w etanolu 50 mg/ml | Rozpuszczalny |
| Farmakologia | |
| A16AX01 ( KTO ) | |
| Farmakokinetyka : | |
| 30% (doustnie) | |
| Związki pokrewne | |
|
Związki pokrewne
|
Lipoamid Kwas asparagusowy |
|
O ile nie zaznaczono inaczej, dane podano dla materiałów w ich stanie standardowym (przy 25 °C [77 °F], 100 kPa). |
|
|
|
|
| Referencje do infoboksu | |
Kwas liponowy ( LA ), znany również jako kwas a-liponowy , kwas alfa-liponowy ( ALA ) i kwas liponowy , to związek siarkoorganiczne pochodzące z kwasu kaprylowego (kwasu kaprylowego). ALA wytwarzany jest normalnie u zwierząt i jest niezbędny dla metabolizmu tlenowego . Jest również produkowany i dostępny jako suplement diety w niektórych krajach, w których jest sprzedawany jako przeciwutleniacz , a w innych jest dostępny jako lek farmaceutyczny .
Fizyczne i chemiczne właściwości
Kwas liponowy (LA), znany również jako kwas α-liponowy, kwas alfa-liponowy (ALA) i kwas tioktanowy to związek siarkoorganiczny pochodzący z kwasu oktanowego . LA zawiera dwa atomy siarki (przy C6 i C8) połączone wiązaniem dwusiarczkowym i dlatego uważa się, że jest utleniony, chociaż każdy atom siarki może występować na wyższych stopniach utlenienia.
Atom węgla w C6 jest chiralny, a cząsteczka występuje jako dwa enancjomery ( R )-(+)-liponowy (RLA) i ( S )-(-)-liponowy (SLA) oraz jako mieszanina racemiczna ( R / S kwas )-liponowy (R/S-LA).
LA pojawia się fizycznie jako żółte ciało stałe i strukturalnie zawiera końcowy kwas karboksylowy i końcowy pierścień ditiolanowy.
Do stosowania w suplement diety materiałów i mieszania składników aptekach The USP wykazała oficjalną monografię R / S-LA.
Funkcja biologiczna
„Liponat” jest sprzężoną zasadą kwasu liponowego i najbardziej rozpowszechnioną formą LA w warunkach fizjologicznych. Większość wytwarzanych endogennie RLA nie jest „wolna”, ponieważ kwas oktanowy, prekursor RLA, wiąże się z kompleksami enzymatycznymi przed enzymatyczną insercją atomów siarki. Jako kofaktor, RLA jest kowalencyjnie przyłączony przez wiązanie amidowe do końcowej reszty lizynowej domen lipoilowych enzymu. Jedną z najbardziej zbadanych ról RLA jest kofaktor kompleksu dehydrogenazy pirogronianowej (PDC lub PDHC), choć jest także kofaktorem w innych układach enzymatycznych (opisanych poniżej).
Tylko ( R )-(+)-enancjomer (RLA) występuje w naturze i jest niezbędny dla metabolizmu tlenowego, ponieważ RLA jest niezbędnym kofaktorem wielu kompleksów enzymatycznych.
Biosynteza i przywiązanie
Prekursor kwasu liponowego, kwas oktanowy , powstaje w wyniku biosyntezy kwasów tłuszczowych w postaci oktanoilo- acylowego białka nośnikowego . U eukariontów wykorzystuje się w tym celu drugi szlak biosyntezy kwasów tłuszczowych w mitochondriach . Oktanian jest przenoszony jako tioester acylowego białka nośnikowego z biosyntezy kwasów tłuszczowych do amidu białka domeny lipoilowej przez enzym zwany oktanoilotransferazą. Dwa wodory oktanianowe są zastępowane grupami siarkowymi poprzez mechanizm rodnikowy SAM , przez syntazę lipoilową . W rezultacie syntetyzowany jest kwas liponowy połączony z białkami i nie powstaje wolny kwas liponowy. Kwas liponowy można usunąć, gdy białka ulegają degradacji i dzięki działaniu enzymu lipoamidazy. Wolny liponian może być stosowany przez niektóre organizmy jako enzym zwany ligazą białkową liponianu, który łączy go kowalencyjnie z właściwym białkiem. Ligazy, aktywność tego enzymu wymaga ATP .
Transport komórkowy
Wraz z sodem i witaminami, biotyną (B7) i kwasem pantotenowym (B5), kwas liponowy wchodzi do komórek przez SMVT (zależny od sodu transporter multiwitaminowy). Każdy ze związków transportowanych przez SMVT jest konkurencyjny w stosunku do innych. Na przykład badania wykazały, że zwiększenie spożycia kwasu liponowego lub kwasu pantotenowego zmniejsza wychwyt biotyny i/lub aktywność enzymów zależnych od biotyny.
Aktywność enzymatyczna
Kwas liponowy jest kofaktorem co najmniej pięciu układów enzymatycznych . Dwa z nich znajdują się w cyklu kwasu cytrynowego, w którym wiele organizmów zamienia składniki odżywcze w energię. Enzymy lipoilowane mają kowalencyjnie przyłączony do nich kwas liponowy. Grupa lipoilowa przenosi grupy acylowe w kompleksach dehydrogenazy 2-oksokwasowej oraz grupę metyloaminową w kompleksie rozszczepiającym glicyny lub dehydrogenazie glicyny .
Reakcje przeniesienia dehydrogenazy 2-oksokwasowej przebiegają według podobnego mechanizmu w:
- Kompleks dehydrogenazy pirogronianowej
- α-ketoglutaran dehydrogenazy lub 2-oksoglutaran dehydrogenazy kompleks
- kompleks dehydrogenazy oksokwasów o rozgałęzionym łańcuchu (BCDH)
- acetoiny dehydrogenazy złożone.
Najbardziej zbadanym z nich jest kompleks dehydrogenazy pirogronianowej. Kompleksy te mają trzy centralne podjednostki: E1-3, które są odpowiednio dekarboksylazą, transferazą lipoilową i dehydrogenazą dihydrolipoamidową . Te kompleksy mają centralny rdzeń E2, a inne podjednostki otaczają ten rdzeń, tworząc kompleks. W przerwie między tymi dwiema podjednostkami, domena lipoilowa prowadzi pośrednie między miejscami aktywnymi. Sama domena lipoilowa jest połączona elastycznym łącznikiem z rdzeniem E2, a liczba domen lipoilowych waha się od jednej do trzech dla danego organizmu. Liczba domen była eksperymentalnie zróżnicowana i wydaje się mieć niewielki wpływ na wzrost, dopóki nie zostanie dodanych ponad dziewięć, chociaż więcej niż trzy obniżyły aktywność kompleksu.
Kwas liponowy służy jako kofaktor kompleksu dehydrogenazy acetoinowej katalizującego konwersję acetoiny (3-hydroksy-2-butanonu) do aldehydu octowego i acetylokoenzymu A .
System rozszczepiania glicyny różni się od pozostałych kompleksów i ma inną nomenklaturę. W tym układzie białko H jest wolną domeną lipoilową z dodatkowymi helisami, białko L jest dehydrogenazą dihydrolipoamidową, białko P jest dekarboksylazą, a białko T przenosi metyloaminę z liponianu do tetrahydrofolianu (THF) dając metyleno-THF i amoniak. Metyleno-THF jest następnie wykorzystywany przez hydroksymetylotransferazę serynową do syntezy seryny z glicyny . System ten jest częścią fotooddychania roślin .
Źródła biologiczne i degradacja
Kwas liponowy jest obecny w wielu produktach spożywczych, w których jest związany z lizyną w białkach, ale nieco bardziej w nerkach, sercu, wątrobie, szpinaku, brokułach i ekstrakcie z drożdży. Naturalnie występujący kwas liponowy jest zawsze związany kowalencyjnie i nie jest łatwo dostępny ze źródeł dietetycznych. Ponadto ilość kwasu liponowego obecnego w źródłach pokarmowych jest niska. Na przykład do oczyszczania kwasu liponowego w celu określenia jego struktury użyto szacunkowo 10 ton pozostałości wątroby, co dało 30 mg kwasu liponowego. W rezultacie cały kwas liponowy dostępny jako suplement jest syntetyzowany chemicznie.
Poziomy wyjściowe (przed suplementacją) RLA i R-DHLA nie zostały wykryte w ludzkim osoczu. RLA wykryto w stężeniu 12,3–43,1 ng/ml po hydrolizie kwasowej, która uwalnia związany z białkami kwas liponowy. Hydroliza enzymatyczna kwasu liponowego związanego z białkiem uwolniła 1,4-11,6 ng/ml i <1-38,2 ng/ml przy użyciu odpowiednio subtylizyny i alkalazy .
Trawienne enzymy proteolityczne rozszczepiają resztę R-lipoillizyny z mitochondrialnych kompleksów enzymatycznych pochodzących z pożywienia, ale nie są w stanie rozszczepić wiązania amidowego kwas liponowy- L - lizyna . Zarówno syntetyczny lipoamid, jak i ( R )-lipoilo- L- lizyna są szybko rozszczepiane przez lipoamidazy surowicy, które uwalniają wolny kwas ( R ) -liponowy oraz L- lizynę lub amoniak. Niewiele wiadomo na temat degradacji i wykorzystania alifatycznych siarczków, takich jak kwas liponowy, z wyjątkiem cysteiny .
Kwas liponowy jest metabolizowany na różne sposoby, gdy jest podawany jako suplement diety u ssaków. Zaobserwowano degradację do kwasu tetranorliponowego, utlenianie jednego lub obu atomów siarki do sulfotlenku i S-metylację siarczku. Koniugację niezmodyfikowanego kwasu liponowego z glicyną wykryto zwłaszcza u myszy. Rozkład kwasu liponowego jest podobny u ludzi, chociaż nie jest jasne, czy atomy siarki ulegają znacznemu utlenieniu. Najwyraźniej ssaki nie są zdolne do wykorzystywania kwasu liponowego jako źródła siarki.
Synteza chemiczna

SLA nie istniał przed syntezą chemiczną w 1952 roku. SLA jest produkowany w równych ilościach z RLA podczas achiralnych procesów produkcyjnych. Forma racemiczna była szerzej stosowana klinicznie w Europie i Japonii w latach 50. do 60., pomimo wczesnego rozpoznania, że różne formy LA nie są biorównoważne. Pierwsze procedury syntetyczne dla RLA i SLA pojawiły się w połowie lat pięćdziesiątych. Postępy w chemii chiralnej doprowadziły do wydajniejszych technologii wytwarzania pojedynczych enancjomerów zarówno poprzez klasyczną rozdzielczość, jak i syntezę asymetryczną. W tym czasie również rosło zapotrzebowanie na RLA. W XXI wieku R/S-LA, RLA i SLA o wysokiej czystości chemicznej i/lub optycznej są dostępne w ilościach przemysłowych. Obecnie większość światowych dostaw R/S-LA i RLA jest produkowana w Chinach, a mniejsze ilości we Włoszech, Niemczech i Japonii. RLA jest wytwarzany przez modyfikacje procesu opisanego po raz pierwszy przez Georga Langa w pracy doktorskiej. teza i później opatentowany przez DeGussa. Chociaż RLA jest preferowany pod względem odżywczym ze względu na jego „podobną do witamin” rolę w metabolizmie, zarówno RLA, jak i R/S-LA są szeroko dostępne jako suplementy diety. Zarówno stereospecyficzne i reakcje niestereospecyficzne zwykle występują in vivo, i przyczyniają się do mechanizmu działania, ale do tej pory dowody wskazują RLA może się eutomer (The odżywczym i terapeutycznie korzystna postać).
Farmakologia
Farmakokinetyka
Badanie farmakokinetyczne sodu RLA z 2007 roku wykazało, że maksymalne stężenie w osoczu i biodostępność są znacznie większe niż w przypadku postaci wolnego kwasu i rywalizują z poziomami w osoczu uzyskanymi po dożylnym podaniu postaci wolnego kwasu. Dodatkowo osiągnięto wysokie poziomy w osoczu porównywalne z tymi w modelach zwierzęcych, w których aktywowano Nrf2.
Różne formy LA nie są biorównoważne. Bardzo niewiele badań porównuje poszczególne enancjomery z racemicznym kwasem liponowym. Nie jest jasne, czy dwa razy więcej racemicznego kwasu liponowego może zastąpić RLA.
Toksyczna dawka LA u kotów jest znacznie niższa niż u ludzi lub psów i powoduje toksyczność komórek wątroby.
Farmakodynamika
Mechanizm i działanie kwasu liponowego dostarczanego z zewnątrz do organizmu budzi kontrowersje. Wydaje się, że kwas liponowy w komórce indukuje przede wszystkim reakcję na stres oksydacyjny, a nie bezpośrednio wymiata wolne rodniki. Ten efekt jest specyficzny dla RLA. Pomimo silnie redukującego środowiska LA wykrywano wewnątrzkomórkowo zarówno w formach utlenionych, jak i zredukowanych. LA jest zdolny do wymiatania reaktywnych form tlenu i reaktywnych form azotu w teście biochemicznym ze względu na długi czas inkubacji, ale niewiele jest dowodów na to, że zachodzi to w komórce lub że wychwytywanie rodników przyczynia się do głównych mechanizmów działania LA. Stosunkowo dobra aktywność wymiatająca LA wobec kwasu podchlorawego (środek bakteriobójczy wytwarzany przez neutrofile, który może powodować zapalenie i uszkodzenie tkanki) jest spowodowana naprężoną konformacją 5-członowego pierścienia ditiolanowego, który jest tracony po redukcji do DHLA. W komórkach LA jest redukowany do kwasu dihydroliponowego, który jest powszechnie uważany za bardziej bioaktywną formę LA i formę odpowiedzialną za większość efektów przeciwutleniających oraz za obniżenie aktywności redoks niezwiązanego żelaza i miedzi. Teoria ta została zakwestionowana ze względu na wysoki poziom reaktywności dwóch wolnych sulfhydrylów, niskie wewnątrzkomórkowe stężenia DHLA, jak również szybką metylację jednej lub obu sulfhydrylów, szybkie utlenianie łańcucha bocznego do krótszych metabolitów i szybki wypływ z komórki. Chociaż zarówno DHLA, jak i LA znaleziono wewnątrz komórek po podaniu, większość wewnątrzkomórkowego DHLA prawdopodobnie istnieje jako mieszane dwusiarczki z różnymi resztami cysteiny z białek cytozolowych i mitochondrialnych. Ostatnie odkrycia sugerują, że efekty terapeutyczne i przeciwstarzeniowe wynikają z modulacji transdukcji sygnału i transkrypcji genów, które poprawiają stan antyoksydacyjny komórki. Jednak prawdopodobnie dzieje się to poprzez mechanizmy prooksydacyjne, a nie przez działanie radykalne lub redukujące.
Wszystkie formy disiarczkowe LA (R/S-LA, RLA i SLA) można zredukować do DHLA, chociaż w układach modelowych donoszono o redukcji zarówno swoistej tkankowo, jak i stereoselektywnej (preferowanie jednego enancjomeru względem drugiego). Co najmniej dwa enzymy cytozolowe, reduktaza glutationowa (GR) i reduktaza tioredoksynowa (Trx1) oraz dwa enzymy mitochondrialne, dehydrogenaza lipoamidowa i reduktaza tioredoksynowa (Trx2), redukują LA. SLA jest stereoselektywnie redukowany przez cytozolowy GR, podczas gdy Trx1, Trx2 i dehydrogenaza lipoamidowa stereoselektywnie redukują RLA. Kwas ( R )-(+)-liponowy jest enzymatycznie lub chemicznie redukowany do kwasu ( R )-(-)-dihydroliponowego, podczas gdy kwas ( S )-(-)-liponowy jest redukowany do kwasu ( S )-(+)-dihydroliponowego . Kwas dihydroliponowy (DHLA) może również tworzyć się wewnątrzkomórkowo i zewnątrzkomórkowo poprzez nieenzymatyczne reakcje wymiany tiolowo -dwusiarczkowej .
RLA może działać in vivo jak witamina B, a w wyższych dawkach jak składniki odżywcze pochodzenia roślinnego, takie jak kurkumina , sulforafan , resweratrol i inne substancje odżywcze, które indukują enzymy detoksykacji fazy II , działając w ten sposób jako środki cytoochronne. Ta reakcja na stres pośrednio poprawia zdolność antyoksydacyjną komórki.
Wykazano, że ( S )-enancjomer LA jest toksyczny po podaniu szczurom z niedoborem tiaminy.
Kilka badań wykazało , że SLA ma niższą aktywność niż RLA lub zakłóca specyficzne działanie RLA poprzez hamowanie kompetycyjne .
Zastosowania
R/S-LA i RLA są szeroko dostępne jako dostępne bez recepty suplementy diety w Stanach Zjednoczonych w postaci kapsułek, tabletek i płynów wodnych i są sprzedawane jako przeciwutleniacze .
Chociaż organizm może syntetyzować LA, może być również wchłaniany z diety. Suplementacja diety w dawkach od 200 do 600 mg prawdopodobnie zapewni nawet 1000-krotność ilości dostępnej w regularnej diecie. Wchłanianie przewodu pokarmowego jest zmienne i zmniejsza się wraz ze spożywaniem pokarmu. Dlatego zaleca się, aby dietetyczny LA był przyjmowany 30–60 minut przed lub co najmniej 120 minut po posiłku. Maksymalny poziom LA we krwi osiąga się 30-60 minut po suplementacji diety i uważa się, że jest on w dużej mierze metabolizowany w wątrobie.
W Niemczech LA jest zatwierdzony jako lek do leczenia neuropatii cukrzycowej od 1966 roku i jest dostępny bez recepty.
Badania kliniczne
Według American Cancer Society z 2013 roku „nie ma obecnie wiarygodnych dowodów naukowych, że kwas liponowy zapobiega rozwojowi lub rozprzestrzenianiu się raka”. Od 2015 r. dożylnie podawany ALA nie jest zatwierdzony nigdzie na świecie z wyjątkiem Niemiec w neuropatii cukrzycowej , ale w czterech badaniach klinicznych udowodniono, że jest dość bezpieczny i skuteczny; jednak inna duża próba trwająca cztery lata nie wykazała różnicy w porównaniu z placebo. Od 2012 roku nie było dobrych dowodów na to, że kwas alfa-liponowy pomaga osobom z zaburzeniami mitochondrialnymi . W przeglądzie z 2018 r. zalecono ALA jako suplement przeciw otyłości w niskiej dawce (<600 mg/dzień) przez krótki okres czasu (<10 tygodni); jest jednak zbyt kosztowny, aby mógł być praktycznym uzupełnieniem terapii otyłości.
Inne kwasy liponowe
- Kwas β-liponowy jest tiosulfinianem kwasu α-liponowego
Bibliografia
Zewnętrzne linki
-
 Multimedia związane z kwasem liponowym w Wikimedia Commons
Multimedia związane z kwasem liponowym w Wikimedia Commons
