Niraparyb - Niraparib
 | |
| Dane kliniczne | |
|---|---|
| Wymowa |
/ N ɪ r ć p ə R ɪ b / nih- RAP -uh żebra |
| Nazwy handlowe | Zejula |
| Inne nazwy | MK-4827 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a617007 |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Ustami |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | 73% |
| Wiązanie białek | 83% |
| Metabolizm | Karboksyesterazy |
| Metabolity | M1 ( kwas karboksylowy ) |
| Okres półtrwania eliminacji | 36 godzin |
| Wydalanie | 48% moczu, 29% kału |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.210.548 |
| Dane chemiczne i fizyczne | |
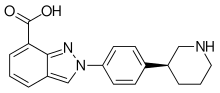
| Formuła | C 19 H 20 N 4 O |
| Masa cząsteczkowa | 320,396 g·mol -1 |
| Model 3D ( JSmol ) | |
| Rozpuszczalność w wodzie | 0,7–1,1 |
| |
| |
Niraparib , sprzedawany pod marką Zejula , jest lekiem przeciwnowotworowym stosowanym w leczeniu nabłonkowego raka jajnika, jajowodu lub pierwotnego raka otrzewnej. Jest przyjmowany doustnie .
Najczęstsze działania niepożądane to nudności (mdłości), małopłytkowość (mała liczba płytek krwi), zmęczenie i osłabienie, niedokrwistość (mała liczba czerwonych krwinek), zaparcia , wymioty , ból brzucha (brzucha), neutropenia (niski poziom neutrofili, rodzaj białych krwinek), bezsenność (trudności ze snem), ból głowy, brak apetytu, biegunka , duszność (trudności w oddychaniu), nadciśnienie (wysokie ciśnienie krwi), ból pleców, zawroty głowy, kaszel, ból stawów, uderzenia gorąca i zmniejszenie białe krwinki.
Niraparyb został dopuszczony do użytku medycznego w Stanach Zjednoczonych i Unii Europejskiej w 2017 roku.
Zastosowania medyczne
Niraparyb jest wskazany w leczeniu podtrzymującym dorosłych z nawrotowym nabłonkowym rakiem jajnika , jajowodu lub pierwotnym rakiem otrzewnej , u których występuje całkowita lub częściowa odpowiedź na chemioterapię opartą na związkach platyny .
W październiku 2019 r. wskazanie do stosowania niraparybu zostało rozszerzone o osoby z zaawansowanym rakiem jajnika, jajowodu lub pierwotnym rakiem otrzewnej leczonych trzema lub więcej wcześniejszymi schematami chemioterapii i których nowotwór jest związany z dodatnim statusem niedoboru rekombinacji homologicznej (HRD). HRD definiuje się jako szkodliwą lub podejrzewaną szkodliwą mutację BRCA lub niestabilność genomową u pacjentów z progresją choroby po ponad sześciu miesiącach od odpowiedzi na ostatnią chemioterapię opartą na platynie.
W kwietniu 2020 r. wskazanie do stosowania niraparybu zostało rozszerzone o leczenie podtrzymujące dorosłych z zaawansowanym nabłonkowym rakiem jajnika, jajowodu lub pierwotnym rakiem otrzewnej, u których występuje całkowita lub częściowa odpowiedź na chemioterapię pierwszego rzutu opartą na związkach platyny.
W Unii Europejskiej niraparyb jest wskazany: w monoterapii w leczeniu podtrzymującym dorosłych z zaawansowanym nabłonkiem (stadium III i IV wg FIGO) wysokim stopniem złośliwości jajnika, jajowodu lub pierwotnym rakiem otrzewnej, u których wystąpiła odpowiedź (całkowita lub częściowa) po zakończeniu leczenia chemioterapia pierwszego rzutu oparta na platynie; oraz w monoterapii w leczeniu podtrzymującym dorosłych z wrażliwym na platynę nawracającym surowiczym nabłonkowym rakiem jajnika, jajowodu lub pierwotnym rakiem otrzewnej o wysokim stopniu złośliwości, którzy są w odpowiedzi (całkowitej lub częściowej) na chemioterapię opartą na platynie.
Przeciwwskazania
W informacjach o przepisaniu nie ma żadnych przeciwwskazań.
Skutki uboczne
Najczęstszymi działaniami niepożądanymi w badaniach była mała liczba krwinek, a mianowicie małopłytkowość (u 61% pacjentów, ciężka u 29%), niedokrwistość (u 50%, ciężka u 25%) i neutropenia (u 30%, ciężka u 20%). ). Inne, przeważnie łagodne do umiarkowanych działania niepożądane obejmowały nudności , zmęczenie i zaparcia . W badaniu trwającym ponad 250 dni ( mediana ) 15% pacjentów musiało na stałe odstawić niraparyb z powodu działań niepożądanych.
Interakcje
Nie przeprowadzono badań interakcji klinicznych. Potencjał interakcji z innymi lekami jest niski , ponieważ niraparyb i jego główny metabolit M1 nie wchodzą w znaczące interakcje z żadnym z ważnych enzymów wątrobowych cytochromu P450 in vitro . Niraparyb, ale nie M1, jest transportowany przez glikoproteinę P i BCRP , ale nie hamuje ich znacząco. Ani niraparyb, ani M1 nie oddziałują znacząco z innymi ważnymi białkami transportowymi.
Farmakologia
Mechanizm akcji
Niraparyb jest inhibitorem enzymów PARP1 i PARP2 .
Farmakokinetyka
73% spożytego niraparybu wchłania się w jelitach i osiąga najwyższe stężenie w osoczu krwi po około trzech godzinach, niezależnie od przyjmowania pokarmu. W krążeniu 83% substancji wiąże się z białkami osocza . Jest inaktywowany przez karboksyloesterazy do głównego metabolitu M1, pochodnej kwasu karboksylowego , który jest następnie glukuronidowany .
Średni biologiczny okres półtrwania wynosi 36 godzin. 47,5% substancji znajduje się w moczu, a 38,8% w kale. Niezmetabolizowany niraparyb stanowi 11% w moczu i 19% w kale.
Chemia
Lek stosuje się w postaci monohydratu tosylanu niraparybu , który ma białe lub prawie białe, niehigroskopijne kryształy.
Studia
Badanie linii komórkowej z 2012 r. wykazało, że inhibitory PARP wykazują działanie cytotoksyczne nie oparte wyłącznie na enzymatycznym hamowaniu PARP, ale poprzez wychwytywanie PARP na uszkodzonym DNA, a siła tej aktywności wychwytywania została uporządkowana jako niraparyb >> olaparyb >> weliparyb .
Historia
Niraparib otrzymał oznaczenie przyspieszone przez amerykańską Agencję ds. Żywności i Leków (FDA), a Tesaro złożyło nowy wniosek o lek w 2016 r. Został on zatwierdzony 27 marca 2017 r. w USA i zatwierdzony w Unii Europejskiej 16 listopada 2017 r.
W badaniu z udziałem 553 pacjentów czas przeżycia wolny od progresji choroby (PFS) u pacjentów ze szkodliwą lub podejrzeniem szkodliwej mutacji BRCA w linii zarodkowej wynosił 21,0 miesięcy w grupie otrzymującej niraparyb w porównaniu z 5,5 miesiąca w grupie placebo . Pacjenci bez takiej mutacji mieli PFS 9,3 miesiąca w grupie niraparybu w porównaniu z 3,9 miesiąca w grupie placebo.
Amerykańska Agencja ds. Żywności i Leków (FDA) zatwierdziła wniosek o przyspieszoną ścieżkę niraparybu , przegląd priorytetowy , przełomową terapię i oznaczenie leku sierocego .
Bibliografia
Zewnętrzne linki
- „Niraparyb” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Tosylan niraparybu” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.
- „Monohydrat tosylanu niraparybu” . Słownik leków NCI . Narodowy Instytut Raka.
- „Monohydrat tosylanu niraparybu” . Narodowy Instytut Raka . 14 kwietnia 2017 r.
