Rywaroksaban - Rivaroxaban
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Xarelto, inni |
| Inne nazwy | ZATOKA 59-7939 |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a611049 |
| Dane licencyjne | |
Kategoria ciąży |
|
| Drogi administracji |
Ustami |
| Kod ATC | |
| Status prawny | |
| Status prawny | |
| Dane farmakokinetyczne | |
| Biodostępność | 80–100%; Cmax = 2–4 godziny (10 mg doustnie) |
| Metabolizm | Mechanizmy niezależne od CYP3A4 , CYP2J2 i CYP |
| Okres półtrwania eliminacji | 5–9 godzin u zdrowych osób w wieku od 20 do 45 |
| Wydalanie | 2/3 metabolizowany w wątrobie i 1/3 wyeliminowane bez zmian |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| CZEBI | |
| CHEMBL | |
| Ligand PDB | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.210.589 |
| Dane chemiczne i fizyczne | |
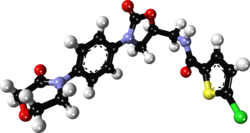
| Formuła | C 19 H 18 Cl N 3 O 5 S |
| Masa cząsteczkowa | 435,88 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
|
| |
Rywaroksaban , sprzedawany między innymi pod marką Xarelto , jest lekiem przeciwzakrzepowym (rozrzedzaczem krwi) stosowanym w leczeniu i zapobieganiu zakrzepom krwi . W szczególności jest stosowany w leczeniu zakrzepicy żył głębokich i zatorowości płucnej oraz zapobieganiu zakrzepom krwi w migotaniu przedsionków i po operacjach stawu biodrowego lub kolanowego. Jest przyjmowany doustnie .
Częste działania niepożądane obejmują krwawienie. Inne poważne działania niepożądane mogą obejmować krwiak kręgosłupa i anafilaksję . Nie jest jasne, czy stosowanie w ciąży i karmieniu piersią jest bezpieczne. W porównaniu do warfaryny ma mniej interakcji z innymi lekami . Działa poprzez blokowanie aktywności białkowego czynnika krzepnięcia Xa .
Rivaroxaban został opatentowany w 2007 r. i dopuszczony do użytku medycznego w Stanach Zjednoczonych w 2011 r. W Stanach Zjednoczonych nie będzie dostępny jako lek generyczny do 2024 r. Znajduje się na liście podstawowych leków Światowej Organizacji Zdrowia . W 2019 roku był to 91. najczęściej przepisywany lek w Stanach Zjednoczonych, z ponad 8 milionami recept.
Zastosowania medyczne
U osób z niezastawkowym migotaniem przedsionków wydaje się być tak samo skuteczny jak warfaryna w zapobieganiu udarom niedokrwiennym i zatorom. Rywaroksaban wiąże się z mniejszą częstością występowania poważnych i śmiertelnych krwawień niż warfaryna, chociaż rywaroksaban wiąże się z większą częstością krwawień z przewodu pokarmowego .
W lipcu 2012 r. brytyjski Narodowy Instytut Zdrowia i Doskonałości Klinicznej zalecił riwaroksaban w zapobieganiu i leczeniu żylnej choroby zakrzepowo-zatorowej .
Przeciwwskazania
Ze względu na trudności związane z opanowaniem krwawienia, rywaroksaban należy odstawić co najmniej 24 godziny przed zabiegiem chirurgicznym, a następnie wznowić natychmiast po uzyskaniu odpowiedniej hemostazy .
Zalecenia dotyczące dawkowania nie zalecają podawania rywaroksabanu z lekami, o których wiadomo, że są silnymi złożonymi inhibitorami CYP3A4 / P-glikoproteiny , ponieważ powoduje to znacznie wyższe stężenia rywaroksabanu w osoczu.
Niekorzystne skutki
Najpoważniejszym działaniem niepożądanym jest krwawienie , w tym ciężkie krwawienie wewnętrzne . Rywaroksaban wiąże się z mniejszą częstością występowania poważnych i śmiertelnych krwawień niż warfaryna, ale wiąże się z większą częstością krwawień z przewodu pokarmowego . Podczas gdy środek odwracający działanie riwaroksabanu jest już dostępny ( Andexanet alfa / AndexXa ); jego bezpieczeństwo i skuteczność nie są tak dobrze ustalone, jak środki odwracające działanie starszego antykoagulanta, warfaryny ( koncentrat witaminy K i kompleksu protrombiny ), co oznacza, że poważne krwawienie może być trudniejsze do opanowania.
Od 2015 r. oceny po wprowadzeniu do obrotu wykazały toksyczne działanie na wątrobę i potrzebne są dalsze badania w celu ilościowego określenia tego ryzyka. Lek jest przeciwwskazany u osób ze znaczną chorobą wątroby i schyłkową niewydolnością nerek, u których lek nie był testowany.
Rywaroksaban zawiera ostrzeżenie w pudełku, aby wyjaśnić, że osoby stosujące lek nie powinny przerywać go przed rozmową z lekarzem, ponieważ przedwczesne odstawienie może zwiększyć ryzyko udaru.
W 2015 r. rywaroksaban stanowił największą liczbę zgłoszonych przypadków poważnych obrażeń wśród regularnie monitorowanych leków w Systemie Zgłaszania Zdarzeń Niepożądanych (AERS) FDA.
Różne badania wskazują, że apiksaban ma przewagę nad rywaroksabanem.
Środek odwrócenia
W październiku 2014 r. firma Portola Pharmaceuticals zakończyła badania kliniczne fazy I i II nad andeksanetem alfa jako antidotum na inhibitory czynnika Xa z kilkoma działaniami niepożądanymi i rozpoczęła badania fazy III. Oczekiwano, że andexanet alfa zostanie zatwierdzony w 2016 roku. Andexanet alfa został zatwierdzony przez amerykańską Agencję ds. Żywności i Leków w maju 2018 roku pod nazwą handlową AndexXa .
Mechanizm akcji
Rywaroksaban hamuje zarówno wolny czynnik Xa, jak i czynnik Xa związane w kompleksie protrombinazy . Jest to wysoce selektywny bezpośredni inhibitor czynnika Xa o szybkim początku działania. Hamowanie czynnika Xa przerywa wewnętrzny i zewnętrzny szlak kaskady krzepnięcia krwi , hamując zarówno tworzenie trombiny, jak i rozwój zakrzepów. Rywaroksaban nie hamuje trombiny (aktywowanego czynnika II) i nie wykazano żadnego wpływu na płytki krwi . Umożliwia przewidywalne dostosowanie antykoagulacji i dawki oraz rutynowe monitorowanie krzepnięcia; ograniczenia dietetyczne nie są potrzebne.
Niefrakcjonowanej heparyny (heparyny niefrakcjonowanej), heparyny o niskiej masie cząsteczkowej (LMWH) i fondaparynuks również hamują aktywność czynnika Xa, pośrednio, poprzez wiązanie się z obiegowym antytrombiny (AT III) i musi być podawany, podczas gdy aktywny ustnej warfarynę , fenprokumonem i acenokumarol są antagonistami witaminy K (VKA), obniżającymi szereg czynników krzepnięcia, w tym czynnik X .
Rywaroksaban ma przewidywalną farmakokinetykę u szerokiego spektrum pacjentów (wiek, płeć, masa ciała, rasa) i ma stałą odpowiedź na dawkę w ośmiokrotnym zakresie dawek (5-40 mg). Biodostępność po podaniu doustnym zmniejsza się wraz z wyższymi dawkami i wzrasta, gdy przyjmuje się ją z jedzeniem.
Chemia
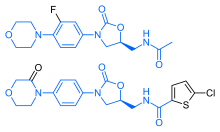
Rywaroksaban wykazuje uderzające podobieństwo strukturalne do antybiotyku linezolid : oba leki mają tę samą strukturę rdzenia, pochodną oksazolidynonu . W związku z tym rywaroksaban badano pod kątem wszelkich możliwych działań przeciwdrobnoustrojowych oraz możliwości toksyczności mitochondrialnej , która jest znanym powikłaniem długotrwałego stosowania linezolidu. Badania wykazały, że ani rywaroksaban, ani jego metabolity nie mają żadnego działania antybiotycznego na bakterie Gram-dodatnie . Jeśli chodzi o toksyczność mitochondrialną, badania in vitro opublikowane przed 2008 r. wykazały, że ryzyko jest niskie.
Historia
Rivaroxaban został początkowo opracowany przez firmę Bayer . W Stanach Zjednoczonych jest sprzedawany przez Janssen Pharmaceutica (część Johnson & Johnson ). Jest to pierwszy dostępny aktywny bezpośredni inhibitor czynnika Xa przyjmowany doustnie.
Społeczeństwo i kultura
Ekonomia
Według Express Scripts Holding Co, największego amerykańskiego menedżera świadczeń aptecznych, stosowanie riwaroksabanu zamiast warfaryny kosztuje 70 razy więcej . Według stanu na 2016 r. Bayer twierdził, że lek jest licencjonowany w 130 krajach i że leczono ponad 23 miliony pacjentów.
Aprobata
We wrześniu 2008 r. Health Canada przyznało pozwolenie na dopuszczenie do obrotu rywaroksabanu w celu zapobiegania żylnej chorobie zakrzepowo-zatorowej (ŻChZZ) u osób, które przeszły planową operację całkowitej alloplastyki stawu biodrowego lub stawu kolanowego .
W tym samym miesiącu Komisja Europejska przyznała również pozwolenie na dopuszczenie do obrotu rywaroksabanu w celu zapobiegania żylnej chorobie zakrzepowo-zatorowej u osób dorosłych poddawanych planowej alloplastyce stawu biodrowego i kolanowego.
1 lipca 2011 r. Amerykańska Agencja ds. Żywności i Leków (US FDA) zatwierdziła rywaroksaban do profilaktyki zakrzepicy żył głębokich (DVT), która może prowadzić do zatorowości płucnej (PE) u dorosłych poddawanych operacji wymiany stawu biodrowego i kolanowego.
4 listopada 2011 r. amerykańska FDA zatwierdziła riwaroksaban do zapobiegania udarom mózgu u osób z niezastawkowym migotaniem przedsionków .
Działania prawne
25 marca 2019 r. ponad 25 000 spraw sądowych dotyczących riwaroksabanu w USA zostało rozstrzygniętych na kwotę 775 milionów dolarów, aby wypłacić poszkodowanym. Powodowie zarzucili producentom leków, że nie ostrzegali o ryzyku krwawienia, twierdząc, że ich urazom można było zapobiec, gdyby lekarze i pacjenci otrzymali odpowiednie informacje.
Badania
Badacze z Duke Clinical Research Institute zostali oskarżeni o ukrywanie danych klinicznych wykorzystywanych do oceny rywaroksabanu. Duke przetestował riwaroksaban w badaniu klinicznym znanym jako badanie ROCKET AF. Badanie kliniczne, opublikowane w 2011 roku w New England Journal of Medicine i kierowane przez Roberta Califfa , ówczesnego komisarza FDA, wykazało, że riwaroksaban jest skuteczniejszy niż warfaryna w zmniejszaniu prawdopodobieństwa udaru niedokrwiennego u pacjentów z migotaniem przedsionków. Ważność badania została zakwestionowana w 2014 r., kiedy sponsorzy farmaceutyczni Bayer i Johnson & Johnson ujawnili, że używane urządzenia do monitorowania krwi INRatio nie działały prawidłowo. Późniejsza analiza zespołu Duke'a opublikowana w lutym 2016 r. wykazała, że nie miało to znaczącego wpływu na skuteczność i bezpieczeństwo w badaniu.
Stwierdzono niedostateczną reprezentację mniejszości rasowych w badaniach klinicznych. W porównaniu z warfaryną skuteczność i bezpieczeństwo okazały się podobne we wszystkich podgrupach rasowych.
Bibliografia
Zewnętrzne linki
- „Rywaroksaban” . Portal informacyjny o narkotykach . Narodowa Biblioteka Medyczna Stanów Zjednoczonych.