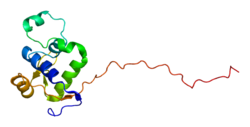
Helikaza zespołu Wernera - Werner syndrome helicase
Helikaza zależna od ATP , znana również jako helikaza DNA, typu RecQ-like typu 3 , jest enzymem, który u ludzi jest kodowany przez gen WRN . WRN jest członkiem rodziny RecQ Helicase . Enzymy helikazy zazwyczaj rozwijają i oddzielają dwuniciowy DNA . Czynności te są konieczne, zanim DNA będzie mogło zostać skopiowane w ramach przygotowań do podziału komórki ( replikacja DNA ). Enzymy helikazy mają również kluczowe znaczenie dla stworzenia planu genu do produkcji białek, procesu zwanego transkrypcją . Dalsze dowody sugerują, że białko Wernera odgrywa kluczową rolę w naprawie DNA . Ogólnie rzecz biorąc, białko to pomaga utrzymać strukturę i integralność DNA danej osoby.
Gen WRN znajduje się na krótkim (p) ramieniu chromosomu 8 pomiędzy pozycjami 12 i 11.2, od pary zasad 31,010,319 do pary zasad 31,150,818.
Struktura i funkcja
WRN jest członkiem rodziny RecQ Helicase . Jest to jedyna Helicase RecQ, która zawiera aktywność egzonukleazy od 3' do 5' . Te aktywności egzonukleazy obejmują degradację zagłębionych końców 3' i inicjację degradacji DNA z luki w dsDNA. WRN jest ważny w naprawie pęknięć dwuniciowych przez rekombinację homologiczną lub łączenie niehomologicznych końców , naprawę uszkodzeń pojedynczego nukleotydu przez naprawę przez wycinanie zasad i jest skuteczny w odzyskiwaniu zatrzymania replikacji. WRN może być również ważny w utrzymywaniu i replikacji telomerów, zwłaszcza replikacji sekwencji bogatych w G.
WRN jest oligomerem, który może działać jako monomer podczas rozwijania DNA, ale jako dimer w roztworze lub tetramer, gdy jest skompleksowany z DNA, i był również obserwowany w postaciach tetramerycznych i heksamerycznych. Dyfuzja WRN została zmierzona do 1,62 w nukleoplazmie i 0,12 w jąderkach. Ortologi WRN znaleziono w wielu innych organizmach, w tym Drosophila , Xenopus i C. elegans . WRN jest ważny dla stabilności genomu, a komórki z mutacjami WRN są bardziej podatne na uszkodzenia i pęknięcia DNA.
Aminowy z WRN uczestniczy zarówno helikazy i nukleazą działania, natomiast karboksylowym współdziała z p53 , ważnym supresorowego. WRN może działać jako egzonukleaza w naprawie, rekombinacji lub replikacji DNA, a także w rozdzielaniu drugorzędowych struktur DNA. Bierze udział w migracji gałęzi na połączeniach Holliday i oddziałuje z innymi pośrednikami replikacji DNA. mRNA kodujący WRN został zidentyfikowany w większości tkanek ludzkich.
Modyfikacja potranslacyjna
Fosforylacja WRN w serynie/treoninie hamuje aktywność helikazy i egzonukleazy, które są ważne dla naprawy DNA po replikacji. Defosforylacja w tych miejscach wzmaga aktywność katalityczną WRN. Fosforylacja może wpływać na inne modyfikacje potranslacyjne, w tym sumoilację i acetylację.
Metylacja WRN powoduje wyłączenie genu. To hamuje produkcję białka WRN i jego funkcje w naprawie DNA.
Znaczenie kliniczne
Zespół Wernera jest spowodowany mutacjami w genie WRN. Wiadomo, że ponad 20 mutacji w genie WRN powoduje zespół Wernera. Wiele z tych mutacji powoduje nieprawidłowo skrócone białko Wernera. Dowody sugerują, że zmienione białko nie jest transportowane do jądra komórkowego , gdzie normalnie oddziałuje z DNA. To skrócone białko może być również zbyt szybko rozkładane, co prowadzi do utraty białka Wernera w komórce. Bez normalnego białka Wernera w jądrze komórki nie mogą wykonywać zadań replikacji, naprawy i transkrypcji DNA. Naukowcy wciąż ustalają, w jaki sposób te mutacje powodują pojawienie się przedwczesnego starzenia obserwowanego w zespole Wernera.
Role WRN w ścieżkach naprawy DNA
Naprawa homologiczna rekombinacyjna
WRN jest aktywny w rekombinacji homologicznej . Komórki uszkodzone w genie WRN wykazują 23-krotne zmniejszenie spontanicznej rekombinacji mitotycznej, ze szczególnym niedoborem zdarzeń typu konwersji. Komórki z uszkodzonym WRN , wystawione na promieniowanie rentgenowskie, mają więcej pęknięć chromosomów i mikrojąder niż komórki z WRN typu dzikiego. Komórki uszkodzone w genie WRN nie są bardziej wrażliwe niż komórki typu dzikiego na promieniowanie gamma, światło UV, 4-6 cyklobutanopirymidyny czy mitomycynę C, ale są wrażliwe na inhibitory topoizomerazy typu I i typu II. Odkrycia te sugerują, że białko WRN bierze udział w homologicznej naprawie rekombinacyjnej i przetwarzaniu zablokowanych widełek replikacyjnych.
Łączenie końców niehomologicznych
WRN odgrywa ważną rolę w naprawie DNA z niehomologicznym łączeniem końców (NHEJ). Jak wykazali Shamanna i wsp., WRN jest rekrutowany do pęknięć dwuniciowych (DSB) i uczestniczy w NHEJ z jego funkcjami enzymatycznymi i nieenzymatycznymi. W DSB, w połączeniu z Ku (białkiem) , promuje standardowe lub kanoniczne NHEJ (c-NHEJ), naprawiając dwuniciowe pęknięcia w DNA z jego funkcjami enzymatycznymi i ze sporym stopniem dokładności. WRN hamuje alternatywną formę NHEJ, zwaną alt-NHEJ lub łączenie końców za pośrednictwem mikrohomologii (MMEJ). MMEJ jest niedokładnym sposobem naprawy pęknięć dwuniciowych.
Naprawa przez wycięcie bazy
WRN odgrywa rolę w naprawie DNA przez wycinanie zasad (BER). Jak wykazali Das i wsp., WRN wiąże się z NEIL1 we wczesnym etapie wykrywania uszkodzeń BER. WRN stymuluje NEIL1 w wycinaniu zmian oksydacyjnych. NEIL1 to glikozylaza DNA, która inicjuje pierwszy etap w BER poprzez rozszczepienie zasad uszkodzonych przez reaktywne formy tlenu (ROS) i wprowadzenie przerwania nici DNA poprzez aktywność liazy związaną z NEIL1. NEIL1 rozpoznaje (celuje) i usuwa niektóre uszkodzone przez ROS zasady, a następnie nacina miejsce abasowe poprzez eliminację β,δ, pozostawiając końce fosforanowe 3′ i 5′. NEIL1 rozpoznaje utlenione pirymidyny , formamidopirymidyny, reszty tyminy utlenione na grupie metylowej i oba stereoizomery glikolu tyminy .
WRN uczestniczy również w BER poprzez interakcję z Polλ . WRN wiąże się z domeną katalityczną Polλ i specyficznie stymuluje wypełnianie luk DNA przez Polλ ponad 8-okso-G, a następnie następuje synteza wypierania nici. Pozwala to WRN na promowanie syntezy naprawy długich fragmentów DNA przez Polλ podczas zainicjowanej przez MUTYH naprawy błędnych par 8-okso-G:A.
Odzyskiwanie zatrzymania replikacji
WRN jest również zaangażowany w odzyskiwanie po zatrzymaniu replikacji. Jeśli WRN jest uszkodzony, zatrzymanie replikacji powoduje akumulację DSB i zwiększoną fragmentację chromosomów. Jak wykazali Pichierri i wsp., WRN oddziałuje z kompleksem RAD9 - RAD1 - HUS1 (9.1.1), jednym z głównych czynników punktu kontrolnego replikacji. W tej interakcji pośredniczy wiązanie podjednostki RAD1 z regionem N-końcowym WRN i ma zasadnicze znaczenie dla relokalizacji WRN do ognisk jądrowych i jego fosforylacji w odpowiedzi na zatrzymanie replikacji. (W przypadku braku uszkodzenia DNA lub zatrzymania widełek replikacyjnych, białko WRN pozostaje zlokalizowane w jąderkach.) Interakcja WRN z kompleksem 9.1.1 skutkuje zapobieganiem tworzeniu się DSB w zablokowanych widełkach replikacyjnych.
Niedobory WRN w chorobach nowotworowych
Komórki eksprymujące ograniczone ilości WRN mają podwyższone częstotliwości mutacji w porównaniu z komórkami typu dzikiego. Zwiększona mutacja może powodować raka. Pacjenci z zespołem Wernera, z homozygotycznymi mutacjami w genie WRN , mają zwiększoną zapadalność na nowotwory, w tym mięsaki tkanek miękkich, kostniakomięsak, rak tarczycy i czerniak.
Mutacje w WRN są rzadkie w populacji ogólnej. Wskaźnik heterozygotycznej mutacji utraty funkcji w WRN wynosi około jeden na milion. W populacji japońskiej wskaźnik wynosi 6 na 1000, czyli jest wyższy, ale wciąż rzadki.
Defekty mutacyjne w genie WRN są stosunkowo rzadkie w komórkach nowotworowych w porównaniu z częstością zmian epigenetycznych w WRN, które zmniejszają ekspresję WRN i mogą przyczyniać się do karcynogenezy. Sytuacja jest podobna do innych genów naprawy DNA, których ekspresja jest zmniejszona w nowotworach głównie z powodu zmian epigenetycznych, a nie mutacji (patrz Częstość epimutacji w genach naprawy DNA ).
W tabeli przedstawiono wyniki analizy 630 ludzkich guzów pierwotnych pod kątem hipermetylacji wysp CpG WRN . Ta hipermetylacja spowodowała zmniejszoną ekspresję białka WRN, co jest częstym zjawiskiem w onkogenezie.
| Nowotwór | Częstotliwość redukcji raka |
|---|---|
| Rak jelita grubego | 37,9% |
| Niedrobnokomórkowego raka płuca | 37,5% |
| Rak żołądka | 25% |
| Rak prostaty | 20% |
| Rak piersi | 17,2% |
| Rak tarczycy | 12,5% |
| Chłoniak nieziarniczy | 23,7% |
| Ostra białaczka mieloblastyczna | 4,8% |
| Chondrosarcoma | 33,3% |
| kostniakomięsaki | 11,1% |
Interakcje
Wykazano, że helikaza zależna od ATP w zespole Wernera wchodzi w interakcje z:
Bibliografia
Dalsza lektura
- Comai L, Li B (2004). „Białko zespołu Wernera na skrzyżowaniu naprawy DNA i apoptozy” . Mech Aging Dev . 125 (8): 521-8. doi : 10.1016/j.mad.2004.06.004 . PMID 15336909 . S2CID 30529954 .
- Lee JW, Harrigan J, Opresko PL, Bohr VA (2005). „Drogi i funkcje białka zespołu Wernera”. Mech Aging Dev . 126 (1): 79–86. doi : 10.1016/j.mad.2004.09.011 . PMID 15610765 . S2CID 39834357 .
- Monnata RJ Jr; Saintigny Y (2004). „Białko zespołu Wernera – funkcja odwijania w celu wyjaśnienia choroby” (PDF) . Środowisko wiedzy Sci Aging . 2004 (13): re3. doi : 10.1126/sageke.2004.13.re3 . PMID 15056797 .
- Ozgenc A, Loeb LA (2005). „Obecne postępy w rozwikłaniu funkcji białka zespołu Wernera”. Mutat Res . 577 (1–2): 237–51. doi : 10.1016/j.mrfmmm.2005.03.020 . PMID 15946710 .
- Swanson C, Saintigny Y, Emond MJ, Monnat RJ Jr (2004). „Białko zespołu Wernera ma rozdzielne funkcje rekombinacji i przeżycia” (PDF) . Naprawa DNA (Amst) . 3 (5): 475–82. doi : 10.1016/j.dnarep.2004.01.002 . PMID 15084309 .
- Moser MJ, Oshima J, Monnat RJ (1999). „Mutacje WRN w zespole Wernera”. Szum. Mutat . 13 (4): 271–9. doi : 10.1002/(SICI)1098-1004(1999)13:4<271::AID-HUMU2>3.0.CO;2-Q . PMID 10220139 .
- Kastan MB, Lim DS (2001). „Wiele podłoży i funkcji ATM”. Nat. Ks. Mol. Biol komórki . 1 (3): 179–86. doi : 10.1038/35043058 . PMID 11252893 . S2CID 10691352 .
Zewnętrzne linki
- Oshima J, Martin GM, Hisama FM (luty 2012). Zespół Wernera . Uniwersytet Waszyngtoński w Seattle. PMID 20301687 . NBK1514.W Pagon RA, Bird TD, Dolan CR i wsp., wyd. (1993). GeneReviews [Internet] . Seattle WA: University of Washington, Seattle.
- Karta genetyczna
- Baza danych mutacji zespołu Wernera