Hormon steroidowy - Steroid hormone
| Hormon steroidowy | |
|---|---|
| Klasa leków | |

| |
| Identyfikatory klas | |
| Synonimy | Steryd nadnerczy; Steryd gonadalny |
| Posługiwać się | Różny |
| Cel biologiczny | Receptory hormonów steroidowych |
| Klasa chemiczna | Sterydowy ; Niesteroidowy |
| W Wikidanych | |
Hormonów steroidowych jest steroid , który działa jako hormonu . Hormony steroidowe można podzielić na dwie klasy: kortykosteroidy (zwykle wytwarzane w korze nadnerczy , stąd kortyko- ) i steroidy płciowe (zwykle wytwarzane w gonadach lub łożysku ). W ramach tych dwóch klas znajduje się pięć typów, w zależności od receptorów, z którymi się wiążą: glukokortykoidy i mineralokortykosteroidy (oba kortykosteroidy) oraz androgeny , estrogeny i progestageny (sterydy płciowe). Pochodne witaminy D są szóstym, blisko spokrewnionym układem hormonalnym z homologicznymi receptorami. Mają one pewne cechy prawdziwych steroidów jako ligandy receptorów .
Hormony steroidowe pomagają kontrolować metabolizm , stany zapalne , funkcje odpornościowe , równowagę soli i wody , rozwój cech płciowych oraz odporność na urazy i choroby. Termin steryd opisuje zarówno hormony wytwarzane przez organizm, jak i sztucznie wytwarzane leki, które powielają działanie naturalnie występujących steroidów.
Synteza

Naturalne hormony steroidowe są zazwyczaj syntetyzowane z cholesterolu w gonadach i nadnerczach . Te formy hormonów to lipidy . Mogą przechodzić przez błonę komórkową, ponieważ są rozpuszczalne w tłuszczach, a następnie wiązać się z receptorami hormonów steroidowych (które mogą być jądrowe lub cytozolowe w zależności od hormonu steroidowego), aby wywołać zmiany w komórce. Hormony steroidowe są zazwyczaj przenoszone we krwi, związane ze specyficznymi białkami nośnikowymi , takimi jak globulina wiążąca hormony płciowe lub globulina wiążąca kortykosteroidy . Dalsze przemiany i katabolizm zachodzą w wątrobie, w innych tkankach „obwodowych” oraz w tkankach docelowych.
| Seks | Hormon płciowy | Faza reprodukcyjna |
Tempo produkcji krwi |
Szybkość wydzielania gonad |
Wskaźnik klirensu metabolicznego |
Zakres referencyjny (poziomy w surowicy) | |
|---|---|---|---|---|---|---|---|
| Jednostki SI | Nie- SI jednostek | ||||||
| Mężczyźni | Androstendion |
–
|
2,8 mg/dzień | 1,6 mg/dzień | 2200 l/dzień | 2,8-7,3 nmol/L | 80–210 ng/dL |
| Testosteron |
–
|
6,5 mg/dzień | 6,2 mg/dzień | 950 l/dzień | 6,9–34,7 nmol/l | 200–1000 ng/dL | |
| Estrone |
–
|
150 μg/dzień | 110 μg/dzień | 2050 l/dzień | 37–250 pmol/l | 10–70 pg/ml | |
| Estradiol |
–
|
60 μg/dzień | 50 μg/dzień | 1600 l/dzień | <37–210 pmol/l | 10–57 pg/ml | |
| Siarczan estronu |
–
|
80 μg/dzień | Nieistotny | 167 l/dzień | 600–2500 pmol/l | 200–900 pg/ml | |
| Kobiety | Androstendion |
–
|
3,2 mg/dzień | 2,8 mg/dzień | 2000 l/dzień | 3,1–12,2 nmol/l | 89–350 ng/dL |
| Testosteron |
–
|
190 μg/dzień | 60 μg/dzień | 500 l/dzień | 0,7–2,8 nmol/l | 20–81 ng/dL | |
| Estrone | Faza folikularna | 110 μg/dzień | 80 μg/dzień | 2200 l/dzień | 110–400 pmol/l | 30–110 pg/ml | |
| Faza lutealna | 260 μg/dzień | 150 μg/dzień | 2200 l/dzień | 310–660 pmol/l | 80–180 pg/ml | ||
| Po menopauzie | 40 μg/dzień | Nieistotny | 1610 l/dzień | 22–230 pmol/l | 6–60 pg/ml | ||
| Estradiol | Faza folikularna | 90 μg/dzień | 80 μg/dzień | 1200 l/dzień | <37–360 pmol/l | 10-98 pg/ml | |
| Faza lutealna | 250 μg/dzień | 240 μg/dzień | 1200 l/dzień | 699–1250 pmol/l | 190–341 pg/ml | ||
| Po menopauzie | 6 μg/dzień | Nieistotny | 910 l/dzień | <37–140 pmol/l | 10-38 pg/ml | ||
| Siarczan estronu | Faza folikularna | 100 μg/dzień | Nieistotny | 146 l/dzień | 700–3600 pmol/l | 250–1300 pg/ml | |
| Faza lutealna | 180 μg/dzień | Nieistotny | 146 l/dzień | 1100–7300 pmol/l | 400–2600 pg/ml | ||
| Progesteron | Faza folikularna | 2 mg/dzień | 1,7 mg/dzień | 2100 l/dzień | 0,3–3 nmol/l | 0,1–0,9 ng/ml | |
| Faza lutealna | 25 mg/dzień | 24 mg/dzień | 2100 l/dzień | 19–45 nmol/l | 6–14 ng/ml | ||
|
Uwagi i źródła
Uwagi: „ Stężenie steroidu w krążeniu zależy od szybkości, z jaką jest on wydzielany z gruczołów, szybkości metabolizmu prekursora lub prehormonów do steroidu oraz szybkości, z jaką jest on ekstrahowany przez tkanki i metabolizowany. Szybkość wydzielania steroidu odnosi się do całkowitego wydzielania związku z gruczołu w jednostce czasu. Szybkość wydzielania oszacowano przez pobieranie próbek żylnych z gruczołu w czasie i odjęcie stężenia hormonów w tętnicach i żyłach obwodowych. Szybkość klirensu metabolicznego steroidu definiuje się jako objętość krwi, która została całkowicie oczyszczona z hormonu w jednostce czasu. Szybkość produkcji hormonu steroidowego odnosi się do wejścia do krwi związku ze wszystkich możliwych źródeł, w tym wydzielania z gruczołów i konwersji prohormony do sterydu będącego przedmiotem zainteresowania. W stanie stacjonarnym ilość hormonu wchodzącego do krwi ze wszystkich źródeł będzie równa tempu, w jakim jest cl ucha (wskaźnik klirensu metabolicznego) pomnożony przez stężenie we krwi (wskaźnik produkcji = tempo klirensu metabolicznego × stężenie). Jeśli jest niewielki udział metabolizmu prohormonów w krążącej puli sterydów, to tempo produkcji będzie zbliżone do tempa wydzielania." Źródła: patrz szablon.
|
|||||||
Sterydy syntetyczne i sterole
Wymyślono również wiele syntetycznych sterydów i steroli. Większość z nich to steroidy, ale niektóre cząsteczki niesteroidowe mogą wchodzić w interakcje z receptorami steroidowymi ze względu na podobieństwo kształtu. Niektóre sterydy syntetyczne są słabsze lub silniejsze niż sterydy naturalne, których receptory aktywują.
Kilka przykładów syntetycznych hormonów steroidowych:
- Glikokortykosteroidy : alklometazon , prednizon , deksametazon , triamcynolon , kortyzon
- Mineralokortykoid : fludrokortyzon
- Witamina D: dihydrotachysterol
- Androgeny: oxandrolone , oksabolon , nandrolon (znany również jako sterydy anaboliczno-androgenne lub po prostu sterydy anaboliczne )
- Estrogeny: dietylostilbestrol (DES) i etynyloestradiol (EE)
- Progestageny: noretysteronu , octan medroksyprogesteronu , hydroksyprogesteron, kapronian .
Niektórzy antagoniści sterydów:
- Androgen: octan cyproteronu
- Progestyny: mifepriston , gestrinon
Transport
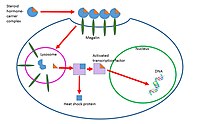
Hormony steroidowe są transportowane przez krew poprzez wiązanie się z białkami nośnikowymi – białkami surowicy, które je wiążą i zwiększają rozpuszczalność hormonów w wodzie. Niektóre przykłady to globulina wiążąca hormony płciowe (SHBG), globulina wiążąca kortykosteroidy i albumina . Większość badań mówi, że hormony mogą wpływać na komórki tylko wtedy, gdy nie są one związane z białkami surowicy. Aby być aktywnym, hormony steroidowe muszą uwolnić się od swoich białek rozpuszczających krew i albo wiązać się z receptorami zewnątrzkomórkowymi, albo biernie przechodzić przez błonę komórkową i wiązać się z receptorami jądrowymi . Ten pomysł jest znany jako hipoteza wolnego hormonu. Ten pomysł pokazano na rysunku 1 po prawej.
Jedno z badań wykazało, że te kompleksy steroid-nośnik są wiązane przez megalinę , receptor błonowy, a następnie są przenoszone do komórek poprzez endocytozę . Jednym z możliwych szlaków jest to, że po wejściu do komórki kompleksy te są przenoszone do lizosomu, gdzie białko nośnikowe ulega degradacji, a hormon steroidowy jest uwalniany do cytoplazmy komórki docelowej. Hormon podąża następnie genomową ścieżką działania. Ten proces pokazano na rysunku 2 po prawej. Rola endocytozy w transporcie hormonów steroidowych nie jest dobrze poznana i jest przedmiotem dalszych badań.
Aby hormony steroidowe mogły przejść przez dwuwarstwę lipidową komórek, muszą pokonać bariery energetyczne, które uniemożliwią im wejście lub wyjście z błony. Energia swobodna Gibbsa jest tutaj ważną koncepcją. Te hormony, które wszystkie pochodzą z cholesterolu, mają hydrofilowe grupy funkcyjne na obu końcach i hydrofobowe szkielety węglowe. Kiedy hormony steroidowe wchodzą do błon, bariery wolnej energii istnieją, gdy grupy funkcyjne wchodzą do hydrofobowego wnętrza błony, ale energetycznie korzystne jest, aby hydrofobowy rdzeń tych hormonów wchodził do dwuwarstw lipidowych. Te bariery energetyczne i studnie są odwrócone dla hormonów wychodzących z błon. Hormony steroidowe łatwo wchodzą i wychodzą z błony w warunkach fizjologicznych. Wykazano eksperymentalnie, że przenikają przez błony z prędkością około 20 μm/s, w zależności od hormonu.
Chociaż energetycznie bardziej korzystne jest, aby hormony znajdowały się w błonie niż w ECF lub ICF, w rzeczywistości opuszczają one błonę po wejściu do niej. Jest to ważna uwaga, ponieważ cholesterol – prekursor wszystkich hormonów steroidowych – nie opuszcza błony, gdy już się w niej osadzi. Różnica między cholesterolem a tymi hormonami polega na tym, że cholesterol znajduje się w znacznie większej ujemnej energii swobodnej Gibba, gdy znajduje się wewnątrz błony, w porównaniu z tymi hormonami. Dzieje się tak, ponieważ ogon alifatyczny na cholesterolu ma bardzo korzystną interakcję z wnętrzem dwuwarstw lipidowych.
Mechanizmy działania i efekty
Istnieje wiele różnych mechanizmów, poprzez które hormony steroidowe wpływają na komórki docelowe. Wszystkie te różne szlaki można sklasyfikować jako mające albo efekt genomowy, albo efekt niegenomowy. Szlaki genomowe są powolne i powodują zmianę poziomów transkrypcji niektórych białek w komórce; szlaki niegenomowe są znacznie szybsze.
Ścieżki genomowe
Pierwszymi zidentyfikowanymi mechanizmami działania hormonów steroidowych były efekty genomowe. W tej ścieżce wolne hormony najpierw przechodzą przez błonę komórkową, ponieważ są rozpuszczalne w tłuszczach. W cytoplazmie steroid może, ale nie musi podlegać zmianom za pośrednictwem enzymów, takim jak redukcja, hydroksylacja lub aromatyzacja. Następnie steryd wiąże się ze specyficznym receptorem hormonu steroidowego , znanym również jako receptor jądrowy , który jest dużą metaloproteiną. Po związaniu steroidów wiele rodzajów receptorów steroidowych ulega dimeryzacji : dwie podjednostki receptora łączą się, tworząc jedną funkcjonalną jednostkę wiążącą DNA , która może wejść do jądra komórkowego. W jądrze kompleks steroid-ligand receptora wiąże się z określonymi sekwencjami DNA i indukuje transkrypcję genów docelowych .
Ścieżki niegenomowe
Ponieważ szlaki niegenomowe obejmują dowolny mechanizm, który nie jest efektem genomowym, istnieją różne szlaki niegenomowe. Jednak we wszystkich tych szlakach pośredniczy pewien rodzaj receptora hormonu steroidowego znajdującego się w błonie komórkowej. Wykazano, że hormony steroidowe mają wpływ na kanały jonowe, transportery, receptory sprzężone z białkiem G (GPCR) i płynność błon. Spośród nich najpowszechniejsze są białka połączone z GPCR. Aby uzyskać więcej informacji na temat tych białek i szlaków, odwiedź stronę dotyczącą receptorów hormonów steroidowych .
Zobacz też
Bibliografia
Dalsza lektura
- Brooka CG (1999). „Mechanizm dojrzewania”. Horm. Res . 51 Suplement 3 (3): 52–4. doi : 10.1159/000053162 . PMID 10592444 .
- Holmes SJ, Shalet SM (1996). „Rola hormonu wzrostu i sterydów płciowych w osiągnięciu i utrzymaniu prawidłowej masy kostnej”. Horm. Res . 45 (1–2): 86–93. doi : 10.1159/000184765 . PMID 8742125 .
- Ottolenghi C, Uda M, Crisponi L, Omari S, Cao A, Forabosco A, Schlessinger D (styczeń 2007). „Determinacja i stabilność płci”. BioEseje . 29 (1): 15–25. doi : 10.1002/bies.20515 . PMID 17187356 .
- Couse JF, Korach KS (czerwiec 1998). „Odkrywanie roli sterydów płciowych poprzez badania myszy z niedoborem receptorów” . J. Mol. Med . 76 (7): 497-511. doi : 10.1007/s001090050244 . PMID 9660168 .
- McEwen BS (1992). „Hormony steroidowe: wpływ na rozwój i funkcjonowanie mózgu”. Horm. Res . 37 Dodatek 3 (3): 1–10. doi : 10.1159/000182393 . PMID 1330863 .
- Simons (sierpień 2008). „działania fizjologiczne a farmakologiczne hormonów steroidowych” . BioEseje . 30 (8): 744–56. doi : 10.1002/bies.20792 . PMC 2742386 . PMID 18623071 .
- Han, Thang S.; Walker, Brian R.; Arlt, Wiebke; Ross, Richard J. (17 grudnia 2013). „Leczenie i wyniki zdrowotne u dorosłych z wrodzonym przerostem nadnerczy”. Recenzje przyrody Endokrynologia . 10 (2): 115–124. doi : 10.1038/nrendo.2013.239 . PMID 24342885 Rycina 2: Szlak steroidogenezy nadnerczy.CS1 maint: postscript ( link )