Kapronian hydroksyprogesteronu - Hydroxyprogesterone caproate
 | |
 | |
| Dane kliniczne | |
|---|---|
| Nazwy handlowe | Delalutin, Proluton, Proluton Depot, Makena, inne |
| Inne nazwy | OHPC; kapronian hydroksyprogesteronu; Heksanian hydroksyprogesteronu; kapronian 17α-hydroksyprogesteronu; 17a-OHPC; kapronian 17-hydroksyprogesteronu; 17-OHPC; 17-HPC; 17α-HPC; HPC; LPCN-1107; 17α-hydroksypregn-4-eno-3,20-dion 17α-heksanian |
| Drogi administracji |
• Wstrzyknięcie domięśniowe • Autowstrzyknięcie podskórne |
| Klasa leków | progestagen ; progestyna ; ester progestagenu ; Antygonadotropina |
| Kod ATC | |
| Dane farmakokinetyczne | |
| Biodostępność |
Doustnie : Bardzo niska (~3% u szczurów) Domięśniowo : 100% (u szczurów) |
| Wiązanie białek | Ekstensywny (na albuminę , nie na CBG lub (prawdopodobnie) SHBG ) |
| Metabolizm | Zmniejszenie i hydroksylowanie (przez CYP3A4 , CYP3A5 , CYP3A7 ) i sprzęgania ( glukuronidacji , sulfatacja , acetylacji ) |
| Okres półtrwania eliminacji | Kobiety niebędące w ciąży: 7,8 dnia Singlet: 16–17 dni Bliźniaki: 10 dni |
| Wydalanie |
Kał : 50% Mocz : 30% |
| Identyfikatory | |
| |
| Numer CAS | |
| Identyfikator klienta PubChem | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| Pulpit nawigacyjny CompTox ( EPA ) | |
| Karta informacyjna ECHA |
100.010.127 |
| Dane chemiczne i fizyczne | |
| Formuła | C 27 H 40 O 4 |
| Masa cząsteczkowa | 428,613 g·mol -1 |
| Model 3D ( JSmol ) | |
| |
| |
| (zweryfikować) | |
Kapronian hydroksyprogesteronu ( OHPC ), sprzedawany między innymi pod markami Proluton i Makena , jest lekiem progestagenowym, który stosuje się w zapobieganiu przedwczesnym porodom u kobiet w ciąży z historią choroby oraz w leczeniu zaburzeń ginekologicznych . Został również opracowany w połączeniu z estrogenami do różnych wskazań (marki Gravibinon i Primosiston ) oraz jako forma długotrwałej kontroli urodzeń w formie zastrzyków (nazwa handlowa Chinese Injectable No. 1 ). Nie stosuje się go doustnie, a zamiast tego podaje się go we wstrzyknięciu do mięśnia lub tkanki tłuszczowej , zazwyczaj raz w tygodniu do raz w miesiącu, w zależności od wskazania.
OHPC jest ogólnie dobrze tolerowany i powoduje niewiele skutków ubocznych . Najczęstszym działaniem niepożądanym OHPC są reakcje w miejscu wstrzyknięcia, takie jak ból i obrzęk . Lek może zwiększać ryzyko cukrzycy ciążowej, gdy jest stosowany u kobiet w ciąży. OHPC jest progesteronu lub syntetycznej progestagen , a więc jest agonistą z receptorem progesteronu The cel biologiczny, progestagenów, takich jak progesteron . Ma pewną aktywność przeciwmineralokortykoidową i nie ma innej ważnej aktywności hormonalnej . Lek wykazuje szereg różnic w stosunku do naturalnego progesteronu .
OHPC został odkryty w 1953 roku i wprowadzony do użytku medycznego w 1954 lub 1955 roku. Był sprzedawany w Stanach Zjednoczonych pod marką Delalutin, aw całej Europie pod marką Proluton. Lek został wycofany w Stanach Zjednoczonych w 1999 roku. Jednak OHPC został następnie ponownie wprowadzony w Stanach Zjednoczonych pod marką Makena do leczenia przedwczesnego porodu w 2011 roku. Ze względu na znacznie wyższą cenę, w tym kraju pojawiły się kontrowersje dotyczące cen . OHPC był wcześniej dostępny po niskich kosztach w aptekach mieszanych w Stanach Zjednoczonych, ale został zakazany w 2016 roku.
Zastosowania medyczne
Przedwczesny poród
Stosowanie OHPC w ciąży w celu zapobiegania porodom przedwczesnym u kobiet z historią porodu przedwczesnego między 20. tygodniem a 36. tygodniem i 6 dniem jest poparte Wytycznymi Kliniki Towarzystwa Medycyny Płodowej Towarzystwa, opublikowanymi w maju 2012 r. jako dowody poziomu I i III, Zalecenie dla kategorii A. Dowody na poziomie I odnoszą się do odpowiednio dobranych randomizowanych badań kontrolowanych , a dowody na poziomie III są poparte opinią ekspertów, podczas gdy zalecenie na poziomie A wskazuje, że zalecenie jest oparte na dobrych i spójnych dowodach naukowych. Zaleca się OHPC 250 mg im. U tych kobiet, jeżeli przezpochwowe USG długość szyjki macicy skraca do <25 mm w <24 tygodni szwu okrężnego mogą być oferowane. W badaniu z 2013 r., na podstawie których oparto zalecenia wytycznych, stwierdzono również znaczne zmniejszenie zachorowalności noworodków, w tym niższy odsetek martwiczego zapalenia jelit (0 w grupie leczonej w porównaniu z 4 w grupie kontrolnej), krwotok dokomorowy (4 w grupie leczonej w porównaniu z 8 w grupie kontrolnej przy względnym ryzyku 0,25) i potrzebie dodatkowego tlenu (14% w grupie leczonej w porównaniu z 24% w grupie placebo przy względnym ryzyku 0,42). Ponadto badanie to obejmowało 463 kobiety, z których 310 otrzymało zastrzyk. Spośród tych kobiet 9 miało niemowlęta z wrodzonymi wadami rozwojowymi (2%), ale nie było spójnego wzorca i żaden nie dotyczył narządów wewnętrznych.
OHPC jest obecnie (stan na czerwiec 2014 r.) kategorią ciąży B, co oznacza, że nie ma dowodów na ryzyko dla płodu przy stosowaniu tego leku podczas ciąży. Chociaż jest to obecnie zalecenie, nie zawsze tak było. Przegląd przeprowadzony przez Marca Keirse z Flinders University wykazał , że brakuje informacji o potencjalnych szkodach. Wszystkie trzy badania kliniczne w ciążach pojedynczych otrzymujących 250 mg/tydzień domięśniowego OHPC wykazały tendencję do wzrostu utraty ciąży z powodu poronienia w porównaniu z placebo. W jednym z nich, w dużym badaniu National Institutes of Health (NIH) z 2003 r., przyjrzano się wpływowi zastrzyków OHPC u kobiet zagrożonych powtórnym przedwczesnym porodem i stwierdzono, że w grupie leczonej przedwczesny poród wystąpił u 37% w porównaniu z 55% w grupie kontrolnej. . Dalsze badanie potomstwa nie wykazało dowodów na to, że OHPC wpływa na dzieci w pierwszych latach życia. Na podstawie tych danych NIH, OHPC został zatwierdzony przez Food and Drug Administration (FDA) w 2011 roku jako lek zmniejszający ryzyko przedwczesnego porodu u wybranych kobiet z grupy ryzyka. (vi)
FDA wyraziła zaniepokojenie poronieniem na posiedzeniu komitetu doradczego w 2006 roku; komisja jednogłośnie głosowała, że potrzebne są dalsze badania, aby ocenić potencjalny związek OHPC ze zwiększonym ryzykiem poronienia w drugim trymestrze i urodzenia martwego dziecka. Badanie toksykologiczne na małpach rezus spowodowało śmierć wszystkich płodów rezusów narażonych na 1 i 10 razy równoważnik dawki OHPC stosowanej u ludzi. Od 2008 r. OHPC był progestynem kategorii D według FDA (to znaczy, że istnieją dowody na uszkodzenie płodu). Istnieją spekulacje, że olej rycynowy w preparacie OHPC może nie być korzystny dla ciąży. Warto zwrócić uwagę na wspomniane wyżej badanie NEJM przeprowadzone przez Meirsa i in. porównuje działanie OHPC (ze składnikiem oleju rycynowego) do wstrzykiwania oleju rycynowego jako placebo.
W badaniu opublikowanym w lutym 2016 r. w The Lancet stwierdzono między innymi następujące wyniki:
OPPTIMUM silnie sugeruje, że skuteczność progesteronu w poprawie wyników jest albo nieistniejąca, albo słaba. Biorąc pod uwagę heterogeniczność zespołu porodu przedwczesnego, nie możemy wykluczyć korzyści w określonych fenotypowych lub genotypowych podgrupach kobiet zagrożonych. Wydaje się jednak, że podgrupy kobiet, które mogą odnieść korzyści, nie są łatwe do zidentyfikowania za pomocą obecnych strategii selekcji, w tym pomiaru długości szyjki macicy i badania fibronektyny. Uspokajająco, nasze badanie sugeruje, że progesteron jest bezpieczny dla tych, którzy chcą go przyjmować w profilaktyce przedwczesnego porodu. Ogólny odsetek zdarzeń niepożądanych u matki lub dziecka był podobny w grupach progesteronu i placebo. Niewiele było różnic w częstości występowania niekorzystnych drugorzędowych punktów końcowych w obu grupach, z wyjątkiem wyższego odsetka powikłań nerkowych, żołądkowo-jelitowych i oddechowych w dzieciństwie w grupach progesteronu. Co ważne, bezwzględny odsetek tych powikłań był niski. Obserwacja innych dzieci narażonych in utero na progesteron dopochwowy byłaby pomocna w ustaleniu, czy zwiększona częstość niektórych powikłań nerkowych, żołądkowo-jelitowych i oddechowych jest rzeczywistym skutkiem, czy błędem typu I.
Recenzent czasopisma Richard Lehman, starszy pracownik naukowy w Departamencie Podstawowej Opieki Zdrowotnej na Uniwersytecie Oksfordzkim, skomentował badanie OPPTIMUM w następujący sposób: „To wszystko. Ta historia się skończyła i nikt nie musi już używać progesteronu dopochwowego w celu zapobiec przedwczesnemu porodowi."
W przeglądzie Cochrane dotyczącym progestagenu w zapobieganiu porodom przedwczesnym stwierdzono, że istnieje niewiele dowodów na to, że progesteron podawany dopochwowo lub domięśniowo pomagał zmniejszyć ryzyko porodu przedwczesnego u kobiet z ciążą mnogą.
Zaburzenia ginekologiczne
OHPC stosuje się w leczeniu poronienia zagrażającego , zaburzeń ginekologicznych, takich jak bolesne miesiączkowanie , zespół napięcia przedmiesiączkowego , choroba włóknisto-torbielowa piersi , gruczolistość i ból piersi . Ponadto OHPC jest stosowany w leczeniu raka endometrium i stwierdzono, że jest on znacząco skuteczny w przedłużaniu życia zarówno u kobiet przed menopauzą, jak i po menopauzie z tą chorobą. Lek był szeroko stosowany w takich wskazaniach w latach pięćdziesiątych i siedemdziesiątych, ale ostatnio najwięcej uwagi poświęcono OHPC w zapobieganiu porodom przedwczesnym .
Kontrola urodzeń
W kilku krajach OHPC jest dostępny w połączeniu z walerianianem estradiolu jako jednorazowy środek antykoncepcyjny do wstrzykiwania raz w miesiącu .
Inne zastosowania
OHPC jest stosowany jako składnik hormonalnej terapii menopauzalnej u kobiet.
OHPC jest stosowany w leczeniu łagodnego przerostu gruczołu krokowego u mężczyzn, chociaż dowody skuteczności są marginalne i niepewne. Jest również stosowany w leczeniu raka prostaty w dawce 1500 mg dwa razy w tygodniu. Mechanizm działania OHPC w tych zastosowaniach polega na hamowaniu produkcji androgenów w jądrach poprzez hamowanie wydzielania hormonu luteinizującego , które są wynikiem progestagenowego i antygonadotropowego działania OHPC. Jednak objawy hipogonadyzmu mogą się rozwinąć, gdy w tym wskazaniu stosuje się OHPC, przy czym dwie trzecie mężczyzn podobno doświadcza impotencji .
OHPC został użyty jako składnik feminizacji terapii hormonalnej dla transpłciowych kobiet . Ze względu na mikronizację częściej stosuje się bioidentyczne progestageny.
Dostępne formy
OHPC jest dostępny samodzielnie w postaci ampułek i fiolek zawierających 125 i 250 mg/ml roztworów olejowych do wstrzykiwań domięśniowych (marki Proluton, Makena). Jest również dostępny samodzielnie w postaci automatycznego wstrzykiwacza 250 mg/ml do stosowania we wstrzyknięciu podskórnym (marka Makena).
OHPC jest lub był dostępny w połączeniu z walerianianem estradiolu w postaci ampułek i fiolek zawierających 250 mg/ml OHPC i 5 mg/ml walerianianu estradiolu do wstrzykiwań domięśniowych (nazwy handlowe Gravibinon, Chinese Injectable No. 1). Lek jest lub był dostępny w połączeniu z benzoesanem estradiolu w postaci ampułek 125-250 mg OHPC i 10 mg benzoesanu estradiolu w roztworze olejowym do wstrzykiwań domięśniowych (marka Primosiston). Ponadto, OHPC był sprzedawany w Japonii w połączeniu z dipropionianem estradiolu w postaci 50 mg/ml OHPC i 1 mg/ml dipropionianu estradiolu (nazwa handlowa EP Hormone Depot) .
Przeciwwskazania
Przeciwwskazania do OHPC obejmują przebytą lub obecną zakrzepicę lub chorobę zakrzepowo- zatorową , rozpoznany lub podejrzewany rak piersi , przebyty lub obecny nowotwór hormonowrażliwy w wywiadzie , nierozpoznane nieprawidłowe krwawienia z pochwy niezwiązane z ciążą , żółtaczkę cholestatyczną ciąży , guzy wątroby lub czynną chorobę wątroby oraz niekontrolowane nadciśnienie . Istnieje również kilka względnych przeciwwskazań dla OHPC.
Skutki uboczne
OHPC jest ogólnie dobrze tolerowany i powoduje stosunkowo niewiele skutków ubocznych . Najczęstszym działaniem niepożądanym OHPC są reakcje w miejscu wstrzyknięcia, takie jak ból , bolesność , obrzęk , swędzenie , siniaki i grudki . Jednak w przeciwieństwie do dużych dawek progesteronu, które wywołują takie reakcje od umiarkowanych do ciężkich, OHPC jest stosunkowo wolny od reakcji w miejscu wstrzyknięcia. Działania niepożądane OHPC, które występują u co najmniej 2% użytkowników, obejmują ból w miejscu wstrzyknięcia (34,8%), obrzęk w miejscu wstrzyknięcia (17,1%), pokrzywkę (12,3%), świąd (7,7%), świąd w miejscu wstrzyknięcia (5,8% %), nudności (5,8%), guzki w miejscu wstrzyknięcia (4,5%) i biegunka (2,3%). Numerycznie zwiększone wskaźniki poronienia (2,4% vs. 0%), urodzenia martwego dziecka (2,0% vs. 1,3%), przyjęcia do porodu przedwczesnego (16,0% vs. 13,8%), stanu przedrzucawkowego lub nadciśnienia ciążowego (8,8% vs. 4,6) %), cukrzycę ciążową (5,6% w porównaniu z 4,6%) i małowodzie (3,6% w porównaniu z 1,3%) obserwowano w przypadku OHPC w badaniach klinicznych, w których podawano go kobietom w ciąży w celu zapobiegania porodom przedwczesnym.
Przedawkować
Nie ma doniesień o przedawkowaniu OHPC. W przypadku przedawkowania leczenie powinno opierać się na objawach . OHPC badano u ludzi w dużych dawkach od 2000 do 5000 mg na tydzień we wstrzyknięciu domięśniowym, bez obaw o bezpieczeństwo .
Interakcje
OHPC prawdopodobnie nie wpływa na większość enzymów cytochromu P450 w stężeniach terapeutycznych. Nie przeprowadzono badań interakcji leków z OHPC.
Farmakologia
Farmakodynamika
OHPC ma działanie progestagenowe , pewne działanie przeciwmineralokortykoidowe i nie wykazuje żadnej innej ważnej aktywności hormonalnej .
| Pogarszać | hPR-A | hPR-B | rbPR | rbGR | rbER | |||
|---|---|---|---|---|---|---|---|---|
| Progesteron | 100 | 100 | 100 | <1 | <1 | |||
| 17α-hydroksyprogesteron | 1 | 1 | 3 | 1 | <1 | |||
| Kapronian hydroksyprogesteronu | 26 | 30 | 28 | 4 | <1 | |||
| Octan hydroksyprogesteronu | 38 | 46 | 115 | 3 | ? | |||
| Uwagi: Wartości są procentami (%). Ligandami odniesienia (100%) były progesteron dla PR2 , deksametazon dla GR i estradiol dla ER . Źródła: Zobacz szablon. | ||||||||
| Pogarszać | Formularz | Dawka do konkretnych zastosowań (mg) | DOA | |||
|---|---|---|---|---|---|---|
| TFD | POICD | CICD | ||||
| Acetofenid algestonu | Roztwór oleju. | - | – | 75–150 | 14-32 dni | |
| kapronian gestonoronu | Roztwór oleju. | 25-50 | – | – | 8-13 dni | |
| Hydroksyprogest. octan | Aq. podejrz. | 350 | – | – | 9-16 dni | |
| Hydroksyprogest. kapronat | Roztwór oleju. | 250–500 | – | 250–500 | 5–21 dni | |
| Medroksyprog. octan | Aq. podejrz. | 50–100 | 150 | 25 | 14–50+ dni | |
| Octan megestrolu | Aq. podejrz. | - | – | 25 | >14 dni | |
| Noretysteron enanthate | Roztwór oleju. | 100–200 | 200 | 50 | 11-52 dni | |
| Progesteron | Roztwór oleju. | 200 | – | – | 2-6 dni | |
| Aq. zm. | ? | – | – | 1-2 dni | ||
| Aq. podejrz. | 50–200 | – | – | 7-14 dni | ||
|
Uwagi i źródła:
|
||||||
Aktywność progestagenowa
OHPC, znany również jako 17α-kapronian hydroksyprogesteronu, jest bliżej progesteronu w odniesieniu do struktury i farmakologicznych niż większość innych progestagenów i jest zasadniczo czysty progestagen - to jest selektywnym agonistą na receptor progesteronu (PR), przy minimalnym lub zerowym inne aktywność hormonalna . Jednak OHPC ma lepszą farmakokinetykę w porównaniu z progesteronem, a mianowicie znacznie dłuższy czas przy wstrzyknięciu domięśniowym w roztworze oleju .
Podawana przez wstrzyknięcie domięśniowe, dawka transformacyjna OHPC endometrium na cykl wynosi od 250 do 500 mg, a tygodniowa dawka substytucyjna OHPC wynosi 250 mg, podczas gdy skuteczna dawka OHPC w teście opóźnienia miesiączki (Greenblatt) wynosi 25 mg na tydzień. Skuteczna dawka OHPC hamująca owulację wynosi 500 mg raz w miesiącu we wstrzyknięciu domięśniowym. Jednak dawka OHPC stosowana w złożonych środkach antykoncepcyjnych do wstrzykiwania raz w miesiącu wynosi 250 mg, a połączenie to jest podobnie skuteczne w hamowaniu owulacji. Dla porównania dawka octanu medroksyprogesteronu (MPA; octan 6α-metylo-17α-hydroksyprogesteronu), bliskiego analogu OHPC, stosowanego we wstrzyknięciu domięśniowym w postaci mikrokrystalicznej zawiesiny wodnej w jednorazowych wstrzykiwanych środkach antykoncepcyjnych, wynosi 25 mg. Stwierdzono również, że 250 mg OHPC w roztworze olejowym podawane we wstrzyknięciu domięśniowym jest równoważne pod względem siły progestagenu z 50 mg octanu medroksyprogesteronu w mikrokrystalicznej zawiesinie wodnej. Chociaż okres półtrwania w fazie eliminacji domięśniowego OHPC w roztworze olejowym u kobiet niebędących w ciąży wynosi około 8 dni, okres półtrwania w fazie eliminacji domięśniowego octanu medroksyprogesteronu w mikrokrystalicznej zawiesinie wodnej u kobiet wynosi około 50 dni. OHPC jest również do pewnego stopnia słabszy niż bliżej spokrewniony ester octanu hydroksyprogesteronu (OHPA; octan 17α-hydroksyprogesteronu).
17α-hydroksyprogesteron (OHP) ma słabą aktywność progestagenową , ale estryfikacja C17α skutkuje wyższą aktywnością progestagenową. Spośród wielu różnych estrów , ester kapronianowy (heksanianowy) okazał się mieć najsilniejszą aktywność progestagenową, co posłużyło jako podstawa do opracowania OHPC, a także innych estrów progestagenu kapronianowego, takich jak kapronian gestonoronu . OHPC jest znacznie silniejszym progestagenem niż 17α-hydroksyprogesteron, ale nie ma tak wysokiego powinowactwa do PR jak progesteron. OHPC ma około 26% i 30% powinowactwa progesteronu odpowiednio do ludzkiego PR-A i PR-B . Lek nie był bardziej skuteczny niż progesteron w aktywowaniu tych receptorów i wywoływaniu związanej z nimi ekspresji genów in vitro .
Efekty antygonadotropowe
Ze względu na aktywację PR, OHPC ma działanie antygonadotropowe lub powoduje zahamowanie osi podwzgórze-przysadka-gonady i może znacząco hamować wydzielanie gonadotropin i produkcję gonadalnych hormonów płciowych w wystarczająco dużych dawkach. Jedno z badań wykazało , że OHPC przez wstrzyknięcie domięśniowe w dawce 200 mg dwa razy w tygodniu przez pierwsze dwa tygodnie , a następnie 200 mg raz w tygodniu przez 12 tygodni nie wpływa znacząco na wydalanie z moczem estrogenów , hormonu luteinizującego lub hormonu folikulotropowego u mężczyzn z łagodny przerost gruczołu krokowego. W innym badaniu, w którym stosowano nieokreśloną dawkę domięśniowego OHPC, wydzielanie testosteronu oceniano u jednego mężczyzny i stwierdzono, że zmniejszyło się z 4,2 mg/dobę do 2,0 mg/dobę (lub o około 52%) w ciągu 6 tygodni leczenia, podczas gdy hormonu luteinizującego pozostała niezmieniona u mężczyzny. Jeszcze inne badanie wykazało, że 3000 mg/tydzień OHPC we wstrzyknięciu domięśniowym obniża poziom testosteronu z 640 ng/dl do 320-370 ng/dl (o 42-50%) u jednego mężczyzny z rakiem prostaty, co było podobne do supresji testosteronu z octanem cyproteronu lub octanem chlormadinonu . Stwierdzono , że kapronian gestonoronu , blisko spokrewniony z OHPC progestyn o około 5- do 10-krotnie silniejszym działaniu u ludzi, obniża poziom testosteronu o 75% w dawce 400 mg/tydzień u mężczyzn z rakiem prostaty. Dla porównania, orchidektomia obniżyła poziom testosteronu o 91%. Ogólnie progestyny są w stanie maksymalnie obniżyć poziom testosteronu o około 70 do 80%. Antygonadotropowe działanie OHPC, a tym samym jego supresja testosteronu, są podstawą zastosowania OHPC w leczeniu łagodnego przerostu prostaty i raka prostaty u mężczyzn. U kobiet zaobserwowano również supresję poziomu hormonu luteinizującego przez OHPC.
Aktywność glukokortykoidów
Mówi się, że OHPC nie ma żadnej aktywności glukokortykoidowej . Zgodnie z tym, stwierdzono, że OHPC nie zmienia poziomów kortyzolu u ludzi nawet przy bardzo wysokich dawkach przez wstrzyknięcie domięśniowe. Ma to znaczenie, ponieważ leki o znacznej aktywności glikokortykosteroidów obniżają poziom kortyzolu z powodu zwiększonego ujemnego sprzężenia zwrotnego na osi podwzgórze-przysadka-nadnercza . OHPC badano u ludzi w dawkach do 5000 mg na tydzień we wstrzyknięciu domięśniowym, z bezpieczeństwem i bez zaobserwowania działania glikokortykoidowego. Lek oddziałuje jednak z receptorem glukokortykoidowym ; ma około 4% powinowactwa deksametazonu do receptora glikokortykoidowego królika. Działa jednak jako częściowy agonista receptora i nie ma większej skuteczności niż progesteron w aktywowaniu receptora i wywoływaniu związanej z nim ekspresji genów in vitro .
Inne czynności
Jako czysty progestagen OHPC nie wykazuje działania androgennego , antyandrogennego , estrogennego ani glukokortykoidowego . Brak działania androgennego i antyandrogennego przy OHPC jest w przeciwieństwie do większości innych progestyn pochodnych 17α-hydroksyprogesteronu . Ze względu na brak właściwości androgennych, podobnie jak progesteron, OHPC nie ma działania teratogennego na płód , dzięki czemu jest bezpieczny do stosowania w ciąży . Chociaż OHPC opisano jako czysty progestagen, istnieją dowody na to, że wykazuje pewną aktywność przeciwmineralokortykoidową , podobnie jak progesteron i 17α-hydroksyprogesteron. Obejmuje to klinicznie istotne działanie moczopędne oraz odwrócenie indukowanej estrogenami retencji płynów i obrzęku . W przeciwieństwie do progesteronu OHPC i jej metabolity nie są przewidywane do interakcji z niegenomowy receptorów , takich jak receptory błonowe progesteronu lub GABA A receptora . Zgodnie z tym uważa się, że OHPC nie posiada neurosteroidowych działań progesteronu lub związanych z nim efektów uspokajających .
W stosunku do cytochromu P450 enzymy , OHPC nie ma wpływu na CYP1A , CYP2D6 , CYP2C9 lub CYP3A4 , ale jest skromny induktorem od CYP2C19 .
Różnice w stosunku do progesteronu
Istnieją różnice farmakodynamiczne między progesteronem a OHPC, co może mieć wpływ na stosowanie w położnictwie . Obejmują one:
- Zmniejszona aktywność mięśniówki macicy z progesteronem in vitro, ale brak efektu lub zwiększona aktywność mięśniówki macicy z OHPC
- Zapobieganie dojrzewaniu szyjki macicy za pomocą progesteronu, ale nieznany efekt z OHPC
- Nieznacznie zwiększona częstość martwych urodzeń i poronień z OHPC (w jednym badaniu)
- Prawdopodobnie zwiększona częstość występowania cukrzycy ciążowej w przypadku OHPC (zwiększona w dwóch badaniach, brak różnicy w jednym badaniu), ale brak takiego efektu w przypadku progesteronu
- Znacząco zwiększone ryzyko okołoporodowych działań niepożądanych, takich jak utrata płodu i poród przedwczesny w ciąży mnogiej z OHPC (w dwóch badaniach)
Różnice w metabolizmie progesteronu i OHPC oraz różnice w tworzeniu i aktywności metabolitów mogą być odpowiedzialne lub zaangażowane w te obserwowane różnice biologiczne i farmakologiczne. Progesteron jest metabolizowany 5α- i 5p-reduktaz , 3a- i 3β hydroksysteroidowej dehydrogenazy i 20α- i 20β-hydroksysteroidowej w różnych tkankach . W tkankach docelowych, zwłaszcza szyjce macicy i mięśniówce macicy, enzymy te regulują lokalne stężenia progesteronu i mogą aktywować lub dezaktywować sygnalizację progesteronu. Ponadto, enzymy te katalizują tworzenie metabolitów progesteronu jak 5p-dihydroprogesterone i allopregnanolone , który to sygnał przez własne niegenomowy receptorów , takich jak receptory progesteronu membrany i GABA A receptora i mają swoje istotne zmiany w ciąży. Jako przykłady stwierdzono, że 5β-dihydroprogesteron odgrywa ważną rolę w hamowaniu aktywności mięśniówki macicy, podczas gdy allopregnanolon ma silne działanie uspokajające i znieczulające u matki, a zwłaszcza u płodu i bierze udział w rozwoju układu nerwowego płodu . W przeciwieństwie do progesteronu, OHPC nie jest metabolizowany przez tradycyjne enzymy przekształcające steroidy, a zamiast tego jest metabolizowany wyłącznie poprzez utlenianie w bocznym łańcuchu kapronianu przez enzymy cytochromu P450 . W związku z tym nie uważa się, że ma te same specyficzne dla tkanki wzorce aktywacji i dezaktywacji, co progesteron, ani takie same niegenomowe działania, jakie posiada progesteron i jego metabolity.
Oczekuje się, że dalsze badania kliniczne dostarczą dodatkowych danych, które pomogą wyjaśnić kwestię bezpieczeństwa stosowania OHPC. W każdym razie American College of Obstetricians and Gynecologists zalecił, aby kobiety w ciąży leczone OHPC otrzymywały porady dotyczące ryzyka i korzyści.
Farmakokinetyka
| Parametr | Singel | Bliźniak |
|---|---|---|
| C max (ng/ml) | 22,6 (15,8–27,4) | 17,3 (12–27) |
| C średnia (0–t) (ng/ml) | 16,8 (12,8–22,7) | 12,3 (8,4–18,7) |
| C minimalne (ng/ml) | 14,1 (10-18,1) | 11,2 (4,8–16,3) |
| AUC 0–t (ng/ml/dzień) | 117,3 (89,9–159,1) | 86,1 (59-131) |
| t 1/2 (dni) | 16,2 (10,6–21,0) | 10 (6-16) |
| T max (dni) | 1,0 (1–3) | 1,2 (1-2) |
| V d / F (x 10 3 ) (L) | 56 (25,2–69,6) | 16,9 (9,1–24,5) |
| Cl/F (×10 3 ) (L) | 2,1 (1,5-2,7) | 1,2 (0,9–1,7) |
| Przypisy: a = OHPC 250 mg raz na tydzień we wstrzyknięciu domięśniowym. Źródła: | ||
Wchłanianie
U zwierząt biodostępność OHPC przy wstrzyknięciu domięśniowym wynosi prawie 100%, ale biodostępność po podaniu doustnym jest bardzo niska i wynosi poniżej 3%. U kobiet OHPC doustnie w dawce 70 mg/dobę ma podobną siłę działania w endometrium jak OHPA 70 mg/dobę doustną i octan medroksyprogesteronu 2,5 mg/dobę doustnie , co wskazuje, że OHPC i OHPA podawane doustnie mają prawie 30-krotnie mniejszą siłę działania niż octan medroksyprogesteronu podawany doustnie. Badania nad progestagennymi zmianami endometrium z doustnym OHPC u kobiet są jednak mieszane, przy czym w jednym stwierdzono słabe efekty przy dawce 100 mg/dobę, podczas gdy w innym stwierdzono, że dawki od 250 do 1000 mg nie dawały żadnych efektów. Ze względu na niską siłę działania doustnego, OHPC nie był stosowany drogą doustną, a zamiast tego był podawany we wstrzyknięciu domięśniowym. Jednak nowa doustna formulacja OHPC (nazwa kodowa rozwojowa LPCN-1107) jest w trakcie opracowywania i okazała się skuteczna, chociaż w badaniu klinicznym wymagała podawania dwa razy dziennie.
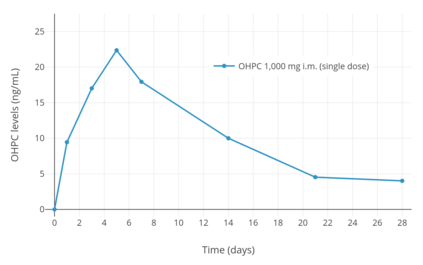
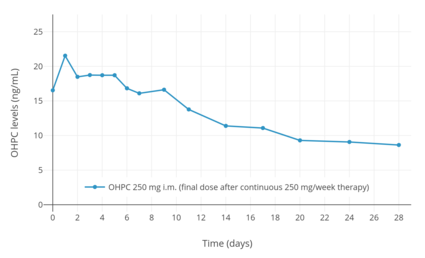
Przedłużonego działania występuje, gdy OHPC wstrzykuje się domięśniowo lub podskórnie tak, że lek ma przedłużony czas działania . Po pojedynczym wstrzyknięciu domięśniowym 1000 mg OHPC u pięciu kobiet z rakiem endometrium , maksymalne stężenie OHPC wyniosło 27,8 ± 5,3 ng/ml, a czas do osiągnięcia maksymalnego stężenia wyniósł 4,6 ± 1,7 (3–7) dni. Po 13 tygodniach ciągłego podawania 1000 mg OHPC na tydzień, minimalne poziomy OHPC wynosiły 60,0 ± 14 ng/ml. Te farmakokinetyczne parametry OHPC 250 mg jeden raz na tydzień przez iniekcję domięśniową badano również u kobiet ciężarnych Singleton i wiele (podwójne i tryplet) ciąży. Poziomy stanu stacjonarnego leku są osiągane w ciągu 4 do 12 tygodni po podaniu u kobiet w ciąży. U kobiet badano również czas trwania klinicznego działania biologicznego OHPC po wstrzyknięciu domięśniowym. Stwierdzono, że pojedyncze wstrzyknięcie domięśniowe 65 do 500 mg OHPC w roztworze olejowym ma czas działania od 5 do 21 dni pod względem działania w macicy i na temperaturę ciała u kobiet.
OHPC stwierdzono, że posiadają podobne właściwości farmakokinetyczne, w tym poziomów szczytowych , czas do poziomów szczytowych , pole pod krzywą stężenie w (to znaczy całkowita ekspozycja) i okresu półtrwania , przy podaniu przez wstrzyknięcie domięśniowe lub podskórne autoinjection . Jednak w przypadku autoiniekcji podskórnej częściej występował ból w miejscu wstrzyknięcia niż w przypadku wstrzyknięcia domięśniowego (37,3% w porównaniu z 8,2%).
Dystrybucja
OHPC silnie wiąże się z białkami osocza , w tym z albuminą . W przeciwieństwie do progesteronu i 17α-hydroksyprogesteronu , OHPC ma bardzo niskie powinowactwo do globuliny wiążącej kortykosteroidy (mniej niż 0,01% kortyzolu ). Progesteron i 17α-hydroksyprogesteron mają niskie powinowactwo do globuliny wiążącej hormony płciowe i z tego powodu tylko niewielka ich część (mniej niż 0,5%) wiąże się z tym białkiem w krążeniu.
Metabolizm
Wydaje się, że OHPC jest metabolizowany głównie przez enzymy CYP3A4 i CYP3A5 cytochromu P450 . Może być również metabolizowany przez CYP3A7 w wątrobie płodu i łożysku . W przeciwieństwie do progesteronu, OHPC nie jest metabolizowany przez tradycyjne enzymy przekształcające steroidy i nie tworzy podobnych metabolitów . Metabolizm OHPC odbywa się poprzez redukcję , hydroksylację i sprzęganie , w tym glukuronidację , siarczanowanie i acetylację . Kapronian estru z OHPC nie jest odcinana w czasie przemiany materii , tak 17α-hydroksyprogesteronu nie tworzy z OHPC. Jako taki, OHPC nie jest prolekiem 17α-hydroksyprogesteronu ani progesteronu .
Stwierdzono, że OHPC ma okres półtrwania w fazie eliminacji wynoszący 7,8 dnia po podaniu domięśniowym w postaci preparatu na bazie oleju kobietom niebędącym w ciąży. Uważa się, że jego całkowity czas trwania wynosi od 10 do 14 dni, czyli znacznie dłużej niż czas trwania domięśniowego podawania progesteronu w preparacie olejowym (2 do 3 dni). U kobiet w ciąży okres półtrwania OHPC w fazie eliminacji wydaje się być dłuższy, około 16 lub 17 dni. Jednak u kobiet w ciąży z bliźniętami, a nie z pojedynczą, okres półtrwania OHPC w fazie eliminacji był krótszy niż ten, wynoszący 10 dni. OHPC wykryto u kobiet w ciąży do 44 dni po podaniu ostatniej dawki.
Eliminacja
OHPC jest wydalany w 50% z kałem i 30% z moczem po podaniu domięśniowym kobietom w ciąży. Zarówno wolny steroid, jak i koniugaty są wydalane tymi drogami, przy czym koniugaty są bardziej widoczne w kale.
Weterynaryjny
Zbadano farmakokinetykę OHPC u różnych zwierząt kopytnych, w tym bydła, bawołów, owiec i kóz.
Krzywe czas-stężenie
Chemia
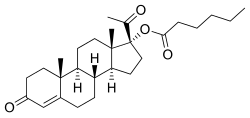
OHPC, znany również jako 17α-kapronian hydroksyprogesteronu lub 17a-hydroksypregn-4-eno-3,20-dion, 17a-heksanian, jest syntetycznym pregnan steroidu oraz pochodne od progesteronu . Jest to konkretnie pochodna 17α-hydroksyprogesteronu z estrem heksanianowym (kapronianowym) w pozycji C17α. Analogi z OHPC zawierać inne pochodne 17α-hydroksyprogesteron, takie jak acetophenide algeston (dihydroxyprogesterone acetophenide), octan chlormadinonu , octan cyproteronu , hydroksyprogesteron octan , hydroksyprogesteron heptanian , octan medroksyprogesteronu i octanu megestrolu , jak również kapronian estry kapronian chlormadinonu , gestonorone kapronian (norhydroxyprogesterone kapronian) medroksyprogesteronu kapronian , megestrolu kapronian i methenmadinone haksanian .
Synteza
Opisano syntezy chemiczne OHPC.
Historia
Wraz z octanu hydroksyprogesteronu , OHPC został opracowany przez Karla Junkmann z Schering AG w 1953 roku i została po raz pierwszy opisana przez niego w literaturze medycznej w roku 1954. Został on podobno pierwszy do obrotu w Japonii w 1954 lub 1955 roku, a następnie został wprowadzony jako Delalutin w United Stany Zjednoczone w 1956 r. Ze względu na znacznie dłuższy czas działania niż progesteron podawany drogą pozajelitową, OHPC w dużej mierze zastąpił progesteron w praktyce klinicznej do 1975 r. Po dziesięcioleciach stosowania producent Squibb dobrowolnie wycofał produkt Delalutin w Stanach Zjednoczonych w 1999 r. Ponowne zainteresowanie OHPC w Stanach Zjednoczonych zostało zapoczątkowane dużym sponsorowanym przez NIH badaniem w 2003 roku, które wykazało, że OHPC zmniejsza ryzyko przedwczesnego porodu u wybranych ciężarnych kobiet z grupy ryzyka. Ponieważ dane z obserwacji nie wykazują żadnych dowodów na szkodliwy wpływ na potomstwo, FDA zatwierdziła lek, sponsorowany przez KV Pharmaceutical jako Makena , jako lek sierocy w lutym 2011 r. W celu zmniejszenia ryzyka przedwczesnego porodu u kobiet przed 37 tygodniem ciąży z pojedynczym płodem, który miał co najmniej jeden przedwczesny poród.
Społeczeństwo i kultura
Nazwy ogólne
Kapronian hydroksyprogesteronu jest nazwą rodzajową OHPC i jego INN , USAN , BANM i JAN , podczas gdy heksanian hydroksyprogesteronu był jego dawnym BANM .
OHPC jest często błędnie oznaczany i mylony z progesteronem i 17α-hydroksyprogesteronem . Nie powinno być mylone z octanu hydroksyprogesteronu , hydroksyprogesteronu heptanianu lub octanu medroksyprogesteronu .
Nazwy marek
OHPC jest sprzedawany na całym świecie pod różnymi markami, w tym między innymi Proluton , Proluton Depot i Makena ( USA ). Był również wcześniej sprzedawany pod markami, w tym między innymi Delalutin , Prodrox i Hylutin , ale od tego czasu te preparaty zostały wycofane. Został on wprowadzony na rynek pod markami Gravibinon i Injectable No. 1 (lub Chinese Injectable No. 1) w połączeniu z walerianianem estradiolu oraz pod marką Primosiston w połączeniu z benzoesanem estradiolu .
Dostępność
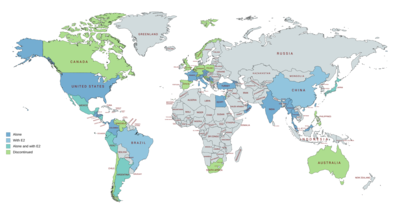
OHPC jest sprzedawany w Stanach Zjednoczonych i na całym Europie , Azji oraz Środkowej i Ameryki Południowej . W szczególności nie jest dostępny w Kanadzie , Wielkiej Brytanii , Nowej Zelandii i Afryce Południowej , a w Australii dostępne są tylko preparaty weterynaryjne . OHPC jest również sprzedawany w połączeniu z walerianianem estradiolu jako złożony środek antykoncepcyjny do wstrzykiwań w wielu krajach, w tym w Ameryce Południowej , Meksyku , Japonii i Chinach . W niektórych krajach jest sprzedawany jako preparat do wstrzykiwania w połączeniu z benzoesanem estradiolu .
Kontrowersje cenowe
Wraz z oznaczeniem OHPC jako leku sierocego przez FDA i zatwierdzeniem Makena w 2011 r., cena OHPC w Stanach Zjednoczonych miała wzrosnąć z 15 USD do 1500 USD za pojedynczą dawkę lub z około 300 USD do między USA 25 000 USD i 30 000 USD za typowy miesiąc leczenia. Był to około 100-krotny wzrost kosztów, przy „minimalnej dodatkowej korzyści klinicznej” i był mocno krytykowaną strategią cenową . FDA ogłosiła następnie, że apteki mieszające mogą nadal sprzedawać OHPC po zwykłej cenie około 10 do 20 USD za dawkę bez obawy przed represjami prawnymi. KV Pharmaceutical zdecydowało się również na obniżenie ceny Makena do 690 USD za dawkę. OHPC nadal była dostępna po niskich kosztach w aptekach mieszających aż do końca 2016 r., po czym FDA opublikowała nowe wytyczne zabraniające aptekom mieszającym sprzedaży produktów, które są „zasadniczo kopiami” dostępnych na rynku leków.
Badania
We wstępnym badaniu stwierdzono, że cykliczna terapia 150 mg OHPC we wstrzyknięciu domięśniowym jest skuteczna w leczeniu 76 kobiet z uporczywym, opornym na leczenie trądzikiem , przy czym 84% odpowiedziało na terapię i doświadczyło poprawy „od dobrej do doskonałej” w objawach.
OHPC był badany przez Schering pod kątem stosowania jako środek antykoncepcyjny zawierający wyłącznie progestagen w dawce 250 do 500 mg raz w miesiącu przez wstrzyknięcie domięśniowe, ale powodował słabą kontrolę cyklu przy tych dawkach i nigdy nie został wprowadzony do obrotu.
Stwierdzono, że sam OHPC ma niewielką lub żadną skuteczność w leczeniu raka piersi u kobiet. Odwrotnie, stwierdzono, że połączenie walerianianu estradiolu i OHPC jest skuteczne w leczeniu raka piersi u kobiet. Wstępne badania oparte na ograniczonych danych klinicznych wykazały, że wskaźnik odpowiedzi raka piersi przy połączeniu walerianianu estradiolu i OHPC wydawał się być wyższy niż w przypadku samego estrogenu (35% vs. 50%). Jednak późniejsze badania z użyciem pokrewnego, ale silniejszego kapronianu gestonoronu progestagenowego wykazały, że połączenie walerianianu estradiolu i kapronianu gestonoronu miało skuteczność, która nie różniła się znacząco od skuteczności samego estrogenu w leczeniu raka piersi u kobiet.
Nowatorski preparat doustny OHPC (kod rozwojowy LPCN-1107) jest opracowywany w celu zapobiegania porodom przedwczesnym . Od września 2017 r. znajduje się w fazie II lub III fazy badań klinicznych dla tego wskazania.
Zobacz też
- Walerianian estradiolu/kapronian hydroksyprogesteronu
- Benzoesan estradiolu/kapronian hydroksyprogesteronu
- Dipropionian estradiolu/kapronian hydroksyprogesteronu
Bibliografia
Dalsza lektura
- Meis PJ (maj 2005). „17 hydroksyprogesteron w zapobieganiu porodowi przedwczesnemu”. Położnictwo i Ginekologia . 105 (5 pkt 1): 1128–35. doi : 10.1097/01.AOG.0000160432.95395.8f . PMID 15863556 .
- Facchinetti F, Vaccaro V (październik 2009). „Farmakologiczne zastosowanie progesteronu i kapronianu 17-alfa-hydroksyprogesteronu w zapobieganiu porodom przedwczesnym”. Minerva Ginecologica . 61 (5): 401–9. PMID 19749671 .
- Deeks ED (październik 2011). „Kapronian 17 α-hydroksyprogesteronu (Makena™): w zapobieganiu porodom przedwczesnym”. Leki pediatryczne . 13 (5): 337–45. doi : 10.2165/11208140-000000000-00000 . PMID 21888448 . S2CID 207297651 .
- Merlob P, Stahl B, Klinger G (styczeń 2012). „17α kapronian hydroksyprogesteronu do zapobiegania nawracającym samoistnym porodom przedwczesnym”. Toksykologia rozrodu . 33 (1): 15–9. doi : 10.1016/j.reprotox.2011.10.017 . PMID 22120850 .
- O'Brien JM (październik 2012). „Bezpieczeństwo podawania kapronianu progesteronu i 17-hydroksyprogesteronu w celu zapobiegania porodom przedwczesnym: ocena oparta na dowodach”. American Journal of Perinatology . 29 (9): 665–72. doi : 10.1055/s-0032-1316444 . PMID 22773279 .
- Romero R, Stańczyk FZ (czerwiec 2013). „Progesteron to nie to samo co kapronian 17α-hydroksyprogesteronu: implikacje dla praktyki położniczej” . American Journal of Obstetrics and Gynecology . 208 (6): 421–6. doi : 10.1016/j.ajog.2013.04.027 . PMC 4120746 . PMID 23643669 .
- Feghali M, Venkataramanan R, Caritis S (grudzień 2014). „Zapobieganie przedwczesnemu porodowi z kapronianem 17-hydroksyprogesteronu: względy farmakologiczne” . Seminaria z Perinatologii . 38 (8): 516–22. doi : 10.1053/j.semperi.2014.08.013 . PMC 4253874 . PMID 25256193 .
- Saccone G, Suhag A, Berghella V (lipiec 2015). „kapronian 17-alfa-hydroksyprogesteronu do tokolizy podtrzymującej: przegląd systematyczny i metaanaliza badań z randomizacją”. American Journal of Obstetrics and Gynecology . 213 (1): 16–22. doi : 10.1016/j.ajog.2015.01.054 . PMID 25659469 .
- O'Brien JM, Lewis DF (styczeń 2016). „Zapobieganie przedwczesnemu porodowi z progesteronem dopochwowym lub kapronianem 17-alfa-hydroksyprogesteronu: krytyczne badanie skuteczności i bezpieczeństwa”. American Journal of Obstetrics and Gynecology . 214 (1): 45–56. doi : 10.1016/j.ajog.2015.10.934 . PMID 26558340 .
- Caritis SN, Feghali MN, Grobman WA, Rouse DJ (sierpień 2016). „Czego dowiedzieliśmy się o roli kapronianu 17-alfa-hydroksyprogesteronu w zapobieganiu porodom przedwczesnym” . Seminaria z Perinatologii . 40 (5): 273–80. doi : 10.1053/j.semperi.2016.03.002 . PMC 4983195 . PMID 27105940 .
- Saccone G, Khalifeh A, Elimian A, Bahrami E, Chaman-Ara K, Bahrami MA, Berghella V (marzec 2017). „Pochwowy progesteron a domięśniowy kapronian 17α-hydroksyprogesteronu w zapobieganiu nawracającym spontanicznym porodom przedwczesnym w ciążach pojedynczych: przegląd systematyczny i metaanaliza randomizowanych badań kontrolowanych” . USG w położnictwie i ginekologii . 49 (3): 315–321. doi : 10.1002/uog.17245 . PMID 27546354 . S2CID 11445977 .
- Oler E, Eke AC, Hesson A (lipiec 2017). „Meta-analiza randomizowanych kontrolowanych badań porównujących kapronian 17α-hydroksyprogesteronu i progesteronu dopochwowego w celu zapobiegania nawracającemu spontanicznemu porodowi przedwczesnemu”. Międzynarodowy Dziennik Ginekologii i Położnictwa . 138 (1): 12-16. doi : 10.1002/ijgo.12166 . hdl : 2027,42/137297 . PMID 28369874 . S2CID 24480427 .
- Manuck TA (grudzień 2017). „Kapronian 17-alfa hydroksyprogesteronu do zapobiegania porodom przedwczesnym: gdzie byliśmy, jak się tu dostaliśmy i dokąd zmierzamy?”. Seminaria z Perinatologii . 41 (8): 461–467. doi : 10.1053/j.semperi.2017.08.004 . PMID 28947068 .