alfa-synukleina - Alpha-synuclein
Alfa-synukleina jest białkiem, które u ludzi jest kodowane przez gen SNCA . Alfa-synukleina jest białkiem neuronalnym, które reguluje ruch pęcherzyków synaptycznych i późniejsze uwalnianie neuroprzekaźników .
Występuje obficie w mózgu, podczas gdy mniejsze ilości znajdują się w sercu, mięśniach i innych tkankach. W mózgu alfa-synukleina znajduje się głównie na końcach neuronów w wyspecjalizowanych strukturach zwanych zakończeniami presynaptycznymi . W obrębie tych struktur alfa-synukleina oddziałuje z fosfolipidami i białkami. Terminale presynaptyczne uwalniają przekaźniki chemiczne, zwane neuroprzekaźnikami , z przedziałów znanych jako pęcherzyki synaptyczne . Uwalnianie neuroprzekaźników przekazuje sygnały między neuronami i ma kluczowe znaczenie dla prawidłowego funkcjonowania mózgu.
Ludzkie białko alfa-synukleiny składa się ze 140 aminokwasów. Wykazano, że fragment alfa-synukleiny, znany jako składnik niebędący Abeta (NAC) amyloidu choroby Alzheimera , pierwotnie występujący we frakcji wzbogaconej w amyloid, jest fragmentem jego białka prekursorowego NACP. Później ustalono, że NACP jest ludzkim homologiem synukleiny Torpedo . Dlatego NACP jest obecnie określany jako ludzka alfa-synukleina.
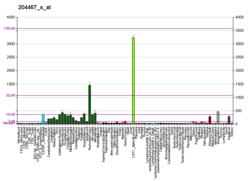
Ekspresja tkankowa
Alfa-synukleina to białko synukleiny o nieznanej funkcji, występujące głównie w tkance nerwowej , stanowiące aż 1% wszystkich białek w cytozolu komórek mózgowych. Wyraża się głównie w korze nowej , hipokampie , istocie czarnej , wzgórzu i móżdżku . Jest to głównie białko neuronalne, ale można go również znaleźć w komórkach neurogleju . W komórkach melanocytowych ekspresja białka SNCA może być regulowana przez MITF .
Ustalono, że alfa-synukleina jest szeroko zlokalizowana w jądrze neuronów mózgu ssaków, co sugeruje rolę alfa-synukleiny w jądrze. Synukleina znajduje się jednak głównie na końcach presynaptycznych , zarówno w postaci wolnej, jak i związanej z błoną, przy czym około 15% synukleiny jest związane z błoną w dowolnym momencie w neuronach.
Wykazano również, że alfa-synukleina jest zlokalizowana w mitochondriach neuronalnych . Alfa-synukleina jest silnie eksprymowana w mitochondriach opuszki węchowej , hipokampie, prążkowiu i wzgórzu, gdzie również bogata jest cytozolowa alfa-synukleina. Jednak kora mózgowa i móżdżek to dwa wyjątki, które zawierają bogatą cytozolową alfa-synukleinę, ale bardzo niskie poziomy alfa-synukleiny mitochondrialnej. Wykazano, że alfa-synukleina jest zlokalizowana w błonie wewnętrznej mitochondriów, a hamujący wpływ alfa-synukleiny na aktywność kompleksu I mitochondrialnego łańcucha oddechowego jest zależny od dawki. Sugeruje się zatem, że alfa-synukleina w mitochondriach jest różnie wyrażana w różnych regionach mózgu, a poziomy tła mitochondrialnej alfa-synukleiny mogą być potencjalnym czynnikiem wpływającym na funkcję mitochondriów i predysponującym niektóre neurony do degeneracji.
Przynajmniej trzy izoformy synukleiny są wytwarzane przez alternatywne splicing . Większa forma białka, i ta najbardziej zbadana, to białko o pełnej długości, składające się ze 140 aminokwasów. Inne izoformy to alfa-synukleina-126, która nie ma reszt 41-54 z powodu utraty eksonu 3; i alfa-synukleina-112, która nie ma reszty 103-130 z powodu utraty eksonu 5.
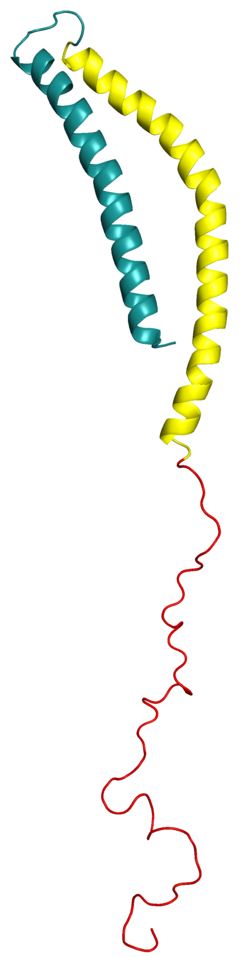
Struktura
Alfa-synukleina w roztworze jest uważana za białko wewnętrznie nieuporządkowane , tzn. brakuje mu pojedynczej stabilnej struktury 3D. Od 2014 r. coraz więcej doniesień sugeruje jednak obecność struktur cząstkowych lub głównie ustrukturyzowanych stanów oligomerycznych w strukturze roztworu alfa-synukleiny nawet przy braku lipidów. Tendencja ta jest również wspierana przez dużą liczbę pomiarów pojedynczych cząsteczek ( pęsetą optyczną ) na pojedynczych kopiach monomerycznej alfa-synukleiny, a także kowalencyjnie wzmocnionych dimerów lub tetramerów alfa-synukleiny.
Alfa-synukleina jest specyficznie podwyższona w odrębnej populacji presynaptycznych zakończeń mózgu podczas okresu przegrupowania synaptycznego związanego z nabywaniem. Wykazano , że alfa- synukleina znacząco oddziałuje z tubuliną i że alfa- synukleina może wykazywać aktywność jako potencjalne białko związane z mikrotubulami , takie jak tau .
Ostatnie dowody sugerują, że alfa-synukleina działa jako molekularny chaperon w tworzeniu kompleksów SNARE . W szczególności wiąże się jednocześnie z fosfolipidami błony komórkowej poprzez swoją domenę N-końcową iz synaptobrewiną -2 poprzez swoją domenę C-końcową, ze zwiększonym znaczeniem podczas aktywności synaptycznej. Rzeczywiście, istnieje coraz więcej dowodów na to, że alfa-synukleina jest zaangażowana w funkcjonowanie neuronalnego aparatu Golgiego i handel pęcherzykami .
Najwyraźniej alfa-synukleina jest niezbędna do prawidłowego rozwoju funkcji poznawczych. Myszy knock-out z celowaną inaktywacją ekspresji alfa-synukleiny wykazują upośledzenie uczenia się przestrzennego i pamięci roboczej.
Interakcja z błonami lipidowymi
Zebrano dowody eksperymentalne dotyczące interakcji alfa-synukleiny z błoną i jej zaangażowania w skład i obrót błony. Badanie przesiewowe genomu drożdży wykazało, że kilka genów zajmujących się metabolizmem lipidów i fuzją mitochondrialną odgrywa rolę w toksyczności alfa-synukleiny. Odwrotnie, poziomy ekspresji alfa-synukleiny mogą wpływać na lepkość i względną ilość kwasów tłuszczowych w podwójnej warstwie lipidowej.
Wiadomo, że alfa-synukleina bezpośrednio wiąże się z błonami lipidowymi, wiążąc się z ujemnie naładowanymi powierzchniami fosfolipidów . Alfa-synukleina tworzy rozciągniętą strukturę spiralną na małych jednolamelarnych pęcherzykach. Stwierdzono preferencyjne wiązanie z małymi pęcherzykami. Wiązanie alfa-synukleiny z błonami lipidowymi ma złożony wpływ na te ostatnie, zmieniając strukturę dwuwarstwy i prowadząc do tworzenia małych pęcherzyków. Wykazano, że alfa-synukleina zgina błony ujemnie naładowanych pęcherzyków fosfolipidowych i tworzy kanaliki z dużych pęcherzyków lipidowych. Stosując krio-EM wykazano, że są to rurki micelarne o średnicy ~5-6 nm. Wykazano również, że alfa-synukleina tworzy cząsteczki podobne do dysków lipidowych, podobne do apolipoprotein . Badania EPR wykazały, że struktura alfa-synukleiny zależy od powierzchni wiążącej. Białko przyjmuje konformację złamaną spiralną na cząsteczkach lipoproteinowych, podczas gdy tworzy rozszerzoną strukturę spiralną na pęcherzykach lipidowych i rurkach błonowych. Badania sugerują również możliwą aktywność antyoksydacyjną alfa-synukleiny w błonie.
Interakcja błonowa alfa-synukleiny moduluje lub wpływa na szybkość jej agregacji. Modulacja agregacji za pośrednictwem błony jest bardzo podobna do obserwowanej dla innych białek amyloidowych, takich jak IAPP i abeta. Zagregowane stany alfa-synukleiny przenikają przez błonę pęcherzyków lipidowych. Powstają w wyniku interakcji z wielonienasyconymi kwasami tłuszczowymi podatnymi na peroksydację (PUFA), ale nie z jednonienasyconymi kwasami tłuszczowymi, a wiązanie promujących samoutlenianie lipidów metali przejściowych, takich jak żelazo lub miedź, powoduje oligomeryzację alfa-synukleiny. Zagregowana alfa-synukleina ma specyficzną aktywność wobec peroksydowanych lipidów i indukuje autooksydację lipidów w bogatych w PUFA błonach zarówno neuronów, jak i astrocytów, zmniejszając odporność na apoptozę. Autooksydacja lipidów jest hamowana, jeśli komórki są wstępnie inkubowane z PUFA wzmocnionymi izotopami (D-PUFA).
Funkcjonować
Chociaż funkcja alfa-synukleiny nie jest dobrze poznana, badania sugerują, że odgrywa ona rolę w ograniczaniu ruchliwości pęcherzyków synaptycznych, w konsekwencji osłabiając recykling pęcherzyków synaptycznych i uwalnianie neuroprzekaźników. Alternatywny pogląd jest taki, że alfa-synukleina wiąże się z VAMP2 ( synaptobrewiną ) i stabilizuje kompleksy SNARE ; chociaż ostatnie badania wskazują, że wiązanie alfa-synukleiny-VAMP2 ma kluczowe znaczenie dla tłumienia za pośrednictwem alfa-synukleiny recyklingu pęcherzyków synaptycznych, łącząc te dwa pozornie rozbieżne poglądy. Może również pomóc w regulacji uwalniania dopaminy , rodzaju neuroprzekaźnika, który ma kluczowe znaczenie dla kontrolowania rozpoczynania i zatrzymywania ruchów zamierzonych i mimowolnych.
Alfa-synukleina moduluje procesy naprawy DNA , w tym naprawę pęknięć dwuniciowych (DSB). Markery odpowiedzi na uszkodzenie DNA znajdują się wspólnie z alfa-synukleiną, tworząc odrębne ogniska w komórkach ludzkich i mózgu myszy. Ubytek alfa-synukleiny w komórkach ludzkich powoduje zwiększone wprowadzanie DSB DNA po ekspozycji na bleomycynę i zmniejszoną zdolność do naprawy tych DSB. Ponadto myszy z nokautem alfa-synukleiny wykazują wyższy poziom DSB, a problem ten można złagodzić przez ponowne transgeniczne wprowadzenie ludzkiej alfa-synukleiny. Alfa-synukleina promuje szlak naprawy DSB określany jako łączenie niehomologicznych końców . Wydaje się, że funkcja naprawy DNA alfa-synukleiny jest osłabiona w neuronach zawierających inkluzje ciałek Lewy'ego , co może wywołać śmierć komórki.
Proneurogenna funkcja alfa-synukleiny
W chorobach neurodegeneracyjnych alfa-synukleina wytwarza nierozpuszczalne wtrącenia. Z drugiej strony choroby te są związane albo z wyższym poziomem normalnej alfa-synukleiny, albo jej zmutowanych wariantów. Jednak normalna fizjologiczna rola Snca nie została jeszcze dokładnie wyjaśniona. W rzeczywistości wykazano, że fizjologiczne Snca mają działanie neuroochronne poprzez hamowanie apoptozy indukowanej przez kilka rodzajów bodźców apoptotycznych lub poprzez regulację ekspresji białek zaangażowanych w szlaki apoptotyczne. Ostatnio wykazano, że regulacja w górę alfa-synukleiny w zakręcie zębatym (neurogenicznej niszy, w której przez całe życie generowane są nowe neurony) aktywuje komórki macierzyste w modelu przedwczesnego starzenia się neuronów. Model ten wykazuje zmniejszoną ekspresję alfa-synukleiny i zmniejszoną proliferację komórek macierzystych, co fizjologicznie obserwuje się podczas starzenia. Egzogenna alfa-synukleina w zakręcie zębatym jest w stanie uratować tę wadę. Ponadto alfa-synukleina zwiększa również proliferację progenitorowych komórek nerwowych zakrętu zębatego u młodych myszy typu dzikiego. Zatem alfa-synukleina reprezentuje efektor dla aktywacji nerwowych komórek macierzystych i progenitorowych. Podobnie stwierdzono, że alfa-synukleina jest wymagana do utrzymania komórek macierzystych SVZ (strefy podkomorowej, tj. innej niszy neurogennej) w stanie cyklicznym.
Sekwencja
Struktura pierwszorzędowa alfa-synukleiny jest zwykle podzielona na trzy odrębne domeny:
- Reszty 1-60: AN amfipatyczne region N-końcowy zdominowane przez cztery powtórzenia 11-aminokwasowe, w tym sekwencji konsensusowej KTKEGV. Sekwencja ta ma strukturalną skłonność do alfa helisy podobną do domen wiążących apolipoproteiny. Jest to wysoce konserwowane terminal, który współdziała z kwasowymi membran lipidowych i wszystkich wykrytych mutacji punktowych w SNCA genu znajdują się w tym terminalu.
- Reszty 61-95: Centralny region hydrofobowy, który obejmuje region nie-amyloidu-β (NAC), zaangażowany w agregację białka. Ta domena jest unikalna dla alfa-synukleiny z rodziny synuklein.
- Reszty 96-140: region silnie kwaśny i bogaty w prolinę , który nie ma wyraźnej skłonności strukturalnej. Domena ta odgrywa ważną rolę w funkcji, rozpuszczalności i interakcji alfa-synukleiny z innymi białkami .
Aktywność autoproteolityczna
Zastosowanie spektrometrii masowej ruchliwości jonów o wysokiej rozdzielczości (IMS-MS) na alfa-synukleinie oczyszczonej metodą HPLC in vitro wykazało, że alfa-synukleina jest autoproteolityczna ( samoproteolityczna ), generując różne fragmenty o małej masie cząsteczkowej po inkubacji. Stwierdzono, że białko 14,46 kDa generuje liczne mniejsze fragmenty, w tym fragmenty 12,16 kDa ( aminokwasy 14-133) i 10,44 kDa (40-140) utworzone przez skrócenie C- i N-końcowe oraz fragment C-końcowy 7,27 kDa (72). -140). Fragment 7,27 kDa, który zawiera większość regionu NAC, ulega agregacji znacznie szybciej niż pełnej długości alfa-synukleina. Możliwe, że te produkty autoproteolityczne odgrywają rolę jako produkty pośrednie lub kofaktory w agregacji alfa-synukleiny in vivo .
Znaczenie kliniczne

Niezmutowana α-synukleina, klasycznie uważana za nieustrukturyzowane rozpuszczalne białko, tworzy stabilnie sfałdowany tetramer, który jest odporny na agregację . Ta obserwacja, choć powtórzona i rozszerzona przez kilka laboratoriów, nadal jest przedmiotem debaty w terenie ze względu na sprzeczne raporty. Niemniej jednak agregaty alfa-synukleiny tworzą nierozpuszczalne włókienka w stanach patologicznych charakteryzujących się obecnością ciałek Lewy'ego , takich jak choroba Parkinsona , otępienie z ciałami Lewy'ego i atrofia wielonarządowa . Zaburzenia te znane są jako synukleinopatie . Modele synukleinopatii in vitro wykazały, że agregacja alfa-synukleiny może prowadzić do różnych zaburzeń komórkowych, w tym zaburzeń mikrotubul, dysfunkcji synaptycznych i mitochondrialnych, stresu oksydacyjnego oraz dysregulacji szlaku sygnałowego wapnia, proteasomalnego i lizosomalnego. Alfa-synukleina jest głównym składnikiem strukturalnym włókienek ciałek Lewy'ego. Czasami ciała Lewy'ego zawierają białko tau ; jednak alfa-synukleina i tau stanowią dwa odrębne podzbiory włókien w tych samych ciałach inkluzyjnych. Patologia alfa-synukleiny występuje również zarówno w sporadycznych, jak i rodzinnych przypadkach choroby Alzheimera.
Mechanizm agregacji alfa-synukleiny jest niepewny. Istnieją dowody na ustrukturyzowany produkt pośredni bogaty w strukturę beta, który może być prekursorem agregacji i ostatecznie ciał Lewy'ego. Badanie pojedynczej cząsteczki w 2008 roku sugeruje, że alfa-synukleina istnieje jako mieszanina nieustrukturyzowanych konformerów alfa-helisowych i bogatych w arkusze beta w równowadze. Mutacje lub warunki buforowe, o których wiadomo, że poprawiają agregację, silnie zwiększają populację konformera beta, co sugeruje, że może to być konformacja związana z agregacją patogenną. Jedna z teorii głosi, że większość agregatów alfa-synukleiny znajduje się w presynapsie jako mniejsze złogi, co powoduje dysfunkcję synaptyczną. Wśród strategii leczenia synukleinopatii są związki, które hamują agregację alfa-synukleiny. Wykazano, że drobnocząsteczkowy aldehyd kuminowy hamuje fibrylację alfa-synukleiny. Wirus Epsteina-Barr został powiązany z tymi zaburzeniami.
W rzadkich przypadkach rodzinnych postaci choroby Parkinsona występuje mutacja w genie kodującym alfa-synukleinę. Dotychczas zidentyfikowano pięć mutacji punktowych : A53T , A30P, E46K, H50Q i G51D. Doniesiono, że niektóre mutacje wpływają na etapy inicjacji i amplifikacji procesu agregacji. Wydaje się, że duplikacja i potrojenie genomu genu są rzadką przyczyną choroby Parkinsona w innych liniach genetycznych, chociaż częściej niż mutacje punktowe. W związku z tym pewne mutacje alfa-synukleiny mogą powodować tworzenie się włókien podobnych do amyloidu, które przyczyniają się do choroby Parkinsona. Nadekspresja ludzkiej alfa-synukleiny typu dzikiego lub zmutowanej A53T u naczelnych prowadzi do odkładania się alfa-synukleiny w brzusznej części śródmózgowia, degeneracji układu dopaminergicznego i upośledzenia zdolności motorycznych.
Pewne sekcje białka alfa-synukleiny mogą odgrywać rolę w tauopatiach .
Postać prionowa białka alfa-synukleiny może być czynnikiem sprawczym zaniku wieloukładowego choroby .
Opisano samoreplikujące się „prionopodobne” zespoły amyloidowe alfa-synukleiny, które są niewidoczne dla barwnika amyloidowego Thioflavin T i które mogą gwałtownie rozprzestrzeniać się w neuronach in vitro i in vivo.
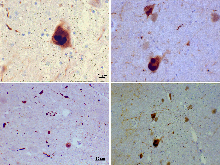
Przeciwciała przeciw alfa-synukleinie zastąpiły przeciwciała przeciw ubikwitynie jako złoty standard barwienia immunologicznego ciał Lewy'ego. Centralny panel na rycinie po prawej pokazuje główny szlak agregacji białek. Monomeryczna α-synukleina jest natywnie rozwinięta w roztworze, ale może również wiązać się z błonami w postaci α-helikalnej. Wydaje się prawdopodobne, że te dwa gatunki istnieją w równowadze w komórce, chociaż nie jest to udowodnione. Z badań in vitro jasno wynika, że niesfałdowany monomer może najpierw agregować w małe cząsteczki oligomeryczne, które można ustabilizować przez oddziaływania podobne do arkusza β, a następnie w nierozpuszczalne włókienka o wyższej masie cząsteczkowej. W kontekście komórkowym istnieją pewne dowody na to, że obecność lipidów może sprzyjać tworzeniu oligomerów: α-synukleina może również tworzyć pierścieniowe struktury podobne do porów, które oddziałują z błonami. Odkładanie α-synukleiny w strukturach patologicznych, takich jak ciała Lewy'ego, jest prawdopodobnie późnym zdarzeniem, które występuje w niektórych neuronach. Po lewej stronie znajdują się niektóre ze znanych modyfikatorów tego procesu. Aktywność elektryczna w neuronach zmienia asocjację α-synukleiny z pęcherzykami i może również stymulować kinazę polo-podobną 2 (PLK2), która, jak wykazano, fosforyluje α-synukleinę w Ser 129. Proponowano również udział innych kinaz. Podobnie jak fosforylacja, skrócenie przez proteazy, takie jak kalpainy , i nitracja, prawdopodobnie przez tlenek azotu (NO) lub inne reaktywne formy azotu obecne podczas zapalenia, wszystkie modyfikują synukleinę tak, że ma większą tendencję do agregacji. Dodanie ubikwityny (pokazanej jako czarna plama) do ciał Lewy'ego jest prawdopodobnie procesem wtórnym do osadzania. Po prawej stronie znajdują się niektóre z proponowanych komórkowych celów dla toksyczności, w których pośredniczy α-synukleina, które obejmują (od góry do dołu) transport ER-golgiego, pęcherzyki synaptyczne, mitochondria i lizosomy oraz inne mechanizmy proteolityczne. W każdym z tych przypadków sugeruje się, że α-synukleina ma szkodliwe działanie, wymienione poniżej każdej strzałki, chociaż w tej chwili nie jest jasne, czy którykolwiek z nich jest konieczny lub wystarczający dla toksyczności w neuronach.
Oddziaływania białko-białko
Wykazano interakcję alfa-synukleiny z
Zobacz też
- Synukleina
- Contursi Terme - wieś we Włoszech, gdzie mutacja w genie α-synukleiny doprowadziła do rodzinnej historii choroby Parkinsona
Bibliografia
Dalsza lektura
- Blakeslee S (27.05.2002). „W składanych białkach, wskazówki do wielu chorób -” . New York Times .
- Polymeropoulos MH, Lavedan C, Leroy E, Ide SE, Dehejia A, Dutra A, et al. (czerwiec 1997). „Mutacja w genie alfa-synukleiny zidentyfikowana w rodzinach z chorobą Parkinsona” . Nauka . 276 (5321): 2045-7. doi : 10.1126/science.276.5321.2045 . PMID 9197268 .
- Neumann M, Kahle PJ, Giasson BI, Ozmen L, Borroni E, Spooren W, et al. (listopad 2002). „Niewłaściwie sfałdowana oporna na proteinazę K hiperfosforylowana alfa-synukleina u starszych myszy transgenicznych z pogorszeniem narządu ruchu oraz w ludzkich alfa-synukleinopatiach” . Journal of Clinical Investigation . 110 (10): 1429–39. doi : 10.1172/JCI15777 . PMC 151810 . PMID 12438441 .
- Jerzego JM (2001). „Synukleiny” . Biologia genomu . 3 (1): RECENZJE 3002. doi : 10.1186/gb-2001-3-1-recenzje3002 . PMC 150459 . PMID 11806835 .
- Lavedan C (wrzesień 1998). „Rodzina synuklein”. Badania genomu . 8 (9): 871–80. doi : 10.1101/gr.8.9.871 . PMID 9750188 .
- Ozawa T, Wakabayashi K, Oyanagi K (luty 2002). „[Ostatnie postępy w badaniach atrofii wieloukładowej ze szczególnym uwzględnieniem alfa-synukleiny i jądra nadskrzyżowaniowego]”. Nie dla Shinkei = Mózg i Nerw . 54 (2): 111–7. PMID 11889756 .
- Cole NB, Murphy DD (2002). „Biologia komórkowa alfa-synukleiny: lepki problem?” . Medycyna neuromolekularna . 1 (2): 95–109. doi : 10.1385/NMM:1:2:95 . PMID 12025860 . S2CID 7313626 .
- Iwatsubo T (czerwiec 2002). „[alfa-synukleina i choroba Parkinsona]”. Seikagaku. Dziennik Japońskiego Towarzystwa Biochemicznego . 74 (6): 477–82. PMID 12138709 .
- Trojanowski JQ, Lee VM (październik 2002). „Choroba Parkinsona i związane z nią synukleinopatie to nowa klasa amyloidoz układu nerwowego”. Neurotoksykologia . 23 (4–5): 457–60. doi : 10.1016/S0161-813X(02)00065-7 . PMID 12428717 .
- Alves da Costa C (luty 2003). „Ostatnie postępy w biologii komórki alfa-synukleiny: funkcje i dysfunkcje”. Aktualna medycyna molekularna . 3 (1): 17-24. doi : 10.2174/1566524033361690 . PMID 12558071 .
- Ma QL, Chan P, Yoshii M, Uéda K (kwiecień 2003). „Agregacja alfa-synukleiny i choroby neurodegeneracyjne”. Dziennik choroby Alzheimera . 5 (2): 139–48. doi : 10.3233/JAD-2003-5208 . PMID 12719631 .
- Di Rosa G, Puzzo D, Sant'Angelo A, Trinchese F, Arancio O (październik 2003). „Alfa-synukleina: między funkcją synaptyczną a dysfunkcją”. Histologia i histopatologia . 18 (4): 1257–66. doi : 10.14670/HH-18.1257 . PMID 12973692 .
- Baptista MJ, Cookson MR, Miller DW (luty 2004). „Parkina i alfa-synukleina: działania przeciwne w patogenezie choroby Parkinsona” . Neurolog . 10 (1): 63-72. doi : 10.1177/1073858403260392 . PMID 14987449 . S2CID 84671340 .
- Kim S, Seo JH, Suh YH (maj 2004). „Alfa-synukleina, choroba Parkinsona i choroba Alzheimera”. Parkinsonizm i pokrewne zaburzenia . 10 Dodatek 1: S9-13. doi : 10.1016/j.parkreldis.2003.11.005 . PMID 15109581 .
- Sidhu A, Wersinger C, Vernier P (maj 2004). „Regulacja alfa-synukleiny transportera dopaminergicznego: możliwa rola w patogenezie choroby Parkinsona”. Listy FEBS . 565 (1–3): 1–5. doi : 10.1016/j.febslet.2004.03.063 . PMID 15135042 . S2CID 84234417 .
- Vekrellis K, Rideout HJ, Stefanis L (sierpień 2004). „Neurobiologia alfa-synukleiny”. Neurobiologia molekularna . 30 (1): 001–022. doi : 10.1385/MN:30:1:001 . PMID 15247485 . S2CID 19841463 .
- Chiba-Falek O, Nussbaum RL (2004). „Regulacja ekspresji alfa-synukleiny: implikacje dla choroby Parkinsona”. Sympozja Cold Spring Harbor na temat biologii ilościowej . 68 : 409–15. doi : 10.1101/sqb.2003.68.409 . PMID 15338643 .
- Pankratz N, Foroud T (kwiecień 2004). „Genetyka choroby Parkinsona” . NeuroRx . 1 (2): 235–42. doi : 10.1602/neurorx.1.2.235 . PMC 534935 . PMID 15717024 .
- Singleton AB (sierpień 2005). „Zmieniona homeostaza alfa-synukleiny powodująca chorobę Parkinsona: potencjalne role dardarinu”. Trendy w neuronaukach . 28 (8): 416–21. doi : 10.1016/j.tins.2005.05.09 . PMID 15955578 . S2CID 53204736 .
- Yu S, Ueda K, Chan P (2005). „Alfa-synukleina i metabolizm dopaminy”. Neurobiologia molekularna . 31 (1–3): 243-54. doi : 10.1385/MN:31:1-3:243 . PMID 15953825 . S2CID 37132914 .
- Lee HG, Zhu X, Takeda A, Perry G, Smith MA (lipiec 2006). „Pojawiające się dowody na neuroprotekcyjną rolę alfa-synukleiny”. Neurologia Eksperymentalna . 200 (1): 1–7. doi : 10.1016/j.expneurol.2006.04.024 . PMID 16780837 . S2CID 54366198 .
- Giorgi FS, Bandettini di Poggio A, Battaglia G, Pellegrini A, Murri L, Ruggieri S, et al. (2006). „Krótki przegląd roli alfa-synukleiny i proteasomu w eksperymentalnych modelach choroby Parkinsona”. Dziennik transmisji neuronowej. Suplement . Dziennik transmisji neuronowej. Suplementa. 70 (70): 105-9. doi : 10.1007/978-3-211-45295-0_17 . Numer ISBN 978-3-211-28927-3. PMID 17017516 .
Zewnętrzne linki
-
 Multimedia związane z alfa-synukleiną w Wikimedia Commons
Multimedia związane z alfa-synukleiną w Wikimedia Commons - alfa-synukleina w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)
- Lokalizacja genomu ludzkiego SNCA i strona szczegółów genu SNCA w przeglądarce genomu UCSC .