Receptor aktywowany przez proliferatory peroksysomów - Peroxisome proliferator-activated receptor
W dziedzinie biologii molekularnej , z peroksysomów receptory aktywowane przez proliferatory ( PPAR ) są grupą receptorów jądrowych białek , które działają jak czynniki transkrypcyjne regulują ekspresję genów . PPAR odgrywają zasadniczą rolę w regulacji różnicowania komórek , rozwoju i metabolizmu ( węglowodanów , lipidów , białek ) oraz nowotworzenia organizmów wyższych.
Nazewnictwo i dystrybucja tkankowa
| Receptor alfa . aktywowany przez proliferatory peroksysomów | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | PPAR | ||||||
| Alt. symbolika | PPAR | ||||||
| Gen NCBI | 5465 | ||||||
| HGNC | 9232 | ||||||
| OMIM | 170998 | ||||||
| RefSeq | NM_001001928 | ||||||
| UniProt | Q07869 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 22 P12-Q13.1 | ||||||
| |||||||
| Receptor gamma aktywowany przez proliferatory peroksysomów | |||||||
|---|---|---|---|---|---|---|---|
 | |||||||
| Identyfikatory | |||||||
| Symbol | PPARG | ||||||
| Gen NCBI | 5468 | ||||||
| HGNC | 9236 | ||||||
| OMIM | 601487 | ||||||
| RefSeq | NM_005037 | ||||||
| UniProt | P37231 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 3 p25 | ||||||
| |||||||
| delta receptora aktywowanego przez proliferatory peroksysomów | |||||||
|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||
| Symbol | PPARD | ||||||
| Gen NCBI | 5467 | ||||||
| HGNC | 9235 | ||||||
| OMIM | 600409 | ||||||
| RefSeq | NM_006238 | ||||||
| UniProt | Q03181 | ||||||
| Inne dane | |||||||
| Umiejscowienie | Chr. 6 p21.2 | ||||||
| |||||||
Zidentyfikowano trzy typy PPAR: alfa, gamma i delta (beta):
- α (alfa) - wyrażany w wątrobie , nerkach , sercu , mięśniach , tkance tłuszczowej i innych
- β/δ (beta/delta) - wyrażany w wielu tkankach, ale wyraźnie w mózgu , tkance tłuszczowej i skórze
-
γ (gamma) - chociaż transkrybowany przez ten sam gen, ten PPAR poprzez alternatywny splicing jest wyrażany w trzech formach:
- γ1 - wyrażany praktycznie we wszystkich tkankach, w tym w sercu , mięśniach , okrężnicy , nerkach , trzustce i śledzionie
- γ2 - wyrażany głównie w tkance tłuszczowej (o 30 aminokwasów dłuższych niż γ1)
- γ3 - wyrażany w makrofagach , jelicie grubym , białej tkance tłuszczowej .
Historia
PPAR zostały pierwotnie zidentyfikowane u żab Xenopus jako receptory, które indukują proliferację peroksysomów w komórkach. Pierwszy PPAR (PPARα) odkryto podczas poszukiwań celu molekularnego dla grupy środków określanych wówczas jako proliferatory peroksysomów , ponieważ oprócz poprawy wrażliwości na insulinę , zwiększały one liczbę peroksysomów w tkance wątroby gryzoni . Środki te, farmakologicznie spokrewnione z fibratami , odkryto na początku lat osiemdziesiątych. Gdy okazało się, że PPAR odgrywają znacznie bardziej wszechstronną rolę w biologii, środki te nazwano z kolei ligandami PPAR . Najbardziej znanymi ligandami PPAR są tiazolidynodiony ; zobacz poniżej więcej szczegółów.
Po zidentyfikowaniu PPARδ (delta) u ludzi w 1992 r., okazało się, że jest on blisko spokrewniony z PPARβ (beta) wcześniej opisanym w tym samym roku u innych zwierząt ( Xenopus ). Nazwa PPARδ jest powszechnie stosowana w Stanach Zjednoczonych, podczas gdy określenie PPARβ pozostało w Europie, gdzie ten receptor został pierwotnie odkryty w Xenopus .
PPAR zostały tak nazwane, ponieważ odkryto, że indukują proliferację peroksysomów u gryzoni, ale uważa się, że indukcja proliferacji peroksysomów nie występuje u ludzi.
Funkcja fizjologiczna
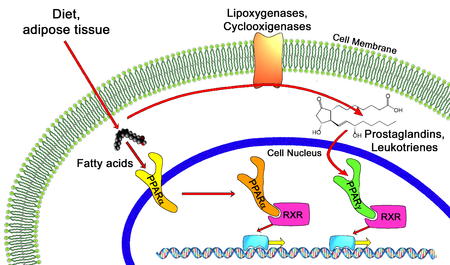
Wszystkie PPAR heterodimeryzują z receptorem retinoidowym X (RXR) i wiążą się z określonymi regionami DNA docelowych genów. Te sekwencje DNA są określane jako PPRE ( elementy odpowiedzi na hormon proliferatora peroksysomów ). Sekwencja konsensusowa DNA to AGGTCANAGGTCA, gdzie N oznacza dowolny nukleotyd . Ogólnie sekwencja ta występuje w regionie promotorowym genu , a gdy PPAR wiąże swój ligand, transkrypcja docelowych genów jest zwiększona lub zmniejszona, w zależności od genu. RXR tworzy także heterodimer z wieloma innymi receptorami (np. witamina D i hormon tarczycy ).
Funkcja PPAR jest modyfikowana przez dokładny kształt ich domeny wiążącej ligand (patrz poniżej) indukowanej przez wiązanie liganda oraz przez szereg białek koaktywatorowych i korepresorowych , których obecność może odpowiednio stymulować lub hamować funkcję receptora.
Endogenne ligandy PPAR obejmują wolne kwasy tłuszczowe , eikozanoidy i witaminę B3 . PPARy jest aktywowany przez PGJ 2 (A prostaglandyn ) i pewnych członków 5-HETE rodziny kwasu arachidonowego metabolitów, w tym 5-okso-15 (S) -HETE i 5-okso-ETE. W przeciwieństwie do tego, PPARa jest aktywowany przez leukotrienów B 4 . Niektórzy członkowie rodziny metabolitów kwasu arachidonowego kwasu 15-hydroksyeikozatetraenowego , w tym 15(S)-HETE, 15(R)-HETE i 15-HpETE, aktywują w różnym stopniu PPAR alfa, beta/delta i gamma. Ponadto doniesiono , że PPARγ jest zaangażowany w patogenezę i wzrost raka. Aktywacja PPARγ przez agonistę RS5444 może hamować wzrost anaplastycznego raka tarczycy. Zobacz przegląd i krytykę ról PPAR gamma w raku.
Genetyka
Trzy główne formy są przepisywane z różnych genów :
- PPARα - chromosom 22q 12-13,1 (OMIM 170998 )
- PPARβ/δ - chromosom 6p 21.2-21.1 (OMIM 600409 )
- PPARγ - chromosom 3p 25 (OMIM 601487 ).
Opisano dziedziczne zaburzenia wszystkich PPAR, prowadzące na ogół do utraty funkcji i towarzyszącej lipodystrofii , insulinooporności i/lub rogowacenia ciemnego . W przypadku PPARγ opisano i zbadano mutację polegającą na przejęciu funkcji ( Pro 12 Ala ), która zmniejsza ryzyko insulinooporności ; jest dość powszechny ( częstotliwość alleli 0,03-0,12 w niektórych populacjach). Natomiast pro 115 gln wiąże się z otyłością . Niektóre inne polimorfizmy mają wysoką częstość występowania w populacjach z podwyższonym wskaźnikiem masy ciała.
Struktura
Podobnie jak inne receptory jądrowe, PPAR mają budowę modułową i zawierają następujące domeny funkcjonalne :
- (A/B) N-końcowy region
- (C) DBD ( domena wiążąca DNA )
- (D) elastyczny obszar zawiasu
- (E) LBD (domena wiążąca ligand)
- (F) region C-końcowy
DBD zawiera dwa motywy palca cynkowego , które wiążą się z określonymi sekwencjami DNA znanymi jako elementy odpowiedzi hormonalnej, gdy receptor jest aktywowany. LBD ma rozbudowaną strukturę drugorzędową składającą się z 13 helis alfa i arkusza beta . Naturalne i syntetyczne ligandy wiążą się z LBD, aktywując lub hamując receptor.
Farmakologia i modulatory PPAR
PPARα i PPARγ są celami molekularnymi wielu sprzedawanych leków . Na przykład fibraty hipolipidemiczne aktywują PPARα, a tiazolidynodiony przeciwcukrzycowe aktywują PPARγ. Syntetyczny chemiczny kwas perfluorooktanowy aktywuje PPARα, podczas gdy syntetyczny kwas perfluoronononowy aktywuje zarówno PPARα, jak i PPARγ. Berberyna aktywuje PPARγ, a także inne naturalne związki z różnych klas chemicznych.
Zobacz też
Bibliografia
Zewnętrzne linki
- [1] (Strona zasobów PPAR, Penn State University).
- [2] (Zasób Receptora Jądrowego).
- Zarys odniesienia PPAR (Rutgers University).
- Receptory peroksysomowe + aktywowane proliferatorami + w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)
- Proteopedia Peroxisome_Proliferator -Activated_Receptors - Struktura receptorów aktywowanych przez proliferatory peroksysomów w interaktywnym 3D