Pasek testowy moczu - Urine test strip
| Pasek testowy moczu | |
|---|---|
 Pasek testowy Multistix do badania moczu z kolorową skalą producenta.
| |
| Cel, powód | określić zmiany patologiczne |
Pasek testowy lub bagnetowy jest podstawowym narzędziem diagnostycznym używanym do określenia zmian patologicznych w moczu pacjenta w standardowej analizie moczu .
| Leukocyty | |
| Azotyn | |
| Urobilinogen | |
| Białko | |
| pH | |
| Hemoglobina | |
| Środek ciężkości | |
| Keton | |
| Bilirubina | |
| Glukoza | |
Standardowy pasek do badania moczu może zawierać do 10 różnych wkładów chemicznych lub odczynników, które reagują (zmieniają kolor) po zanurzeniu w próbce moczu , a następnie wyjęciu z niej . Test można często odczytać w ciągu zaledwie 60 do 120 sekund po zanurzeniu, chociaż niektóre testy wymagają więcej czasu. Rutynowe badanie moczu za pomocą wieloparametrowych pasków jest pierwszym krokiem w diagnostyce szerokiego zakresu chorób. Analiza obejmuje badanie na obecność białek , glukozy , ketonów , hemoglobiny , bilirubiny , urobilinogenu , acetonu , azotynów i leukocytów , a także badanie pH i ciężaru właściwego lub test na zakażenie różnymi patogenami .
Paski testowe składają się z taśmy wykonanej z tworzywa sztucznego lub papieru o szerokości około 5 milimetrów , plastikowe paski mają wkładki impregnowane chemikaliami, które reagują ze związkami obecnymi w moczu, tworząc charakterystyczny kolor. W przypadku pasków papieru reagenty są absorbowane bezpośrednio na papierze. Paski papierowe są często specyficzne dla jednej reakcji (np. pomiaru pH), podczas gdy paski z wkładkami umożliwiają kilka oznaczeń jednocześnie.
Istnieją paski, które służą różnym celom, takie jak paski jakościowe, które określają tylko, czy próbka jest dodatnia czy ujemna, lub są paski półilościowe, które oprócz zapewnienia reakcji dodatniej lub ujemnej zapewniają również oszacowanie wyniku ilościowego, w w tym ostatnim przypadku reakcje barwne są w przybliżeniu proporcjonalne do stężenia badanej substancji w próbce. Odczyt wyników odbywa się poprzez porównanie kolorów podkładek ze skalą kolorów dostarczoną przez producenta, nie jest potrzebne żadne dodatkowe wyposażenie.
Ten rodzaj analizy jest bardzo powszechny w kontroli i monitorowaniu pacjentów z cukrzycą. Czas potrzebny do pojawienia się wyników testu na pasku może wahać się od kilku minut po badaniu do 30 minut po zanurzeniu paska w moczu (w zależności od marki używanego produktu).
Wartości półilościowe są zwykle podawane jako: śladowe, 1+, 2+, 3+ i 4+; chociaż testy można również oszacować w miligramach na decylitr. Automatyczne czytniki pasków testowych dostarczają również wyniki przy użyciu jednostek Międzynarodowego Układu Jednostek Miar .
Metoda badania
Metoda badania polega na całkowitym zanurzeniu paska testowego w dobrze wymieszanej próbce moczu na krótki okres czasu, a następnie wyjęciu go z pojemnika i podparciu krawędzi paska nad otworem pojemnika w celu usunięcia nadmiaru moczu. Następnie pasek pozostawia się na czas niezbędny do zajścia reakcji (zwykle 1 do 2 minut), a na koniec pojawiające się kolory porównuje się ze skalą chromatyczną dostarczoną przez producenta.
Niewłaściwa technika może dawać fałszywe wyniki, na przykład leukocyty i erytrocyty wytrącają się na dnie pojemnika i mogą nie zostać wykryte, jeśli próbka nie zostanie odpowiednio wymieszana, a także jeśli nadmiar moczu pozostanie na pasku po został usunięty z próbki testowej, może spowodować wyciek odczynników z elektrod na sąsiednie elektrody, powodując zmieszanie i zniekształcenie kolorów. Aby do tego nie doszło, zaleca się wysuszenie brzegów paska na papierze chłonnym.
Reakcje na testy uogólnione

pH
Płuca i nerki są głównymi regulatorami równowagi kwasowo-zasadowej organizmu. Równowaga utrzymywana jest poprzez kontrolowane wydalanie kwaśnych wodorów w postaci jonów amoniaku , monouwodornionego fosforanu , słabych kwasów organicznych oraz poprzez reabsorpcję wodorowęglanów poprzez filtrację kłębuszkową w krętych kanalikach nefronu. pH moczu zwykle waha się od 4,5 do 8, przy czym pierwszy mocz oddawany rano jest na ogół bardziej kwaśny, a mocz oddawany po posiłkach na ogół bardziej zasadowy. Nie podano normalnych wartości referencyjnych dla pH moczu, ponieważ rozbieżność jest zbyt duża i wyniki należy rozpatrywać w kontekście innych wymiernych parametrów.
Oznaczanie pH moczu ma dwa główne cele, jeden jest diagnostyczny, a drugi terapeutyczny. Z jednej strony dostarcza informacji o równowadze pomiędzy kwasami i zasadami u pacjenta oraz pozwala na identyfikację substancji obecnych w moczu w postaci krystalicznej. Z drugiej strony, niektóre choroby wymagają od pacjenta utrzymywania pH moczu w określonych wąskich granicach, czy to w celu ułatwienia eliminacji środków chemioterapeutycznych, unikania wytrącania soli, które sprzyjają tworzeniu się kamieni nerkowych, czy w celu ułatwienia kontrola infekcji dróg moczowych. Dieta regulacyjna kontroluje przede wszystkim pH moczu, chociaż można to również kontrolować za pomocą leków. Diety bogate w białko zwierzęce mają tendencję do wytwarzania kwaśnego moczu, podczas gdy diety składające się głównie z warzyw mają tendencję do wytwarzania moczu alkalicznego.
Marki handlowe mierzą pH w przyrostach 0,5 lub 1 jednostki pH między pH 5 a 9. W celu zróżnicowania pH w tym szerokim zakresie powszechnie stosuje się system podwójnego wskaźnika obejmujący czerwień metylową i błękit bromotymolowy . Czerwień metylowa powoduje zmianę koloru z czerwonego na żółty w zakresie pH 4 do 6, a błękit bromotymolowy zmienia się z żółtego na niebieski między pH 6 a 9. W zakresie od 5 do 9 paski pokazują kolory, które zmieniają się z pomarańczowego przy pH 5 , przechodzący przez kolor żółty i zielony do ciemnoniebieskiego przy pH 9.
Środek ciężkości
Jedną z ważnych funkcji nerek jest ponowne wchłanianie wody po filtracji kłębuszkowej. Złożony proces reabsorpcji jest zwykle jedną z pierwszych funkcji nerek dotkniętych chorobą. Ciężar właściwy moczu jest miarą jego gęstości w porównaniu z H 2 O i zależy od ilości i gęstości substancji rozpuszczonych (cząsteczki o większej masie na objętość zwiększają miarę ciężaru właściwego). Pomiaru ciężaru właściwego nie należy mylić z pomiarem stężenia osmotycznego , które jest bardziej związane z liczbą cząstek niż z ich masą.
Test moczu pasek testowy do ciężaru opiera się na zmianę stałej dysocjacji (pKa a ) anionowego polielektrolitu (poli (eter metylowo-winylowy / bezwodnik maleinowy)), w środowisku alkalicznym zjonizowanego i uwalnia jony wodorowe w stosunku do liczba kationów obecnych w roztworze. Im większe stężenie kationów w moczu, tym więcej jonów wodorowych jest uwalnianych, co zmniejsza pH. Wkładka zawiera również błękit bromotymolowy, który mierzy tę zmianę pH. Należy pamiętać, że pasek testowy mierzy jedynie stężenie kationów, dlatego możliwe jest, że mocz o wysokim stężeniu niejonowych substancji rozpuszczonych (takich jak glukoza lub mocznik) lub ze związkami o dużej masie cząsteczkowej (takich jak media stosowane do kontrast) da wynik, który będzie błędnie niższy niż wynik zmierzony densytometrycznie. Kolory różnią się od ciemnoniebieskiego z odczytem 1.000 do żółtego przy odczycie 1.030.
- W środowisku alkalicznym Polielektrolit-H n + Kationy n+ → Polielektrolit-Kationy + nH +
- W środowisku alkalicznymH + + Błękit bromotymolowy (niebieski) → Błękit bromotymolowy-H + (żółty)
Podwyższone stężenia białka dają nieznacznie podwyższone wyniki gęstości właściwej w wyniku błędu wskaźnika białka; ponadto próbki o pH powyżej 6,5 dają niższe odczyty w wyniku błędu systematycznego wskaźnika. Z tego powodu producenci zalecają dodanie 5 jednostek do odczytu ciężaru właściwego, gdy pH jest większe niż 6,5.
Krew
Krew może być obecna w moczu w postaci nienaruszonych czerwonych krwinek (krwiomocz) lub jako produkt destrukcji czerwonych krwinek, hemoglobina (hemoglobinuria). Krew obecną w dużych ilościach można wykryć wizualnie. Hematuria wytwarza mętny czerwony mocz, a hemoglobinuria pojawia się jako wyraźnie czerwona próbka. Każda ilość krwi większa niż pięć komórek na mikrolitr moczu jest uważana za istotną klinicznie; nie można polegać na badaniu wzrokowym w celu wykrycia obecności krwi. Badanie mikroskopowe osadu moczu pokazuje nienaruszone czerwone krwinki, ale nie wykryto wolnej hemoglobiny wytwarzanej przez zaburzenia hemolityczne lub lizę czerwonych krwinek. Dlatego testy chemiczne hemoglobiny zapewniają najdokładniejszą średnią do określania obecności krwi. Po wykryciu krwi badanie mikroskopowe można wykorzystać do odróżnienia krwiomoczu od hemoglobinurii.
Testy chemiczne krwi wykorzystują aktywność pseudoperoksydazy hemoglobiny do katalizowania reakcji między składnikiem hemowym hemoglobiny i mioglobiny a chromogenem (substancją, która nabiera koloru po reakcji chemicznej) tetrametylobenzydyną w celu wytworzenia utlenionego chromogenu, który ma zielono-niebieski kolor. Producenci pasków odczynnikowych wprowadzają nadtlenek i tetrametylobenzydynę do obszaru badania krwi. Dostarczono dwa wykresy kolorów, które odpowiadają reakcjom zachodzącym w przypadku hemoglobinurii, mioglobinurii i krwiomoczu (RBC). W obecności wolnej hemoglobiny/mioglobiny na poduszce pojawia się jednolity kolor od ujemnego żółtego przez zielony do silnie dodatniego zielono-niebieskiego. W przeciwieństwie do tego, nienaruszone czerwone krwinki są poddawane lizie, gdy stykają się z poduszką, a uwolniona hemoglobina wywołuje izolowaną reakcję, której efektem jest plamkowaty wzór na poduszce. Testy paskowe z odczynnikami mogą wykryć stężenia tak niskie, jak pięć czerwonych krwinek na mikrolitr; należy jednak zachować ostrożność podczas porównywania tych danych z rzeczywistymi wartościami mikroskopowymi, ponieważ chłonna natura podpaski przyciąga część moczu. Terminy ślad, mały, średni i duży (lub ślad, 1+, 2+ i 3+) są używane do raportowania.
Można zaobserwować fałszywie dodatnie reakcje z powodu zakażenia menstruacyjnego. Występują również wtedy, gdy w pojemniku na próbki znajdują się silnie utleniające detergenty. Peroksydaza roślinna i enzymy bakteryjne, w tym peroksydaza Escherichia coli , mogą również powodować reakcje fałszywie dodatnie. Dlatego osady zawierające bakterie należy dokładnie sprawdzać pod kątem obecności czerwonych krwinek. Tradycyjnie kwas askorbinowy (witamina C) jest kojarzony z fałszywie ujemnymi reakcjami paska odczynnikowego dla krwi. Zarówno Multistix, jak i Chemstrip zmodyfikowały swoje paski z odczynnikami, aby zredukować tę interferencję do bardzo wysokich poziomów kwasu askorbinowego, a Chemstrip pokrywa wkładkę z odczynnikiem siatką impregnowaną jodanem, która utlenia kwas askorbinowy przed dotarciem do wkładu reakcyjnego. Reakcje fałszywie ujemne mogą wystąpić, gdy mocz o wysokim ciężarze właściwym zawiera krepowane krwinki czerwone, które nie ulegają lizie w kontakcie z wkładką z odczynnikiem. Zmniejszoną reaktywność można również zaobserwować, gdy jako konserwant stosuje się formalinę lub gdy obecny jest lek na nadciśnienie kaptopril lub wysokie stężenie azotynów. Czerwone krwinki osadzają się na dnie pojemnika na próbki, a brak wymieszania próbki przed badaniem powoduje fałszywie zaniżony odczyt.
Zidentyfikowane choroby
Za pomocą rutynowych badań można zidentyfikować wczesne objawy następujących czterech grup:
- Choroby nerek i dróg moczowych
- Zaburzenia metabolizmu węglowodanów (cukrzyca)
- Choroby wątroby i zaburzenia hemolityczne
- Infekcje dróg moczowych
Dróg moczowych
Parametry przesiewowe: Wiele chorób nerek i dróg moczowych może być bezobjawowych przez długi czas. Rutynowa analiza moczu jest zalecana jako podstawowy, ale fundamentalny krok w wykrywaniu uszkodzenia nerek i/lub choroby układu moczowego na wczesnym etapie, szczególnie w populacjach wysokiego ryzyka, takich jak cukrzycy , osoby z nadciśnieniem , Afroamerykanie , Polinezyjczycy i osoby z wywiadem rodzinnym .
Specyficzne choroby nerek i dróg moczowych, które można zidentyfikować obejmują: przewlekłą chorobę nerek , kłębuszkowe zapalenie nerek , białkomocz i krwiomocz .
Testowanie białka
Spośród rutynowych testów chemicznych wykonywanych na moczu najbardziej wskazującym na chorobę nerek jest oznaczanie białka. Proteinuria jest często związana z wczesną chorobą nerek, co sprawia, że badanie białka w moczu jest ważną częścią każdego badania fizykalnego. Normalny mocz zawiera bardzo mało białka, zwykle mniej niż 100–300 mg/l lub 100 mg na 24 godziny jest wydalane. Białko to składa się głównie z białek surowicy o niskiej masie cząsteczkowej, które zostały przefiltrowane przez kłębuszki oraz białek wytwarzanych w układzie moczowo-płciowym. Ze względu na niską masę cząsteczkową albumina jest głównym białkiem surowicy występującym w osoczu, normalna zawartość albuminy w moczu jest niska, ponieważ większość albumin obecnych w kłębuszkach nerkowych nie jest filtrowana, a duża część przefiltrowanej albuminy jest ponownie wchłaniana przez kanaliki. Inne białka obejmują niewielkie ilości mikroglobulin surowicy i kanalików. Uromodulina wytwarzana przez komórki nabłonka kanalików nerkowych i białka z wydzielin gruczołu krokowego, nasienia i pochwy. Uromodulina jest rutynowo wytwarzana w dystalnej rurce krętej i tworzy matrycę odlewów.
Tradycyjne testy paskowe dla białek wykorzystują zasadę błędu białkowego wskaźników w celu wytworzenia widocznej reakcji kolorymetrycznej. Wbrew powszechnemu przekonaniu, że wskaźniki wytwarzają określone kolory w odpowiedzi na określone poziomy pH, niektóre wskaźniki zmieniają kolor w obecności białka, mimo że pH podłoża pozostaje stałe. Dzieje się tak, ponieważ białko przyjmuje jony wodorowe ze wskaźnika. Test jest bardziej czuły na albuminę, ponieważ albumina zawiera więcej grup aminowych akceptujących jony wodorowe niż inne białka. W zależności od producenta, obszar białkowy paska zawiera różne chemikalia. Multistix zawiera błękit tetrabromofenolowy, a Chemstrip zawiera 3',3”,5',5”-tetrachlorofenol, 3,4,5,6-tetrabromosulfonftaleinę. Oba zawierają bufor kwasowy, aby utrzymać pH na stałym poziomie. Przy poziomie pH 3 oba wskaźniki wydają się żółte przy braku białka. Jednak wraz ze wzrostem stężenia białka kolor przechodzi przez różne odcienie zieleni, a na końcu na niebieski. Odczyty są podawane jako ujemne, śladowe, 1+, 2+, 3+ i 4+ lub wartości półilościowe 30, 100, 300 lub 2000 mg/dl odpowiadające każdej zmianie koloru. Uważa się, że wartości śladowe są mniejsze niż 30 mg/dl. Interpretacja odczytów śladów może być trudna.
Głównym źródłem błędów w paskach z odczynnikami jest silnie zbuforowany, zasadowy mocz, który zastępuje system buforów kwasowych, powodując wzrost pH i zmianę koloru niezwiązaną ze stężeniem białka. Podobnie błąd techniczny polegający na tym, że wkładka z odczynnikiem pozostaje w kontakcie z moczem przez dłuższy czas, może spowodować usunięcie buforu. Fałszywie dodatnie odczyty uzyskuje się, gdy reakcja nie zachodzi w warunkach kwasowych. Silnie zabarwiony mocz i zanieczyszczenie pojemnika czwartorzędowymi związkami amonu, detergentami i środkami antyseptycznymi również powodują fałszywie dodatnie odczyty. Fałszywie dodatni odczyt śladu może wystąpić w próbkach o wysokim ciężarze właściwym.
Badanie hemoglobiny i mioglobiny
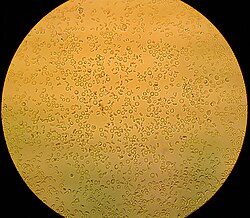
Spośród wszystkich normalnie badanych parametrów obecność krwi w moczu jest najściślej związana z urazowym uszkodzeniem nerek lub układu moczowo-płciowego. Najczęstszymi przyczynami krwiomoczu są: kamica nerkowa , choroba kłębuszków nerkowych , nowotwory , odmiedniczkowe zapalenie nerek , narażenie na nefrotoksyny oraz leczenie antykoagulantami . Niepatologiczny krwiomocz można zaobserwować po dużym wysiłku fizycznym i podczas menstruacji . Normalna liczba czerwonych krwinek w moczu zwykle nie powinna przekraczać 3 na pole wysokiej mocy.
Pasek testowy moczu wykazujący dodatni wynik badania krwi może również wskazywać na hemoglobinurię , której nie można wykryć pod mikroskopem ze względu na lizę czerwonych krwinek w drogach moczowych (szczególnie w moczu o odczynie zasadowym lub rozcieńczonym) lub hemolizę wewnątrznaczyniową . W normalnych warunkach tworzenie się kompleksów haptoglobina- hemoglobina zapobiega filtracji kłębuszkowej, ale jeśli hemoliza jest nasilona, zdolność wychwytu haptoglobiny jest przekroczona i hemoglobina może pojawić się w moczu. Hemoglobinuria może być spowodowana anemią hemolityczną, przetoczeniami krwi, rozległymi oparzeniami , ugryzieniem pająka pustelnika (Loxosceles), infekcjami i dużym wysiłkiem fizycznym.
Test paskowy moczu na krew opiera się na aktywności pseudoperoksydazy hemoglobiny, która katalizuje reakcję między nadtlenkiem wodoru a chromogenem tetrametylobenzydyną w celu wytworzenia ciemnoniebieskiego produktu utleniania. wynikowy kolor może zmieniać się od zielonego do ciemnoniebieskiego w zależności od ilości hemoglobiny.
- Katalizowany przez hemoglobinę działającą jako peroksydaza H 2 O 2 + Chromogen → Chromogen utleniony (kolorowy) + H 2 OReakcja jest katalizowana nie tylko przez hemoglobinę we krwi, inne globiny z grupą hem, takie jak mioglobina, mogą również katalizować tę samą reakcję.
Obecność mioglobiny w moczu daje dodatni wynik w badaniu krwi z paska testowego, ale mocz wydaje się przejrzysty z zabarwieniem od czerwonego do brązowego. Obecność mioglobiny w miejscu hemoglobiny może być spowodowana patologiami związanymi z uszkodzeniem mięśni ( rabdomioliza ), takimi jak urazy , zespół zmiażdżenia , przedłużająca się śpiączka, konwulsje , postępujący zanik mięśni , alkoholizm , nadużywanie heroiny i wzmożona aktywność fizyczna.
Frakcja hemowa tych białek jest toksyczna dla kanalików nerkowych, a podwyższone stężenia mogą powodować ostre uszkodzenie nerek .
W celu odróżnienia hemoglobinurii od mioglobinurii można zastosować test strącania siarczanem amoniaku. Polega to na dodaniu 2,8 g siarczanu amoniaku do 5 ml odwirowanego moczu, dokładnym wymieszaniu, a po 5 minutach odfiltrowaniu próbki i ponownym odwirowaniu. Hemoglobina wytrąca się z siarczanem amoniaku, ale nie z mioglobiną. Analiza supernatantu na obecność krwi za pomocą paska testowego da wynik dodatni w przypadku obecności mioglobiny i ujemny w przypadku obecności hemoglobiny.
Test może dać fałszywie pozytywne wyniki, jeśli na materiale laboratoryjnym użytym do analizy znajdują się silne pozostałości utleniaczy lub nadtlenków.
Zaburzenia węglowodanowe
- Glukoza – zidentyfikowana jako glikozuria
- Ketony - Zidentyfikowane jako Ketonuria (patrz także kwasica ketonowa i ketoza )
Około 30-40% cukrzyków typu I i około 20% cukrzyków typu II cierpi z czasem na nefropatię, dlatego wczesne rozpoznanie cukrzycy ma duże znaczenie dla dalszego stanu zdrowia tych pacjentów.
Specyficzne zaburzenia metabolizmu węglowodanów, które można zidentyfikować, obejmują cukrzycę , glukozurię i ketonurię .
Test glukozy
W normalnych warunkach prawie cała glukoza usunięta w kłębuszkach jest ponownie wchłaniana w proksymalnym kanaliku krętym. Jeśli poziom glukozy we krwi wzrasta, jak to ma miejsce w przypadku cukrzycy, zdolność kanalików krętych do reabsorpcji glukozy zostaje przekroczona (efekt znany jako nerkowy próg reabsorpcji ). Dla glukozy próg ten wynosi 160–180 mg/dl. Stężenia glukozy różnią się u poszczególnych osób, a zdrowa osoba może wykazywać przejściową glukozurię po posiłku bogatym w cukry; dlatego najbardziej reprezentatywne wyniki pochodzą z próbek uzyskanych co najmniej dwie godziny po spożyciu pokarmu.
Wykrywanie glukozy za pomocą pasków testowych opiera się na reakcji enzymatycznej oksydazy glukozowej . Enzym ten katalizuje utlenianie glukozy przez tlen atmosferyczny, tworząc D-glukono-δ-lakton i nadtlenek wodoru . Druga powiązana reakcja, w której pośredniczy peroksydaza , katalizuje reakcję między nadtlenkiem a chromogenem (substancją, która nabiera koloru po reakcji chemicznej), tworząc barwny związek, który wskazuje stężenie glukozy.
- 1) Katalizowany przez oksydazę glukozową Glukoza + O 2 → D-glukono-δ-lakton + H 2 O 2
- 1) Katalizowany przez oksydazę glukozową
- 2) Katalizowane przez peroksydazę H 2 O 2 + Chromogen → Chromogen utleniony (kolorowy) + H 2 O
- 2) Katalizowane przez peroksydazę
Reakcja jest specyficzna dla glukozy, jak to ma miejsce we wszystkich reakcjach enzymatycznych, ale może dawać wyniki fałszywie dodatnie ze względu na obecność śladów silnych utleniaczy lub nadtlenku ze środków dezynfekujących stosowanych w instrumentach laboratoryjnych.
Test ketonowy
Termin ketony lub ciała ketonowe w rzeczywistości odnosi się do trzech produktów pośrednich w metabolizmie kwasów tłuszczowych ; aceton , kwas acetooctowy i kwas beta- hydroksymasłowy . Podwyższone stężenia ketonów na ogół nie występują w moczu, ponieważ wszystkie te substancje są całkowicie metabolizowane, wytwarzając energię, dwutlenek węgla i wodę. Jednak zakłócenie metabolizmu węglowodanów może prowadzić do zaburzeń równowagi metabolicznej i pojawienia się ketonów jako produktu ubocznego metabolizmu rezerw tłuszczowych organizmu.
Wzrost metabolizmu tłuszczów może być skutkiem wygłodzenia lub złego wchłaniania , niezdolności do metabolizowania węglowodanów (jak to ma miejsce np. w cukrzycy) lub strat spowodowanych częstymi wymiotami.
Kontrola ketonów w moczu jest szczególnie przydatna w leczeniu i monitorowaniu cukrzycy typu 1 . Ketonuria wskazuje na niedobór insuliny, który wskazuje na potrzebę regulacji jej dawkowania. Wzrost stężenia ketonów we krwi powoduje zaburzenia równowagi wodno-elektrolitowej , odwodnienie, a jeśli nie zostanie skorygowane, kwasicę, aw końcu śpiączkę cukrzycową .
Trzy związki ketonowe pojawiają się w moczu w różnych proporcjach, chociaż proporcje te są względnie stałe w różnych próbkach, ponieważ zarówno aceton, jak i kwas beta-hydroksymasłowy są wytwarzane z kwasu acetooctowego. Proporcje to 78% kwas beta-hydroksymasłowy, 20% kwas acetooctowy i 2% aceton.
Test stosowany w paskach do badania moczu opiera się na reakcji nitroprusydku sodu (nitrożelazicyjanek). W tej reakcji kwas acetooctowy w środowisku alkalicznym reaguje z nitroprusydkiem sodu tworząc kompleks w kolorze magenta:
- Na 2 [Fe(CN) 5 NO] + CH 3 COCH 2 COOH + 2Na(OH) → Na 4 [Fe(CN) 5 -N=CHCOCH 2 COOH] (magenta) + H 2 O
- Nitroprusydek sodu + kwas acetooctowy + środowisko alkaliczne → kompleks różowo-magenta + woda
Test nie mierzy kwasu beta-hydroksymasłowego i jest tylko słabo wrażliwy na aceton po dodaniu do reakcji glicyny . Jednakże, ponieważ związki te pochodzą od kwasu acetooctowego, można założyć ich istnienie i dlatego nie jest konieczny oddzielny test. Leki zawierające grupy sulfhydrylowe, takie jak merkaptoetanosulfonian Na ( Mesna ) oraz kaptopril i L-DOPA, mogą dawać nietypowe zabarwienie. Fałszywie ujemny wynik może wystąpić w próbkach, które nie były odpowiednio przechowywane z powodu ulatniania się i degradacji bakteryjnej.
Choroby wątroby i krwi
W wielu chorobach wątroby pacjenci często wykazują oznaki patologii dopiero w późnym stadium. Wczesna diagnoza pozwala na wdrożenie odpowiednich środków terapeutycznych w odpowiednim czasie, unikając szkód następczych i dalszych infekcji.
Specyficzne choroby wątroby i zaburzenia hemolityczne, które można zidentyfikować, obejmują chorobę wątroby (z towarzyszącą żółtaczką ), marskość wątroby , urobilinogenuria i bilirubinuria .
Test bilirubiny
Bilirubina jest silnie pigmentowanym związkiem, który jest produktem ubocznym rozkładu hemoglobiny. Hemoglobina, która jest uwalniana po wycofaniu z obiegu starych czerwonych krwinek przez system fagocytów jednojądrzastych (zlokalizowanych w wątrobie i śledzionie ), jest rozkładana na jej składniki; żelazo , protoporfiryna i białko . Komórki układu przekształcają protoporfirynę w nieskoniugowaną bilirubinę, która przechodzi przez układ krążenia związana z białkiem, zwłaszcza albuminą. Nerki nie są w stanie odfiltrować tej bilirubiny, ponieważ jest ona związana z białkiem, jednak jest sprzężona z kwasem glukuronowym w wątrobie, tworząc rozpuszczalną w wodzie sprzężoną bilirubinę. Ta sprzężona bilirubina normalnie nie pojawia się w moczu, ponieważ jest wydalana bezpośrednio z jelita wraz z żółcią . Bakterie jelitowe redukują bilirubinę do urobilinogenu , który jest później utleniany i wydalany z kałem jako sterkobilina lub z moczem jako urobilina .
Bilirubina sprzężona pojawia się w moczu, gdy normalny cykl degradacji ulega zmianie z powodu niedrożności dróg żółciowych lub gdy uszkodzona jest funkcjonalna integralność nerek. Pozwala to na ucieczkę sprzężonej bilirubiny do krążenia, co ma miejsce w zapaleniu wątroby i marskości wątroby .
Wykrycie bilirubiny w moczu jest wczesnym wskaźnikiem choroby wątroby, a jej obecność lub brak może posłużyć do określenia przyczyn żółtaczki klinicznej .
Żółtaczka spowodowana przyspieszonym niszczeniem krwinek czerwonych nie powoduje bilirubinurii, ponieważ wysoki poziom bilirubiny w surowicy występuje w postaci nieskoniugowanej i nerki nie są w stanie jej wydalić.
Paski testowe wykorzystują reakcję diazowania w celu wykrycia bilirubiny. Bilirubina łączy się z solą diazoniową (2,4-dichloroaniliną lub 2,6-dichlorobenzeno-diazoniowo-tetrafluoroboranem) w środowisku kwaśnym, tworząc barwnik azowy o zabarwieniu od różowego do fioletowego:
- W środowisku kwaśnym Glukuronid bilirubiny + sól diazoniowa→ Barwnik azowy (fioletowy)
- W środowisku kwaśnym
Fałszywie dodatnie reakcje mogą być spowodowane nietypowymi pigmentami w moczu (na przykład żółtawo-pomarańczowe metabolity fenazopirydyny , indican i metabolity leku Lodine ( Etodolac )). Fałszywie negatywy mogą być również podane przez źle przechowywane próbki, ponieważ bilirubina jest światłoczuła i ulega fotooksydacji do biliwerdyny pod wpływem światła lub może wystąpić hydroliza glukuronidu, wytwarzając wolną bilirubinę, która jest mniej reaktywna.
Test urobilinogenu
Bakterie jelitowe przekształcają sprzężoną bilirubinę, która jest wydalana przez przewód żółciowy do jelita w urobilinogen i sterkobilinogen . Część urobilinogenu jest ponownie wchłaniana w jelicie, a następnie krąży we krwi do wątroby, gdzie jest wydalana. Niewielka część recyrkulowanego urobilinogenu jest odfiltrowywana przez nerki i pojawia się w moczu (mniej niż 1 mg/dl moczu). Sterkobilinogen nie może zostać wchłonięty i pozostaje w jelicie.
Każde pogorszenie funkcji wątroby zmniejsza jej zdolność do przetwarzania recyrkulowanego urobilinogenu. Nadmiar, który pozostaje we krwi, jest odfiltrowywany przez nerki i pojawia się w moczu. W przypadku wystąpienia zaburzeń hemolitycznych ilość niezwiązanej bilirubiny we krwi wzrasta, powodując zwiększenie wydalania bilirubiny sprzężonej przez wątrobę, co skutkuje zwiększeniem ilości urobilinogenu, co z kolei powoduje zwiększenie wchłaniania zwrotnego, recyrkulacji i wydalania nerkowego.
Reakcje zachodzące na pasku testowym różnią się w zależności od producenta, ale w rzeczywistości najczęściej stosuje się dwie reakcje. Niektórzy producenci stosują reakcję Ehrlicha (1), w której urobilinogen reaguje z p-dimetyloaminobenzaldehydem ( odczynnik Ehrlicha ) w celu wytworzenia kolorów od jasnego do ciemnego różu. Inni producenci stosują reakcję sprzęgania diazowego (2), w której wykorzystuje się tetrafluoroboran 4-metoksybenzeno-diazoniowy do wytworzenia kolorów od białego do różowego. Ta ostatnia reakcja jest bardziej specyficzna.
- (1) Reakcja na Multistix (w środowisku kwaśnym) Urobilinogen + p-dimetyloaminobenzaldehyd → Czerwony barwnik
- (1) Reakcja na Multistix (w środowisku kwaśnym)
- (2) Reakcja na Chemstrip (w środowisku kwaśnym) Urobilinogen + 4-metoksybenzeno-diazoniowy tetrafluoroboran → Czerwony barwnik azowy
- (2) Reakcja na Chemstrip (w środowisku kwaśnym)
Szereg substancji zakłóca reakcję Ehrlicha na pasku Multistix: porfobilinogen, indican, kwas p-aminosalicylowy, sulfonamid, metylodopa, prokaina i chlorpromazyna. Test należy przeprowadzić w temperaturze pokojowej, ponieważ czułość reakcji wzrasta wraz z temperaturą. Źle przechowywane próbki mogą dawać wyniki fałszywie ujemne, ponieważ urobilinogen ulega fotooksydacji do urobiliny, która nie reaguje. Formaldehyd użyty jako środek konserwujący daje wyniki fałszywie ujemne w obu reakcjach.
Infekcje dróg moczowych
Można zidentyfikować infekcje dróg moczowych, w tym bakteriomocz i ropomocz .
Test azotynów
Test na azotyny to szybka metoda przesiewowa pod kątem możliwych bezobjawowych infekcji wywołanych przez bakterie redukujące azotany. Niektóre gatunki bakterii Gram-ujemnych, które najczęściej powodują infekcje dróg moczowych ( Escherichia coli , Enterobacter , Klebsiella , Citrobacter i Proteus ) posiadają enzymy, które redukują azotany obecne w moczu do azotynów. Test jest szybkim badaniem przesiewowym pod kątem możliwych infekcji przez bakterie jelitowe, ale nie zastępuje testów moczu ani badania mikroskopowego jako narzędzi diagnostycznych ani późniejszego monitorowania, ponieważ wiele innych mikroorganizmów, które nie redukują azotanów ( bakterie Gram-dodatnie i drożdże) może również powodować infekcje dróg moczowych.
Paski reaktywne wykrywają azotyn za pomocą reakcji Griessa, w której azotyn reaguje w środowisku kwaśnym z aromatyczną aminą (kwasem para-arsanilowym lub sulfanilamidem) w celu utworzenia soli diazoniowej, która z kolei reaguje z tetrahydrobenzochinoliną, tworząc różowy barwnik azowy .
- 1) W środowisku kwaśnym Kwas para-arsanilowy lub sulfanilamid + NO−
2 → Sól diazoniowa
- 1) W środowisku kwaśnym
- 2) W środowisku kwaśnym Sól diazoniowa + tetrahydrobenzochinolina → Różowy barwnik azowy
- 2) W środowisku kwaśnym
Test azotynowy nie jest szczególnie wiarygodny, a ujemne wyniki w obecności objawów klinicznych nie należą do rzadkości, co oznacza, że nie należy go traktować jako rozstrzygającego. Negatywne wyniki można uzyskać w obecności mikroorganizmów nieredukujących azotanów. Bakterie redukujące azotyny muszą pozostawać w kontakcie z azotanami wystarczająco długo, aby wytworzyć wykrywalne ilości (pierwszy mocz produkowany rano lub przynajmniej z zatrzymaniem moczu wynoszącym 4 godziny). Duża liczba bakterii może reagować redukując azotyny do azotu, co daje fałszywie ujemny wynik. Stosowanie antybiotyków hamuje metabolizm bakterii, powodując negatywne wyniki, mimo że bakterie są obecne. Ponadto niektóre substancje, takie jak kwas askorbinowy, będą konkurować z reakcją Greissa, dając niereprezentatywnie niskie odczyty.
Test leukocytów

Normalne jest znalezienie do 3 (czasami 5) leukocytów na pole wysokiej mocy (40X) w próbce moczu, przy czym kobiety uzyskują nieco wyższe wyniki z powodu zakażenia pochwy. Wyższe liczby wskazują na infekcję dróg moczowych. Test paskowy moczu na obecność białych krwinek wykrywa esterazę leukocytarną, która jest obecna w azurofilnych ziarnistościach monocytów i granulocytów ( neutrofilowych , eozynofilowych i bazofilowych ). Bakterie, limfocyty i komórki nabłonkowe z układu moczowo-płciowego nie zawierają esteraz. Granulocyty neutrofili to leukocyty najczęściej związane z infekcjami dróg moczowych. Dodatni wynik testu na esterazy leukocytów zwykle wskazuje na obecność bakterii i dodatni test azotynowy (choć nie zawsze tak jest). Infekcje wywołane przez Trichomonas , Chlamydia i drożdżaki powodują leukocyturię bez bakteriomoczu. Zapalenie tkanek nerek ( śródmiąższowe zapalenie nerek ) może powodować leukocyturię, w szczególności toksyczne śródmiąższowe zapalenie nerek z przewagą eozynofili.
Test na esterazy leukocytów ma charakter wyłącznie orientacyjny i nie powinien być stosowany wyłącznie do diagnozy, ponieważ nie zastępuje badań mikroskopowych ani badań posiewu moczu.
Reakcja paska testowego moczu opiera się na działaniu esterazy leukocytów katalizującej hydrolizę estru kwasu indolokarboksylowego. Uwolniony indoksyl łączy się z solą diazoniową w celu wytworzenia fioletowego barwnika azolowego.
- 1) Reakcja katalizowana przez esterazę leukocytów Ester kwasu indolokarboksylowego → Indoksyl + kwas
- 1) Reakcja katalizowana przez esterazę leukocytów
- 2) W środowisku kwaśnym Indoksyl + sól diazoniowa → Fioletowy barwnik azolowy
- 2) W środowisku kwaśnym
Reakcja esterazy trwa około 2 minut. Obecność silnych utleniaczy lub formaldehydu może powodować fałszywie dodatnie wyniki. Wyniki fałszywie ujemne są związane z podwyższonymi stężeniami białka (powyżej 500 mg/dl), glukozy (powyżej 3 g/dl), kwasu szczawiowego i askorbinowego . Mocz o wysokim ciężarze właściwym może również powodować tworzenie się leukocytów, co może utrudniać uwalnianie esteraz.
Granica wykrywalności
Granica wykrywalności testu to stężenie, przy którym test zaczyna się zmieniać z negatywnego na pozytywny. Chociaż granica wykrywalności może się różnić w zależności od próbek moczu, granica wykrywalności jest definiowana jako stężenie analitu, które powoduje pozytywną reakcję w 90% badanych moczu.
| Parametr |
Zakres odniesienia |
Praktyczna granica wykrywalności |
|---|---|---|
|
Środek ciężkości
Zakres odniesienia Zakres fizjologiczny |
1,016 - 1,022 1.002 - 1.035 |
Zakres: 1.000 - 1.030 |
|
wartość PH
Pierwszy poranny mocz W ciągu dnia |
5 - 6 4,8 - 7,4 |
Zakres: 5 - 9 |
|
Leukocyty
Zakres odniesienia Szara strefa |
< 10 Leu/µl 10 - 20 Leu/µl |
10-25 leu/µl |
| Azotyn | - | 0,05 mg/dl (11 µmol/l) |
|
Białko
Albumina |
< 2 mg/dl |
6 mg/dl |
|
Glukoza
Pierwszy poranny mocz W ciągu dnia |
< 20 mg/dl < 30 mg/dl |
40 mg/dl (2,2 mmol/l) |
|
Ketony
kwas acetooctowy Aceton |
< 5 mg/dl - |
5 mg/dl (0,5 mmol/l) 40 mg/dl (7 mmol/l) |
| Urobilinogen | < 1 mg/dl | 0,4 mg/dl (7 µmol/l) |
| Bilirubina | < 0,2 mg/dl | 0,5 mg/dl (9 µmol/l) |
|
Krew
Erytrocyty Hemoglobina |
0 - 5 ery/µl - |
5 ery/µl 0,03 mg/dl Hb |
Zastosowania medyczne
Paski testowe moczu mogą być używane w wielu obszarach opieki zdrowotnej, w tym w badaniach przesiewowych do rutynowych badań, monitorowania leczenia, samokontroli pacjentów i/lub ogólnej profilaktyce.
Ekranizacja
Paski testowe moczu są używane do badań przesiewowych zarówno w szpitalach, jak i w praktyce ogólnej. Celem badań przesiewowych jest wczesna identyfikacja prawdopodobnych pacjentów poprzez badanie dużych grup populacji. Znaczenie badań przesiewowych w kierunku cukrzycy i chorób nerek w populacjach wysokiego ryzyka staje się bardzo duże.
Monitorowanie leczenia
Monitorowanie leczenia za pomocą pasków do badania moczu pozwala pracownikowi służby zdrowia sprawdzić wyniki przepisanej terapii, a w razie potrzeby wprowadzić zmiany w przebiegu terapii.
Samokontrola
Samokontrola za pomocą pasków testowych moczu pod kierunkiem pracownika służby zdrowia jest skuteczną metodą monitorowania stanu chorobowego. Dotyczy to zwłaszcza diabetyków , u których idea samokontroli stanu metabolicznego (oznaczenia glukozy i ketonów) jest oczywista.
Weterynaryjny
W weterynarii, zwłaszcza u kotów i psów, pasek testowy można wykorzystać do analizy moczu.
Historia
W wielu kulturach mocz był kiedyś uważany za mistyczny płyn, aw niektórych kulturach jest uważany za taki do dnia dzisiejszego. Jego zastosowania obejmowały gojenie ran, stymulację mechanizmów obronnych organizmu oraz badania w celu diagnozowania obecności chorób.
Dopiero pod koniec XVIII wieku lekarze zainteresowani chemią zwrócili uwagę na naukowe podstawy analizy moczu i jej zastosowanie w medycynie praktycznej.
- 1797 - Carl Friedrich Gärtner (1772-1850) wyraził życzenie łatwego badania moczu pod kątem choroby przy łóżku pacjenta.
- 1797 – William Cumberland Cruikshank (1745–1800) po raz pierwszy opisał właściwość koagulacji przy ogrzewaniu, wykazywaną przez wiele moczu.
- 1827 – angielski lekarz Richard Bright opisuje kliniczny objaw zapalenia nerek w „Raportach z przypadków medycznych”.
- 1840 – Pojawienie się chemicznej diagnostyki moczu mającej na celu wykrywanie patologicznych składników moczu
- 1850 - paryski chemik Jules Maumené (1818-1898) opracowuje pierwsze „paski testowe”, kiedy impregnuje pasek wełny merynosów „protochlorkiem cyny” (chlorkiem cynawym). Po nałożeniu kropli moczu i podgrzaniu nad świecą pasek natychmiast robił się czarny, jeśli mocz zawierał cukier.
- 1883 - angielski fizjolog George Oliver (1841–1915) sprzedaje swoje „Publiki testowe moczu”
- około. 1900 – Papiery odczynnikowe stają się dostępne w handlu z firmy chemicznej Helfenberg AG.
- 1904 - Znany jest test na obecność krwi metodą chemiczną na mokro z użyciem benzydyny.
- około. 1920 - wiedeński chemik Fritz Feigl (1891–1971) publikuje swoją technikę „ analizy punktowej ”.
- Lata 30. XX wieku – Diagnostyka moczu robi duży postęp, ponieważ poprawia się niezawodność, a wyniki testów stają się coraz łatwiejsze.
- Lata 50. XX wieku – Paski do badania moczu w znaczeniu używanym dzisiaj zostały po raz pierwszy wyprodukowane na skalę przemysłową i oferowane komercyjnie.
- 1964 – Firma Boehringer Mannheim , dziś Roche , wprowadziła na rynek swoje pierwsze paski testowe Combur.
Mimo że paski testowe niewiele się zmieniły od lat 60. XX wieku, teraz zawierają szereg innowacji. Nowe techniki impregnacji, bardziej stabilne wskaźniki barwne oraz stała poprawa gradacji barw przyczyniły się do tego, że stosowanie pasków testowych moczu stało się obecnie niezawodnym narzędziem diagnostycznym w praktyce klinicznej i ogólnej. Oferowane menu parametrów stale się wydłużało w kolejnych dziesięcioleciach.
Interferencja kwasu askorbinowego
Wiadomo, że kwas askorbinowy (witamina C) wpływa na reakcję utleniania krwi i poduszeczki glukozowej na zwykłych paskach testowych moczu. Niektóre paski do badania moczu są zabezpieczone przed ingerencją jodanu, który eliminuje kwas askorbinowy poprzez utlenianie. Niektóre paski testowe zawierają test na askorbinian w moczu.
Osad w moczu
Podczas rutynowych badań przesiewowych, jeśli zostanie stwierdzony pozytywny wynik testu na leukocyty, krew, białko, azotyny i pH większe niż 7, osad moczu jest analizowany mikroskopowo w celu dalszego ustalenia diagnozy.
Analizatory automatyczne
Automatyczna analiza pasków testowych moczu przy użyciu automatycznych analizatorów paskowych moczu to ugruntowana praktyka we współczesnej analizie moczu. Mogą mierzyć wapń , krew, glukozę, bilirubinę, urobilinogen, ketony, leukocyty, kreatyninę , mikroalbuminę , pH, kwas askorbinowy i białko.
Bibliografia
Dalsza lektura
- Kompendium analizy moczu: analiza moczu za pomocą pasków testowych. Dr EF Hohenberger, Dr H Kimling (2002) http://www.diavant.com/diavant/servlet/MDBOutput?fileId=1392
- Strasinger, Susan K.; Di Lorenzo Schaub, Marjorie (2008). "5" . Análisis de orina y de los líquidos corporales (w języku hiszpańskim) (5ª wyd.). Redakcja panamericana. s. 56-57. Numer ISBN 978-950-06-1938-7. Źródło 14 marca 2012 .
- Graff, Laurine (1987). "2" . Análisis de orina - Atlas Color (w języku hiszpańskim) (1ª wyd.). Wyd. Medica Panamericana. P. 60. Numer ISBN 978-950-06-0841-1. Źródło 14 marca 2012 .
- Wein, Alan J.; Kavoussi, Louis R.; Nowick, Andrew C.; Partin, Alan W.; Peters, Craig A. (2007). „3” . Campbell-Walsh Urología (w języku hiszpańskim) (9ª wyd.). Od redakcji Médica Panamericana. P. 104. Numer ISBN 978-950-06-8268-8. Źródło 14 marca 2012 .
- Instrukcje dotyczące pasków do analizy moczu
