Receptor progesteronu - Progesterone receptor
Receptora progesteronu ( PR ), znany również jako NR3C3 lub receptorów jądrowych podrodziny 3, grupa C, człon 3 jest białko znajdujące się wewnątrz komórek. Jest aktywowany przez hormon steroidowy progesteron .
U ludzi PR jest kodowany przez pojedynczy gen PGR znajdujący się na chromosomie 11q 22, ma dwie izoformy PR-A i PR-B , które różnią się masą cząsteczkową. PR-B jest pozytywnym regulatorem działania progesteronu, podczas gdy PR-A służy do antagonizowania efektów PR-B.
Mechanizm
Progesteron jest niezbędny do indukcji receptorów progesteronu. Gdy nie występuje hormon wiążący, koniec karboksylowy hamuje transkrypcję . Wiązanie się z hormonem indukuje zmianę strukturalną, która usuwa działanie hamujące. Antagoniści progesteronu zapobiegają rekonfiguracji strukturalnej.
Po tym, jak progesteron zwiąże się z receptorem, następuje restrukturyzacja z dimeryzacją, a kompleks wchodzi do jądra i wiąże się z DNA . Następuje tam transkrypcja, w wyniku której powstaje informacyjny RNA, który jest tłumaczony przez rybosomy w celu wytworzenia określonych białek.
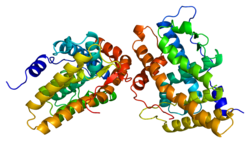
Struktura
| Receptor progesteronu, N-końcowy | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identyfikatory | |||||||||
| Symbol | Progest_rcpt_N | ||||||||
| Pfam | PF02161 | ||||||||
| InterPro | IPR000128 | ||||||||
| |||||||||
Podobnie jak inne receptory steroidowe, receptor progesteronu ma N-końcową domenę regulatorową, domenę wiążącą DNA , sekcję zawiasową i C-końcową domenę wiążącą ligand. Specjalna funkcja aktywacji transkrypcji (TAF), zwana TAF-3, jest obecna w receptorze progesteronu-B, w segmencie B-upstream (BUS) na końcu aminokwasu. Ten segment nie występuje w receptorze-A.
Izoformy
Jak wykazano u myszy z niedoborem receptora progesteronu, fizjologiczne efekty progesteronu zależą całkowicie od obecności ludzkiego receptora progesteronu (hPR), członka nadrodziny receptorów steroidowych receptorów jądrowych. Ludzki gen jednokopiowy (hPR) wykorzystuje oddzielne promotory i miejsca startu translacji do wytworzenia dwóch izoform, hPR-A i -B, które są identyczne z wyjątkiem dodatkowych 165 aminokwasów obecnych tylko na N-końcu hPR-B. Chociaż hPR-B dzieli wiele ważnych domen strukturalnych z hPR-A, są one w rzeczywistości dwoma funkcjonalnie odrębnymi czynnikami transkrypcyjnymi, pośredniczącymi we własnych genach odpowiedzi i efektach fizjologicznych z niewielkim nakładaniem się. Selektywna ablacja PR-A w modelu mysim, skutkująca wyłączną produkcją PR-B, nieoczekiwanie ujawniła, że PR-B przyczynia się raczej do niż hamuje proliferację komórek nabłonka zarówno w odpowiedzi na sam estrogen, jak i w obecności progesteronu i estrogenu . Wyniki te sugerują, że w macicy izoforma PR-A jest niezbędna, aby przeciwdziałać proliferacji wywołanej przez estrogeny, jak również proliferacji zależnej od PR-B.
Polimorfizmy funkcjonalne
W ludzkim genie PR zidentyfikowano sześć miejsc zmiennych, w tym cztery polimorfizmy i pięć wspólnych haplotypów. Polimorfizm jednego regionu promotora, +331G/A, tworzy unikalne miejsce startu transkrypcji. Testy biochemiczne wykazały, że polimorfizm +331G/A zwiększa transkrypcję genu PR, faworyzując produkcję hPR-B w linii komórek raka endometrium Ishikawy.
Kilka badań wykazało obecnie brak związku między polimorfizmami genu receptora progesteronu +331G/A a rakiem piersi lub endometrium. Jednak w tych badaniach uzupełniających brakowało wielkości próby i mocy statystycznej, aby wyciągnąć jakiekolwiek ostateczne wnioski, ze względu na rzadkość występowania SNP +331A. Obecnie nie wiadomo, czy jakiekolwiek polimorfizmy w tym receptorze mają znaczenie dla raka. Badanie 21 populacji pozaeuropejskich zidentyfikowało dwa markery w obrębie haplotypu PROGINS genu PR jako dodatnio skorelowane z rakiem jajnika i piersi.
Badania na zwierzętach
Rozwój
Stwierdzono, że myszy z nokautem z PR mają poważnie zaburzony rozwój zrazikowo-pęcherzykowy gruczołów sutkowych, jak również opóźniony, ale poza tym normalny rozwój przewodów sutkowych w okresie dojrzewania .
Zachowanie
Wiadomo, że w okresie okołoporodowym gryzonia receptor progesteronu (PR) ulega przejściowo ekspresji zarówno w obszarze brzusznej nakrywki (VTA), jak i przyśrodkowej korze przedczołowej (mPFC) mezokorowego szlaku dopaminergicznego. Aktywność PR w tym okresie wpływa na rozwój unerwienia dopaminergicznego mPFC z VTA. Jeśli aktywność PR jest zmieniona, widoczna jest zmiana unerwienia dopaminergicznego mPFC i będzie to również miało wpływ na hydroksylazę tyrozynową (TH), enzym ograniczający szybkość syntezy dopaminy, w VTA. Ekspresja TH w tym obszarze jest wskaźnikiem aktywności dopaminergicznej, która, jak się uważa, bierze udział w normalnym i krytycznym rozwoju złożonych zachowań poznawczych, w których pośredniczy mezokortyczny szlak dopaminergiczny, takich jak pamięć robocza, uwaga, hamowanie behawioralne i elastyczność poznawcza.
Badania wykazały, że gdy antagonista PR, taki jak RU 486, jest podawany szczurom w okresie noworodkowym, zmniejsza się gęstość komórek immunoreaktywnych wobec hydroksylazy tyrozynowej (TH-ir), silnej koekspresji z immunoreaktywnością PR (PR-ir). jest widoczne w mPFC młodych gryzoni. Później, w wieku dorosłym, wykazano również obniżone poziomy TH-ir w VTA. Wykazano, że ta zmiana w ekspresji włókien TH-ir, wskaźnik zmienionej aktywności dopaminergicznej wynikającej z podania noworodka antagonisty PR, upośledza późniejsze wykonywanie zadań, które mierzą hamowanie behawioralne i impulsywność, a także elastyczność poznawczą w wieku dorosłym. Podobne zaburzenia elastyczności poznawczej zaobserwowano również u myszy z nokautem PR w wyniku zmniejszonej aktywności dopaminergicznej w VTA.
Odwrotnie, gdy agonista PR, taki jak kapronian 17α-hydroksyprogesteronu, jest podawany gryzoniom w okresie okołoporodowym, gdy rozwija się mezokortyczny szlak dopaminergiczny, unerwienie dopaminergiczne mPFC wzrasta. W rezultacie zwiększa się również gęstość włókien TH-ir. Co ciekawe, ten wzrost włókien TH-ir i aktywności dopaminergicznej jest również powiązany z upośledzoną elastycznością poznawczą ze zwiększoną perseweracją w późniejszym życiu.
W połączeniu, odkrycia te sugerują, że ekspresja PR podczas wczesnego rozwoju wpływa na późniejsze funkcjonowanie poznawcze u gryzoni. Ponadto wydaje się, że nieprawidłowe poziomy aktywności PR podczas tego krytycznego okresu rozwoju mezokorowego szlaku dopaminergicznego mogą mieć głęboki wpływ na określone behawioralne obwody neuronalne zaangażowane w tworzenie późniejszych złożonych zachowań poznawczych.
Ligandy
Agoniści
- Endogenne progestagenów (na przykład progesteronu )
- Progestageny syntetyczne (np. noretisteron , lewonorgestrel , octan medroksyprogesteronu , octan megestrolu , dydrogesteron , drospirenon )
Mieszany
- Selektywne modulatory receptora progesteronu (na przykład octan uliprystalu , octan telapristone , vilaprisan , asoprisnil , asoprisnil ecamate )
Antagoniści
- Antyprogestogeny (np. mifepriston , aglepriston , onapriston , lonapriston , lilopriston , toripristone )
Interakcje
Wykazano, że receptor progesteronu wchodzi w interakcje z:
Zobacz też
Bibliografia
Dalsza lektura
- Butnor KJ, Burchette JL, Robboy SJ (lipiec 1999). „Aktywność receptora progesteronu w leiomyomatosis peritonealis disseminata”. Międzynarodowy Dziennik Patologii Ginekologicznej . 18 (3): 259–64. doi : 10.1097/00004347-199907000-00012 . PMID 12090595 .
- Leonhardt SA, Boonyaratanakornkit V, Edwards DP (listopad 2003). „Transkrypcja receptora progesteronu i mechanizmy sygnalizacji nietranskrypcyjnej”. Sterydy . 68 (10-13): 761-70. doi : 10.1016/S0039-128X(03)00129-6 . PMID 14667966 . S2CID 7533810 .
- Conneely OM, Mulac-Jericevic B, Lydon JP (listopad 2003). „Zależna od progesteronu regulacja aktywności rozrodczej kobiet przez dwie odrębne izoformy receptora progesteronu”. Sterydy . 68 (10-13): 771-8. doi : 10.1016/S0039-128X(03)00126-0 . PMID 14667967 . S2CID 13600266 .
- Bagchi MK, Tsai SY, Tsai MJ, O'Malley BW (kwiecień 1992). „Zależna od liganda i DNA fosforylacja ludzkiego receptora progesteronu in vitro” . Materiały Narodowej Akademii Nauk Stanów Zjednoczonych Ameryki . 89 (7): 2664-8. Kod Bibcode : 1992PNAS...89.2664B . doi : 10.1073/pnas.89.7.2664 . PMC 48722 . PMID 1557371 .
- Kastner P, Krust A, Turcotte B, Stropp U, Tora L, Gronemeyer H, Chambon P (maj 1990). „Dwa różne promotory regulowane przez estrogen generują transkrypty kodujące dwie funkcjonalnie różne formy A i B ludzkiego receptora progesteronu” . Dziennik EMBO . 9 (5): 1603–14. doi : 10.1002/j.1460-2075.1990.tb08280.x . PMC 551856 . PMID 2328727 .
- Guiochon-Mantel A, Loosfelt H, Lescop P, Sar S, Atger M, Perrot-Applanat M, Milgrom E (czerwiec 1989). „Mechanizmy lokalizacji jądrowej receptora progesteronu: dowody interakcji między monomerami” . Komórka . 57 (7): 1147–54. doi : 10.1016/0092-8674(89)90052-4 . PMID 2736623 .
- Fernandez MD, Carter GD, Palmer TN (styczeń 1983). „Interakcja kanrenonu z receptorami estrogenowymi i progesteronowymi w cytozolu ludzkiej macicy” . Brytyjski Czasopismo Farmakologii Klinicznej . 15 (1): 95-101. doi : 10.1111/j.1365-2125.1983.tb01470.x . PMC 1427833 . PMID 6849751 .
- Oñate SA, Tsai SY, Tsai MJ, O'Malley BW (listopad 1995). „Sekwencja i charakterystyka koaktywatora dla nadrodziny receptorów hormonów steroidowych”. Nauka . 270 (5240): 1354-7. Kod Bibcode : 1995Sci...270.1354O . doi : 10.1126/science.270.5240.1354 . PMID 7481822 . S2CID 28749162 .
- Zhang Y, Beck CA, Poletti A, Edwards DP, Weigel NL (grudzień 1994). „Identyfikacja miejsc fosforylacji unikalnych dla formy B ludzkiego receptora progesteronu. Fosforylacja in vitro przez kinazę kazeinową II” . Czasopismo Chemii Biologicznej . 269 (49): 31034-40. doi : 10.1016/S0021-9258(18)47386-3 . PMID 7983041 .
- Mansour I, Reznikoff-Etievant MF, Netter A (sierpień 1994). „Brak dowodów na ekspresję receptora progesteronu na limfocytach krwi obwodowej podczas ciąży”. Reprodukcja człowieka . 9 (8): 1546-9. doi : 10.1093/oxfordjournals.humrep.a138746 . PMID 7989520 .
- Kalkhoven E, Wissink S, van der Saag PT, van der Burg B (marzec 1996). „Negatywne oddziaływanie między podjednostką RelA(p65) NF-kappaB a receptorem progesteronu” . Czasopismo Chemii Biologicznej . 271 (11): 6217-24. doi : 10.1074/jbc.271.11.6217 . PMID 8626413 .
- Wang JD, Zhu JB, Fu Y, Shi WL, Qiao GM, Wang YQ, Chen J, Zhu PD (luty 1996). „Immunoreaktywność receptora progesteronu na styku matczyno-płodowym ciąży w pierwszym trymestrze: badanie populacji trofoblastów” . Reprodukcja człowieka . 11 (2): 413–9. doi : 10.1093/humrep/11.2.413 . PMID 8671234 .
- Thénot S, Henriquet C, Rochefort H, Cavaillès V (maj 1997). „Różnicowe oddziaływanie receptorów jądrowych z domniemanym ludzkim koaktywatorem transkrypcji hTIF1” . Czasopismo Chemii Biologicznej . 272 (18): 12062-8. doi : 10.1074/jbc.272.18.12062 . PMID 9115274 .
- Jenster G, Spencer TE, Burcin MM, Tsai SY, Tsai MJ, O'Malley BW (lipiec 1997). „Indukcja receptora steroidowego transkrypcji genów: model dwuetapowy” . Materiały Narodowej Akademii Nauk Stanów Zjednoczonych Ameryki . 94 (15): 7879-84. Kod Bibcode : 1997PNAS...94.7879J . doi : 10.1073/pnas.94.15.7879 . PMC 21523 . PMID 9223281 .
- Shanker YG, Sharma SC, Rao AJ (wrzesień 1997). „Ekspresja mRNA receptora progesteronu w pierwszym trymestrze ludzkiego łożyska”. Biochemia i Biologia Molekularna International . 42 (6): 1235–40. doi : 10.1080/15216549700203701 . PMID 9305541 . S2CID 24959703 .
- Bogatszy JK, Lange CA, Wierman AM, Brooks KM, Tung L, Takimoto GS, Horwitz KB (kwiecień 1998). „Warianty receptora progesteronu znajdujące się w komórkach piersi tłumią transkrypcję przez receptory typu dzikiego”. Badania i leczenie raka piersi . 48 (3): 231-41. doi : 10.1023/A:1005941117247 . PMID 9598870 . S2CID 27266907 .
- Williams SP, Sigler PB (maj 1998). „Struktura atomowa progesteronu skompleksowanego z jego receptorem”. Natura . 393 (6683): 392-6. Kod Bibcode : 1998Natur.393..392W . doi : 10.1038/30775 . PMID 9620806 . S2CID 4424486 .
- Boonyaratanakornkit V, Melvin V, Prendergast P, Altmann M, Ronfani L, Bianchi ME, Taraseviciene L, Nordeen SK, Allegretto EA, Edwards DP (sierpień 1998). „Białka chromatyny 1 i 2 o wysokiej ruchliwości oddziałują funkcjonalnie z receptorami hormonów steroidowych w celu zwiększenia ich wiązania DNA in vitro i aktywności transkrypcyjnej w komórkach ssaków” . Biologia molekularna i komórkowa . 18 (8): 4471–87. doi : 10.1128/mcb.18.8.4471 . PMC 109033 . PMID 9671457 .
- Nawaz Z, Lonard DM, Smith CL, Lev-Lehman E, Tsai SY, Tsai MJ, O'Malley BW (luty 1999). „Białko związane z zespołem Angelmana, E6-AP, jest koaktywatorem nadrodziny jądrowych receptorów hormonalnych” . Biologia molekularna i komórkowa . 19 (2): 1182–9. doi : 10.1128/mcb.19.2.1182 . PMC 116047 . PMID 9891052 .
Zewnętrzne linki
- Progesteron + Receptory w Narodowej Bibliotece Medycznej USA Medical Subject Headings (MeSH)